Os doentes com intestinos irritáveis sofrem de reacções de intolerância aos alimentos. Uma dieta pobre em FODMAP ou uma dieta sem glúten pode aliviar significativamente estes sintomas.
Em doentes com síndrome do intestino irritável (SII), a barreira intestinal, a motilidade, a secreção e/ou a sensibilidade visceral são perturbadas. Muitas vezes, a SII está associada a um equilíbrio imunitário entérico deficiente, com processos microinflamatórios ou neuroimunológicos na mucosa intestinal que levam a uma proliferação local de células imunitárias e/ou células CE [1].
“Está agora bem estabelecido que os doentes com síndrome do intestino irritável não estão simplesmente a imaginar coisas”, diz o Prof. Dr. med. Yurdagül Zopf, Chefe de Medicina Nutricional do Hospital Universitário de Erlangen (D), “mas que os processos inflamatórios ocorrem em SII que não se encontram em controlos saudáveis”. Sabe-se através de estudos histológicos que os pacientes com SII aumentaram as proporções de linfócitos intra-epiteliais, mastócitos e células CE. As biópsias Mucosal também mostraram um aumento da densidade das fibras nervosas [2–4]. Além disso, os pacientes com SII mostraram níveis significativamente aumentados de serotonina, histamina e triptase nas medições das concentrações de mediadores [5]. Este perfil alterado do mediador da mucosa activa o sistema nervoso entérico e os nervos aferentes primários (nociceptivos) [1].
O diagnóstico é feito por procedimento de exclusão. Os instrumentos de diagnóstico incluem a medição de patogénicos nas fezes (diagnóstico microbiano e virológico com foco nos turnos relacionados com a inflamação; ovos de vermes), ileocolonoscopia com biópsias por passos, esofagogastroduodenoscopia com biópsias duodenais, e testes de respiração de lactose, frutose e sorbitol H2. Os diagnósticos laboratoriais avançados incluem electrólitos séricos, valores de retenção renal, enzimas hepáticas e pancreáticas, TSH, glucose no sangue/HbA1c, anticorpos celíacos (transglutaminase-AK) e calprotectina A nas fezes.
Regulação através da nutrição
A etiopatogenia da SII é complexa e varia de indivíduo para indivíduo. Consequentemente, existem muitas abordagens terapêuticas que são predominantemente orientadas para o tratamento do sintoma principal. Estas incluem medidas farmacológicas (por exemplo, laxantes, espasmolíticos, antidepressivos, loperamida), fitoterapia, psico-higiene e exercício, bem como dieta [6].
A nutrição, em particular, desempenha um papel importante na regulação da SII (Fig. 1). Vários estudos demonstraram que os pacientes com SII reagem a diferentes alimentos. As mulheres tendem a sofrer mais frequentemente de reacções de intolerância do que os homens, o que pode ser explicado pela maior densidade de mastócitos nas mulheres. Contudo, as reacções de intolerância ocorrem independentemente do sexo, tipo de SII, ansiedade ou local de tratamento (hospital vs. ambulatório) [7].
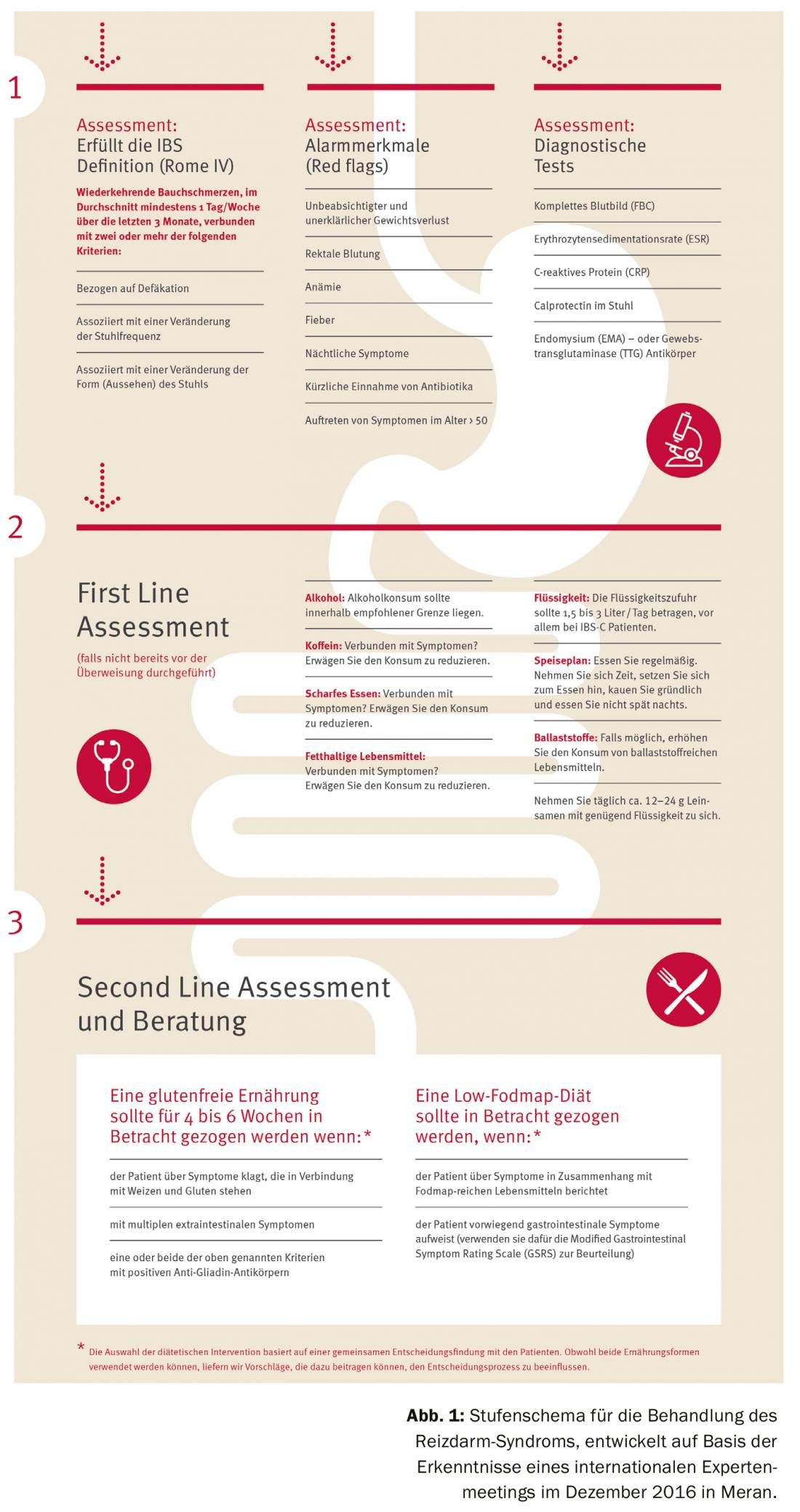
A tolerabilidade da fibra alimentar tem sido bem estudada. É essencial consumir fibras dietéticas solúveis em vez de insolúveis, uma vez que estas últimas podem mesmo agravar os sintomas: A hemicelulose, por exemplo (contida no trigo e no centeio), resulta no aumento da produção de gás. “O paciente tem queixas mais graves do que antes e é mesmo incomodado com outras modulações dietéticas ao longo do tempo”, adverte o Professor Zopf.
Foi também confirmado que as alergias e intolerâncias são mais prevalentes nos doentes com SII [8]. Embora apenas as alergias induzidas por IgE possam ser detectadas de forma diagnóstica, os pacientes com aumento da triptase, histamina e actividade dos mastócitos no intestino têm um risco mais elevado de reacções imunológicas.
A dieta sem glúten também ajuda os doentes com SII
Uma proteína em particular é frequentemente o foco de interesse: o glúten. Aqui é importante diferenciar quem realmente não pode tolerar o glúten – porque uma dieta pobre em glúten não é automaticamente mais saudável para todos.
Uma dieta para toda a vida sem glúten é a base do tratamento da doença celíaca. Os doentes com intolerância ao glúten/ trigo também beneficiam de uma dieta adaptada, embora não seja recomendada para indivíduos saudáveis, uma vez que, de acordo com os estudos actuais, não existe benefício clínico para indivíduos saudáveis.
Em muitos doentes com SII, os sintomas são desencadeados ou intensificados por trigo ou glúten. Nestes casos, uma dieta sem glúten leva a uma melhoria significativa dos sintomas, como mostra o estudo IBS (GIBS) publicado em 2017. Aí, os sintomas de 34% dos pacientes com SII melhoraram de forma estatisticamente significativa e clinicamente relevante no decurso de uma dieta de quatro meses sem glúten. A adesão à mudança alimentar manteve-se em muitos assuntos mesmo após o estudo: Uma proporção muito elevada (todos os respondentes, 55% dos não respondentes) continuou a comer uma dieta sem glúten [9].
FODMAP – observe o nível de tolerância individual!
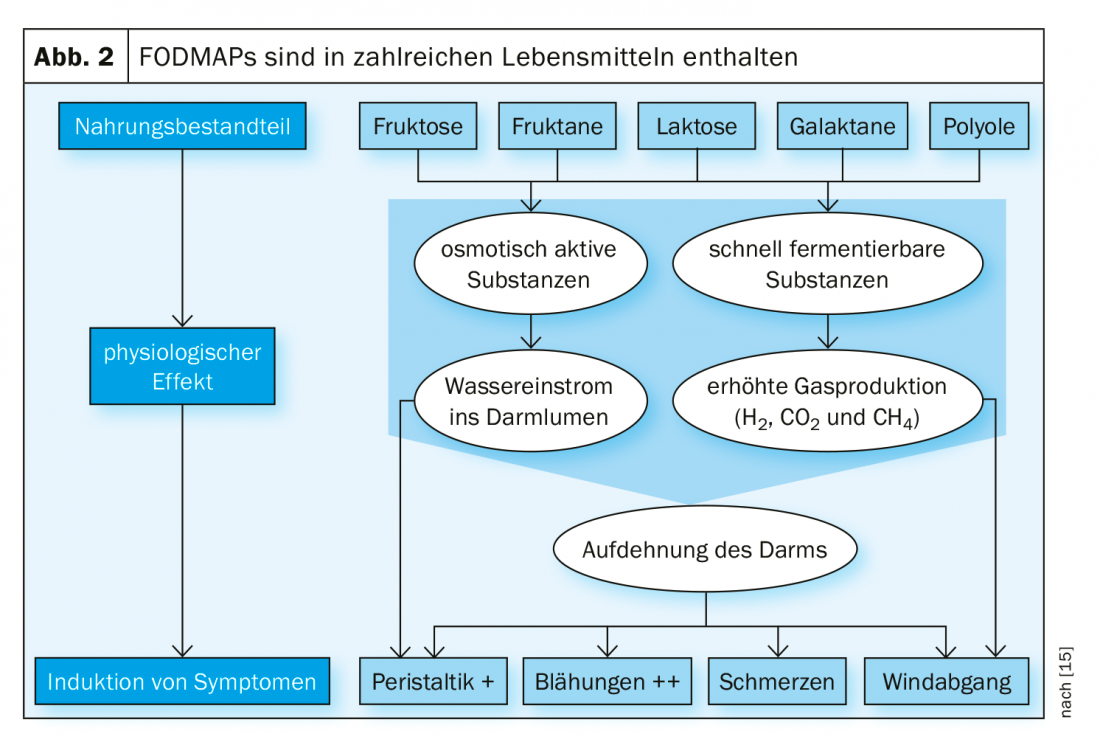
Os FODMAPs – oligo-, di- e monossacarídeos fermentáveis, bem como os polióis – são pouco ou nada absorvidos no intestino delgado. Os processos osmóticos e a fermentação levam ao aumento do afluxo de água e à formação de gás. A má absorção destes hidratos de carbono é normal, muitas pessoas não sentem quaisquer efeitos negativos quando consomem FODMAPs. Os pacientes com SII, por outro lado, experimentam por vezes sintomas graves em resposta aos FODMAPs, tais como flatulência, dor e desconforto, flatulência, mudança nas fezes e/ou letargia (Fig. 2). Reagem com uma produção de gás significativamente superior à dos controlos saudáveis [10]. Uma dieta pobre em FODMAP leva a uma melhoria dos sintomas em 68-76% dos pacientes [11].
Zopf sublinha a importância de uma abordagem adaptada individualmente: “Cada um de nós tem um nível de tolerância diferente do FODMAP. A dieta FODMAP não significa: redução a zero. O limiar que é tolerável para o indivíduo deve ser detectado. Assim, uma dieta pobre em FODMAP nem sempre tem de ser seguida na sua forma máxima. Pode ser suficiente para reduzir as acções.
Para evitar a desnutrição, é importante em qualquer caso que a dieta seja levada a cabo na companhia de um terapeuta de nutrição profissional. Isto guia o doente através de três fases:
- Dieta de eliminação
- Re-introduzir (para verificar que substâncias estão a causar problemas)
- Adaptação
Uma preocupação associada à dieta pobre em FODMAP é a redução associada das bifidobactérias [12]. Uma tal mudança na flora intestinal é compreensível, especialmente porque os FODMAPs produzem várias substâncias que mantêm a integridade da mucosa. Contudo, um estudo posterior mostrou que a terapia probiótica concorrente pode estabilizar a população de bifidobactérias [13].
Uma mudança na dieta também tem efeitos positivos sobre os níveis alterados de serotonina e PYY em pacientes com SII [14].
Fonte: Zopf Y: “Influência da dieta na IBS”. Palestra no simpósio satélite Dr. Schär “Nutrição na síndrome do intestino irritável”, DGIM 2019, Wiesbaden (D).
Literatura:
- Layer P, et al.: S3-Leitlinie Irritable Bowel Syndrome: Definição, Fisiopatologia, Diagnóstico e Terapia. Directriz conjunta da Sociedade Alemã de Doenças Digestivas e Metabólicas (DGVS) e da Sociedade Alemã de Neurogastroenterologia e Motilidade (DGNM). Z Gastroenterol 2011; 49(2): 237-293.
- Akbar A, et al: Aumento do receptor de capsaicina TRPV1-expressão das fibras sensoriais na síndrome do intestino irritável e a sua correlação com a dor abdominal. Trip 2008; 57(7): 923-929.
- Guilarte M, et al.: Pacientes com Diarreia-predominante IBS mostram activação de mastócitos e hiperplasia no jejuno. Trip 2007; 56(2): 203-209.
- Spiller RC: Síndrome do cólon irritável pós-infeccioso. Gastroenterologia 2003; 124(6): 1662-1671.
- Buhner S, et al.: Activação de neurónios entéricos humanos através de sobrenadantes de espécies de biopsia cólica de doentes com síndrome do cólon irritável. Gastroenterologia. 2009; 137(4): 1425-1434.
- Schaub N, Schaub N: Síndrome do intestino irritável. Insights e Perspectivas 2012. SMF 2012; 12(25): 505-513.
- Simrén M: Alteração da Flora Gastrointestinal em Pacientes com Distúrbios Intestinais Funcionais: Um Caminho em Frente? Therap Adv Gastroenterol 2009; 2(4 Suppl): 5-8.
- Boettcher E, Crowe SE: Proteínas dietéticas e perturbações gastrointestinais funcionais. Am J Gastro-enterol 2013; 108(5): 728-736.
- Barmeyer C, et al.: Resposta a longo prazo a uma dieta sem glúten como prova da sensibilidade não celíaca do trigo em um terço dos doentes com síndrome do intestino irritável do tipo diarreia e misto. Int J Colorectal Dis 2017; 32(1): 29-39.
- Ong DK, et al.: Manipulação de hidratos de carbono de cadeia curta dietética altera o padrão de produção de gás e a génese dos sintomas na síndrome do intestino irritável. J Gastroenterol Hepatol 2010; 25(8): 1366-1373.
- Tuck CJ, et al.: Oligossacarídeos fermentáveis, dissacarídeos, monossacarídeos e polióis: papel na síndrome do cólon irritável. Perito Rev Gastroenterol Hepatol 2014; 8(7): 819-834.
- Staudacher HM, et al.: Fermentable Carbohydrate Restriction Reduces Luminal Bifidobacteria and Gastrointestinal Symptoms in Patients with Irritable Bowel Syndrome. J Doença Nutricional 2012; 142(8): 1510-1518.
- Staudacher HM, et al: A Diet Low in FODMAPs Reduz os Sintomas em Pacientes com Síndrome do Colón Irritável e A Probiotic Restores Bifidobacterium Species: A Randomized Controlled Trial. Gastroenterologia 2017; 153(4): 936-947.
- Mazzawi T, El-Salhy M: Efeito da dieta e da orientação alimentar individual sobre as células endócrinas gastrointestinais em doentes com síndrome do intestino irritável (Revisão). Int J Mol Med 2017; 40(4): 943-952.
- Beatrice Schilling: conceito FODMAP. https://fodmap.ch/de/fodmap-konzept, acedido pela última vez a 13 de Agosto de 2019.
- Leiß O: Fibra, Intolerâncias Alimentares, FODMAPs, Glúten e Doenças Intestinais Funcionais – Actualização 2014. Z Gastroenterol 2014; 52(11): 1277-1298.
PRÁTICA DO GP 2019; 14(8): 40-41