O objectivo da terapia medicamentosa para o carcinoma da próstata (PCa) é o de prolongar a sobrevivência com efeitos secundários aceitáveis. Hoje em dia, vários medicamentos estão disponíveis para alcançar a privação efectiva de androgénio (ADT). O objectivo é reduzir o nível de testosterona abaixo dos 20 ng/dl. Há uma indicação para a iniciação primária do ADT na PCa sintomática metastática. A um doente assintomático também pode ser oferecido ADT, mas neste caso deve ter lugar uma pesagem detalhada das possíveis vantagens e desvantagens. Se a progressão do PSA ocorrer apesar da manipulação hormonal, isto é referido como PCa resistente à castração. As opções de tratamento para estes pacientes são a quimioterapia (principalmente docetaxel), a abiraterona e a enzalutamida.
O carcinoma da próstata (PCa) é a forma mais comum de cancro na Suíça, com cerca de 6000 novos casos por ano. Com uma idade média de início de 70 anos, a PCa é uma doença dos homens mais velhos. Dependendo da fase do tumor e da diferenciação, o curso é frequentemente progressivo, mas pode muitas vezes ser favoravelmente influenciado pelo uso de medicamentos [1]. Estes são resumidos brevemente a seguir.
Terapia hormonal do carcinoma da próstata
A terapia hormonal é a primeira linha de terapia medicamentosa para PCa. Em 1941, Huggins e Hodges foram os primeiros a descrever a influência positiva da privação de androgénio (ADT) por orquiectomia bilateral no cancro da próstata, pelo qual foram galardoados com o Prémio Nobel em 1966 [2]. Actualmente, estão disponíveis vários medicamentos para conseguir um ADT eficaz (Fig. 1). Uma redução do valor de testosterona sérica abaixo de 50 ng/dl é indicada como eficaz [3]. Contudo, dados mais recentes mostram que a castração cirúrgica pode mesmo reduzir a testosterona para menos de 20 ng/dl – este valor deve, por conseguinte, ser também visado na castração com medicação [4].
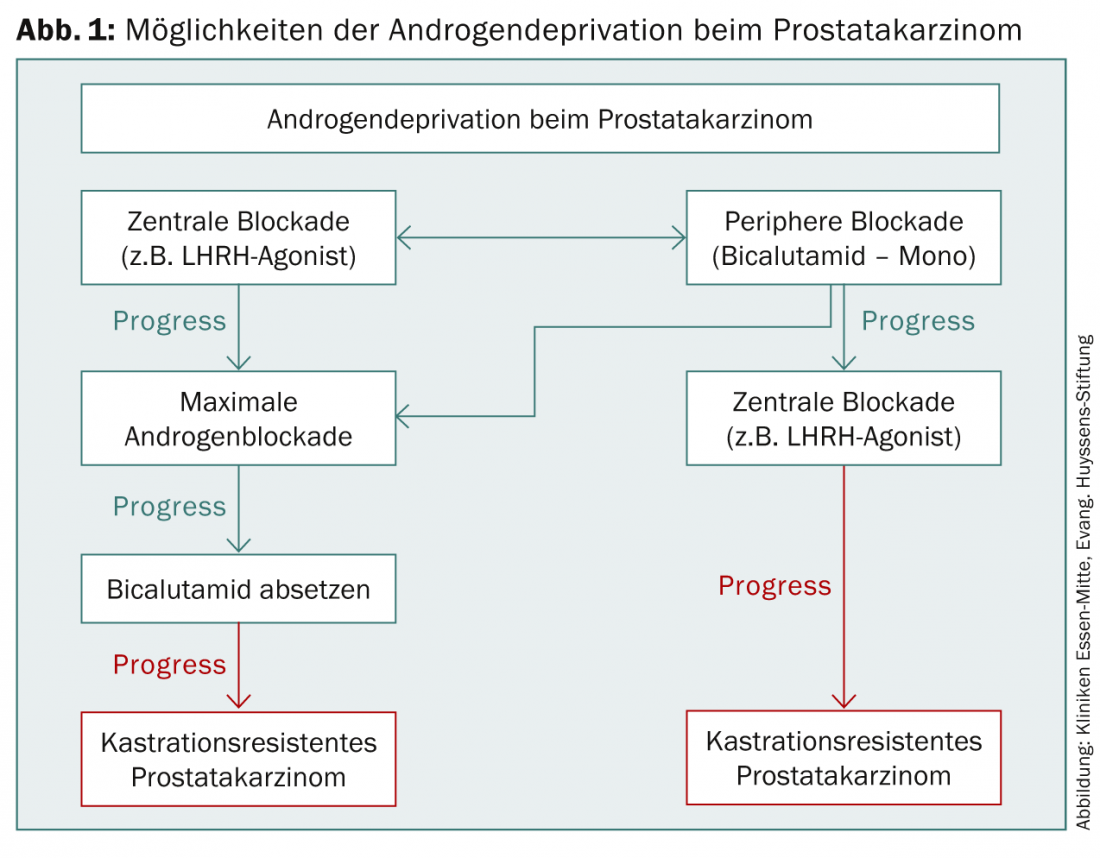
Uma das indicações para a iniciação primária do ADT está na PCa sintomática metastática. A um doente assintomático pode também ser oferecido ADT primário, mas neste caso deve ser feita uma consideração detalhada entre possíveis efeitos secundários adversos, um possível impacto na qualidade de vida, a natureza paliativa do tratamento e o prolongamento do intervalo sem progressão. No caso de progressão tumoral após terapia anterior, a TDA deve ser iniciada com um tempo de duplicação do PSA inferior a três meses, progressão local sintomática ou metástase distante comprovada. O ADT é também utilizado periintervencionalmente em pacientes de alto risco como parte da radioterapia percutânea. Antes da braquiterapia, crioterapia ou ultra-som de alta intensidade focalizada (HIFU), o ADT pode reduzir o volume da próstata [4].
LHRH agonistas
O ADT mais frequentemente utilizado é um agonista da LHRH [3]. Isto liga-se aos receptores LHRH e interrompe a produção de testosterona, regulando para baixo os receptores na glândula pituitária. Inicialmente, há um aumento de testosterona porque a ligação do agonista ao receptor leva a um aumento da produção de LH e, portanto, também de testosterona. Isto deve ser contrariado pela administração de um bloqueador de receptores andrógenos como a bicalutamida 150 mg durante quinze dias antes e duas semanas após a administração inicial do agonista LHRH. O nível de castração é normalmente atingido dentro deste tempo [5,6]. Os agonistas LHRH são injectados por via subcutânea ou intramuscular e estão disponíveis como depósitos mensais durante 1-12 meses, dependendo da preparação. As preparações comuns incluem leuprorelina, goserelina e buserelina. Efeitos secundários comuns são os fluxos quentes, perda de libido e impotência, e com administração prolongada, osteoporose e atrofia muscular.
O bloqueio intermitente de androgénio como alternativa para minimizar os efeitos secundários do ADT não é actualmente recomendado como tratamento de rotina nas directrizes da Sociedade Alemã de Urologia, devido à falta de dados a longo prazo sobre a sobrevivência global e específica do tumor. No entanto, após a educação prévia sobre os dados ainda em falta a longo prazo, o TDA intermitente pode ser utilizado para reduzir o impacto da medicação na qualidade de vida. A duração mais comum da terapia é de 6-9 meses com uma pausa terapêutica subsequente, que pode variar em duração dependendo da dinâmica do PSA [3,7].
Durante o ADT, para além das determinações regulares do PSA, os níveis de testosterona também devem ser verificados regularmente. Se o nível de castração não for alcançado pelo agente escolhido, deve ser iniciada uma mudança de agente, a administração adicional de um bloqueador de receptores androgénicos (mais comumente bicalutamida 50 mg) para o bloqueio completo dos androgénicos ou uma orquiectomia subcapsular [3].
Antagonistas de LHRH
Uma alternativa aos agonistas da LHRH são os antagonistas da LHRH Abarelix (não aprovados na Suíça) e Degarelix (Firmagon®). Estes bloqueadores dos receptores LHRH não levam a um aumento da testosterona e já reduzem a testosterona abaixo dos níveis de castração em poucos dias, o que constitui uma alternativa à castração em PCa altamente sintomática metastática. Com a administração de Abarelix existe a possibilidade de uma reacção alérgica até ao choque anafiláctico, este efeito secundário não é observado com Degarelix [8,9].
Bloqueador de receptores de androgénio
Existe uma variedade de esteróides (por exemplo, acetato de ciproterona) e bloqueadores de receptores de androgénio não esteróides que inibem a acção da diidrotestosterona directamente a nível celular. O nível de testosterona não é diminuído por isto. Por razões de praticabilidade, discutiremos aqui apenas a preparação mais comum com menos efeitos secundários, a bicalutamida não esteróide (Casodex® e genéricos).
A bicalutamida, tomada por via oral, é aprovada para monoterapia em cancro da próstata não-metastático mas localmente avançado. Foi demonstrado que tempos de sobrevivência semelhantes podem ser alcançados através de uma dose de 150 mg diários como por castração cirúrgica [10]. Os doentes com PCa metastático e um PSA >400 ng/ml mostraram uma sobrevivência sem progressão mais curta e uma sobrevivência global mais curta, mas também nestes doentes – tendo em conta a melhor qualidade de vida em comparação com o ADT – a monoterapia com bicalutamida pode ser administrada após informação apropriada [11]. Um dos efeitos secundários mais comuns é frequentemente a ginecomastia dolorosa, pelo que se recomenda a irradiação profiláctica das glândulas mamárias antes de se iniciar a terapia.
Bloqueio máximo de androgénio
Se houver um aumento de PSA com monoterapia LHRH, é adicionado um bloqueador de receptores andrógenos. A isto chama-se bloqueio total ou máximo de androgénio. É também utilizada quando os níveis de testosterona não descem abaixo dos níveis de castração com monoterapia LHRH ou quando há um aumento de PSA com monoterapia bicalutamídica. No entanto, a possibilidade de aumento dos efeitos secundários deve ser discutida em pormenor com o doente. Num doente assintomático com um aumento de PSA, é também possível esperar inicialmente enquanto se mantém a monoterapia e só iniciar o bloqueio máximo de androgénio quando os sintomas aparecem [3].
Manipulação de hormonas secundárias
Se o PSA subir novamente sob bloqueio máximo de androgénio, a descontinuação do bloqueador do receptor de androgénio pode causar a queda do PSA devido a uma mutação pontual em desenvolvimento no receptor de testosterona [12]. Além disso, numerosas outras substâncias estão disponíveis para manipulação de hormonas secundárias, por exemplo corticosteróides, cetoconazol, aminoglutetimida, estrogénios, progestagénio, tamoxifeno, inibidores de somatostatina, retinóides e calcitriol. O Ketoconazol, em particular, pode prolongar o tempo para iniciar a quimioterapia [13]. Antes de iniciar a terapia, o paciente deve ser informado em pormenor sobre a natureza paliativa da terapia, possíveis efeitos secundários e a falta de provas de sobrevivência prolongada [3].
Quimioterapia
Se a progressão do PSA ocorrer apesar da manipulação hormonal secundária, isto é referido como carcinoma da próstata resistente à castração. Num doente assintomático, é possível fazer mais esperas. As indicações para iniciar a quimioterapia são metástase progressiva ou um PSA rápido que duplica o tempo e um PSA >15 ng/ml (Fig. 2).
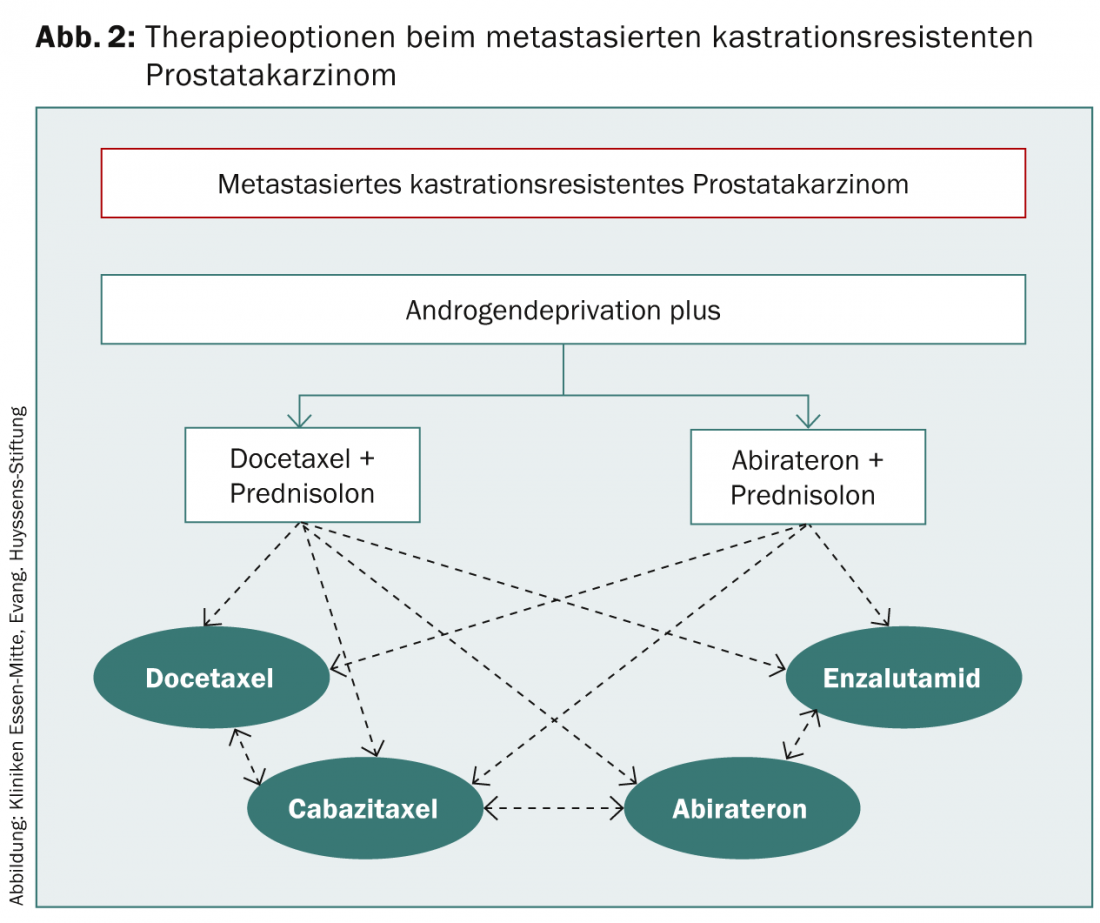
Devido aos efeitos secundários a esperar, deve ser considerada cuidadosamente num doente assintomático quando faz sentido iniciar a terapia.
Docetaxel é utilizado para quimioterapia de primeira linha. Docetaxel é administrado 75 mg/m² a intervalos de três semanas juntamente com 2× 5 mg de prednisolona diariamente durante 6-10 ciclos. O ADT pré-existente deve ser mantido, mas os bloqueadores dos receptores de androgénio devem ser descontinuados pelo menos quatro semanas antes de se iniciar a quimioterapia [3]. Se a doença progredir com docetaxel, pode ser considerada uma mudança para cabazitaxel 25 mg/m² a cada três semanas em combinação com prednisolona. Em ensaios, um benefício de sobrevivência só ocorreu após receber pelo menos três ciclos de cabazitaxel. Novos dados também mostram uma vantagem de sobrevivência para docetaxel na terapia de primeira linha antes da ADT, o que provavelmente levará a uma mudança na sequência da terapia.
Abiraterone (Zytiga®)
Abiraterona (Zytiga®), um inibidor de CYP17, reduz os níveis de testosterona ao inibir a síntese de testosterona nos testículos, próstata e glândulas supra-renais. Desde Outubro de 2011, a abiraterona foi aprovada para o tratamento da PCa resistente à castração metastática após a progressão do tumor após a quimioterapia docetaxel, sendo assim também recomendada nas directrizes das sociedades urológicas. A abiraterona é agora também aprovada como terapia de primeira linha para PCa resistente à castração metastática, mas apenas para doentes assintomáticos a moderadamente sintomáticos. É de notar que os doentes tratados com docetaxel antes da docetaxel mostram uma progressão mais rápida da doença após a administração de docetaxel do que os doentes ingénuos com docetaxel [14].
A abiraterona é tomada sob a forma de comprimidos numa dosagem de 1000 mg diários em combinação com prednisolona; o ADT existente é continuado. Os efeitos secundários relevantes são principalmente hipertensão, hipocalemia e retenção de fluidos devido ao excesso de mineralocorticóides.
Enzalutamida (Xtandi®)
A enzalutamida (Xtandi®) foi aprovada na Europa em Junho de 2013 para o tratamento da PCa resistente à castração metastática após a terapia de docetaxel. O inibidor do receptor de androgénio é tomado diariamente na forma de comprimidos com ou sem prednisolona. Os efeitos secundários relevantes são dores de cabeça e afrontamentos. Existe uma contra-indicação em caso de disfunção hepática grave. Em ensaios, a administração oral de 160 mg de enzalutamida diariamente resultou numa sobrevivência global significativamente prolongada vs. placebo; portanto, a enzalutamida é outra terapia alternativa ao cabazitaxel e à abiraterona [15]. Além disso, a aprovação da enzalutamida antes da quimioterapia docetaxel é esperada para o Outono de 2014.
Terapia de metástases ósseas
Para o tratamento de metástases ósseas, a directriz recomenda actualmente o ácido zoledrónico bisfosfonato (Zometa® e genéricos) ou o denosumab de anticorpos monoclonais (Prolia®) [3]. Além disso, o rádio-223 também está disponível para indicações rigorosas. No entanto, uma discussão detalhada sobre estes medicamentos excederia o âmbito deste artigo, pelo que é feita referência à literatura específica do tema.
Conclusão
Existem actualmente muitos medicamentos diferentes disponíveis para o tratamento de PCa avançados. Especialmente no campo da PCa resistente à castração metastática, a aprovação de numerosos novos medicamentos resultou em promissoras alternativas de tratamento. No entanto, são urgentemente necessários mais estudos para desenvolver uma terapia sequencial baseada em provas.
Mensagens Take-home-messages
- O objectivo da terapia medicamentosa para PCa é de prolongar a sobrevivência com efeitos secundários aceitáveis.
- O ADT deve também ser continuado na fase de castração resistente à metástase.
- Uma alternativa à quimioterapia primária é actualmente a abiraterona.
- A enzalutamida é outra alternativa depois (e a partir do Outono de 2014 também antes) da docetaxeloterapia.
- Ainda não há provas suficientes para desenvolver um plano faseado de selecção de drogas na fase resistente à castração metastática.
- Estão disponíveis medicamentos eficazes para o tratamento de metástases ósseas: ácido zoledrónico, denosumabe e radium-223.
Literatura:
- Cancro na Alemanha 2007/2008. 8ª edição. Instituto Robert Koch (ed.) e a Sociedade de Registos Epidemiológicos do Cancro na Alemanha (ed.). Berlim, 2012.
- Huggins C, et al: Estudos sobre o cancro da próstata. II. os efeitos da castração no carcinoma avançado da glândula prostática. Arch Surg 1941; 43: 209-223.
- Directriz interdisciplinar de qualidade S3 para a detecção precoce, diagnóstico e terapia das diferentes fases do carcinoma da próstata.
- Gomella LG: Supressão eficaz da testosterona para o cancro da próstata: existe uma melhor terapia de castração? Rev Urol 2009; 11(2): 52-60.
- www.awmf.org/uploads/tx_szleitlinien/043-022OLl_S3_Prostatakarzinom_2011.pdf. (Recuperado em 11.08.2014)
- Auclair C, et al.: Inibição do nível de receptor da hormona luteinizante testicular por tratamento com uma potente hormona luteinizante agonista da gonadotropina coriónica humana. Biochem Biophys Res Commun 1977; 76(3): 855-862.
- Huhtaniemi I, et al: Resposta dos níveis de gonadotropina circulante ao tratamento agonista de GnRH no cancro da próstata. J Androl 1991; 12(1): 46-53.
- Tunn U: O estado actual da terapia de privação intermitente de androgénio (DAI) para o cancro da próstata: colocar a DAI sob as luzes da ribalta. BJU Int 2007; 99 Suppl 1: 19-22; discussão 23-24.
- Trachtenberg J, et al: Uma fase 3, rótulo aberto multicêntrico, estudo aleatório de abarelix versus leuprolide mais antiandrogénio diário em homens com cancro da próstata. J Urol 2002; 167: 1670-1674.
- Van Poppel H, et al: Degarelix: um novo bloqueador de receptores da hormona libertadora de gonadotropina (GnRH) – resulta de um estudo de dosagem de 1 ano, multicêntrico, aleatório, fase 2 no tratamento do cancro da próstata. Eur Urol 2008; 54(4): 805-813.
- Iversen P, et al: Casodex (bicalutamida) monoterapia de 150 mg em comparação com a castração em pacientes com cancro da próstata não-metastático previamente não tratado: resultados de dois ensaios multicêntricos aleatórios com um seguimento mediano de 4 anos. Urologia 1998; 51(3): 389-396.
- Kaisary AV, et al: Existe um papel para a monoterapia antiandrogénica em doentes com cancro da próstata metastásico? Prostate Cancer Prostatic Dis 2001; 4(4): 196-203.
- Pequeno EJ, et al: terapia hormonal de segunda linha para o cancro da próstata avançado: um paradigma em mudança. J Clin Oncol 1997; 15(1): 382-388.
- Lam JS, et al: Terapia hormonal secundária para o cancro da próstata avançado. J Urol 2006; 175(1): 27-34.
- Schweizer MT, et al: The Influence of Prior Abiraterone Treatment on the Clinical Activity of Docetaxel in Men with Metastatic Castration-resistant Prostate Cancer. Eur Urol 2014; pii: S0302-2838(14)00069-4. doi:10.1016/ j.eururo. 2014.01.018.
- Scher H, et al: Aumento da sobrevivência com enzalutamida no cancro da próstata após quimioterapia. N Engl J Med 2012; 367: 1187-1197.
InFo ONCOLOGy & HEMATOLOGy 2014; 2(8): 10-13