A diabetes é a causa mais comum de doença renal crónica (CKD).
A organização internacional Kidney Disease: Improving Global Outcomes (KDIGO) publicou recentemente novas directrizes sobre a gestão da diabetes tipo 2 em pessoas com CKD. Propaga-se uma abordagem de tratamento que se baseia em vários pilares. Uma das mensagens chave: a progressão da doença renal pode ser retardada com novos medicamentos, para que muitas pessoas possam ser poupadas à diálise por um longo período de tempo.
Embora no passado houvesse apenas algumas opções de tratamento disponíveis que podiam parar a progressão do CKD associado à diabetes, existem actualmente várias classes modernas de medicamentos que podem retardar significativamente a perda da função renal se forem utilizados a tempo. É portanto importante que as pessoas afectadas recebam cuidados atempados de um nefrologista [1]. “Os critérios para apresentar a pessoa com diabetes mellitus ao nefrologista são, por exemplo: gota eGFR nova ou significativa, eGFR ≤60 ml/min/1,73 m², eritrocitúria ou uma albuminúria de grau 2 ou 3”, explicou a Prof.ª Dra. Julia Weinmann-Menke, Mainz, assessora de imprensa da Sociedade Alemã de Nefrologia [1,3].
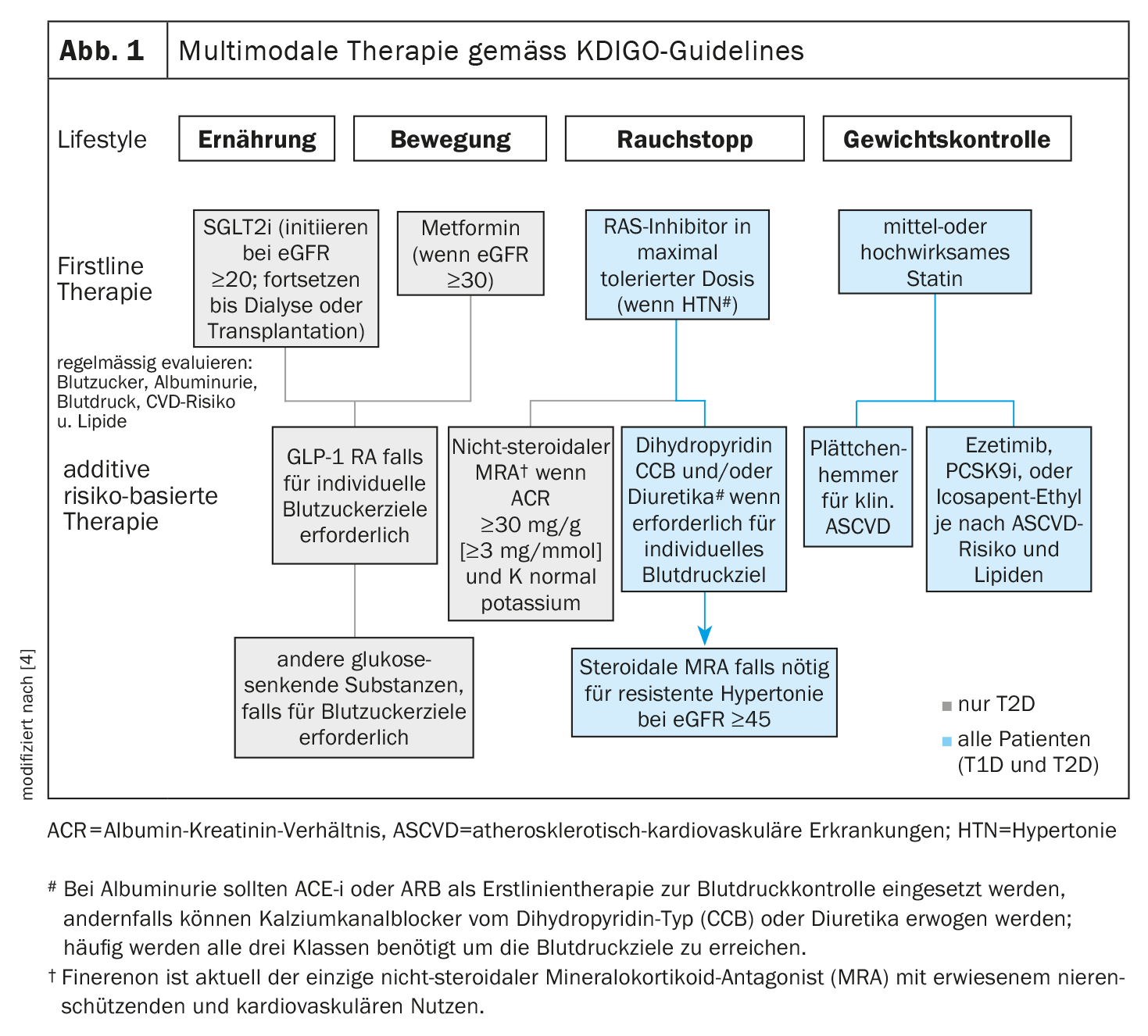
O facto de as directrizes do KDIGO emitidas em 2020 já estarem disponíveis numa versão revista em 2022 reflecte o rápido progresso no campo do tratamento da nefropatia associada à diabetes [4]. O KDIGO propaga uma abordagem de terapia multimodal (Fig. 1).
- Todos os pacientes devem prestar atenção aos factores do estilo de vida como o exercício, a dieta e a cessação do tabagismo. As terapias medicamentosas de primeira linha devem ser seleccionadas de acordo com as características clínicas individuais.
- O controlo da glicemia na diabetes tipo 2 (T2D) é baseado numa combinação de metformina e cotransportador de sódio-glucose 2 inibidores (SGLT-2-i). Para pacientes em que SGLT-2-i e metformina não são eficazes para atingir os objectivos de glicose no sangue, os agonistas do receptor do peptídeo 1 tipo glucagon (GLP-1 RA) são o medicamento preferido para a diminuição do glucose-baixo.
- Em doentes com albuminúria e hipertensão (HTN), aconselha-se a inibição do sistema renina-angiotensina (RAS). A estatina é recomendada para todos os doentes com T1D ou T2D e CKD.
- Um antagonista não esteróide dos receptores de mineralocorticóides (ns-MRA) pode ser acrescentado à terapia de primeira linha em pacientes com T2D e um elevado risco residual de progressão de CKD e eventos cardiovasculares**.
- A aspirina é geralmente utilizada para a prevenção secundária ao longo da vida em pacientes com doenças cardiovasculares estabelecidas, a menos que existam contra-indicações, e pode ser considerada para a prevenção primária em pacientes de alto risco de doença cardiovascular aterosclerótica (ASCVD).
** Indicador de risco residual elevado para a progressão de CKD e eventos cardiovasculares: albuminúria persistente (>30 mg/g [>3 mg/mmol])

SGLT-2-i: o limiar eGFR foi reduzido
Os pacientes com T2D, CKD e um eGFR ≥20 ml/min por 1,73 m² foram agora extensamente estudados em TCR no SGLT-2-i. Com base nestes estudos, reitera-se a forte recomendação de tratar pacientes com T2D e CKD com um SGLT-2-i, independentemente da albuminúria. Uma mudança importante é o limiar eGFR mais baixo em que o SGLT-2-i deve ser iniciado. A directriz de 2022 recomenda a introdução de um SGLT-2-i para pacientes com T2D e CKD que tenham um eGFR ≥20 ml/min por 1,73 m², em oposição a ≥30 ml/min por 1,73 m² na directriz de 2020 [4].

Os estudos Dapagliflozina e Prevenção de Resultados Adversos na Doença Crónica dos Rins (DAPA-CKD) e Efeito da Sotagliflozina em Eventos Cardiovasculares e Renais em Pacientes com Diabetes Tipo 2 e Deficiência Renal Moderada que Estão em Risco Cardiovascular (SCORED) incluía doentes com CKD com um eGFR de até 25 ml/min por 1,73 m². [5,6].
O Estudo de Protecção do Coração e Rim com Empagliflozina (EMPA-KIDNEY), realizado exclusivamente com populações de CKD e parado precocemente devido ao benefício, incluiu também participantes com um eGFR ≥20 ml/min por 1,73 m² [7]. Análises de subgrupos de estudos individuais e meta-análises demonstraram benefícios renais e cardiovasculares em todas as categorias de eGFR, incluindo participantes com eGFR <30 ml/min por 1,73 m² e aqueles sem albuminúria [8,9].

Agonistas de receptores GLP-1: novos conhecimentos
Em 2021, foram publicados os resultados de um novo grande estudo sobre efpeglenatide, que foram incorporados nas novas directrizes do KDIGO. O estudo AMPLITUDE-O (Effect of Efpeglenatide on Cardiovascular Outcomes) apoiou a evidência dos benefícios cardiovasculares da AR GLP-1 e reforçou a hipótese de que a AR GLP-1 também pode melhorar os resultados renais [2]. Consequentemente, a GLP-1 RA continua a ser a terapia de segunda linha recomendada para a redução dos níveis de glicose no sangue em T2D e CKD. O benefício cardiovascular comprovado da AR da GLP-1 foi demonstrado para todas as categorias de eGFR e serviu como a principal razão para recomendar a AR da GLP-1 como o medicamento de escolha para baixar a glicemia em pacientes com T2D e CKD que não alcançaram os seus objectivos de glicemia apesar da utilização de SGLT-2-i e metformina (ou nos quais SGLT-2-i e/ou metformina não puderam ser utilizados).
Finerenone – antagonista não esteróide de mineralocorticóides como o mais recente jogador
Também eficaz na prevenção da progressão da doença renal diabética é o novo antagonista selectivo, não esteróide, dos receptores mineralocorticóides finerenona [1]. Isto foi demonstrado pelos dois grandes ensaios clínicos FIDELIO-DKD (Finerenone in Reducing Kidney Failure and Disease Progression in Diabetic Kidney Disease) [10] e FIGARO-DKD (Finerenone in Reducing Cardiovascular Mortality and Morbidity in Diabetic Kidney Disease) [11] bem como pela análise combinada FIDELITY [12] baseada neles. Os resultados mais importantes num relance:
No ensaio FIDELIO-DKD, a finerenona reduziu significativamente a incidência tanto do resultado renal composto primário (insuficiência renal, declínio sustentado no eGFR pelo ≥40% ou morte devido a doença renal; razão de perigo [HR](morte por causas cardiovasculares, enfarte do miocárdio não fatal, acidente vascular cerebral não fatal ou hospitalização por insuficiência cardíaca; FC: 0,86; IC 95%: 0,75-0,99) e o resultado cardiovascular composto secundário (morte por causas cardiovasculares, enfarte do miocárdio não fatal, acidente vascular cerebral não fatal ou hospitalização por insuficiência cardíaca; FC: 0,86; IC 95%: 0,75-0,99). [10].
No FIGARO-DKD, a finerenona reduziu significativamente o ponto final cardiovascular combinado (HR: 0,87; 95% CI: 0,76-0,98) [11].
No ensaio FIDELITY, os resultados cardiovasculares globais foram reduzidos em doentes tratados com finerenona (HR: 0,86; 95% CI: 0,78-0,95), sem heterogeneidade significativa nas características dos doentes na linha de base [12].
Os doentes tratados com finerenona também tinham menos probabilidades de experimentar insuficiência renal, um decréscimo da taxa de filtração glomerular (TFGE) superior a 57% ou morte renal (FC: 0,77; IC 95%: 0,67-0,88), e menos probabilidades de experimentar insuficiência renal definida como início de diálise crónica ou transplante renal (FC: 0,80; IC 95%: 0,64-0,99).
Literatura:
- “Dia Mundial da Diabetes: A diálise não é um destino inevitável para as pessoas com diabetes mellitus”, Sociedade Alemã de Nefrologia, 11.11.2022
- Gerstein HC, et al: N Engl J Med 2021; 385: 896-907.
- Documento de posição Cooperação Diabetologia/Nefrologia. Sociedade Alemã de Diabetes/Sociedade Alemã de Nefrologia/Associação de Nefrologistas de Hospital Sénior 2018. www.ddg.info,(último acesso 10.01.2023)
- Rossing P, et al: Executive summary of the KDIGO 2022 Clinical Practice Guideline for Diabetes Management in Chronic Kidney Disease: an update based on rapidly emerging new evidence. Kidney Int 2022; 102(5): 990-999.
- Bhatt DL, et al: N Engl J Med 2021; 384: 117-128.
- Heerspink HJL, et al: N Engl J Med 2020; 383: 1436-1446.
- EMPA-Kidney Collaborative Group: Nephrol Dial Transplant 2022; 37; 1317-1329.
- Bakris G, et al: Clin J Am Soc Nephrol 2020; 15: 1705-1714.
- Chertow GM, et al: J Am Soc Nephrol 2021; 32: 2352-2361.
- Bakris GL, et al: N Engl J Med 2020; 383: 2219-2229.
- Pitt B, et al: N Engl J Med 2021; 385: 2252-2263.
- Rossing P, et al.: FIDELIO-DKD e FIGARO-DKD Investigadores: Diabetes Care. Publicado online, 15 de Agosto (2022), 10.2337/dc22-0294
- Seidu S, et al: 2022 actualização da declaração de posição por Primary Care Diabetes Europe: uma abordagem do estado da doença à gestão farmacológica da diabetes tipo 2 nos cuidados primários. Diabetes de Cuidados Primários 2022; 16(2): 223-244.
- “Chronic Kidney Diseaseassociated Pruritus: From Epidemiology To Treatment”, 25 Nov 2021, www.emjreviews.com,(último acesso 14 Dez 2022).
- Sukul N, et al: Kidney Med 2020; 3(1): 42-53.e1
- Yan B, et al: J Am Heart Assoc 2021; 10(7): e016201.
- “CHMP Meeting Highlights February 2022”, 17/03/2022, www.basg.gv.at, (último acesso 14/12/2022).
- Fishbane S; KALM-1 Trial Investigators: N Engl J Med 2020; 382(3): 222-232.
- Sociedade Americana de Nefrologia: Abstract FR-OR24, www.asn-online.org (último acesso: 14 de Dezembro de 2022).
PRÁTICA DO GP 2023; 18(1): 20-21











