Os procedimentos de ressecção no tratamento do linfedema têm estado em desenvolvimento desde o início do século passado. São invasivos e têm muitas complicações. Com o avanço da microcirurgia, as anastomoses linfovenosas desempenham um papel importante na melhoria da qualidade de vida do paciente.
Os procedimentos de ressecção no tratamento do linfedema são métodos que removem cirurgicamente o excesso de tecido. Vários procedimentos, parcialmente históricos, têm sido descritos para a terapia do linfedema cirúrgico desde o final do século XIX (Tab. 1).
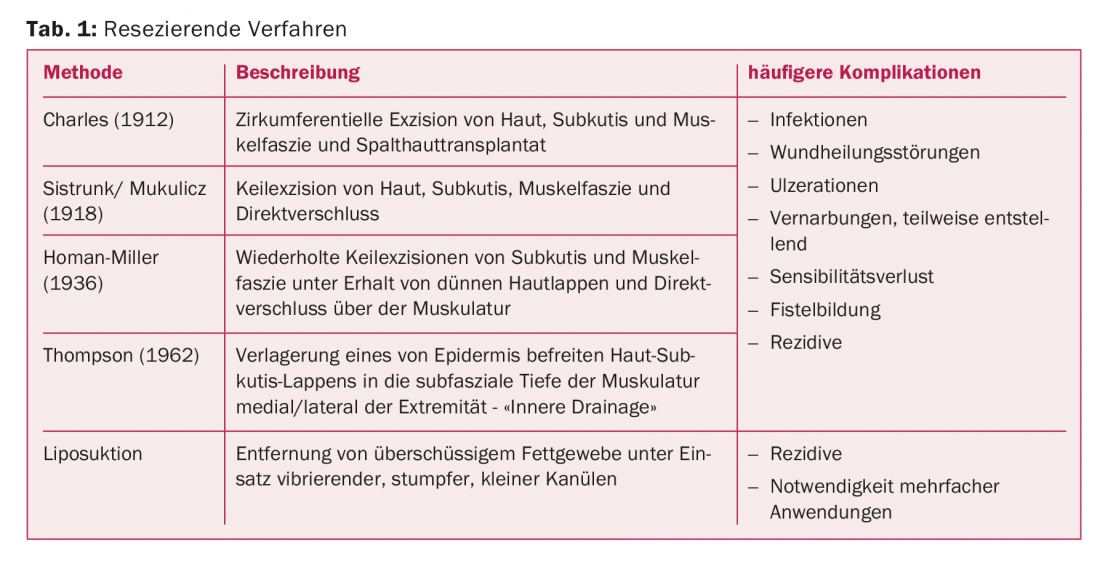
Em 1912, foi desenvolvido o procedimento Charles em que a pele, subcutis e fáscia muscular são excisadas circunferencialmente e cobertas com pele fendida [1]. Segundo Sistrunk, as excisões em cunha da pele, subcutis e fáscias musculares são realizadas com fecho directo, sendo que no procedimento de acordo com Homan a pele foi poupada pela primeira vez e fechada sobre o defeito do tecido ressecado [2]. Este procedimento é repetido até se atingir a circunferência desejada. A ideia de ligar os linfáticos superficiais e profundos foi estabelecida pela primeira vez em 1962, quando Thompson ressecou o tecido subcutâneo e deslocou um retalho subcutâneo de pele fina e profunda para a profundidade subfascial da musculatura. Como resultado, existem não só cicatrizes desfigurantes, mas também fístulas linfáticas frequentes e sinusóides pilonóides [3].
O processo de cura é muitas vezes complicado por infecções e pela formação de cicatrizes instáveis durante os procedimentos de ressecção. Estes métodos devem ser explorados em casos de incapacidade e falha de tratamento na fase final do linfedema e podem aumentar a eficácia das terapias causais, reduzindo a chamada “carga linfática”. Podem ser combinados com métodos reconstrutivos. No edema genital, estes procedimentos são frequentemente considerados mais cedo.
Lipoaspiração
A lipoaspiração é um procedimento especial de ressecção que pode efectivamente reduzir a circunferência do linfedema de membros. A lipoaspiração é a remoção do tecido gordo em excesso por sucção utilizando cânulas vibrantes, rombas e pequenas. A transformação do linfedema em tecido gordo (a chamada transformação gorda) ocorre muito frequentemente no decurso posterior da doença. O cirurgião sueco Hakan Brorson foi pioneiro na utilização da lipoaspiração para linfedema de membros e tem publicado resultados promissores nos últimos anos. Num estudo prospectivo de 56 pacientes com linfedema (29 primários, 27 secundários após terapia do cancro), a circunferência do membro inferior tratado por lipoaspiração era ainda significativamente semelhante ao lado saudável após dez anos [4]. No entanto, as pessoas afectadas continuaram a usar meias de compressão continuamente. Num outro estudo prospectivo de 146 doentes com cancro da mama que tinham desenvolvido linfedema dos membros superiores, o volume em excesso foi efectivamente removido e a circunferência reduzida dos membros foi mantida a longo prazo através do uso consistente de meias de compressão [5]. Um grande estudo de inquérito encontrou um elevado nível de satisfação psicológica e física entre aqueles que recebem tratamento [6].
O risco de danos adicionais dos vasos linfáticos devido à lipoaspiração ainda não foi observado, nem experimentalmente nem clinicamente. Os exames anatómicos após aspiração no sentido longitudinal das extremidades não puderam demonstrar quaisquer danos nos vasos linfáticos epifasciais. Em regra, não são aspirados mais de quatro litros de gordura por procedimento, a fim de evitar problemas circulatórios e turnos de electrólitos. Várias intervenções podem ser necessárias.
Anastomoses linfovenosas (LVA)
Embora o interesse pelo papel do sistema linfático nos processos fisiológicos e patológicos tenha aumentado nos últimos anos, o conhecimento do sistema linfático permanece limitado em comparação com o conhecimento do sistema cardiovascular. Os mecanismos patológicos no linfedema estão agora a ser cada vez mais pesquisados e as possibilidades de tratamento cirúrgico estão em constante expansão. Para restaurar fisiologicamente a drenagem linfática, as anastomoses linfáticas, que permitem a drenagem linfática extra-anatómica, são criadas supramicrosurgicamente. A supercirurgia é uma nova técnica e um maior desenvolvimento da microcirurgia que torna possível preparar e suturar juntos vasos muito pequenos com um diâmetro inferior a 1 mm (0,3-0,8 mm). São especialmente fabricados instrumentos cirúrgicos muito finos e são utilizados microscópios com uma ampliação de até 40x. São utilizados materiais de sutura muito finos, que têm uma espessura de 12-0 de acordo com a classificação USP (< 0,1 mm de espessura de fio). Estas delicadas anastomoses são normalmente inseridas sob anestesia geral para melhor conforto do paciente, mas em princípio também podem ser inseridas sob anestesia local.
Os próprios vasos linfáticos são difíceis de visualizar em geral porque são de pequeno calibre e transportam principalmente fluido linfático claro e quase sem células. A maioria das técnicas de visualização dependem da capacidade natural dos vasos linfáticos para absorver os traçadores injectados no espaço tecidular. O marcador é então transportado e concentrado no recipiente linfático, permitindo várias modalidades de imagem.
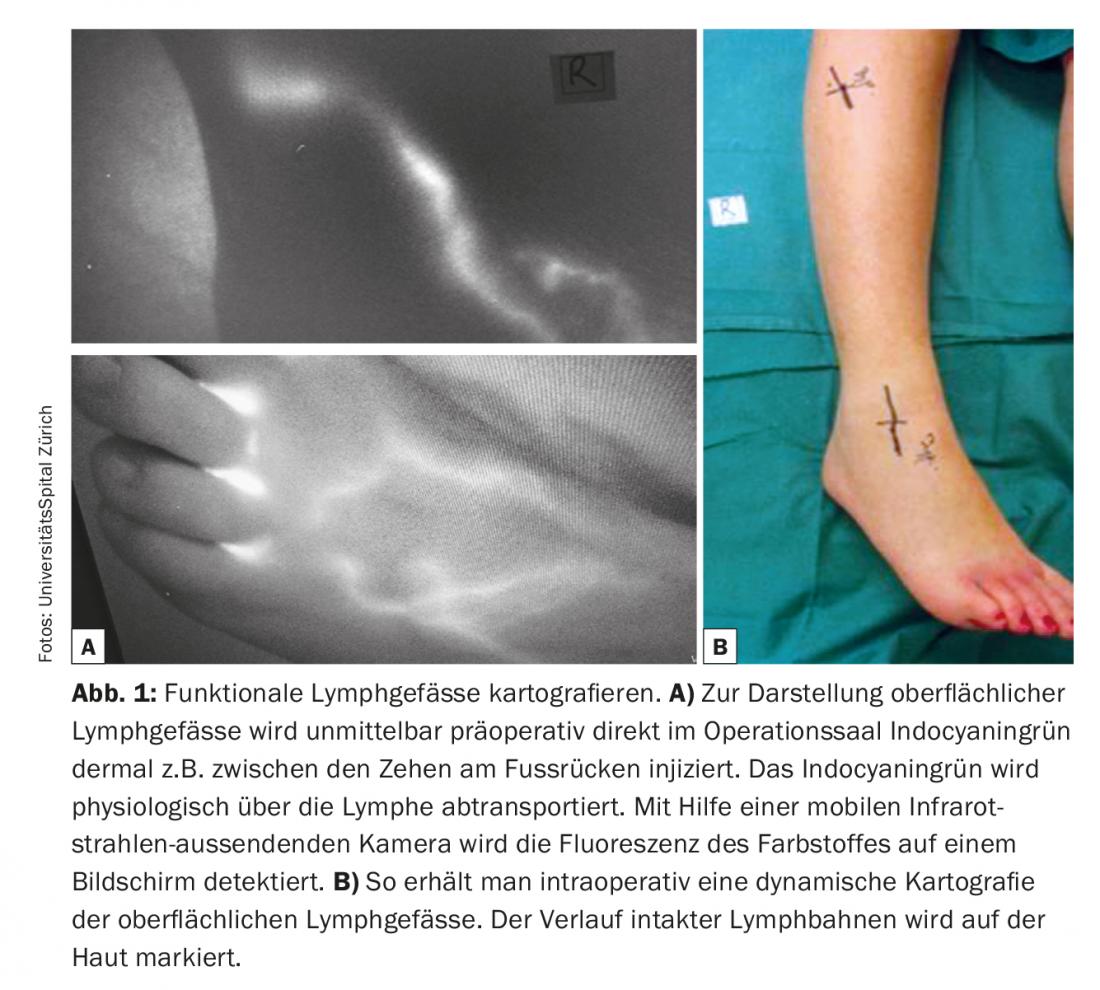
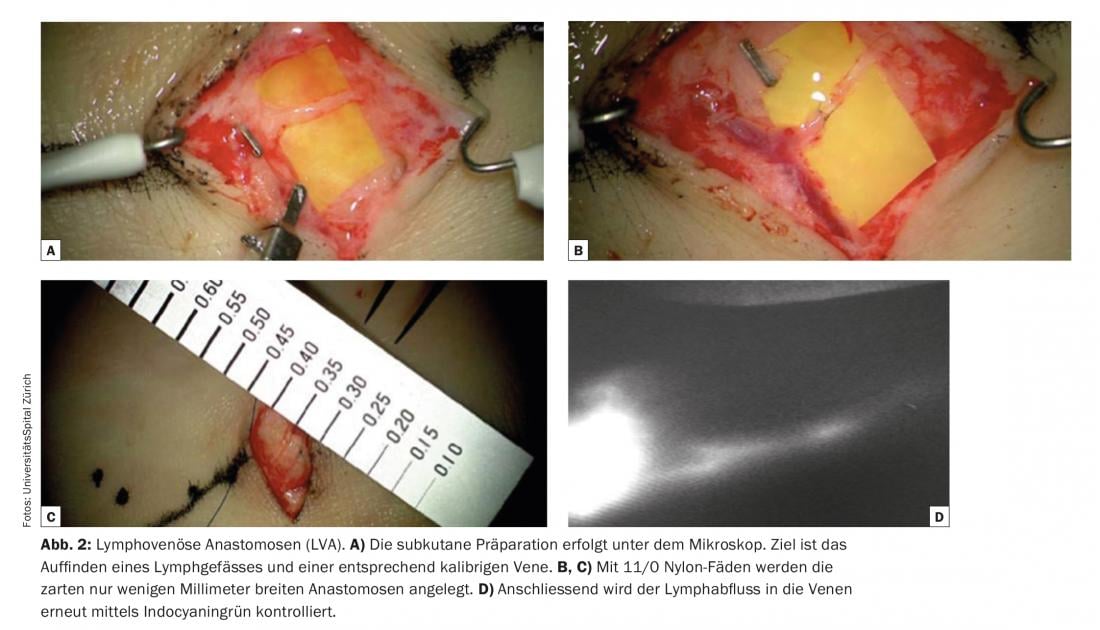
Uma das condições elementares para o sucesso da anastomose linfovenosa é a identificação de vasos linfáticos adequados que não sejam fibróticos mas que tenham uma elevada capacidade de transporte. A linfangiografia verde indocianina (ICG) é actualmente utilizada como uma técnica relativamente simples e rapidamente informativa para a imagiologia de vasos linfáticos. Em vasos linfáticos funcionais – por exemplo, das extremidades – o verde de indocianina é rapidamente absorvido e transportado em canais linfáticos lineares para a virilha ou axila. Muitas vezes até o peristaltismo pode ser observado. A ICG é utilizada como uma navegação viável e rentável pré e intra-operatória. O verde indocianina é injectado dermatologicamente imediatamente antes da operação na sala de operações para visualizar os vasos linfáticos superficiais, por exemplo entre os dedos dos pés no dorso do pé, e o curso dos vasos linfáticos é marcado na pele. (Fig. 1). A preparação subcutânea é realizada sob o microscópio (Fig. 2). O objectivo é encontrar um recipiente linfático e uma veia de calibre correspondente. As anastomoses são criadas com fios de nylon 11/0 ou 12/0. Subsequentemente, a drenagem linfática para a veia é verificada novamente utilizando a ICG. Muitas vezes, os vasos linfáticos adicionais numa determinada área cirúrgica, que não foram visualizados e registados pela ICG pré-operatoriamente, só são detectados intra-operatoriamente. Estes recipientes adicionais são frequentemente maiores e quase mais adequados em diâmetro. A drenagem linfática é parcialmente visível a olho nu. Estes chamados vasos linfáticos ICG-negativos são cada vez mais utilizados para gerar anastomoses adicionais na área cirúrgica e para potenciar a função de drenagem.
Até agora, estas observações clínicas ainda não foram descritas na literatura. Existe uma investigação experimental muito limitada neste campo em geral. As funções diferenciais de transporte entre dois recipientes de recolha foram demonstradas num modelo de ratazana [7]. Pensa-se que existem padrões preferenciais de drenagem linfática para que, para um determinado espaço de tecido, a drenagem linfática seja a principal responsabilidade de um único recipiente, com quaisquer recipientes adicionais na área servindo apenas quando o sistema está sobrecarregado ou como via de transporte de apoio para grandes cargas linfáticas [7]. As diferenças de profundidade e diâmetro dos vasos podem favorecer a drenagem linfática através de um determinado vaso linfático [7]. Os efeitos do verde indocianina na contratilidade linfática normal e na função de drenagem também podem causar artefactos significativos [8].
A identificação das pequenas veias é também problemática nos doentes com linfedema, porque a gordura subcutânea é frequentemente espessada e o tecido fibrótico. Uma veia adequada deve estar presente na proximidade imediata de um recipiente linfático funcional detectado. Os sistemas de visualização sem contacto para identificação pré-operatória de vênulas subcutâneas com um diâmetro de cerca de 0,5-1,0 mm são descritos na literatura como promissores [9].
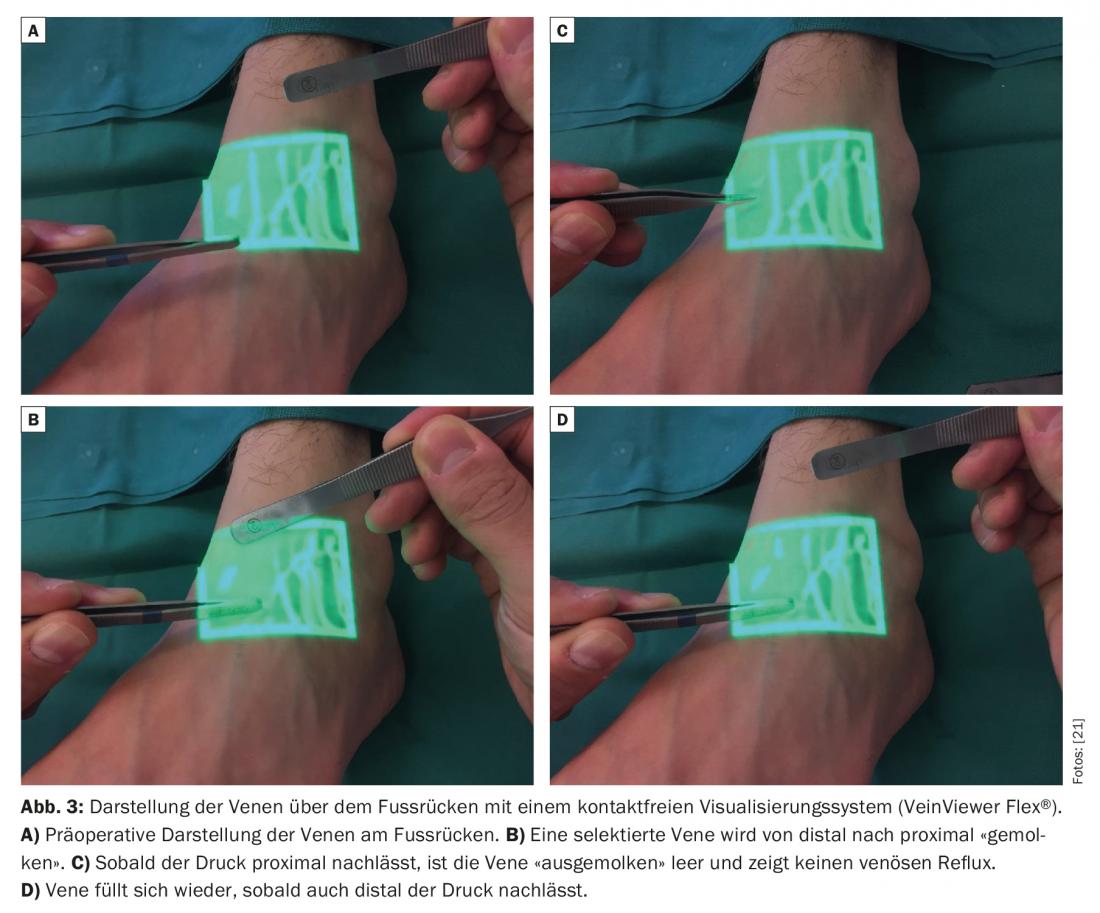
A pressão venosa é normalmente mais elevada do que no sistema linfático [10,11]. Por conseguinte, a ausência de refluxo venoso é também de importância elementar. Se a veia tiver um sistema de válvulas inadequado ou um curso desfavorável, pode ocorrer refluxo venoso para o vaso linfático. Assim, a trombose e fibrose das anastomoses pode limitar significativamente a longevidade das anastomoses [12]. Assim, os sistemas de visualização padrão sem contacto são cada vez mais utilizados para obter um mapeamento venoso rápido e para identificar bifurcações ocultas, bem como válvulas localizadas de forma desfavorável nas veias que podem potencialmente ter uma influência negativa na qualidade das anastomoses linfovenosas criadas (Fig.3). Após a cirurgia, é usado um ligeiro penso de compressão para não pôr em perigo as anastomoses delicadas recentemente aplicadas. Os doentes permanecem hospitalizados durante uma noite. As lesões cutâneas em sobreviventes de cancro da mama com linfedema do membro superior poderiam assim ser reduzidas [13]. Muitos estudos clínicos referem uma redução na circunferência de 35% a 50% em doentes com cancro da mama com linfedema do braço um ano após a colocação destas anastomoses [14–16]. A discrepância nestes resultados deve-se muito provavelmente aos resultados retrospectivos com apenas um pequeno número de casos. Num estudo prospectivo mais amplo com 100 casos, os investigadores determinaram mais recentemente uma redução da circunferência até 38% após três anos e mostraram que também houve um alívio significativo dos sintomas subjectivamente [17]. A dor associada à linfedema-associada foi aliviada [18]. Num outro estudo clínico com 49 pacientes que sofrem de linfedema secundário das extremidades inferiores, verificou-se que a combinação de anastomoses linfovenosas com lipoaspiração também pode reduzir significativamente a textura da pele, bem como a circunferência [19]. Globalmente, postula-se que a eficácia do ALA é aumentada nas fases iniciais (Fig. 4) . Existem relatos de casos e revisões na literatura que mostram que a ocorrência de linfedema após a linfadenectomia pode ser significativamente reduzida pela colocação profiláctica de anastomoses linfovenosas [20].
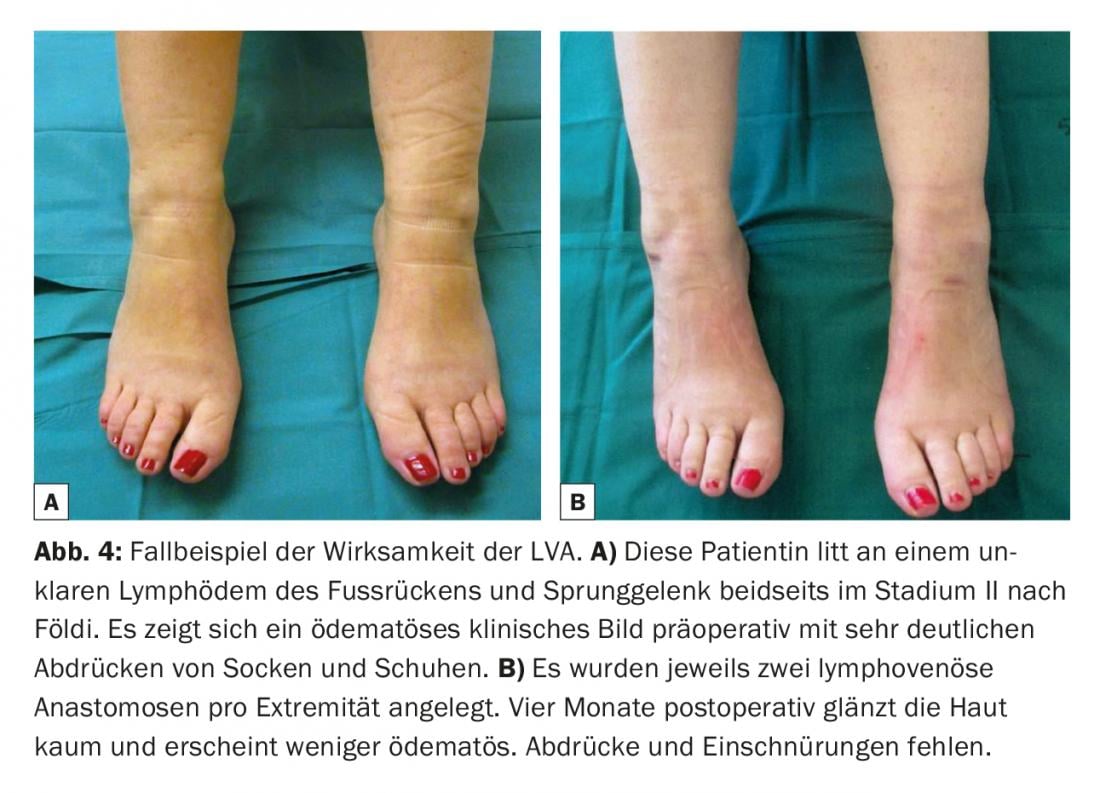
Em resumo, os procedimentos de ressecção são invasivos e repletos de complicações e só são considerados nas fases finais da doença. A lipoaspiração é um procedimento especial de ressecção porque é menos invasivo e tem produzido excelentes resultados em muitos estudos clínicos. Os procedimentos de ressecção podem ser combinados com a criação de anastomoses linfovenosas em certos casos. A criação de anastomoses linfovenosas é um procedimento cirúrgico seguro até à data e tem mostrado resultados de melhoria da qualidade da pele e de redução da circunferência nos estudos clínicos e experimentais disponíveis até à data, embora os resultados a longo prazo ainda estejam pendentes. Em suma, são necessários mais estudos experimentais e estudos clínico-prospectivos a longo prazo com números de doentes mais elevados no futuro, a fim de se poder provar melhor a evidência desta terapia e optimizar continuamente o procedimento do ponto de vista técnico.
As anastomoses linfovenosas são reconhecidas internacionalmente como parte integrante da terapia do linfedema cirúrgico.
Mensagens Take-Home
- Os procedimentos de ressecção são invasivos e repletos de complicações. Só são considerados nas fases finais da doença.
- A criação de anastomoses linfovenosas é um procedimento cirúrgico seguro até à data e tem mostrado resultados de melhoria da qualidade da pele e de redução da circunferência nos estudos clínicos e experimentais disponíveis.
- As anastomoses linfovenosas são reconhecidas internacionalmente como parte integrante da terapia do linfedema cirúrgico.
Literatura:
- Charles H: Elefantíase da perna. In: Latham A, English TC, editores. Um sistema de tratamento. Vol. Londres: Churchill 1912: 516.
- Sistrunk WE: Contribuição para a cirurgia plástica: remoção de cicatrizes por fases; uma operação aberta para laceração extensa do esfíncter anal; a operação de Kondoleon para elefantíase. Ann surgery 1927; 85: 185-193.
- Thompson N: Operação de retalho dérmico enterrado para linfedema crónico da extremidade. Plast Reconstruir Surg 1970; 45: 541-548.
- Brorson H: A lipoaspiração normaliza o linfedema induzido pela hipertrofia do tecido adiposo em elefantíase da perna. Plast Reconstr Surg 2015; 136 (4): 133-134.
- Brorson H: Redução completa do linfedema do braço após o cancro da mama – Um estudo prospectivo de vinte e um anos. Plast Reconstruir Surg 2015; 136 (4): 134-135.
- Hoffner M, et al: SF-36 mostra o aumento da qualidade de vida após a redução completa do linfedema pós-mastectomia com lipoaspiração. Lymphat Res Biol 2017; 15 (1): 87-98.
- Gashev AA et al: Indocyanine Green and Lymphatic Imaging: Current Problems. Investigação Linfática e Biologia. 2010; 8 (2): 127-130.
- Weiler M, Dixon JB: função diferencial de transporte dos vasos linfáticos no modelo de cauda de rato e os efeitos a longo prazo da Indocianina Verde, avaliados com imagens quase infravermelhas. Fronteiras em Fisiologia. 2013; 4: 215.
- Makoto M, et al: Linfedema dos membros inferiores tratado com anastomose linfáticaovenosa baseada em linfografia icg pré- e intra-operatória e visualização de veias sem contacto: um relato de caso. Microcirurgia 2012; 32: 227-230.
- Wardhan R, Shelley K: Forma de onda de pressão venosa periférica. Curr Opinião Anaesthesiol 2009; 22: 814-821
- Munn LL: Mecanobiologia das contracções linfáticas. Semin Cell Dev Biol 2015; 38: 67-74.
- Yamamoto T, Koshima I: Neo-valvuloplastia para a supercirurgia linfática. JPlast Reconstruir Aesthet Surg 2014; 67: 587-588.
- Jeremy ST, et al: Lymphaticovenous bypass diminui as alterações patológicas da pele no câncer de mama das extremidades superiores rel. Linfedema. Res Biol Linfático. 2015; 13: 46-53.
- Koshima I, et al: Anastomose linfatovenular supra-cirúrgica para o tratamento do linfedema nas extremidades superiores. J Reconstruir Microsurg 2000; 16: 437-442
- Furukawa H, et al: Implantação linfática microcirúrgica com vista ao refluxo linfático dérmico usando linfografia de fluorescência verde indocina no tratamento do linfedema pós-mastectomia. Plast Reconstruir Surg 2011; 127: 1804-1811.
- Chang DW: bypass linfovenular para a gestão do linfedema em doentes com cancro da mama: Um estudo prospectivo. Plast Reconstruir Surg 2010; 126: 752-758.
- Chang DW, et al: Uma análise prospectove de 100 casos consecutivos de bypass linfovenoso para tratamento de linfedema da extremidade. Plastic Reconst Surg 2013; 132: 1305-1314.
- Mihara M, et al: A anastomose linfática tecidular liberta a extremidade inferior da dor associada à linfedema. Plast Reconst Surg Global Open. 2017; 5 (1): e1205.
- Chang K1, et al: Lipoaspiração combinada com anastomose linfático-venosa para tratamento de linfedema secundário dos membros inferiores: um relatório de 49 casos. Zhonghua Wai Ke Za Zhi 2017; 55 (4): 274-278.
- Jorgensen MG, et al: O efeito da anastomose linfovenosa profiláctica e shunts para prevenir o linfedema relacionado com o cancro: uma revisão sistemática e uma meta-análise. Microsurg 2017; 00: 1-10.
- Scaglioni M, et al: Optimização dos resultados da anastomose linfática-venosa (ALAV) através da identificação pré-operatória da veia livre de refluxo: Escolher sabiamente a veia. Manuscrito submetido à Microcirurgia, 2017.
CARDIOVASC 2017; 16(5): 11-15











