No congresso da DGHO em Viena, vários aspectos foram abordados na prática clínica no cancro do pulmão não de pequenas células (NSCLC), cancro de células renais (RCC) e leucemia mielóide crónica. Em particular, foi discutida a situação actual da investigação sobre os novos inibidores da tirosina quinase crizotinibe, sunitinibe e bosutinibe.
O cancro do pulmão de células não pequenas (NSCLC) corre normalmente assintomático durante um longo período de tempo. Mais de metade dos pacientes já se encontram numa fase avançada quando são diagnosticados pela primeira vez.
“A terapia com medicamentos para NSCLC metastáticos não é actualmente muito eficaz, os citostáticos clássicos têm-se esgotado. O tempo de sobrevivência em estudos actuais sem biologia é de 10-12 meses”, diz o Prof. Norbert Frickhofen, Wiesbaden, Alemanha. “No entanto, a genética é bem compreendida. O ALK translocado é um potente oncogene e um factor chave na carcinogénese numa proporção de pacientes com NSCLC. Normalmente ocorre com o parceiro de fusão EML4, mas há também parceiros mais raros como o KIF5B e a TFG. No NSCLC com um gene de fusão ALK, a inibição direccionada é, portanto, uma boa opção terapêutica porque a fusão descrita resulta na activação constitutiva da cinase ALK”.

Crizotinibe causa tal inibição da tirosina cinase ALK. É uma aminopiridina oral que também bloqueia MET e ROS1. É aprovado na Suíça como Xalkori®. A FDA aprovou-o em 2011 para ALK-positivo localmente avançado ou metastásico (avaliado por um teste aprovado pela FDA) NSCLC. A EMA aprovou-a em 2012 como terapia para NSCLC pré-tratamento local avançado ou metastático ALK-positivo.
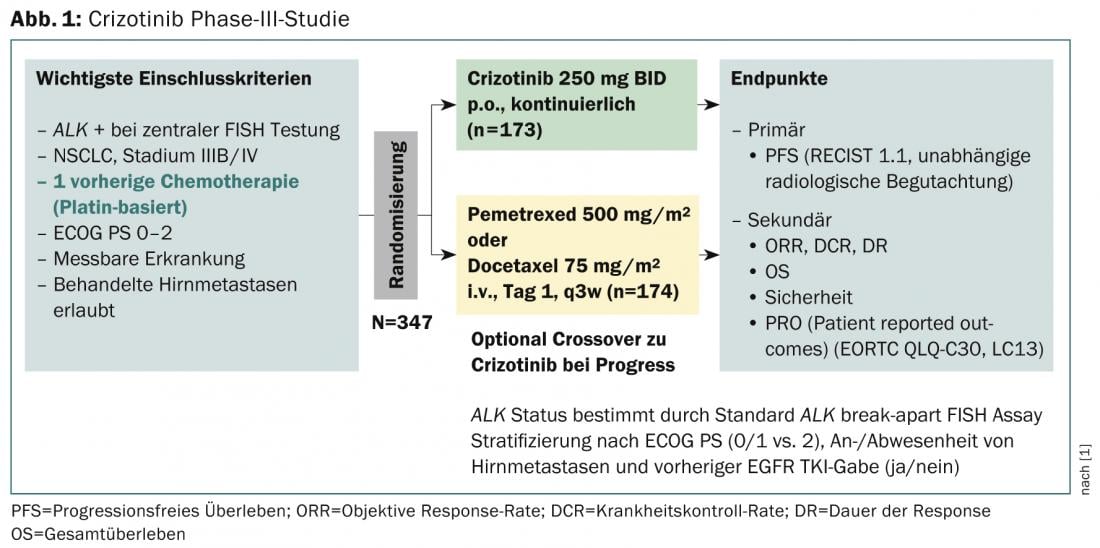
Um estudo da fase III com o ponto final primário de sobrevivência sem progressão (RECIST 1.1, avaliação radiológica independente) investigou a eficácia após a pré-terapia (Fig. 1) [1]. Conclui que o crizotinibe é superior à quimioterapia padrão em pacientes com ALK-positivo NSCLC previamente tratado. A média de sobrevivência sem progressão foi de 7,7 meses no crizotinibe (n=173) e três meses no grupo de quimioterapia (n=174), os resultados são estatisticamente significativos (p<0,001). As taxas de resposta foram também significativamente mais elevadas com o crizotinibe (65 vs. 20%, p<0,001) e o tempo médio de resposta foi mais rápido (6,3 vs. 12,6 semanas). No entanto, uma análise provisória não mostrou qualquer melhoria significativa na sobrevivência global. Os efeitos secundários mais comuns foram perturbações visuais, efeitos secundários gastrointestinais e aumento dos níveis de aminotransferase hepática. Em geral, os pacientes que tomavam crizotinibe versus quimioterapia notaram uma maior redução dos sintomas do cancro do pulmão e uma maior melhoria da qualidade de vida em geral.
Crizotinib na prática
Na prática, a questão é: Quem deve ser testado para a ALK? “A resposta é: cada paciente para quem a inibição de ALK é uma opção terapêutica. O diagnóstico ALK prossegue através do rastreio IHC e do rastreio FISH. Relativamente aos efeitos secundários, perturbações visuais tais como traçadores no campo visual periférico na fronteira da luz, objectos que ficam presos, flashes de luz sem referência ou inversão de contraste são funcionais e não críticos. O efeito secundário mais crítico é a hepatotoxicidade, atingindo grau 3/4 em 16%, o que pode resultar em morte e, portanto, precisa de ser cuidadosamente controlado e tratado rapidamente. Se houver um aumento de alanina-aminotransferase (ALT) ou aspartato aminotransferase (AST) grau 3 ou 4 e bilirrubina total ≤grade 1, recomenda-se a descontinuação até à recuperação para ≤grade 1 ou linha de base, depois reiniciar com 2×200 mg/d. Se a bilirrubina total também subir para o grau 2, 3 ou 4 (na ausência de colestase ou hemólise), é necessária a interrupção da terapia”, diz o Prof. “Globalmente, a terapia específica com crizotinib é eficaz e tolerável no NSCLC ALK-positivo”.
Opções para mRCC
“As possibilidades de uma terapia para o carcinoma de células renais metastasisadas devem ser esgotadas de forma óptima. Em termos concretos, isto significa um tratamento consistente com uma substância durante o máximo de tempo possível e a obtenção da melhor remissão possível. Além disso, a segunda linha já deve ser considerada na primeira linha terapêutica. A gestão dos efeitos secundários deve ser optimizada e a educação e envolvimento do paciente e dos co-terapeutas (clínicos gerais) deve ser promovida”, diz o PD Dr. Jochen Casper, Oldenburg.
Para a primeira linha, sunitinibe, bevacizumab mais IFN, e pazopanibe podem ser considerados se houver uma histologia celular clara e um prognóstico bom/intermediário. Embora não num estudo comparativo frente a frente, o Dr Casper mostrou que os três factores de sobrevivência global e sem progressão, bem como a resposta, tendem a ser melhores com o sunitinib (Sutent®) do que com as outras opções de tratamento, com base em vários ensaios aleatórios de fase III em cenários de baixo e médio risco. Uma análise retrospectiva [2] do sunitinib também conclui que a resposta está correlacionada com a sobrevivência global. Foi significativamente mais elevado nos respondentes, com uma longa sobrevivência global mesmo em respondentes tardios.
“Não só a retracção tumoral está relacionada com a sobrevivência global, tanto na primeira como na segunda linha, mas a resposta e a extensão da resposta também são relevantes para isto. Tanto quanto foi estudado, este efeito é independente da terapia utilizada (inibidor da tirosina cinase [TKI], mTOR, citocina). A inclusão da terapia de primeira linha ou a sequência certa na escolha do tratamento de segunda linha pode ter um impacto significativo na sobrevivência global. São necessários mais estudos nesta área. Mas o objectivo deve ser sempre a sobrevivência global, e isto tem melhorado significativamente desde a introdução das TKIs”, conclui o Dr. Casper.
Optimizar a terapia TKI também em CML
O PD Dr. med. Philipp le Coutre, Berlim, falou sobre a leucemia mielóide crónica (CML). Um novo inibidor da tirosina quinase aprovado pela FDA em 2012 para o tratamento de CML é chamado bosutinibe. É utilizado em doentes para os quais outros TKIs não trabalham ou são mal tolerados. Na Europa, a substância activa foi aprovada condicionalmente pela Comissão Europeia em 2013 como um medicamento para o tratamento de uma doença órfã (ainda não aprovada na Suíça).
“Esta nova opção terapêutica poderia oferecer uma alternativa potencial em casos de resposta e resistência inadequadas, comorbilidades específicas dos pacientes ou factores de risco, e intolerância de terapias anteriores”, concluiu a apresentação do Dr. le Coutre.
Fonte: “Evidence and clinical practice in NSCLC, RCC and CML”, simpósio satélite da Pfizer Pharma GmbH no Congresso da DGHO, 18-22 de Outubro de 2013, Viena.
Literatura:
- Shaw AT, et al: Crizotinib versus quimioterapia no cancro do pulmão avançado ALK-positivo. N Engl J Med 2013; 368: 2385-2394.
- Molina AM, et al: Sunitinib resposta objectiva no carcinoma metastático de células renais: análise de 1059 doentes tratados em ensaios clínicos. Eur J Cancer 2013 Set 16. pii: S0959-8049(13)00789-2. doi: 10.1016/j.ejca.2013.08.021. [Epub ahead of print].
InFo Oncologia & Hematologia 2014; 2(2): 36-38