A insuficiência cardíaca aguda é uma situação de risco de vida que requer uma acção rápida e planeada. Como se realiza o esclarecimento? Que medidas terapêuticas estão disponíveis? Um olhar sobre a estabilização inicial no hospital.
A insuficiência cardíaca aguda (IAH) é definida como um início rápido ou agravamento dos sintomas (frequentemente dispneia e ortopneia) e/ou clínicos
Sinais de insuficiência cardíaca (esp. congestionamento). Trata-se de uma situação médica com risco de vida que requer avaliação e tratamento urgentes e muitas vezes hospitalização [1].
Cerca de 80% dos doentes com IHA têm insuficiência cardíaca crónica pré-existente. Mais de 50% têm insuficiência cardíaca com fração de ejeção ventricular esquerda preservada (HFpEF) [2]. Em mais de metade dos pacientes, é possível identificar um gatilho. A doença arterial coronária e a fibrilação atrial são as condições cardíacas subjacentes mais comuns, e a diabetes é uma comorbidade muito comum. A maioria dos pacientes são hiper ou normotensos na admissão. Apenas cerca de 5-7% de todo o IAH são hipotensos (tensão arterial sistólica <90 mmHg), o que está associado a um prognóstico desfavorável. Isto é especialmente verdade se a hipoperfusão estiver presente ao mesmo tempo (periferia fria) [3].
Diagnóstico e avaliação prognóstica inicial
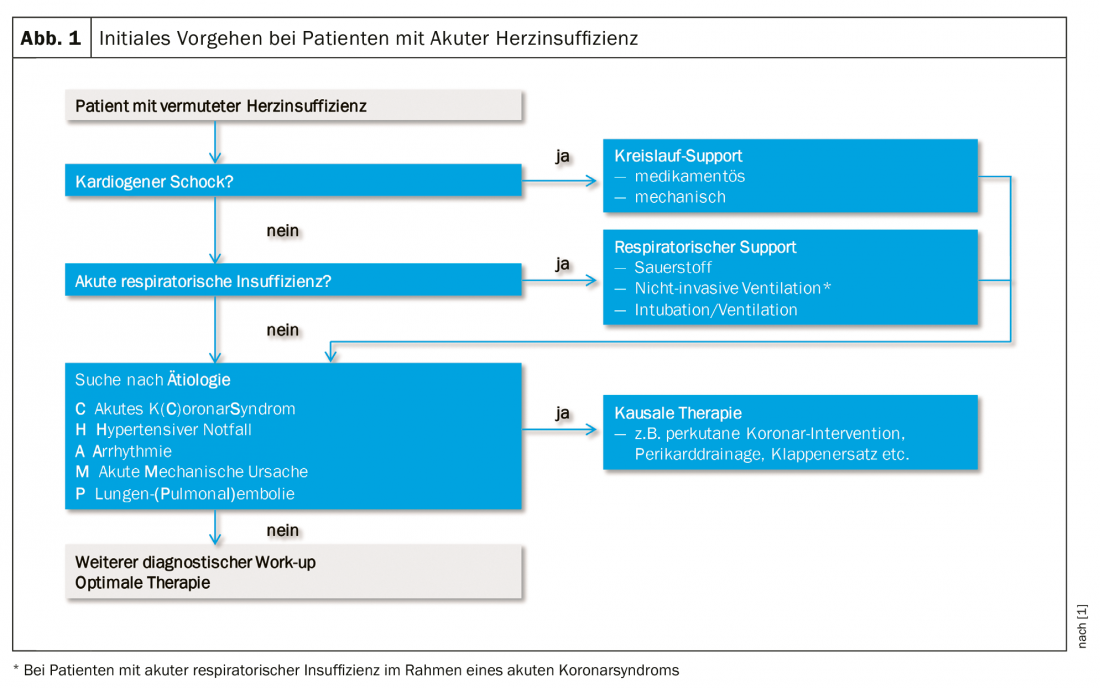
O trabalho de diagnóstico deve ser iniciado o mais cedo possível (idealmente na fase pré-hospitalar, especialmente ECG) para que a terapia causal possa ser iniciada mais cedo. O benefício do diagnóstico precoce e da terapia é bem estabelecido para o IAH no contexto da síndrome coronária aguda. Na gestão do AHI, o diagnóstico e a terapia andam de mãos dadas, procurando sistematicamente condições e mecanismos que põem a vida em risco e tratando-os o mais rapidamente possível (Fig. 1). Parte do trabalho imediato é também a procura de causas alternativas de dispneia aguda, principalmente pneumonia, anemia grave e insuficiência renal aguda. Para além da avaliação clínica do perfil hemodinâmico, o diagnóstico inicial de suspeita de IHA inclui os seguintes componentes de diagnóstico:
BNP ou NT-proBNP: Um AHI pode ser excluído nos valores <100 ng/l ou <300 ng/l. Os valores elevados são proporcionais à extensão do stress do miocárdio. Quanto mais altos forem os peptídeos natriuréticos, menos favorável será o prognóstico.
ECG de 12 derivações: Valores normais de ECG tornam improvável um AHI. O ECG também pode fornecer pistas sobre o mecanismo da insuficiência cardíaca (enfarte agudo, bradicardia, taquicardia).
Raio-X ao tórax: Isto mostrará se há congestão venosa pulmonar, derrames pleurais, edema intersticial ou alveolar ou cardiomegalia. Também é utilizado para procurar causas não cardíacas de dispneia aguda, como pneumonia ou pneumotórax.
Vários parâmetros laboratoriais: Marcadores como a hemoglobina, TSH, CRP, creatinina e transaminases podem ser utilizados para investigar mecanismos e co-factores, bem como os efeitos do AHI. A troponina cardíaca é também um parâmetro, mas deve ser considerada como um marcador quantitativo não específico de danos miocárdicos e nem sempre indicativo de enfarte agudo.
Ecocardiografia: Deve ser realizada em 24 a 48 horas em todos os pacientes com IHA se a patologia cardíaca for desconhecida ou insuficientemente conhecida. Os pacientes em choque cardiogénico, por outro lado, requerem ecocardiografia imediata, entre outras coisas no que diz respeito a problemas mecânicos que requerem tratamento agudo, tais como complicação de enfarte mecânico e insuficiência valvar grave aguda.
Perfil hemodinâmico como ponto de partida
Se a terapia causal for possível (especialmente na síndrome coronária aguda, emergência hipertensiva, taquicardia ou bradicardia, embolia pulmonar aguda e complicações mecânicas de enfarte), isto deve ser realizado o mais cedo possível. Caso contrário, a terapia de apoio geral é iniciada de acordo com o perfil clínico e hemodinâmico [1,4]. Estas medidas de apoio são estabelecidas com base na experiência clínica, mas não têm efeito comprovado no prognóstico [5]. Ainda não há nenhum medicamento cuja administração na fase aguda reduza a mortalidade a curto ou longo prazo. O objectivo destas medidas é uma rápida melhoria dos sintomas e estabilização clínica, para que a terapia da insuficiência cardíaca crónica possa ser estabelecida. As formas de tratamento para o AHI podem ser divididas em medidas agudas, medidas durante a hospitalização e medidas antes da alta. Este artigo centra-se no diagnóstico e nas medidas iniciais de estabilização durante a hospitalização. Dependendo da gravidade, o tratamento inicial tem lugar na ala de emergência/ ala normal ou na ala de emergência/unidade de cuidados intensivos, se necessário com monitorização invasiva.
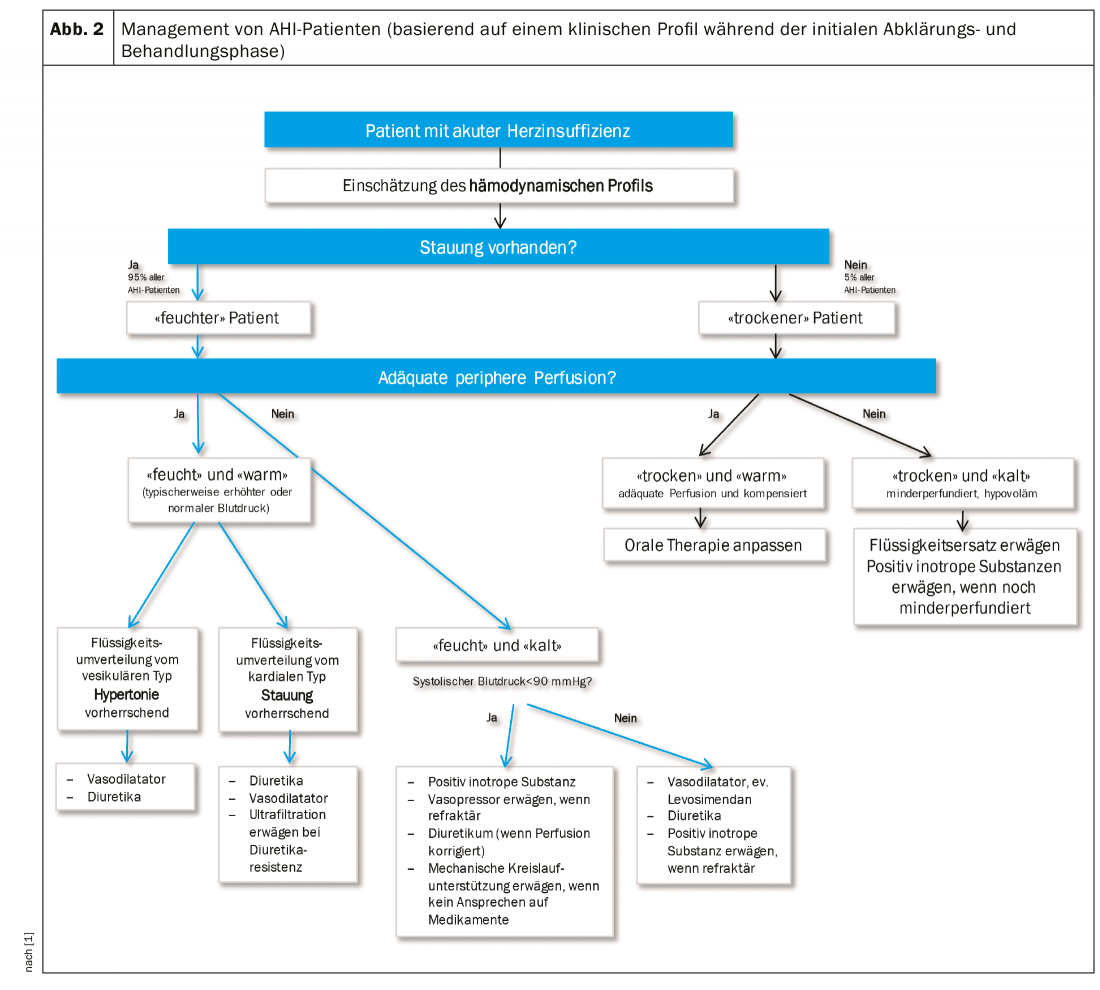
Com base no estado de hidratação (“húmido” ou “seco”) e perfusão dos tecidos (“quente” ou “frio”, frequentemente sinónimo de normotónico vs. hipotónico), podem distinguir-se quatro perfis hemodinâmicos, que determinam a direcção aproximada da terapia (Fig.2).
Medidas gerais
A administração de oxigénio deve ser limitada aos doentes com hipoxemia (SpO2 <90%). A ventilação não-invasiva (CPAP/BiPAP) deve ser considerada em casos de dispneia pronunciada ou hipoxemia (frequência respiratória >25/min, SpO2 <90%) e iniciada o mais cedo possível para evitar a entubação. Se for necessária intubação ou electrocardioversão, a sedação com propofol deve ser utilizada com precaução (risco de hipotensão, cardiodepressão). A sedação com midazolam é menos problemática, uma vez que são de esperar menos efeitos secundários cardíacos.
Terapia com medicamentos
No caso de um agravamento agudo da insuficiência cardíaca crónica pré-existente, o tratamento medicamentoso pré-existente com inibidores da ECA, bloqueadores dos receptores de angiotensina ou sacubitril-valsartan, bloqueadores beta e bloqueadores dos receptores de mineralocorticóides deve ser geralmente continuado. Em caso de hipotensão (tensão arterial sistólica<85 mmHg), deve ser efectuada uma redução da dose ou uma pausa temporária da terapia de insuficiência cardíaca oral. A seguinte visão geral da terapia para insuficiência cardíaca medicinal pretende ser um esquema que deve ser adaptado à situação individual do doente com insuficiência cardíaca.
Nitratos/vasodilatadores: Todos os vasodilatadores têm um duplo efeito na redução do tom venoso (pré-carga do coração) e arterial (redução de pós-carga). Os vasodilatadores estão contra-indicados a uma tensão arterial sistólica <90 mmHg. O uso muito cauteloso é também indicado em casos de estenose mitral e da válvula aórtica significativa. A administração contínua de nitratos pode levar ao desenvolvimento da tolerância.
A administração peroral de nitroglicerina é feita inicialmente em duas doses de nitroglicerina a 0,4 mg ou uma cápsula a 0,8 mg. As repetições após 5-10 minutos são permitidas, enquanto se controla a tensão arterial. No curso, é possível uma alteração à aplicação transdérmica (5-10 mg).
Os vasodilatadores intravenosos (nitroglicerina, dinitrato de isosorbida, nitroprussiato ou nesiritideo) são muito eficazes na redução da dispneia sob monitorização em unidades de cuidados intermédios ou de cuidados intensivos, embora não haja provas científicas até à data [6].
Diuréticos: Nas directrizes actuais, o diurético é o principal medicamento para o tratamento do AHI [7]. Contudo, isto só se aplica a doentes com sobrecarga de volume, principalmente o doente “húmido quente” e o “frio húmido” se a tensão arterial sistólica for >90 mmHg. Se for principalmente um descarrilamento hipertensivo que tenha levado à descompensação cardíaca esquerda, o diurético deve ser descontinuado a favor do nitrato, se possível.
A abordagem inicial para tratar a sobrecarga de volume é uma combinação de diuréticos e vasodilatadores se a pressão sanguínea permitir (>90 mmHg). É necessária uma estreita monitorização do estado de hidratação através da verificação clínica (ou seja, enchimento da veia jugular, congestão pulmonar, edema periférico, peso corporal) e laboratorial (soro de potássio e creatinina) [6]. A caixa resume as linhas de direcção das doses.

Inotrópicos/vasopressores: Drogas com vasoconstrição periférica pronunciada, tais como norepinefrina ou dopamina em doses mais elevadas (>5 µg) podem ser consideradas para utilização a curto prazo na situação aguda se a perfusão dos tecidos for insuficiente, apesar do estado de enchimento adequado de modo a fornecer órgãos vitais. No entanto, isto vem ao preço de um aumento da pós-carga e de um aumento do risco de arritmia. Como alternativa, o levosimendan pode ser utilizado para valores de tensão arterial sistólica >85 mmHg. Detalhes relativos à dosagem podem ser encontrados na directriz europeia sobre o AHI [1].
Beta-bloqueador/Digoxina: No caso de um agravamento agudo da insuficiência cardíaca crónica pré-existente com terapia de beta-bloqueador estabelecida, o beta-bloqueador não deve ser completamente descontinuado sempre que possível, mas a dose deve ser temporariamente reduzida. Para o tratamento da insuficiência cardíaca aguda, a nova utilização de um beta-bloqueador só é indicada em casos excepcionais, por exemplo, no caso de obstrução dinâmica intraventricular. A administração de um beta-bloqueador para controlar a frequência cardíaca (especialmente por via intravenosa) sem conhecimento da função do VE pode causar choque cardiogénico. No entanto, na fibrilação atrial taquicárdica e na função sistólica preservada do VE, conforme determinado pela ecocardiografia, o beta-bloqueador pode ser administrado para controlo da taxa. A digoxina é também uma opção para o controlo da taxa de fibrilação atrial, mesmo com LVEF deficiente.
Profilaxia do tromboembolismo, anticoagulação, inibição da agregação plaquetária: A profilaxia do tromboembolismo, principalmente com uma heparina de baixo peso molecular, é claramente recomendada para a redução do risco de trombose/embolia pulmonar. Para fibrilação/flutuação atrial e síndrome coronária aguda, aplicam-se as directrizes existentes para anticoagulação e terapia antitrombótica.
Antiarrítmicos/cardioversão: Para além da cardioversão eléctrica, podem ser utilizados antiarrítmicos como amiodarona, digoxina e (se se souber que a função LV é preservada) beta-bloqueadores em casos de AHI predominantemente relacionado com taquicardia. Se a FA taquicárdica for mal tolerada hemodinamicamente, pode necessitar de conversão imediata (electroconversão). Em alternativa, com vista a uma electroconversão bem sucedida com um efeito duradouro de um a três dias, a saturação com amiodaronas pode ser realizada. Os antiarrítmicos da classe IB/C estão contra-indicados na disfunção do LV [8,11].
Opiáceos, ansiolíticos e sedativos: os opiáceos podem ser considerados para uso cauteloso em doentes ansiosos com agitação severa e dispneia. No entanto, uma possível hipopneia deve ser detectada precocemente através de uma monitorização adequada. O uso prudente de benzodiazepinas (diazepam, lorazepam) é uma alternativa aos opiáceos em doentes agitados.
Outras opções terapêuticas
Procedimentos de substituição renal: O envolvimento precoce de nefrologistas é importante em pacientes com piora da função renal no IAH. O uso interdisciplinar da terapia de substituição renal é limitado aos doentes com IAH “quentes e húmidos” que não respondem ou respondem inadequadamente à terapia diurética. Os seguintes critérios são mencionados nas actuais directrizes europeias: Oligúria sem resposta adequada a doses mais elevadas de diuréticos, soro de potássio >6,5 mmol/l, ureia sérica >25 mmol/l, creatinina sérica >300 µmol/l e pH <7,2 [1].
Opções de terapia mecânica: A abordagem depende da situação clínica e da causa postulada do AHI. No caso de isquemia grave com choque cardiogénico, o vaso responsável pela isquemia aguda é tratado principalmente através de intervenção coronária percutânea. Resultados recentes mostram que o tratamento imediato de todos os vasos coronários não melhora o resultado [9]. A utilização de dispositivos de apoio circulatório (bomba de balão intra-aórtica, dispositivos de assistência ventricular) deve ser discutida e determinada na equipa cardíaca com o envolvimento dos médicos de urgência e de cuidados intensivos.
A indicação convencional para bomba de balão intra-aórtica (IABP) é anterior à correcção cirúrgica de problemas mecânicos agudos específicos (em regurgitação mitral aguda grave, possivelmente em ruptura do septo ventricular) e em NSTEMI com doença grave de 3 vasos, tendo em vista a cirurgia cardíaca urgente. Para outras causas de choque cardiogénico, não há boas provas científicas para o benefício do IABP. Os dispositivos de assistência ventricular e outras formas de apoio mecânico são utilizados ou como ponte para a decisão ou, em pacientes seleccionados, a longo prazo [1]. Para determinar o momento adequado da cirurgia cardíaca para endocardite, a opinião interdisciplinar de toda a equipa cardíaca ou endocardite deve ser procurada precocemente. A inserção aguda de VA-ECMO em pacientes em choque cardiogénico, esp. após ressuscitação com um tempo relativamente curto “sem fluxo”, também deve ser discutido cedo e de forma interdisciplinar com o envolvimento de médicos de emergência e de cuidados intensivos.
Punção pleural e ascítica: A punção pleural pode levar a uma rápida diminuição da dispneia. A punção das ascite pode, através de uma diminuição da pressão intra-abdominal, contribuir para uma melhoria da pressão transrenal e indirectamente para uma melhoria da função renal [10].
Mensagens Take-Home
- A insuficiência cardíaca aguda é a primeira manifestação de doença cardíaca em cerca de 20% dos casos. É geralmente uma expressão de um agravamento agudo da insuficiência cardíaca crónica.
- É uma situação de risco de vida que requer uma acção rápida e estruturada.
- As medidas terapêuticas são baseadas no perfil hemodinâmico, avaliando a perfusão (“quente” vs. “frio”) por um lado e o congestionamento (“húmido” vs. “seco”) por outro.
- Em doentes com dispneia aguda e suspeita de insuficiência cardíaca aguda, a medição de peptídeos natriuréticos ajuda no diagnóstico diferencial. Também fornece informação prognóstica (recomendação de classe IA).
Literatura:
- Ponikowski P, Voors AA, Anker S, et al: 2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. Eur Heart J 2016; 37: 2129-2200.
- Maeder MT, Buser M, Rickli H, et al: Insuficiência cardíaca com função ventricular esquerda preservada (HFpEF). Therapeutische Umschau 2018; 75: 161-169.
- Ambrosy AP, Fornarow GC, Butler J, et al: The global health and economic burden of hospitalizations for heart failure: lessons learned from hospitalized heart failure registraries. J Am Coll Cardiol 2014; 63: 1123-1133.
- Nohria A, Tsang SW, Fang JC, et al: A avaliação clínica identifica perfis hemodinâmicos que predizem resultados em doentes admitidos com insuficiência cardíaca. J Am Coll Cardiol 2003; 41: 1797-1804.
- Cheema B, Ambrosy AP, Kaplan RM, et al: Lições aprendidas em insuficiência cardíaca aguda. Eur J Insuficiência Cardíaca 2018; 20: 630-641.
- Wakai A, McCabe A, Kidney R, et al: Nitratos para síndromes de insuficiência cardíaca aguda. Cochrane Database Syst Rev 2013; 8: CD005151.
- Felker GM, Lee KL, Bull DA, et al: Estratégias diuréticas em doentes com insuficiência cardíaca descompensada aguda. N Engl J Med 2011; 364: 797-805.
- Orientações ERC para a Ressuscitação 2015. Ressuscitação 2015; 95: 1-80.
- Thiele H, Akin I, Sandri M, et al: Resultados de um ano após as estratégias de PCI em choque cardiogénico. N Engl J Med 2018; doi: 10.1056/NEJMoa1808788 (Epub antes da impressão).
- Mullens W, Abrahams Z, Francis GS, et al: A redução imediata da pressão intra-abdominal após a remoção de grande volume de fluido mecânico melhora a insuficiência renal na insuficiência cardíaca descompensada refratária. J Card Fail 2008; 14: 508-514.
PRÁTICA DO GP 2019; 14(8): 9-13