A psoríase vulgar ou psoríase em placas é a manifestação clínica mais comum da psoríase. A psoríase gutata ocorre frequentemente em jovens e apresenta-se com placas até ao tamanho de uma lentilhas, vermelhas e ligeiramente escamosas. O eritroderma psoriásico e a psoríase pustulosa generalizada de Zumbusch representam as variantes máximas da psoríase (todo o tegumento é fortemente avermelhado e coberto com escamas facilmente destacadas ou coberto com pústulas do tamanho de um alfinete e frequentemente confluentes). A psoríase inversa encontra-se nos espaços intertriginosos, axilas, zonas inguinais e perianais (máculas nitidamente demarcadas, avermelhadas, húmidas e brilhantes das quais as escamas se destacaram devido ao microclima quente e húmido). A infestação psoriásica das unhas ocorre em até 50% dos doentes. A psoríase também afecta as articulações em até 20% dos casos (artrite psoriásica). Manifesta-se com dor e inchaço, mais frequentemente nas articulações dos dedos e joelhos, mas também no esqueleto axial.
A psoríase é uma doença de pele caracterizada externamente por placas vermelhas bem definidas devido à infiltração inflamatória da pele e à firme aderência de escamação branco-prateado devido à hiperproliferação epidérmica e à paraqueratose. A psoríase é uma doença sistémica primária, auto-imune e genética, queratinocitária e mediada por células T, com manifestações inflamatórias na pele, unhas e articulações (artrite psoriásica), bem como uma série de comorbilidades. Consequentemente, as abordagens terapêuticas são anti-inflamatórias, anti-proliferativas e queratolíticas. Baseiam-se na gravidade da doença, relacionada com a extensão da área e eflorescência individual (PASI), no comprometimento da qualidade de vida (DLQI) e localizações especiais (psoríase inversa, psoríase palmo-plantar, psoríase das unhas), bem como na idade do paciente e comorbidades (artrite, síndrome metabólico, doenças cardiovasculares, auto-imunidade, depressão, suicídio). Em 80% dos casos, a psoríase é suave e pode ser adequadamente controlada com tratamento externo (corticosteróides, análogos de vitamina D) e fototerapia (PUVA, UVBnb). Contudo, 20% requerem terapia sistémica clássica (metotrexato, ciclosporina, acitretina) ou terapia com moléculas biológicas e moléculas alvo devido à extensão ou gravidade da doença. Especialmente nas formas graves de psoríase, sofrimento psicológico, comorbilidades e considerações médicas económicas devem ser tidas em conta no plano de tratamento individual.
Epidemiologia e fisiopatologia
A psoríase tem uma prevalência de 2-3% da população e é uma das doenças dermatológicas mais comuns e importantes de todas. Pode ocorrer em qualquer idade e sem preferência de sexo, embora a manifestação inicial tenha dois picos de frequência: cerca de dois terços de todos os doentes sofrem de psoríase tipo I com um início antes dos 40 anos e um pico entre os 16 e os 21 anos de idade. O curso é frequentemente severo e extenso, a história familiar é geralmente positiva, e existe uma associação com HLA-Cw6 [1]. A psoríase tipo II, que é mais crónica e estática, começa após os 40 anos de idade, é esporádica e associada ao HLA-Cw2 [2].
Dentro das placas psoriásicas, há até quatro vezes hiperproliferação acelerada da epiderme, secundária a uma resposta inflamatória. Os queratinócitos podem libertar peptídeos antimicrobianos de ligação ao ADN quando irritados de qualquer forma. Como um complexo peptídeo-ADN, estes causam uma libertação pronunciada de interferon-α [3], que é considerado um dos factores mais importantes para a activação das células T [4]. Linfócitos T activados do tipo Th-1 e Th-17 infiltram-se depois na pele e libertam citocinas pró-inflamatórias tais como o factor de necrose tumoral(TNF)-α, interleucina(IL)-17 e IL-23.
Manifestações clínicas da psoríase
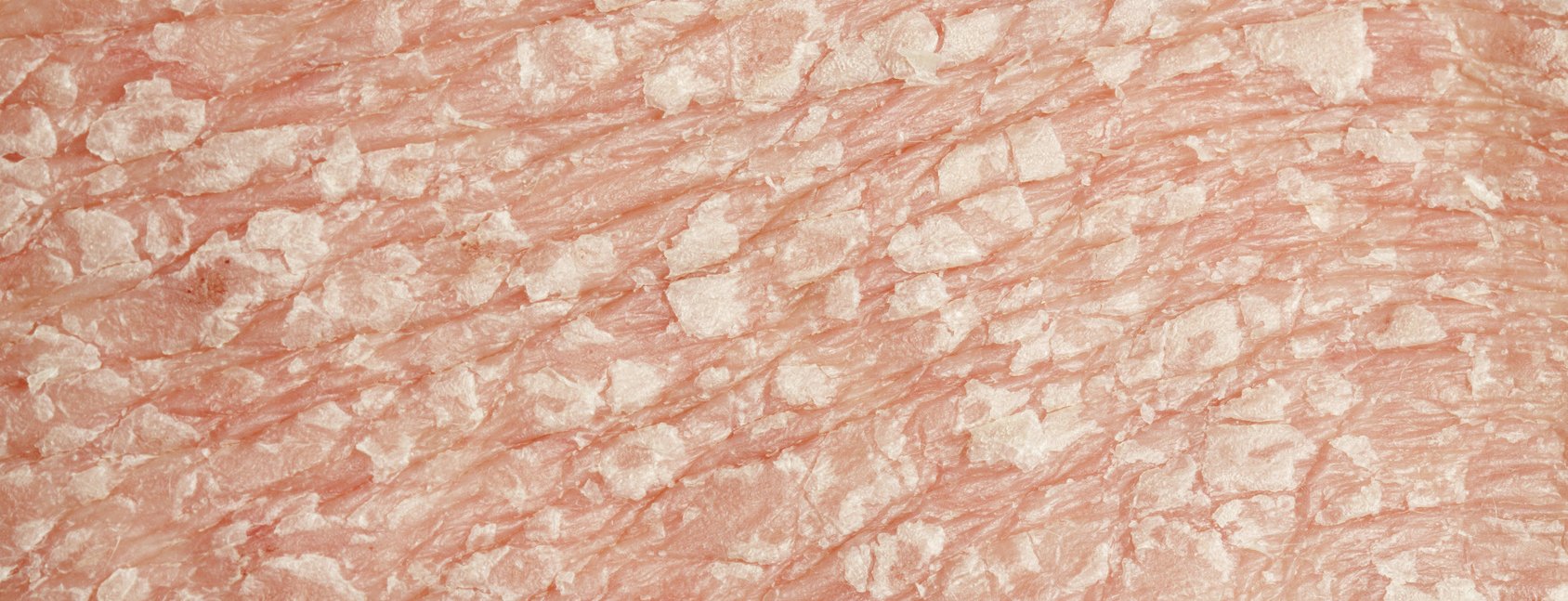
A mudança típica da pele é a placa psoriásica, que mostra três fenómenos característicos que também têm relevância diagnóstica: Primeiro, a remoção mecânica das escamas com, por exemplo, uma espátula de madeira revela material branco prateado (paraqueratósico) como o “fenómeno da cera de vela”, segundo, as camadas celulares mais profundas podem ser removidas até à chamada “última cutícula” e, terceiro, o coçar posterior revela hemorragia puntiforme dos capilares gigantes abertos nas pontas das papilas dérmicas como o “fenómeno de Auspitz” ou “fenómeno do orvalho hemorrágico”.
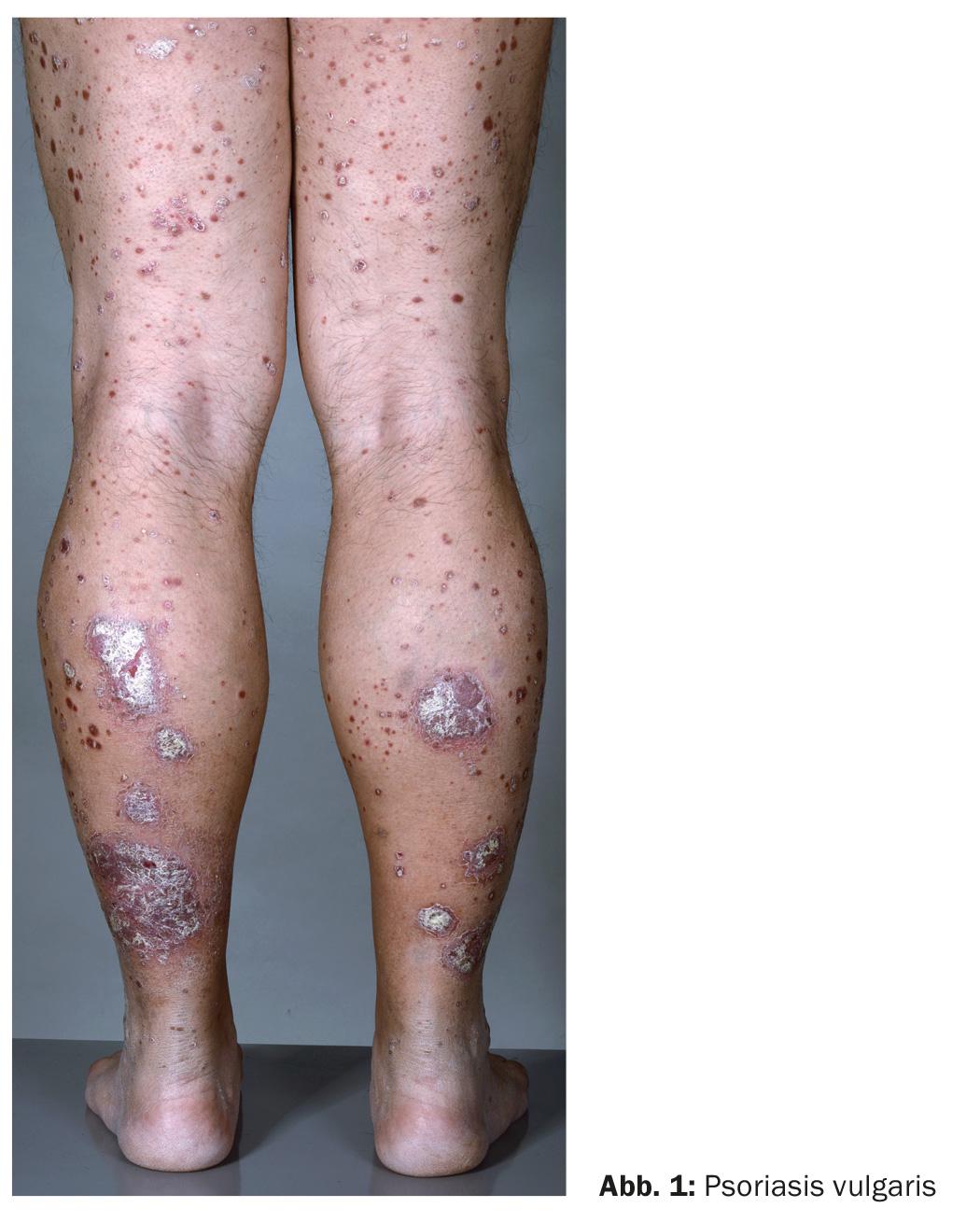
Psoríase vulgaris (Fig. 1): A psoríase vulgar ou psoríase em forma de placa é a manifestação clínica mais comum da psoríase. Manifesta-se com as placas características, nitidamente definidas, avermelhadas, infiltradas e escamosas nos cotovelos, rótulas e couro cabeludo sob o cabelo, mas também no cóccix, nos nós dos dedos e sob o lóbulo da orelha. Geralmente, de acordo com uma provocabilidade mecânica de eflorescência psoriásica (efeito de estímulo isomórfico ou fenómeno de Köbner), são afectadas áreas da pele que são muitas vezes tensas, tais como as articulações mencionadas e as canelas, ou que de outra forma são mecanicamente stressadas, por exemplo, debaixo da cintura. Os focos variam em tamanho, e em casos de infestação extensiva podem ser dispostos num anel com cicatrização central ou confluentes em forma de grinalda.
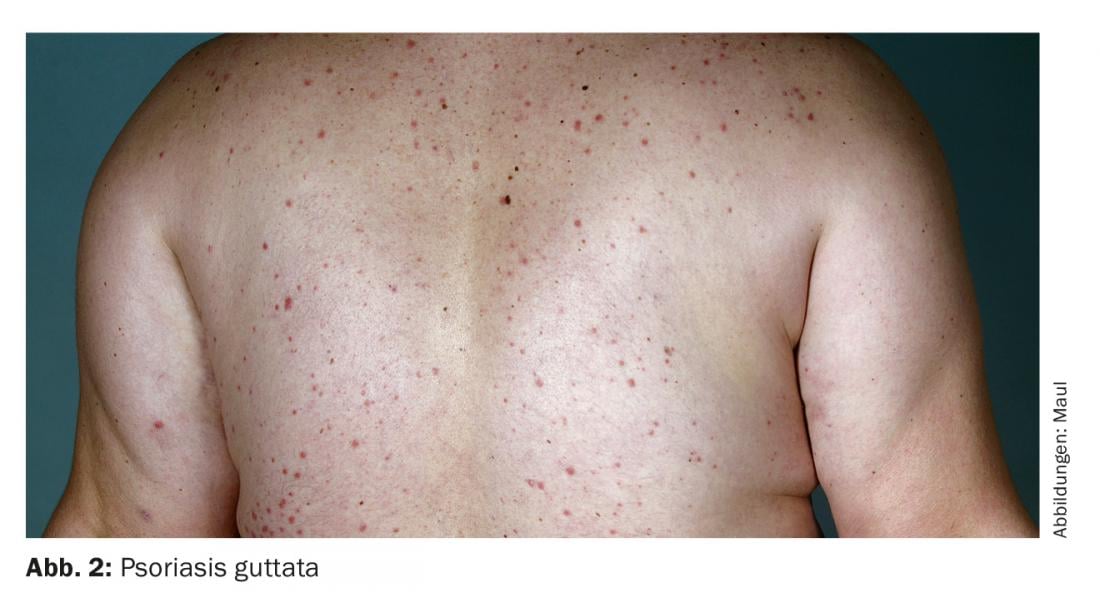
Psoríase guttata (Fig. 2): A psoríase gutata ocorre frequentemente em adolescentes e apresenta-se com placas até ao tamanho de uma lentilhas, vermelhas e ligeiramente escamosas. Uma infecção por estreptococos perianais ou amigdalar é frequentemente o gatilho. Os seus superantigénios podem causar a activação das células T, mantendo-se uma reacção imunitária contra a própria queratina do corpo com a bactéria M-proteína [5].
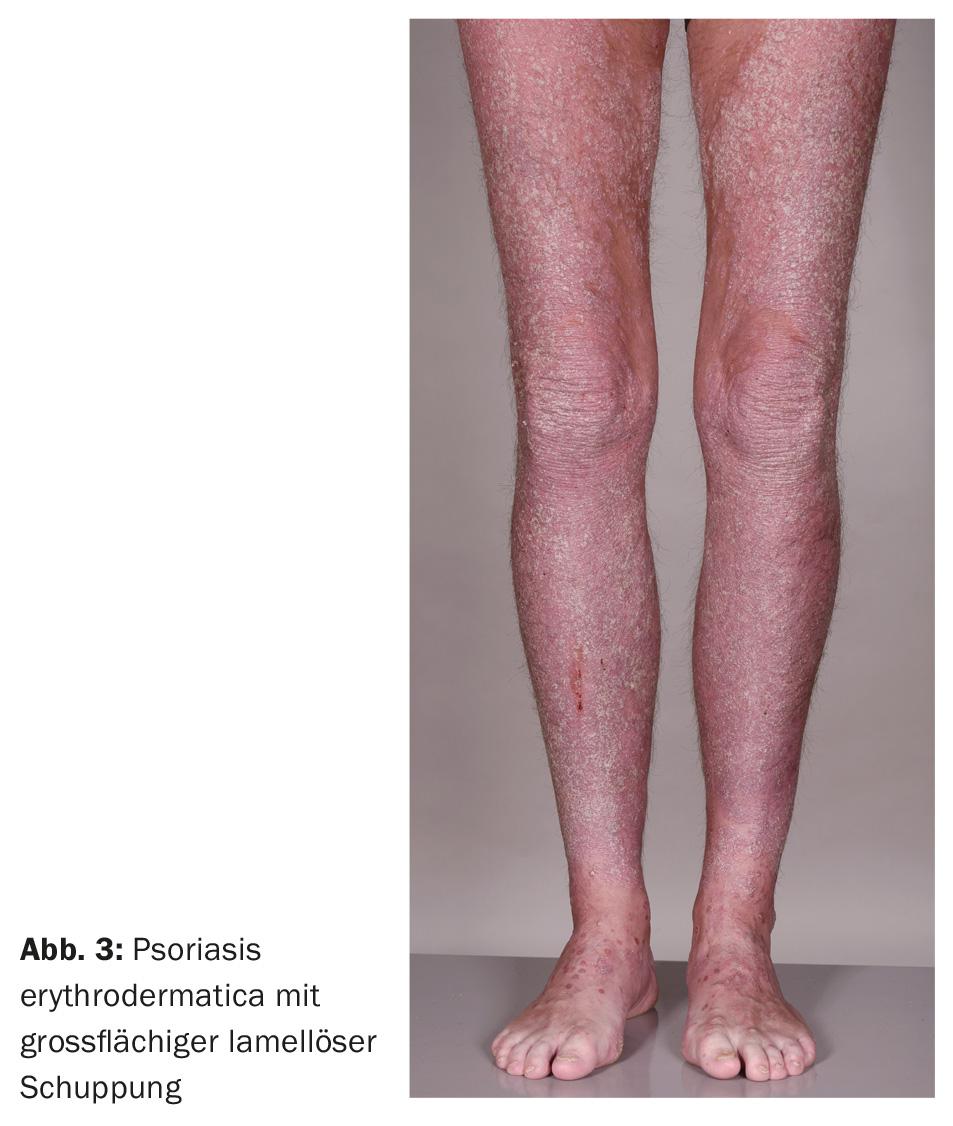
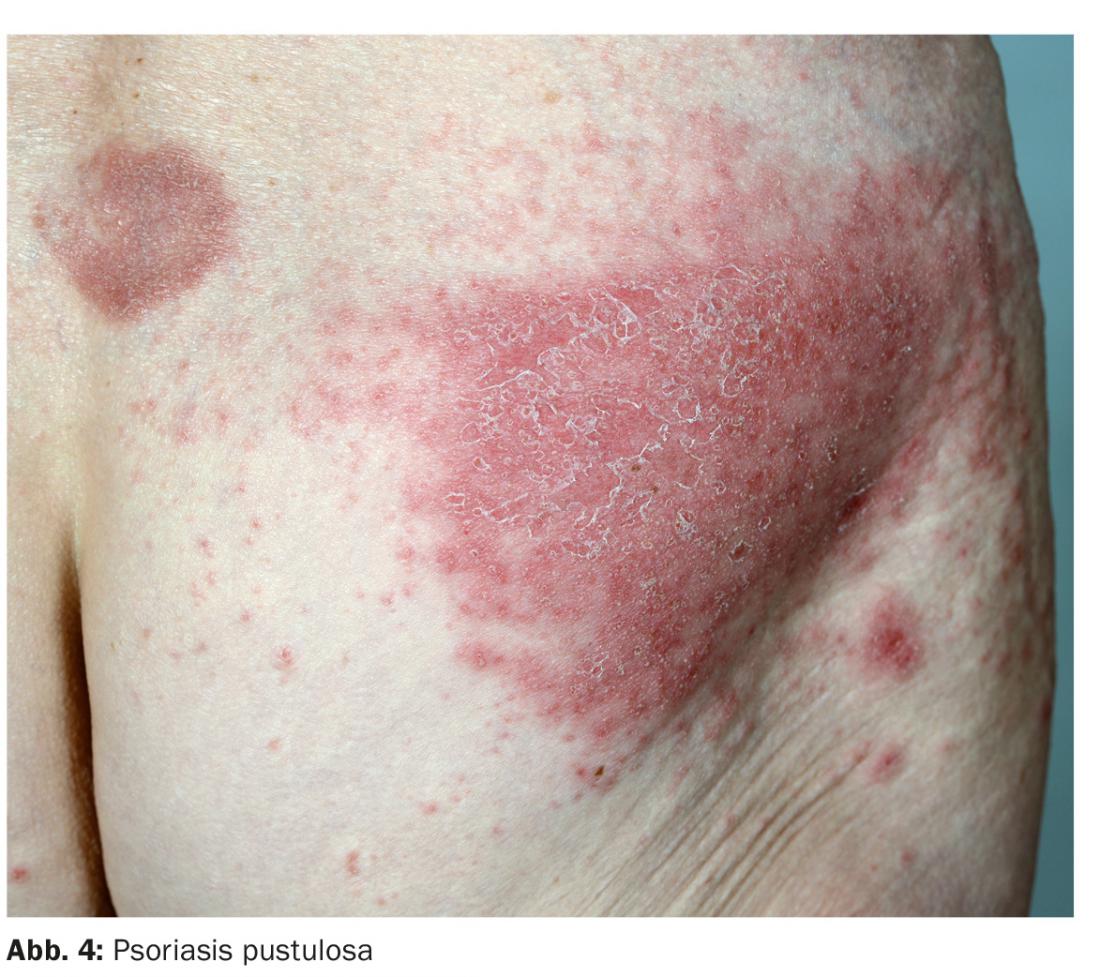
Eritrodermia psoriásica: a eritrodermia psoriásica (Fig. 3) e a psoríase pustulosa generalizada de Zumbusch (Fig. 4) representam as variantes máximas de psoríase mais graves, por vezes com risco de vida. Todo o tegumento é muito vermelho e coberto com escamas facilmente destacáveis ou coberto com pústulas do tamanho de um alfinete e frequentemente confluentes. Há sinais laboratoriais de inflamação com leucocitose frequentemente pronunciada. Recentemente, o gene IL36RN foi identificado como o sítio das mutações que podem desencadear a psoríase pustulosa [6–9].
Psoríase em localizações específicas: A psoríase inversa encontra-se nos espaços intertriginoso, axila, inguinal e perianal. Os achados cutâneos são caracterizados como máculas marcadas, avermelhadas, húmidas e brilhantes, das quais as escamas se destacaram devido ao microclima quente e húmido. Factores locais tais como maceração, infecções bacterianas ou micotrópicas podem provocar ou agravar a psoríase nestes locais.
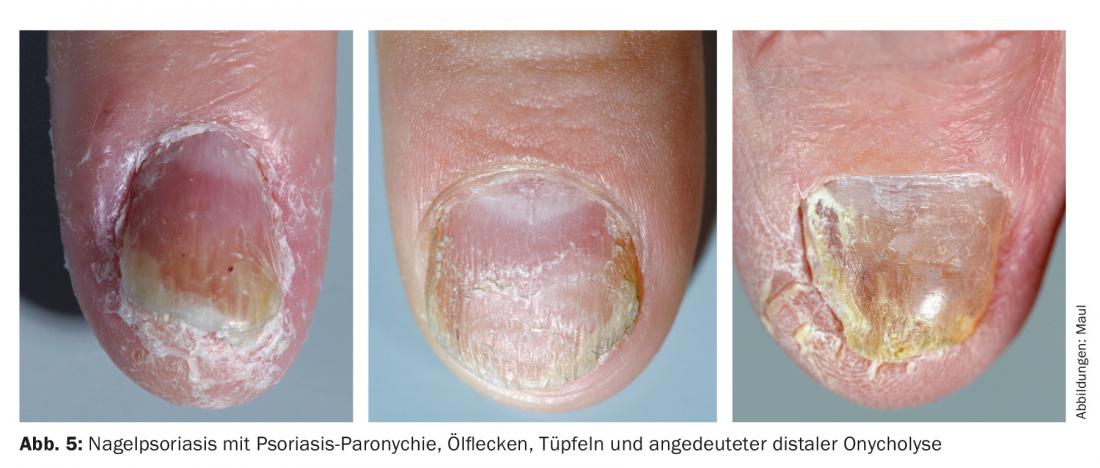
A infestação psoriásica das unhas (Fig. 5) ocorre em até 50% dos pacientes e está associada à artrite psoriásica em 85% dos casos, tendo assim uma função marcadora. 93% dos doentes sentem-se cosmeticamente afectados pela infestação das unhas [10].
Artrite psoriásica: A psoríase também afecta as articulações em até 20% dos casos [11]. A artrite psoriásica manifesta-se com dor e inchaço, mais frequentemente nas articulações dos dedos e joelhos, mas também no esqueleto axial. Na maioria dos casos, as alterações da pele psoriásica precedem o envolvimento conjunto. Antes de se poder objectivar a participação conjunta, também pode ocorrer entesite, ou seja, inflamação dos locais de fixação dos tendões. Uma característica marcante é a alta associação entre a artrite psoriásica e as alterações das unhas, que assumem assim uma função marcadora para o risco da doença articular.
Severidade
A psoríase é considerada grave quando atinge dez pontos numa das três pontuações [12]: PASI (Psoriasis Area and Severity Index), BSA (Body Surface Area) e DLQI (Dermatology Life Quality Index). A pontuação mais importante é o PASI, que mede o eritema, a infiltração, a escamação e a extensão da superfície nos locais correspondentes. Uma fórmula dá uma pontuação de 0 a 72, em que um resultado de >10 é considerado psoríase grave. Uma superfície corporal afectada de 10% ou mais e uma DLQI de dez ou mais pontos indicam também psoríase grave (“regra dos 10” [12]), sendo a DLQI particularmente importante na psoríase das unhas e na psoríase inversa.
Comorbidades
200 anos após a separação da dermatologia da medicina interna na era de Alibert (1768-1837) e Wilson (1809-1894), a psoríase é agora novamente considerada uma doença sistémica. Recentemente, uma base de dados anónima de dados a longo prazo dos médicos de clínica geral mostrou que os principais factores de risco cardiovascular estão agrupados em doentes com psoríase [13]. Os doentes com psoríase grave são mais frequentemente afectados do que os com psoríase ligeira: 20,7% dos doentes com psoríase grave sofriam de obesidade, em comparação com 13,2% no grupo de controlo. 30,1% eram fumadores (grupo de controlo 21,3%), 20% tinham hipertensão (grupo de controlo 11,9%), 7,1% tinham diabetes mellitus (grupo de controlo 3,3%) e 6% tinham hiperlipidemia (grupo de controlo 3,3%). Todas estas condições colocam os doentes numa categoria de alto risco para a mortalidade cardiovascular precoce. O risco de ter um ataque cardíaco é triplicado para um psoriásico grave de 30 anos, e pela metade para um psoriásico de 60 anos. Também está a ser discutido se, para além dos factores de risco cardiovascular mencionados, a inflamação sistémica crónica na psoríase não promove também a arterio- e a esclerose coronária. Afinal, um quinto de todos os pacientes psoriásicos sofre de artrite psoriásica, que também está associada a dores e restrições de mobilidade significativas em mais de metade deles. Estes resultados mostram-nos mais uma vez que a psoríase é uma doença grave com uma série de comorbilidades associadas [14].
Literatura:
- Christophers E, Mrowietz U, Sterry W: Psoríase. 2ª edição. Berlim: Blackwell 2003.
- Henseler T: A genética da psoríase. J Am Acad Dermatol 1997; 37: S1-11.
- Lande R, et al: As células dendríticas plasmocitóides sentem o autoDNA associado ao peptídeo antimicrobiano. Natureza 2007; 449: 564-569.
- Nestlé FO, et al: As células plasmocitóides predendriticas iniciam a psoríase através da produção de interferon-alfa. J Exp Med 2005; 202: 135-143.
- Rasmussen JE: A relação entre a infecção com estreptococos beta hemolíticos do grupo A e o desenvolvimento da psoríase. Pediatr Infect Dis J 2000; 19: 153-154.
- Hussain S, et al: As mutações IL36RN definem um fenótipo autoinflamatório grave de psoríase pustulosa generalizada. J Allergy Clin Immunol 2015; 135: 1067-1070.e9.
- Navarini AA, et al: Mutação homozigota de missense em IL36RN em dermatose pustular generalizada com envolvimento intraoral compatível tanto com AGEP como com psoríase pustular generalizada. JAMA Dermatol 2015; 151: 452-453.
- Navarini AA, et al: Raras variações na IL36RN em reacções adversas graves a medicamentos manifestando-se como pustulose exantematica generalizada aguda. J Invest Dermatol 2013; 133: 1904-1907.
- Setta-Kaffetzi N, et al: As variantes patogénicas raras na IL36RN estão subjacentes a um espectro de fenótipos pustulares associados à psoríase. J Invest Dermatol 2013; 133: 1366-1369.
- de Jong EM, et al: Psoríase das unhas associada à deficiência num grande número de doentes: resultados de uma entrevista recente com 1.728 doentes. Dermatologia 1996; 193: 300-303.
- Reich K, et al: Epidemiologia e padrão clínico da artrite psoriásica na Alemanha: um estudo epidemiológico interdisciplinar prospectivo de 1511 pacientes com psoríase tipo placa. Br J Dermatol 2009; 160(5): 1040-1047.
- Finlay AY: Psoríase grave actual e a regra das dezenas. Br J Dermatol 2005; 152: 861-867.
- Neimann AL, et al: Prevalência de factores de risco cardiovascular em doentes com psoríase. J Am Acad Dermatol 2006; 55: 829-835.
- Katsambas A: Tratar a psoríase como uma doença inflamatória sistémica crónica. Br J Dermatol 2008; 159(Suplemento 2): 1.
PRÁTICA DE DERMATOLOGIA 2016; 26(2): 6-9