As doses em pediatria representam um grande desafio para os pediatras, porque em muitos casos não há informação vinculativa disponível. Este é também o caso da fitoterapia, porque os dados vinculativos só podem ser encontrados com estudos clínicos correspondentes, que quase nunca são realizados por razões éticas, ou quase nunca são concedidas autorizações para os mesmos.
Fitoterapia adequada para crianças
A fitoterapia oferece-se como uma forma adequada de terapia para crianças, por várias razões. Muitos medicamentos à base de plantas têm uma vasta gama terapêutica, pelo que o risco de overdose é muito pequeno na maioria dos casos. Devido ao seu efeito maioritariamente suave, muitas plantas medicinais são adequadas para aplicações pediátricas, quer como tratamento único, quer como tratamento adicional. Além disso, os medicamentos ervanários são muito adequados para indicações que muitas vezes precisam de ser tratadas em crianças, tais como doenças das vias respiratórias, queixas do tracto gastrointestinal, agitação e distúrbios do sono, bem como aplicações dermatológicas. É de grande vantagem se profissionais como médicos e farmacêuticos tiverem informação suficiente para a dosagem de medicamentos à base de plantas para que possam aconselhar da melhor forma os pais e utilizar com segurança os medicamentos à base de plantas nas indicações apropriadas.
Dosagem básica
Para o cálculo das dosagens de medicamentos para crianças são utilizadas fórmulas que tentam fazer justiça à natureza da criança (Tab. 1). Há pouca literatura sobre a dosagem de medicamentos à base de plantas em crianças [1–3]. Se a informação sobre as dosagens das crianças for dada na bula de um medicamento, esta informação é obviamente válida, porque foi aprovada pelo Swissmedic. O quadro 2 lista os medicamentos à base de plantas na lista de especialidades (SL) para os quais as dosagens das crianças são indicadas no folheto informativo.
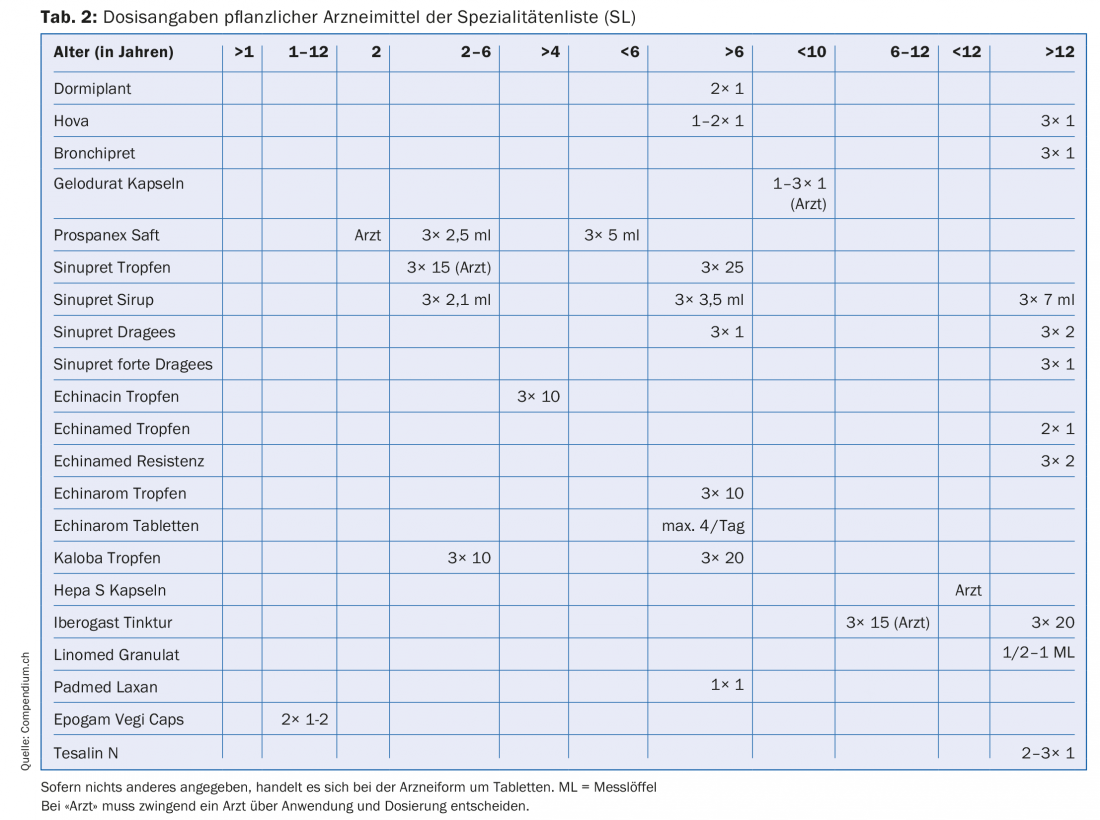
As idades
O quadro 2 mostra que existem indicações de dosagem para grupos etários bastante diferentes. O intervalo de idades vai de >1 ano a >12 anos com numerosos subgrupos no meio.
Além disso, existe informação do paciente que torna obrigatório para certos grupos etários o envolvimento de um médico relativamente a uma utilização planeada. Ex. xarope para a tosse Prospanex: em bebés com menos de dois anos de idade, apenas um médico deve decidir sobre a utilização e a dose. Há também medicamentos para os quais a informação do paciente dá doses para um determinado grupo etário, mas mesmo assim refere-se ao médico, que é o responsável final. É o caso, por exemplo, das gotas Iberogast para crianças dos 6-12 anos de idade.
Porque é que existem grupos etários tão diferentes? Há várias razões para isto.
Agência Médica Europeia (EMA)
A Agência Médica Europeia, a autoridade de registo da União Europeia com sede em Londres, estipula que quando um medicamento é recentemente autorizado, o medicamento em questão está contra-indicado em crianças e adolescentes com menos de 12 anos de idade, a menos que o requerente possa fornecer dados clínicos adequados [4].
Assim, se uma empresa farmacêutica quiser registar utilizações em crianças como parte de uma autorização de comercialização ou renovação de uma autorização de comercialização de um medicamento, deve apresentar um chamado Plano de Investigação Pediátrica (PIP). Este documento, criado pela EMA, regula exactamente quais os documentos e que tipo de estudos são necessários para uma tal autorização. Um PIP apresentado é revisto pelo Comité Pediátrico (PDCO), uma organização da EMA. O PDCO decide sobre as aprovações das candidaturas destas crianças.
Conferência Internacional sobre Harmonização (ICH)
A Conferência Internacional sobre Harmonização dos Requisitos Técnicos para o Registo de Medicamentos para Uso Humano, uma organização fundada em 1990, é responsável pela definição das classes etárias das crianças. De acordo com o seu website, o seu objectivo é conseguir uma melhor harmonização no desenvolvimento e registo de medicamentos eficazes e seguros em todo o mundo. Promove o diálogo entre os fabricantes e as autoridades de registo. Nas Directrizes “Investigação Clínica de Medicamentos na População Pediátrica” [5], aprovadas a 20 de Julho de 2000, a ICH define os seguintes grupos etários pediátricos:
- Recém-nascido: 0-27 dias
- Bebés/toddlers: 28 dias a 23 meses
- Crianças: 2-11 anos
- Adolescentes: 12 a 16-18 anos
Esta classificação é justificada pelas diferenças no desenvolvimento do sistema nervoso central (SNC), do sistema imunitário, da depuração renal e hepática, e das alterações hormonais (adolescentes) destes grupos etários.
Aprovação sem PIP
Se uma empresa farmacêutica pretender obter uma recomendação de dosagem para um ou mais destes grupos etários para uma indicação específica no contexto da autorização de comercialização de um medicamento, deve apresentar um PIP com a informação correspondente, como já foi mencionado. A menos que o faça, ou que a informação no PIP seja aprovada, a EMA declara que a utilização deste medicamento está contra-indicada para crianças e adolescentes com menos de 18 anos de idade. É o caso, por exemplo, do medicamento à base de plantas Kardionin, uma preparação de Crataegus que está registada desde 2013. Uma vez que o fornecedor de cardionina não pôde ou não quis apresentar documentação para uso em crianças, o que é bastante possível dada a indicação do medicamento, a bula apenas menciona o uso para adultos. >A idade de 18 anos é declarada, bem como a informação “A utilização e segurança da Kardionin em crianças e adolescentes não foi estudada até agora”.
Informação desviante
Na lista de medicamentos à base de plantas abaixo (Tab. 2), que inclui informação sobre as dosagens das crianças, existem muitas indicações que não correspondem à classificação etária ICH, por exemplo dosagens para crianças com mais de seis anos de idade ou entre 2-6 anos de idade. Estas alegações podem ser feitas porque os medicamentos correspondentes foram autorizados pela EMA e ICH antes da entrada em vigor dos regulamentos e foram autorizados a fazer as alegações correspondentes com base nos regulamentos da altura.
Resumo
Uma vez que os medicamentos à base de plantas são bem adequados para uso pediátrico, é importante que os profissionais tenham uma base fiável para dosear os grupos etários apropriados. Na ausência de tais informações, podem ser feitas aproximações às dosagens adequadas utilizando a área da superfície corporal, peso ou idade da criança. No entanto, estas são aproximações e devem ser tratadas com cautela. No caso de um novo registo de um medicamento, ou seja, também de um produto à base de plantas, o requerente deve, de acordo com os regulamentos da EMA e da ICH, fornecer informações precisas sobre a eficácia e segurança do medicamento, substanciadas com estudos clínicos, para que possam ser feitas as alegações correspondentes. Caso contrário, a droga está contra-indicada em crianças e adolescentes <18 anos.
Literatura:
- Schicher H, Dorsch W: Fitoterapia em Pediatria. Wissenschaftliche Verlagsgesellschaft Stuttgart 2006.
- Kooperation Phytopharmaka, Bonn: “Kinderdosierungen von Phytopharmaka” – 3ª edição revista e ampliada 2002.
- von Mandach U, et al: Aplicação de medicamentos fitoterápicos em pediatria. Fitoterapia 2002(5); 2: 8-16.
- www.ema.europa.eu
- www.ich.org
PRÁTICA DO GP 2017; 12(8): 2-4












