Os DOAcs são pelo menos iguais à terapia VKA padrão para FVC não-valvular e tromboembolismo venoso em termos de segurança e eficácia. O risco de hemorragia intracraniana é reduzido para metade. Consequentemente, representam uma alternativa válida à VKA. Em caso de insuficiência renal, os limites de utilização devem ser observados de perto. Com uma curta meia-vida de DOAcs e, portanto, uma grande procura de adesão aos medicamentos, o cumprimento e uma boa instrução desempenham um papel importante. Outros estudos que comparam directamente os DOAK entre si e testam outras indicações são importantes para permitir um tratamento individualizado.
Durante mais de 50 anos, os antagonistas de vitamina K (VKA) foram a única forma peroral de anticoagulação. Apesar da sua excelente eficácia e elevado grau de familiaridade, a sua utilização está sujeita a várias limitações, tais como interacções com medicamentos e dietas, controlo rigoroso da terapia e ajustamentos de dose. Estes, por sua vez, juntamente com o respeito pela hemorragia grave, têm um impacto crítico na aceitação do paciente e do médico e podem, em última análise, ser parcialmente responsáveis pela sub-representação da VKA na fibrilação atrial (cerca de 50%) [1, 2].
Nos últimos anos, chegaram ao mercado anticoagulantes orais directos (DOACs) com um rápido início de acção sem necessidade de uma ponte parenteral e farmacocinética favorável com uma relação dose-resposta preditiva e sem necessidade de um acompanhamento terapêutico próximo. Com a boa eficácia e segurança destes preparados, há pontos a ter em conta, tais como a dependência da função renal, interacções medicamentosas, e antídotos específicos ainda não disponíveis na prática clínica. Segue-se uma visão geral dos aspectos clínicos da anticoagulação oral do ponto de vista da medicina interna. O objectivo é facilitar as opções crescentes de selecção terapêutica no sentido da medicina individualizada.
Novo DOAK – Uma visão geral (Tab. 1)
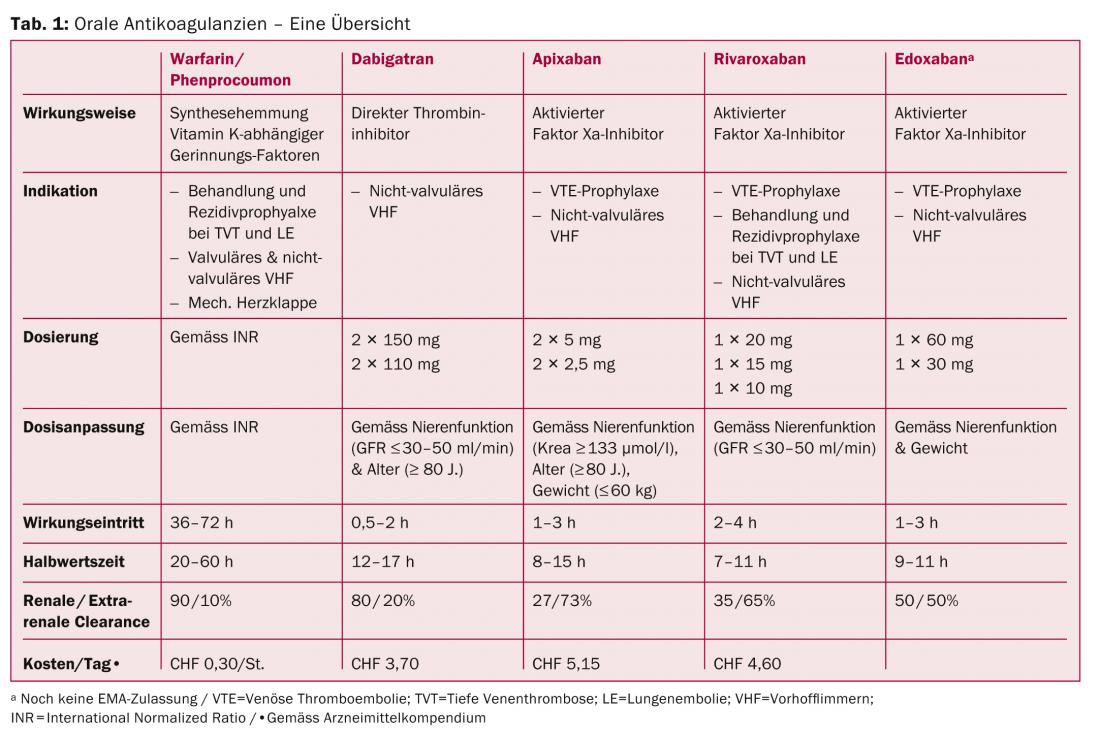
Inibidores directos do factor Xa (rivaroxaban; apixaban; edoxaban): O efeito anticoagulante desdobra-se através da inibição directa do factor Xa (Fig. 1) e secundariamente através da inibição indirecta da geração de trombina.
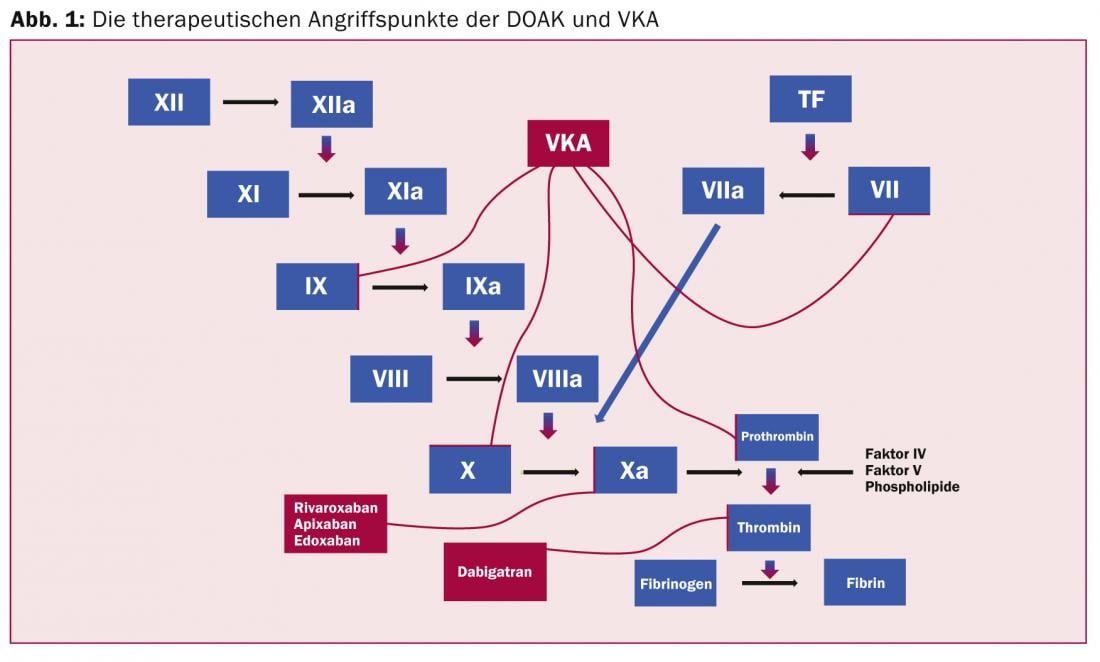
Um factor Xa molécula pode gerar mais de 1000 moléculas de trombina no complexo da protrombinase.
Inibidor directo da trombina (dabigatran): A enzima trombina converte o fibrinogénio em fibrina e amplifica a sua própria formação ao activar os factores V, VIII e XI. Além disso, activa o factor estabilizador do fibrinogénio XIII, bem como as plaquetas de uma forma dependente do receptor. A inibição indirecta da trombina via antitrombina é conhecida há anos com a heparina não fracturada. O mecanismo indirecto, contudo, apenas inibe o livre, mas não a trombina ligada à fibrina, que, no entanto, também desempenha um papel importante no crescimento dos trombos. Os inibidores directos de trombina são capazes de inibir tanto a trombina livre como a trombina ligada [3].
Tromboembolismo venoso (VTE) e DOAKs
Até agora, o tratamento padrão para o tromboembolismo venoso (VTE) era o afinamento do sangue parenteral com uma preparação de heparina durante pelo menos cinco dias, seguido de tratamento com VKA. Para além da necessidade de monitorização regular, isto também implicava um risco acrescido de hemorragia no contexto de anticoagulação sobreposta.
Os estudos RECORD e EINSTEIN demonstraram um efeito do rivaroxaban na prevenção da trombose após cirurgia ortopédica (TP da anca e joelho) e no tratamento e prevenção secundária da embolia pulmonar, incluindo o TEV, que era equivalente à terapia padrão (recorrência do TEV de 2,1% para o rivaroxaban e 3% para o VKA) com uma taxa de hemorragia estatisticamente significativa mais baixa (1,1% vs. 2,2%; HR 0,49, CI 0,31 – 0,79; p=0,003) [4, 5]. A forma directa de administração peroral é uma vantagem importante.
Apixaban como tromboprofilaxia pós-operatória após cirurgia ortopédica e como tratamento e profilaxia secundária de eventos tromboembólicos venosos foi investigada nos ensaios ADVANCE e AMPLIFY, respectivamente. O resultado foi a paridade com a terapia padrão em termos de parâmetros primários (VTE, morte) com uma taxa de sangramento mais baixa (0,6% vs. 1,8%, HR 0,31; 95% CI 0,17- 0,55) [6, 7].
Nos ensaios RE-COVER, a dabigatran teve um efeito preventivo equivalente em TEV recorrente (HR 1,08, IC 95% 0,45-1,48) após uma anticoagulação parenteral inicial de aproximadamente nove dias de duração em comparação com uma VKA, com taxas de hemorragia comparáveis (1,6% para a dabigatran vs. VKA) 1,9% para VKA, HR 0,82; 95% CI 0,45-1,48) e taxa de hemorragia global mais baixa (16,1% vs. 21,9%, HR 0,71; 95% CI 0,59-0,85).
As taxas de hemorragia intracraniana foram mais baixas com todos os preparativos em comparação com a VKA.
Todos os três DOAK têm estudos de extensão bem sucedidos, apixaban também com uma dose reduzida de 2×2,5 mg e dabigatran também em comparação com VKA.
Actualmente aprovado na Suíça para o tratamento e profilaxia secundária de TEV é rivaroxaban a uma dose de 2×15 mg durante três semanas seguido de 1× 20 mg. Apixaban e rivaroxaban estão ambos licenciados para tromboprofilaxia pós-operatória após a anca e o joelho TP na dose de 2×2,5 mg e 1×10 mg respectivamente.
Fibrilação atrial e DOAK
A fibrilação atrial é a arritmia cardíaca mais comum com grande relevância clínica e económica para a saúde.
Para além do VKA, a rivaroxaban, dabigatran e apixaban estão agora também aprovados para a profilaxia de eventos tromboembólicos em VCF não-valvulares.
O ensaio ROCKET-AF mostrou que o rivaroxaban não é inferior ao tratamento VKA na prevenção de AVC e eventos embólicos sistémicos em mais de 14 000 pacientes (taxa de eventos 2,12% vs. 2,42%, HR 0,88), com uma superioridade mesmo significativa na análise do tratamento. Além disso, houve uma taxa de hemorragia intracerebral significativamente reduzida (HR 0,67, CI 0,47-0,94, p=0,019) e também significativamente menos hemorragia fatal (HR 0,50, CI 0,31-0,79, p=0,003) com um aumento do risco de hemorragia gastrointestinal (HR 1,25, CI 1,01-1,55, p=0,04) [8].
O ensaio ARISTOTLE comparou o apixaban com o VKA em mais de 18 000 doentes com eficácia semelhante contra AVC isquémico (0,97% vs. 1,05%, FC 0,92, IC 0,74 -1,13, p=0,42) com redução significativa do AVC hemorrágico (FC 0,51, IC 0,35-0,75, p<0,001) e mortalidade (HR 0,89, CI 0,80 – 0,99, p=0,047) [9].
O estudo RE-LY mostrou uma taxa significativamente reduzida de AVC isquémico (RR 0,76, CI 0,60 – 0,98, p=0,03, ARR 0,28%/paciente-ano) com uma redução do risco de hemorragia intracraniana para dabigatran na dose mais elevada em comparação com a terapia VKA. Além disso, houve um ligeiro aumento na taxa de eventos coronários (0,82% vs. 0,64%, p=0,09), que se tornou significativo na meta-análise, sem influência na mortalidade por todas as causas [10, 11].
Uma meta-análise dos estudos da fase III dos quatro DOAK mostrou um perfil favorável de risco-benefício de todo o grupo com uma redução significativa da mortalidade em cerca de 10% e da taxa de hemorragia intracraniana em cerca de 50% com a mesma eficácia contra eventos isquémicos e, no entanto, uma taxa aumentada de hemorragia gastrointestinal.
Do mesmo modo, para grupos de risco clinicamente relevantes para eventos isquémicos e hemorrágicos (idade >75 anos, história de IVC, insuficiência renal), poderia ser demonstrada a consistência da eficácia e segurança do tratamento DOAK
[12].

Farmacocinética e interacções medicamentosas
Embora os DOAKs tenham menos interacções do que os VKAs, existem algumas questões farmacocinéticas a considerar pelo médico que prescreve.
Assim, uma re-segregação intestinal significativa através do transportador de P-glycoprotein (P-gp) é significativa com todos os DOAKs excepto o rivaroxaban. A inibição competitiva desta via provoca um aumento dos níveis de plasma. Muitos medicamentos, frequentemente utilizados em doentes com FCR, são substratos P-gp e devem ser utilizados com precaução ou não, especialmente com dabigatran (verapamil, dronedarona, amiodarona, quinidina).
O sistema enzimático CYP3A4 está significativamente envolvido na eliminação hepática do rivaroxaban e do apixaban. Neste sentido, as combinações com fortes inibidores desta via (claritromicina, eritromicina, ritonavir, cetoconazol, fluconazol) e indutores (rifampicina, erva de São João, carbamazepina, fenitoína, fenobarbital) devem ser evitadas, se possível (Tab. 2) [13].
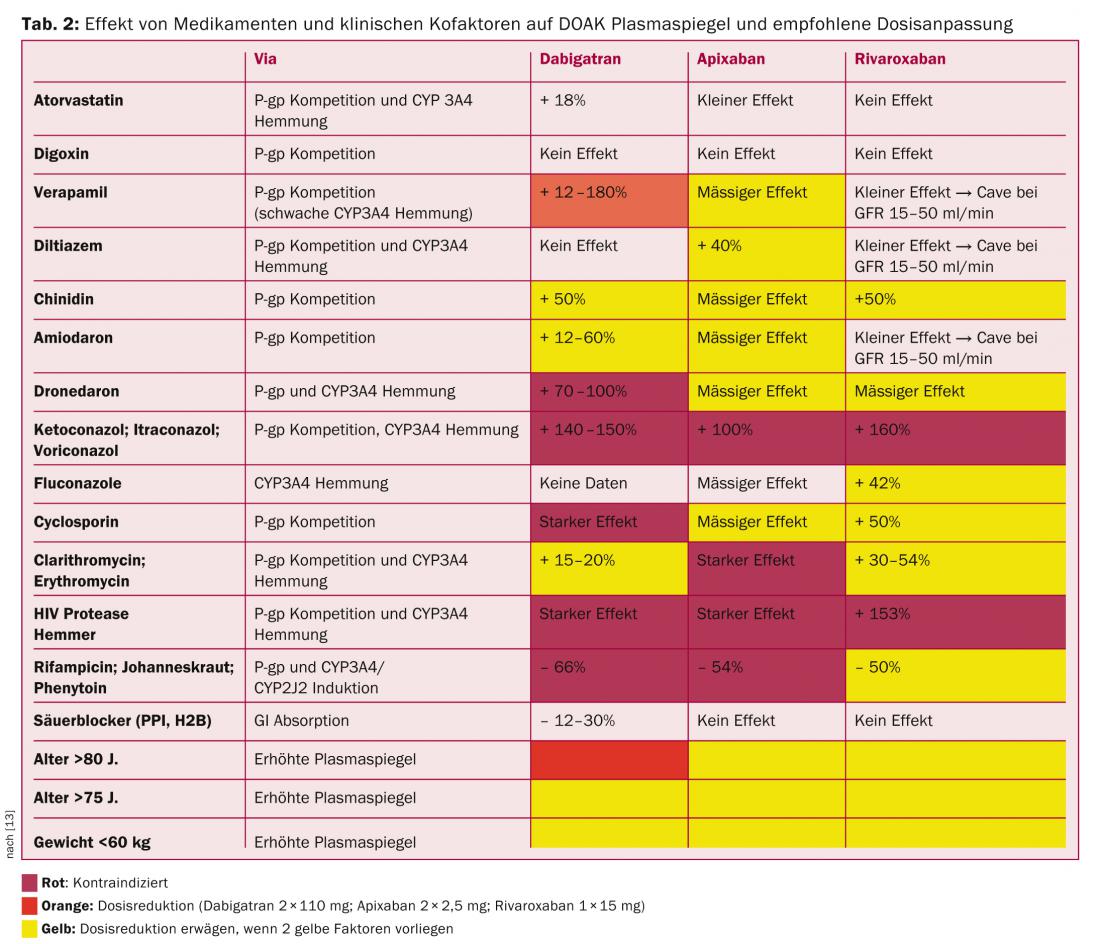
Os próprios DOAKs não afectam os sistemas enzimáticos mencionados e podem ser combinados com outros substratos (midazolam, atorvastatina, digoxina).
As combinações de todos os DOAK com agentes antiplaquetários e AINEs aumentam o risco de hemorragia em pelo menos 60% [14, 15] e devem ser tratadas com cautela, com até 30% dos doentes com agentes antiplaquetários adicionais nos grandes ensaios.
Se houver um aumento de 30-40% na biodisponibilidade do rivaroxaban com acompanhamento alimentar, este deve ser tomado com refeições.
Controlo terapêutico sob DOAK
Uma vantagem importante do DOAK é que os controlos terapêuticos regulares já não são necessários. Em certos casos, contudo, as declarações sobre o efeito anticoagulante de um tratamento seriam de relevância clínica. Por exemplo, em caso de hemorragia grave, evento tromboembólico, intervenção cirúrgica urgente, possível overdose ou cumprimento problemático.
No caso dos inibidores de trombina, o “Ecarin Clotting Time” (ECT) fornece informação directa sobre a sua actividade, embora com uma disponibilidade limitada. O prolongamento do aPTT para o dobro após 12 horas (nível do vale) pode indicar um risco acrescido de hemorragia com dabigatran. Uma medição normalizada do tempo de trombina (por exemplo Hemoclot® para dabigatran) pode reflectir com maior precisão o estado de coagulação, com um tempo de trombina directa de >65 segundos e uma concentração de plasma dabigatran de >200 ng/ml (vale) indicando um risco acrescido de hemorragia.
Para os antagonistas do factor Xa, há um prolongamento dependente da concentração do tempo de protrombina (PT). Além disso, a actividade do Factor Xa pode ser especificamente determinada com a ajuda de plasma calibrado para o medicamento correspondente, embora as associações directas entre os parâmetros de coagulação e o risco de hemorragia ainda não sejam certas (Tab. 3) [13].
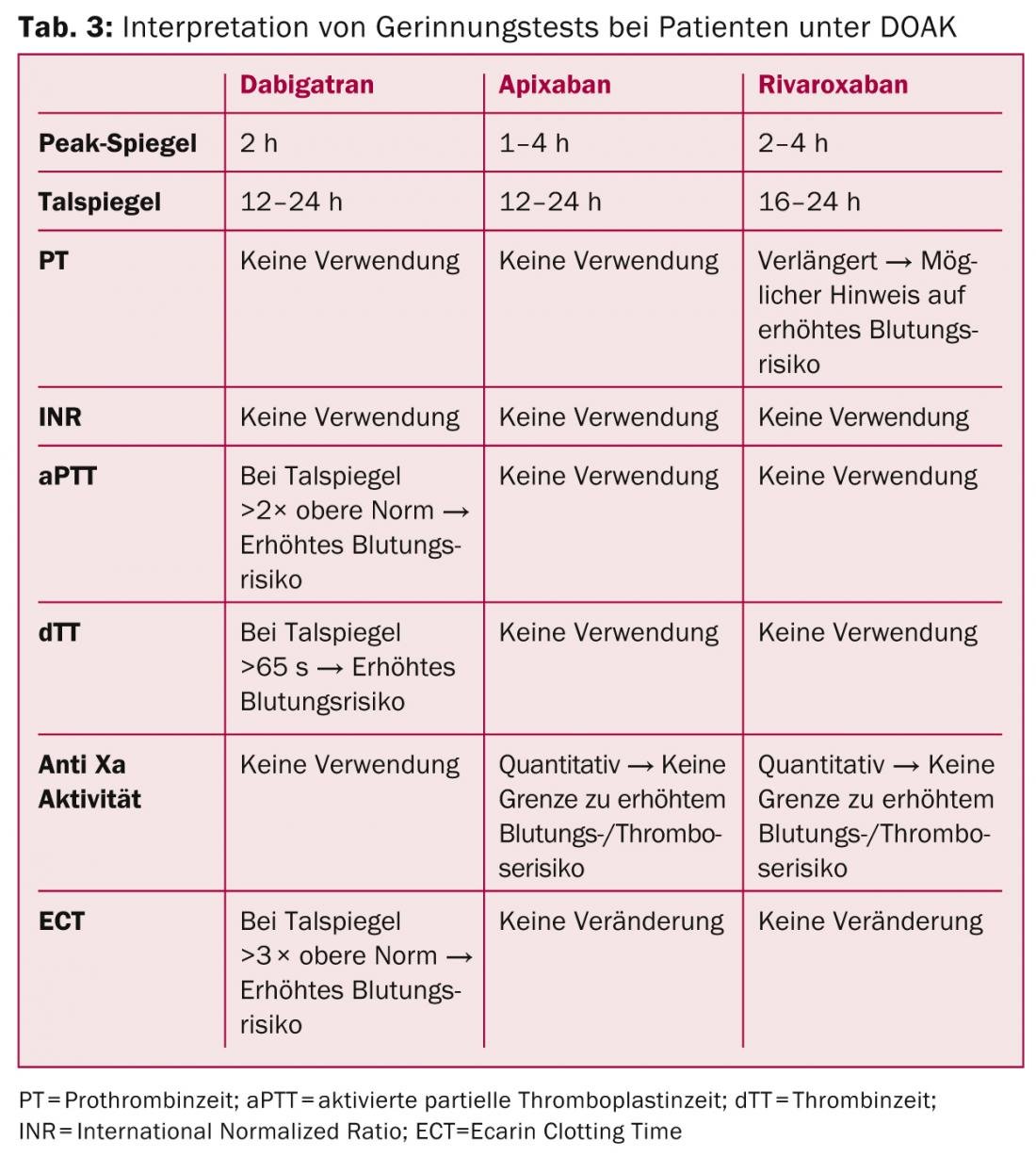
DOAK em insuficiência renal
A insuficiência renal crónica é considerada um factor de risco tanto para eventos tromboembólicos como hemorrágicos em doentes com FCR [16].
Na ausência de dados clínicos, os DOAcs não são utilizados em insuficiência renal avançada (GFR <30 ml/min) de acordo com as actuais directrizes ESC, enquanto que parecem ser uma alternativa válida aos VKAs em função moderadamente deficiente (GFR 30 -50 ml/min) em doses ajustadas [17]. Pessoalmente, os autores já são cautelosos a partir de um GFR de 40 ml/min.
Em geral, os doentes com função renal debilitada que tomam DOAK devem ser acompanhados pelo menos de seis em seis meses. Ainda mais frequente em doentes idosos e polimorbidos e em factores de risco de deterioração aguda (por exemplo, infecções, insuficiência cardíaca).
Complicações hemorrágicas com DOAK
Como todos os anticoagulantes, os DOAKs também apresentam um risco acrescido de hemorragias graves. Em particular, a terapia antiagregatória aditiva, uma combinação com AINS e disfunção renal aumentam a taxa de hemorragia. Ainda não estão disponíveis antídotos específicos (actualmente em ensaios da fase II). Para além das medidas habituais, não específicas, os peritos recomendam a administração de concentrado de complexo de protrombina activado ou regular (PKK, por exemplo Beriplex®; aPKK Feiba®), bem como o factor VII activado (Novoseven®).
Se o dabigatran for dialisável, existe a possibilidade de hemodiálise terapêutica (especialmente em insuficiência renal).
Doença das artérias coronárias e VHF sob OAK
A combinação de DCV e doença arterial coronária não é apenas comum, mas também complexa e associada a um aumento significativo da mortalidade [18].
No cenário agudo, as actuais directrizes devem ser seguidas e a OAC deve ser pausada em favor da terapia antiplaquetária dupla com anticoagulação parenteral.
Na doença arterial coronária estável, a relação benefício/risco da terapia combinada deve ser avaliada utilizando escores comuns para tromboembólicos (CHA2DS2-VASc), aterotrombóticos (GRACE) e risco de hemorragia (escore HAS-BLED).
É importante notar que a terapia tripla com antiagregação dupla e OAKs pelo menos duplica o risco de sangramento e deve ser mantida o mais curta possível [19]. Os DOAKs são também uma alternativa aos VKAs em terapia combinada. Os novos inibidores P2Y12 (prasugrel, ticagrelor) não são recomendados na terapia tripla devido à tendência crescente de sangramento (excepção: alergia ao clopidogrel, trombose de stent sob clopidogrel). O Quadro 4 dá uma visão geral das actuais recomendações do CES em diferentes cenários clínicos [20].
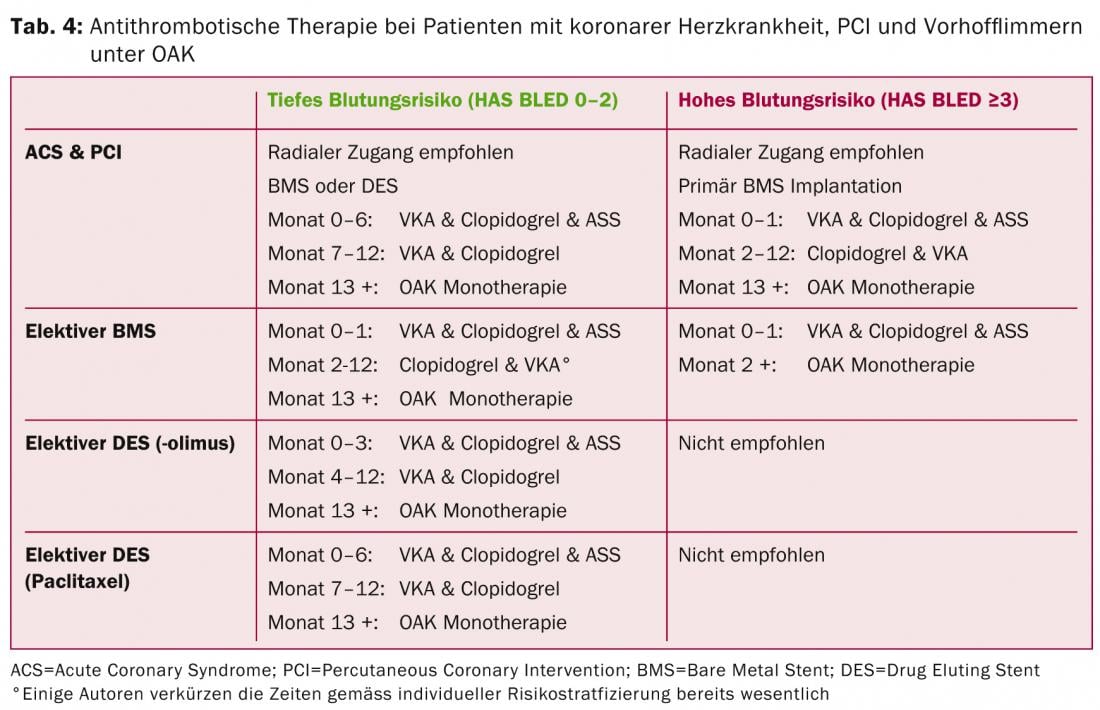
Válvulas cardíacas mecânicas e DOAK
O ensaio RE-ALIGN comparou a dabigatran com VKA em pacientes com válvulas protéticas mecânicas.
O ensaio teve de ser interrompido no início da fase II após um aumento da taxa de AVC (5% vs. 0%), juntamente com um aumento da taxa de hemorragia importante (4% vs. 2%; HR 1,76, 95% CI 0,37-8,46) [21].
Neste sentido, os VKAs continuam a ser a única forma peroral de anticoagulação em pacientes com válvulas cardíacas mecânicas.
Conclusões
Os DOAcs são pelo menos iguais e, em alguns casos, significativamente superiores à terapia VKA padrão para fibrilação atrial não-valvar e tromboembolismo venoso em termos de segurança e eficácia, ao mesmo tempo que reduzem para metade o risco de hemorragia intracraniana, e representam uma alternativa válida aos VKAs (recomendação ESC classe IIa, nível de evidência A). A verificação de rotina do efeito anticoagulante é omitida. Em caso de insuficiência renal, os limites de utilização devem ser observados de perto. Os controlos laboratoriais da função renal são recomendados anualmente em pacientes com função preservada e pelo menos de seis em seis meses em pacientes com função deficiente (<40 ml/min; formalmente de GFR 30-60 ml/min). Além disso, subgrupos como “frágeis e idosos”, doentes oncológicos, eventos especiais (infecção, desidratação, insuficiência cardíaca, etc.), o risco acrescido de hemorragias gastrointestinais e interacções medicamentosas devem ser tidos em conta. Com uma curta meia-vida de DOAcs e, portanto, uma grande procura de adesão aos medicamentos, o cumprimento e uma boa instrução são particularmente importantes. Todos os pacientes devem levar um cartão de medicação e ter instruções de utilização claramente definidas. Estudos adicionais com uma comparação directa do DOAK e testes de indicação em grupos adicionais de doentes (por exemplo, doentes pediátricos e oncológicos) são importantes para permitir um tratamento individualizado.
Nicole R. Bonetti
Literatura:
- Birman-Deych E, et al: Utilização e eficácia da warfarina em beneficiários de Medicare com fibrilação atrial. Stroke 2006; 37: 1070-1074.
- Hylek EM, et al: Grande hemorragia e tolerabilidade da warfarina no primeiro ano de terapia entre doentes idosos com fibrilação atrial. Circulação 2007; 115: 2689 -2696.
- Weitz JI, Crowther M: Inibidores directos de trombina. Thrombosis research 2002; 106: V275 – 84.
- Os investigadores do EINSTEIN: Rivaroxaban oral para tromboembolismo venoso sintomático. N Engl J Med 2010; 363: 2499-2510.
- Os investigadores do EINSTEIN: Rivaroxaban oral para embolia pulmonar sintomática. N Engl J Med 2012; 366: 1287-1297.
- Agnelli G., et al: Apixaban oral para o tratamento do tromboembolismo venoso agudo. N Engl J Med 2013; 369: 799 – 808.
- Lassen MR, et al: Apixaban versus enoxaparina para tromboprofilaxia após substituição da anca. N Engl J Med 2010; 363: 2487-2498.
- Patel MR, et al: Rivaroxaban versus warfarin em fibrilação atrial não-valvar. N Engl J Med 2011; 365: 883-891.
- Granger CB, et al: Apixaban versus warfarin em doentes com fibrilhação atrial. N Engl J Med 2011; 365: 981-992.
- Connolly SJ, et al: Dabigatran versus warfarin em doentes com fibrilação atrial. N Engl J Med 2009; 361: 1139-1151.
- Hohnloser SH, et al: Eventos isquémicos miocárdicos em doentes com fibrilação atrial tratados com dabigatran ou warfarin no ensaio RE-LY. Circulação 2012; 125: 669-676.
- Ruff CT, et al: Comparação da eficácia e segurança dos novos anticoagulantes orais com warfarina em doentes com fibrilação atrial: uma meta-análise de ensaios aleatórios. The Lancet 2013; DOI: 10.1016/S0140-6736(13)62343-0.
- 13 Heidbuchel H, et al: European Heart Rhythm Association Practical Guide on the use of new oral anticoagulants in patients with non-valvular atrial fibrillation. European Society of Cardiology 2013; doi:10.1093/europace/eut083.
- Mega JL, et al: Rivaroxaban em doentes com uma síndrome coronária aguda recente. N Engl J Med 2012; 366: 9-19.
- Alexander JH, et al: Apixaban com terapia antiplaquetária após síndrome coronária aguda. N Engl J Med 2011; 365: 699 -708.
- Olesen JB, et al: AVC e hemorragia em fibrilhação atrial com doença renal crónica. N Engl J Med 2012; 367: 625-635.
- Fox KA, et al: Prevenção de AVC e embolia sistémica com rivaroxaban em comparação com a warfarina em doentes com fibrilação atrial não valvular e insuficiência renal moderada. Eur Heart J 2011; 32: 2387-2394.
- Lopes RD, et al: Terapia antitrombótica e resultados de pacientes com fibrilação atrial após intervenção coronária percutânea primária: resultados do ensaio APEX-AMI. Eur Heart J 2009; 30: 2019 -2028.
- Lamberts M, et al: Sangramento após o início de múltiplos medicamentos antitrombóticos, incluindo a terapia tripla, em doentes com fibrilação atrial após enfarte do miocárdio e intervenção coronária: um estudo de coorte a nível nacional. Circulação 2012; 126: 1185-1193.
- Freek WA Verheugt: Terapia Antitrombótica Durante e Após Intervenção Coronária Percutânea em Pacientes com Fibrilhação Atrial. Circulação 2013; 128: 2058-2061.
- Eikelboom J, et al: Dabigatran versus Warfarin em Pacientes com Válvulas Cardíacas Mecânicas. N Engl J Med 2013; 369: 1206-1214.
CARDIOVASC 2014; 13(2): 5-10