O apoio do médico de família ao doente e aos seus familiares/caridos é crucial para o melhor curso possível da doença. A farmacoterapia é apenas uma componente na gestão integral e multifactorial da demência. Os factores de polimedicação e os perfis de risco de benefício individual devem ser sempre incluídos no conceito de tratamento. Existem algumas novas descobertas relativamente ao uso de drogas tradicionais e modernas contra a demência, tais como inibidores da colinesterase, memantine ou extracto de ginkgo.
Apesar dos enormes investimentos financeiros por parte da indústria farmacêutica, ainda não há nenhuma terapia curativa para a demência à vista. Após os numerosos recuos no desenvolvimento da terapia no campo amilóide, a amplitude das abordagens de investigação teve de ser mais aberta. Para além da imunoterapia com anticorpos tau (tau como segundo depósito típico além do amilóide na demência de Alzheimer), outras abordagens inovadoras, tais como a terapia anti-inflamatória através da alteração direccionada da flora intestinal, estão também a ser cientificamente testadas.
As perturbações cognitivas na velhice são comuns e podem – se diagnosticadas cedo e correctamente – provavelmente não ser curadas com medidas medicinais e não medicamentosas actualmente disponíveis, mas podem ser influenciadas positivamente de uma forma decisiva. A avaliação, bem como a terapia, são adaptadas ao paciente individual e dependem essencialmente do consentimento do paciente, do seu estado de saúde e das circunstâncias sociais.
Introdução
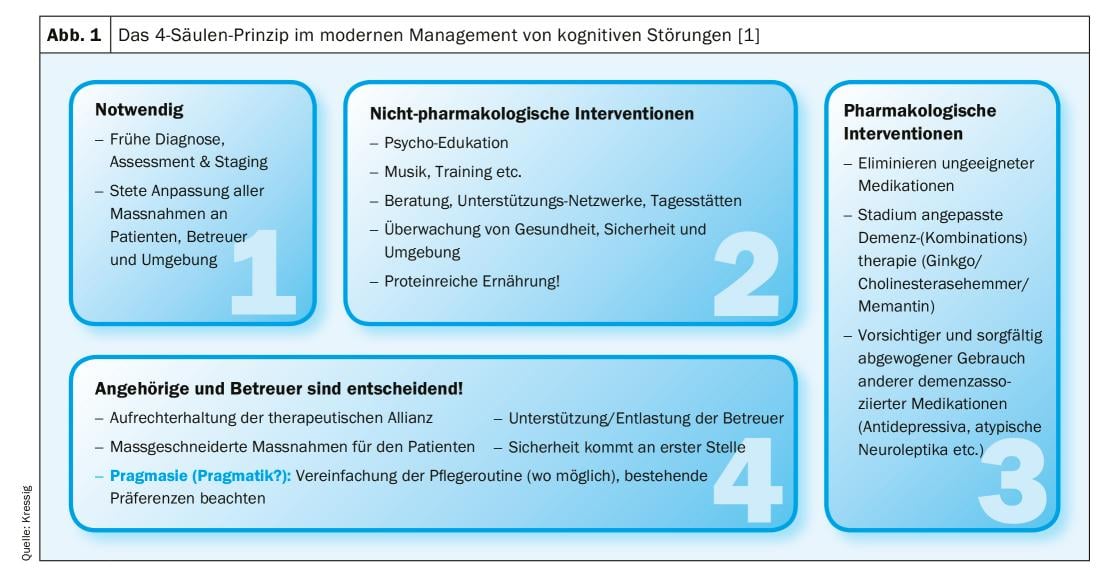
Podemos lidar com queixas de doentes com perturbações cognitivas em adultos mais jovens, mas mais especificamente no 3. e A 4ª idade é confrontada. Em qualquer caso, tais queixas devem ser levadas a sério, porque se o diagnóstico for feito correctamente e as medidas terapêuticas forem iniciadas precocemente, o curso posterior da doença pode ser alterado significativamente. Embora desde a introdução do DSM-5 o termo “demência” já não exista na realidade e se fale agora apenas de “perturbações neurocognitivas graves”, este quadro clínico, que é comum na velhice (cada terceira pessoa com mais de 85 anos é afectada!), não desapareceu, evidentemente. Embora a incidência de demência tenha diminuído até 50% nos últimos 20 anos como resultado de um tratamento significativamente melhor dos factores de risco vascular – a evolução demográfica praticamente neutralizou este progresso médico em termos de números. A gestão moderna das perturbações cognitivas no desenvolvimento da demência baseia-se em 4 pilares (Fig. 1) : Diagnóstico precoce e preciso, terapia medicamentosa, medidas de terapia não medicamentosa e apoio/orientação direccionada para familiares e prestadores de cuidados [1].
Existem perturbações cognitivas “normais” na velhice?
Os pacientes – como nós, médicos – têm tendência a culpar o envelhecimento ou a idade em geral por um maior esquecimento e outras “menores” disfunções cerebrais. O facto é diferente. O envelhecimento normal do cérebro é muito bem estudado cientificamente e está apenas associado a uma discreta desaceleração dos processos de pensamento e reacção. Portanto, se um nome não pode ser lembrado imediatamente, mas pode ser lembrado após um certo tempo, isto ainda é “normal”. Se sempre teve uma má memória para os nomes, não deve esperar qualquer melhoria a este respeito à medida que envelhece! Contudo, se o esquecimento for novo e o sofrimento subjectivo resultante dos doentes estiver presente (mesmo com exame neuropsicológico com resultados normais), então, de acordo com os últimos resultados, isto deve ser avaliado como “Declínio Cognitivo Subjectivo”, o que leva a demência em 25% dos casos no prazo de 6 anos [2]. Infelizmente, muitas pessoas ainda reduzem as perturbações cerebrais principalmente à memória e ao esquecimento. No entanto, o nosso cérebro faz muito mais! Muitos processos de demência começam noutras áreas do cérebro onde a deterioração (enquanto a memória é preservada) se torna principalmente visível através de comportamentos diferentes (por exemplo, mais problemas com tarefas complexas como a gestão de assuntos financeiros ou mesmo cozinhar ementas mais complicadas! Tais mudanças não são normais e devem ser esclarecidas!
Demarcação de “normal” versus “patológico
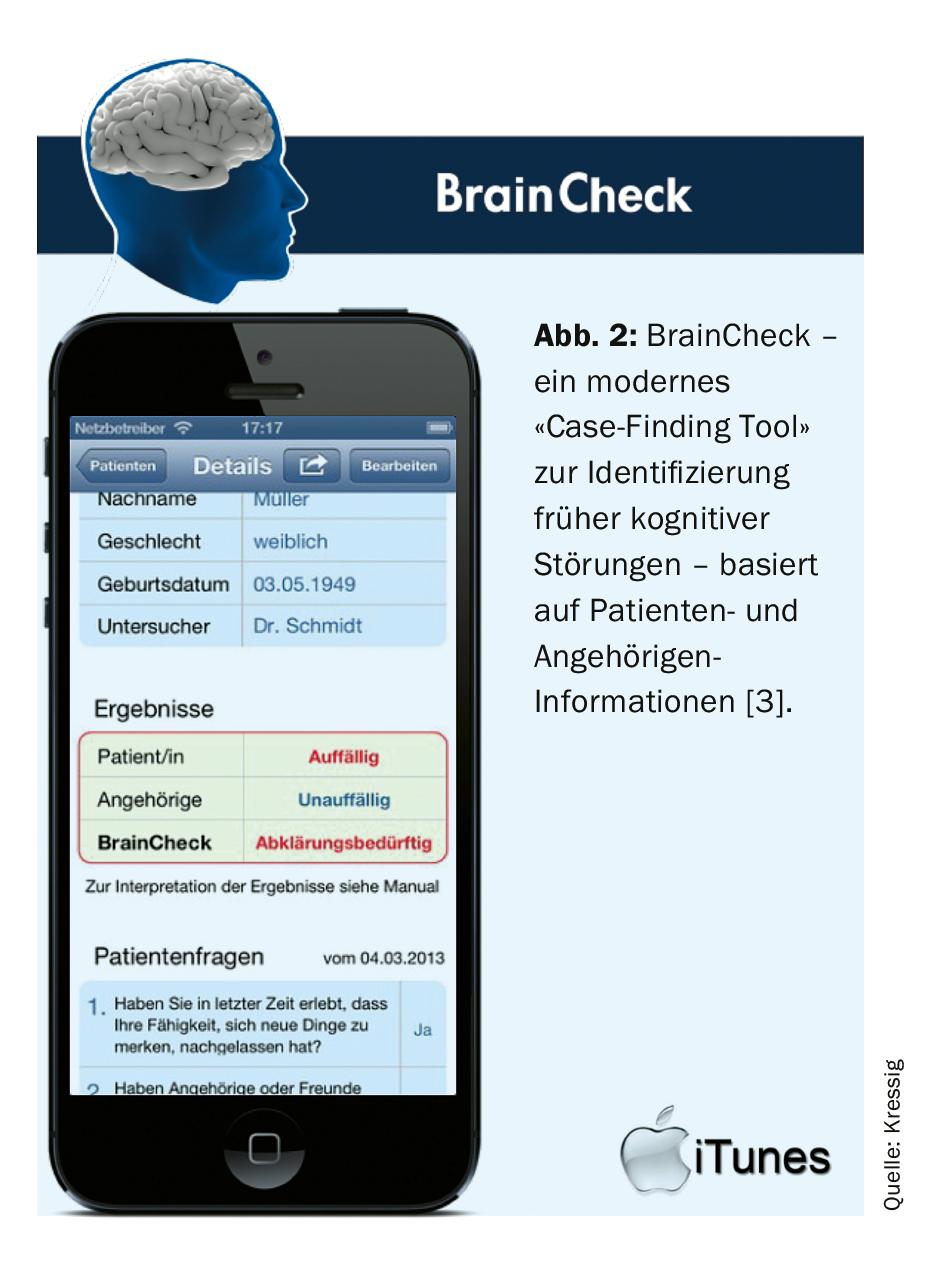
Na prática quotidiana, deve ser possível decidir rapidamente e com pouco tempo se as perturbações cognitivas precisam de ser esclarecidas mais rapidamente, se é necessária mais observação ou se não é necessária mais acção! O primeiro (demorado) rastreio de perturbações cognitivas através de MMSE e teste de relógio foi substituído nos últimos anos pelo mais sensível e direccionado “descoberta de casos” através de uma “aplicação”. (Fig. 2). A aplicação “BrainCheck”, desenvolvida pelas “Swiss Memory Clinics” e pelos GPs suíços, separa “normal” de “patológico” em apenas alguns minutos com uma selectividade de 90% [3]! Para isso, o paciente tem de responder a três perguntas simples e completar um teste de relógio. Ao mesmo tempo, são feitas 7 breves perguntas ao seu parente/parceiro mais próximo. Todos os resultados podem ser registados e avaliados imediatamente na aplicação. A breve avaliação pode ser facilmente integrada na história médica electrónica como um ficheiro PDF.
Para além de anomalias puramente cognitivas, outros sintomas clínicos tais como perda de peso, alterações comportamentais ou humor depressivo podem também reforçar a suspeita precoce de desenvolvimento de demência.
Se houver necessidade de mais esclarecimentos, deve ser tomada uma decisão em conjunto com o doente e os seus familiares sobre como proceder com o diagnóstico. Como primeiro passo, a (simples) exclusão de causas rapidamente tratáveis é certamente um “must” absoluto aqui. Uma doença da tiróide pode ser excluída por meio de determinação TSH, a depressão pode ser detectada por meio da Escala de Depressão Geriátrica (GDS) e uma situação de stress psicossocial (carga de stress) pode ser detectada com uma anamnese cuidadosa e, no caso positivo, tratada com contramedidas adequadas. Se houver uma suspeita razoável baseada na anamnese, um estado de vitamina B e uma serologia da sífilis também pode ser útil. Se se encontrar algo nas áreas acima mencionadas e, consequentemente, se estiver activo na terapia, é aconselhável acompanhar a cognição cerca de 6 meses mais tarde usando BrainCheck.
Perturbações cognitivas que requerem esclarecimento
O tipo de avaliação adicional das perturbações cognitivas é muito individual e depende do consentimento do paciente, do seu estado de saúde/esperança de vida e das circunstâncias sociais. Para os idosos mais jovens e em melhor forma, uma avaliação especializada deve ser sempre realizada por um especialista em demência ou por uma clínica de memória. Para além de um exame médico com marcadores laboratoriais e biomarcadores, isto inclui uma avaliação neuropsicológica com imagens do cérebro (MRI). Em doentes muito velhos e frágeis, também pode ser realizada uma avaliação cognitiva abreviada (por exemplo, utilizando a avaliação MoCa [4]). Isto pode – com alguma experiência – ser realizado e diagnosticado na prática do GP. Isto também inclui imperativamente a imagiologia cerebral (RM ou TAC) para determinar a causa neuropatológica mais provável do desenvolvimento da demência. Isto é decisivo para o tipo de terapia a ser iniciada.
Perturbações cognitivas: Opções terapêuticas
De acordo com o DSM-5, se as perturbações cognitivas forem “leves”, estão dentro de duas variações padrão de um achado cognitivo normal. Opções terapêuticas aqui, além de medicinais (Ginkgo Biloba 240 mg/d e vitamina D 24.000 unidades por mês), o principal enfoque é em medidas não medicamentosas: actividade física e social (cognitiva) regular, uma dieta saudável adequada à idade (proteínas regulares e suficientes – pelo menos 1,2 g/kg de peso corporal por dia; dieta mediterrânica com ácidos ómega-3 suficientes) e um bom controlo por parte dos médicos de família dos factores de risco vascular (tipo de hipertensão, diabetes, hipercolesterolemia). No estudo finlandês FINGER [5], foram conseguidas melhorias cognitivas significativas após 2 anos apenas com estas medidas de estilo de vida.
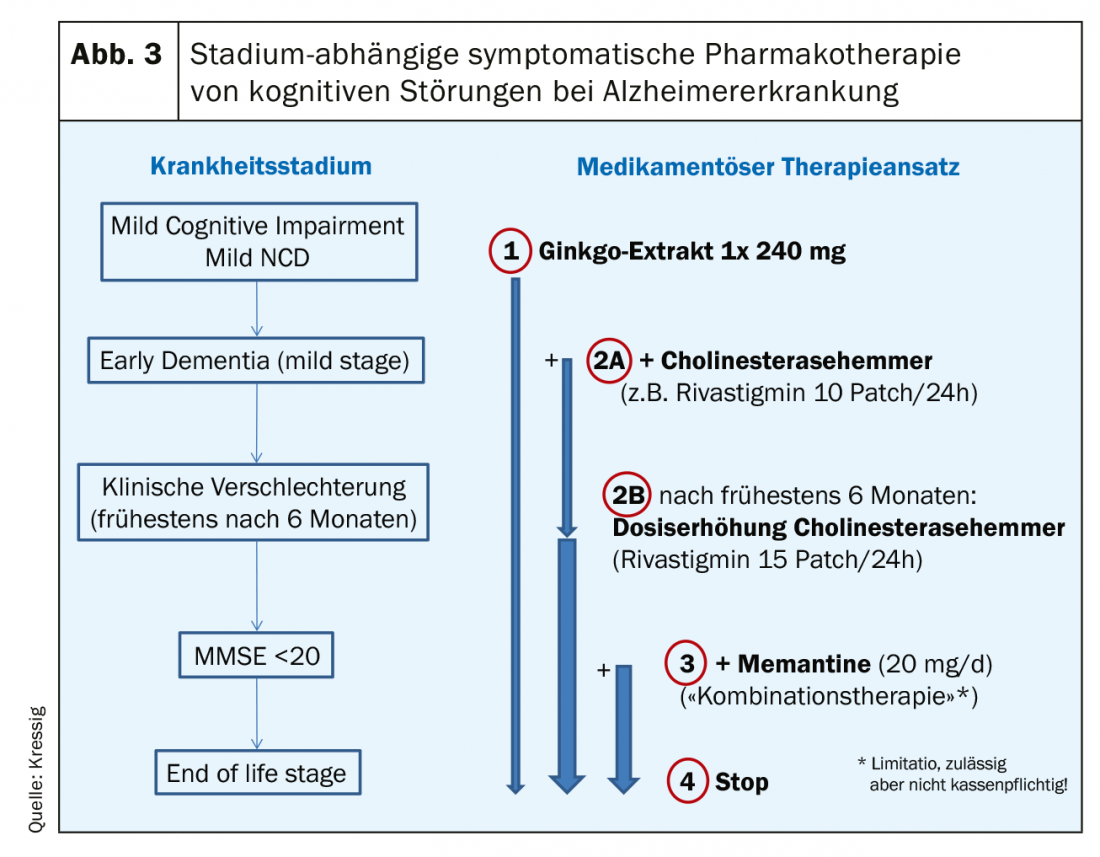
Opções de medicação: Antes de serem utilizados novos medicamentos, é essencial verificar qualquer polifarmácia existente para substâncias anticolinérgicas cognitivamente nocivas. Se, de acordo com o DSM-5, for uma perturbação cognitiva “maior” (demência), a neuropatologia subjacente ao processo é decisiva para determinar a terapêutica medicamentosa. Para tal, é geralmente obrigatória a obtenção de imagens apropriadas com ou sem biomarcadores. Se for um processo neurodegenerativo (doença de Alzheimer), os inibidores de ginkgo, colinesterase e memantine são as drogas de primeira escolha, dependendo da fase (Fig. 3).
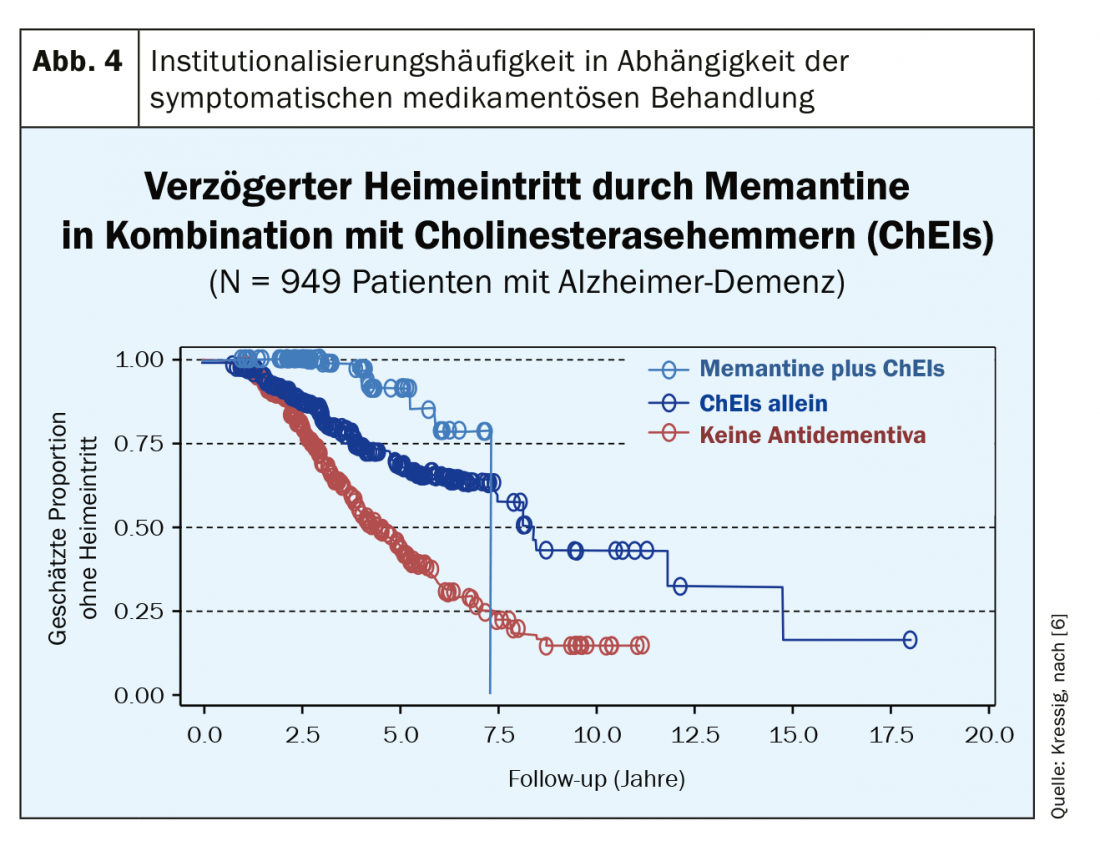
Após mais de 20 anos de experiência com estas opções terapêuticas sintomáticas, tornou-se claro que não é a melhoria das funções puramente cognitivas (por exemplo, a memória) que faz a diferença para nenhum tratamento medicamentoso. Esta terapia sintomática (se iniciada cedo) melhora significativamente o curso da doença em termos de manutenção da funcionalidade e independência. Estes medicamentos funcionam extremamente lentamente, mas têm uma alta taxa de resposta graças a um Número Necessário de Tratamento (NNT) inferior a 10 (para as três classes de substâncias!). No entanto, em comparação com as populações de controlo não tratadas, as primeiras diferenças clinicamente perceptíveis só aparecem após um ano de tratamento; estas tornam-se muito relevantes nos anos seguintes, no entanto, uma vez que o tratamento leva a impressionantemente menos admissões em lares de idosos (Fig. 4) [6]. Aqui, a terapia de combinação de memantina com inibidores de colinesterase (no MMSE <20) provou ser muito bem sucedida. Na Suíça, no entanto, isto só é possível fora do rótulo e não está totalmente coberto por um seguro básico devido a uma limitação. No entanto, muitos pacientes estão felizes por pagarem eles próprios as poucas centenas de francos por ano (tendo em conta a queda abrupta do preço dos medicamentos contra a demência) se isso poupar os custos financeiros muito mais elevados da institucionalização. Para além da preservação mais prolongada da funcionalidade quotidiana com os medicamentos contra a demência, ocorrem significativamente menos problemas de comportamento associados à demência (agressão, choro, agitação motora, etc.) com esta terapia.
Se a patologia subjacente ao desenvolvimento da demência for puramente vascular, os medicamentos antidemência acima mencionados (excepto ginkgo) não são eficazes e, consequentemente, não são indicados. Aqui, é importante abrandar por todos os meios a progressão da doença, com medidas de estilo de vida e o controlo dos factores de risco vascular. Os medicamentos anti-demência podem ser utilizados para formas mistas de demência vascular-neurodegenerativa. Para patologias demenciais mais raras como a doença de Lewis-Body, doença de Parkinson ou demência fronto-temporal, vale a pena consultar especialistas apropriados.
Opções sem drogas: As intervenções não medicamentosas para doentes com demência são recomendadas pelas principais sociedades profissionais e grupos de peritos – excepto em situações de emergência – principalmente e como abordagem primária para as perturbações psico-sociais de comportamento associadas à demência (BPSD) [7]. De acordo com Cohen-Mansfield [8], a maioria dos médicos são treinados para prescrever medicação para a BPSD, mas apenas alguns têm conhecimento de medidas terapêuticas não medicamentosas e da sua eficácia. Consequentemente, os medicamentos antipsicóticos são frequentemente utilizados antes de se tentarem intervenções não medicamentosas.
Em contraste com as capacidades cognitivas que são prejudicadas ou perdidas precocemente na demência, as competências emocionais e psicossociais são muitas vezes muito menos afectadas pela deterioração até às fases tardias da demência. É aqui que entram as intervenções não relacionadas com a droga, ao aceder aos recursos existentes de desempenho cerebral – longe do foco do défice – e ao utilizá-los e promovê-los de uma forma orientada. A actividade física, as actividades baseadas na música e as dietas com alto teor de proteínas suplementadas com vitamina D demonstraram ser as mais bem sucedidas na manutenção da saúde muscular na demência [9]. O efeito cerebral das actividades de movimento combinadas com música, como a dança e os ritmos, é excitante e repetidamente o tema de investigação. No estudo de coorte “Einstein Envelhecimento”, a dança regular como actividade de lazer foi associada a uma redução até 80% do risco de demência mais tarde na vida [10]. Num estudo de intervenção com recurso a ritmos de acordo com Dalcroze, a capacidade de dupla tarefa motor-cognitiva dos idosos que vivem em casa foi melhorada e o risco de quedas foi reduzido em mais de 50% [11]. Em fases avançadas da demência, o ritmo Dalcroze parece promover as competências linguísticas em particular, para além de influenciar positivamente os sintomas do BPSD [12].
As intervenções não farmacológicas para pacientes com demência são uma parte essencial da gestão moderna da demência em 4 pilares. O principal efeito esperado de tais medidas é influenciar positivamente e sem efeitos secundários o BPSD. Os programas de actividade física mostram benefícios adicionais para a funcionalidade quotidiana, que podem ser mantidos significativamente por mais tempo, especialmente com uma dieta simultânea de alta proteína e suplemento de vitamina D. A necessidade diária de pelo menos 1,2 g de proteína por kg de peso corporal para manter a saúde muscular em demência só pode ser satisfeita frequentemente através da utilização de suplementos proteicos. Estes são cobertos pelo seguro básico após aprovação dos custos (http://geskes.ch, “Home Care”) e podem ser entregues no domicílio do paciente. Os programas de música e movimento baseados na música, tais como a dança e o ritmo, parecem ser particularmente adequados para mobilizar reservas de cérebros e assim melhorar significativamente a cognição.
Conclusão para a prática
A terapia sintomática não-droga e medicamentosa para a deficiência cognitiva é apenas um componente na gestão multifactorial de 4-pilares da demência. As abordagens sem drogas mostram efeitos cognitivos marginais a não detectáveis, mas são eficazes para problemas de comportamento, sintomas psiquiátricos e carga de cuidados. Na terapia farmacológica, é importante reduzir ao máximo a polimedicação existente e descontinuar as substâncias potencialmente nocivas (lista Priscus). Actualmente, não existem razões racionais para não utilizar os fármacos antidemência sintomáticos actualmente disponíveis (inibidores da colinesterase, memantine e extracto de ginkgo). Embora os efeitos clínicos imediatos no início da terapia sejam relativamente baixos, as principais vantagens estão no longo prazo (institucionalização atrasada por anos, significativamente menos perturbações comportamentais).
Mensagens Take-Home
- A farmacopeia é apenas uma componente na gestão integral e multifactorial da demência.
- Para além do diagnóstico precoce, o apoio do médico de cuidados primários ao doente e aos seus familiares/caridos é essencial para o melhor curso possível da doença.
- O principal objectivo da terapia farmacológica é reduzir a polimedicação existente e descontinuar as substâncias potencialmente nocivas (anticolinérgicas) (lista Priscus).
- Actualmente, não existem razões racionais para não utilizar os fármacos antidemência sintomáticos (inibidores da colinesterase, memantina e extracto de ginkgo normalizado) que estão disponíveis há anos.
- A nível internacional, a combinação de inibidores de colinesterase e memantine na gama MMSE aprovada, bem como uma terapia concomitante de Ginkgo Biloba, é hoje em dia o estado da arte na terapia para a demência de Alzheimer.
- Em estudos a longo prazo, a terapia combinada (inibidor de colinesterase + memantine), que só está disponível fora do rótulo na Suíça, atrasou a institucionalização em anos e reduziu significativamente as perturbações de comportamento.
Literatura:
- Kressig RW: Demência do tipo Alzheimer: terapia sem drogas e medicamentosa. Ther Umsch 2015; 72(4): 233-238.
- Wolfsgruber S, et al: Differential Risk of Incident Alzheimer’s Disease Dementia in Stable Versus Unstable Patterns of Subjective Cognitive Decline. J Alzheimers Dis 2016; 54: 1135-1146.
- Ehrensperger M, et al.: BrainCheck – uma ferramenta muito breve para detectar o declínio cognitivo incipiente: procura optimizada de casos combinando dados baseados em pacientes e informadores. Alz Res Ther 2014; 6: 69.
- Nasreddine, et al: The Montreal Cognitive Assessment, MoCA: uma breve ferramenta de rastreio para uma ligeira deficiência cognitiva. J Am Geriatr Soc 2005; 53: 695-699.
- Kivipelto M, et al.: The Finnish Geriatric Intervention Study to Prevent Cognitive Impairment and Disability (FINGER): study design and progress. Alzheimer e Demência 2013; 9: 657-665.
- Lopez OL, et al.: Efeitos a longo prazo do uso concomitante de memantine com inibição da colinesterase na doença de Alzheimer. J Neurol Neurosurg Psychiatry 2009; 80: 600-607.
- Savaskan E, et al: Recomendações para o diagnóstico e terapia dos sintomas comportamentais e psicológicos na demência (BPSD). Praxis (Berna 1994) 2014; 103(3): 135-148.
- Cohen-Mansfield J: Intervenções não-farmacológicas para comportamentos inadequados na demência: uma revisão, resumo, e crítica. Am J Geriatr Psychiatry 2001; 9: 361-381.
- Kressig RW: Opções de tratamento não farmacológico para a demência. Clínica Médica Interna 2017; 58: 1-7.
- Verghese J, et al: Actividades de lazer e o risco de demência nos idosos. N Engl J Med 2003; 348: 2508-2516.
- Trombetti A, et al.: Efeito da formação multitarefa baseada na música sobre a marcha, equilíbrio, e risco de queda em pessoas idosas: um ensaio aleatório controlado. Arch Intern Med 2011; 171(6): 525-533.
- Winkelmann A, et al.: La rythmique Jaques-Dalcroze: Une activité physique novatrice pour les personnes âgées. GERIATRIE PRATIQUE 2005; 3: 1-5.
PRÁTICA DO GP 2020: 15(5): 16-19