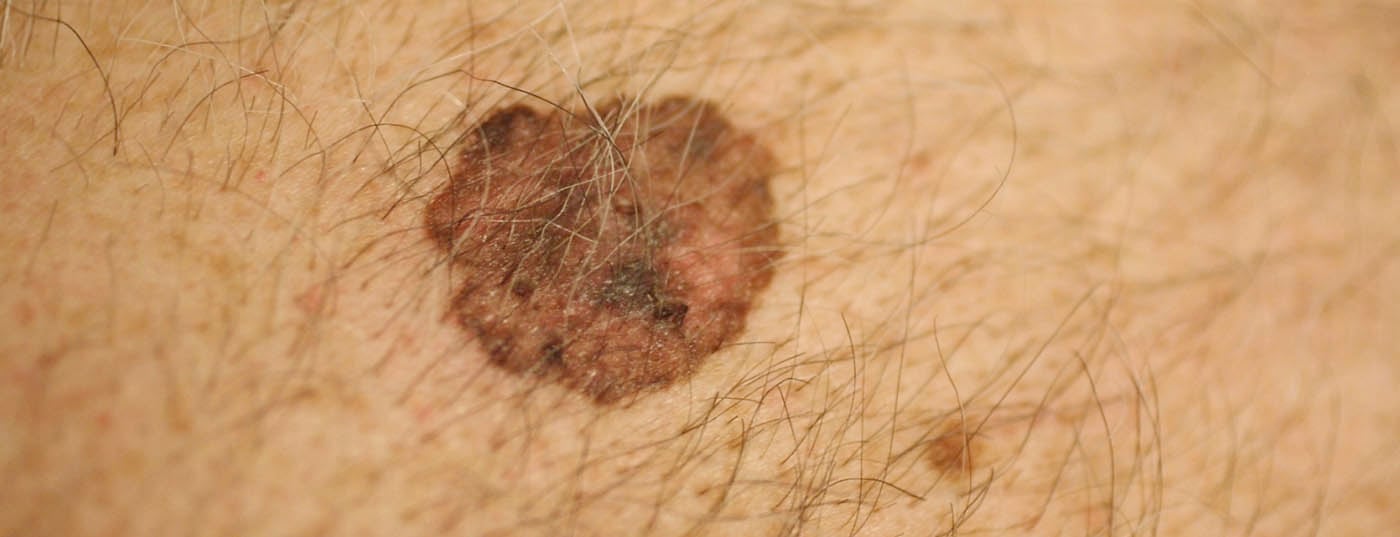
De acordo com os dados do estudo actual, mais de metade dos doentes que receberam tratamento adjuvante com o anticorpo anti-PD-1 estavam livres de recaídas ao fim de quatro anos. Esta é mais uma confirmação do historial desta opção terapêutica no tratamento de tumores melanocíticos em fase avançada com ou sem mutação de BRAF.
No campo das opções de tratamento para tumores melanocíticos, houve muitos avanços ao longo da última década. No passado, apenas estavam disponíveis quimioterapias para doentes com melanoma metastático, o que geralmente resultava apenas numa resposta menor e a curto prazo [1]. Actualmente, os padrões clínicos actuais para imunoterapia ou terapia direccionada em melanoma metastático incontestável são os anticorpos de bloqueio PD-1, a combinação do inibidor PD-1 nivolumab e o inibidor CTLA-4 ipilimumab, bem como a combinação dos inibidores BRAF e MEK [2]. Com estas opções terapêuticas, poder-se-ia conseguir uma melhoria significativa na sobrevivência a longo prazo dos pacientes em estado avançado.
Os inibidores de pontos de verificação são eficazes independentemente do estado de mutação do BRAF
Apenas cerca de 40-50% de todos os doentes com melanoma têm uma mutação BRAF adequadamente bloqueável [3]. Os inibidores de ponto de controlo imunitário estão disponíveis como opção de tratamento para doentes com melanoma, independentemente do estado de mutação. Dados recentes a longo prazo sobre inibidores de pontos de controlo imunitários são promissores. Com a combinação de ipilimumab e nivolumab, foram conseguidas taxas de sobrevivência significativamente melhores em doentes com metástases distantes não previsíveis em comparação com opções terapêuticas anteriores. Tanto as directrizes EADO/EORTC como as actuais directrizes ESMO recomendam a imunoterapia com inibidores de pontos de controlo como terapia de primeira linha para o melanoma metastásico [4,5]. Também no cenário adjuvante após cirurgia completa para metástases locorregionais, os anticorpos PD-1 nivolumab e pembrolizumab mostram aproximadamente uma redução para metade da taxa de recidivas, de modo a que não haja uma fase metastática distante.
CheckMate 238 – impressionante Dados de 4 anos sobre nivolumab
Os inibidores PD-1 podem ser utilizados adjuvantes em melanoma maligno de fase avançada III ou IV. Em 2018, o nivolumab foi aprovado pela EMA como terapia adjuvante. O principal objectivo da terapia adjuvante é o de prolongar a sobrevivência global. No entanto, como o benefício de tal terapia só pode ser provado após vários anos, a sobrevivência sem recorrência estabeleceu-se como outro ponto final. O estudo CheckMate 238 (síntese 1) demonstrou a superioridade da terapia adjuvante com nivolumab em comparação com ipilimumab nas fases IIIB/C e IV [6]. O braço nivolumab mostrou uma melhoria significativa da sobrevivência sem recidivas (RFS): 70% vs. 60% estavam livres de recidivas aos 12 meses, 66% vs. 53% aos 18 meses e 63% vs. 50% aos 24 meses. A sobrevivência sem recaída aos 36 meses foi de 58% com nivolumab vs. 45% com ipilimumab, e a toxicidade foi significativamente menor em comparação com o ipilimumab, com menos eventos adversos de grau 3-4 (14,4% vs. 45,9%) [7].

Os dados de 4 anos do estudo CheckMate 238 publicados em 2020 também foram favoráveis [8]. A superioridade do nivolumab em termos de sobrevivência sem recaída (RFS) em comparação com o ipilumab persistiu durante este período. Aos 4 anos, a RFS com nivolumab era de 51,7% (95% CI; 46,8-56,3) contra 41,2% (36,4-45,9) com ipilimumab (hazard ratio 0,71; 95% CI; 0,60-0,86; p=0,0003). A sobrevivência global (OS) a 4 anos foi de 77,9% (95% CI; 73,7-81,5) no grupo nivolumab e 76,6% (72,2-80,3) no grupo ipilimumab (HR 0,87; 95% CI; 0,66-1,14; p=0,31).
Estudo IMMUNED – resultados provisórios do tratamento combinado
Neste ensaio da fase II, 167 doentes da fase IV após ressecção completa sem evidência de metástase recente receberam nivolumab 3 mg/kg pb ou nivolumab 1 mg/kg pb em combinação com ipilimumab 3 mg/kg pb para quatro administrações seguidas de nivolumab 3 mg/kg pb e um terceiro grupo recebeu placebo [9]. Após 24 meses, a sobrevivência sem recaídas foi de 70% no tratamento combinado, 42% no grupo nivolumab e 14% com placebo.
Literatura:
- Ugurel S, et al: Survival of patients with advanced metastatic melanoma: the impact of novel therapies – update 2017. Eur J Cancer 2017; 83: 247-257.
- Hoeller C: Melanoma: As questões abertas dos padrões terapêuticos actuais são abordadas sucessivamente. Bússola Oncol 2020; 7: 117-118.
- Schadendorf D, et al: Lancet 2018; 392: 971-984.
- Garbe C, et al. : Eur J Cancer 2020; 126: 159-177.
- Michielin O, et al: Cutaneous melanoma: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-updagger. Ann Oncol 2019; 30(12): 1884-1901.
- Jeffrey S, et al: Adjuvant therapy with nivolumab (NIVO) versus ipilimumab (IPI) após ressecção completa do melanoma de fase III/IV: resultados actualizados de um ensaio de fase III (CheckMate 238). J Clin Oncol 2018; 36(15): 9502.
- Lamos C, Hunger RE. Inibidores Checkpoint – indicação e utilização em doentes com melanoma [Checkpoint inhibitors-indications and application in melanoma patients]. Z Rheumatol 2020;79(8): 818-825.
- Ascierto PA, et al: Adjuvant nivolumab versus ipilimumab na fase IIIB-C ressecada e melanoma da fase IV (CheckMate 238): resultados de 4 anos de um ensaio multicêntrico, duplo-cego, aleatorizado, controlado, fase 3. The Lancet – Oncology 2020; 21(11): 1465-1477.
- Zaremba A, et al: Imunoterapia no melanoma maligno. Internista 2020; 61, 669-675.
- Clinicaltrials.gov: https://clinicaltrials.gov/ct2/show/NCT02388906, (último acesso 07.04.2021)
PRÁTICA DA DERMATOLOGIA 2021; 31(2): 40