O prognóstico do carcinoma gástrico avançado é ainda extremamente desfavorável. Novas abordagens de tratamento são, portanto, urgentemente necessárias. Os resultados actuais sugerem que a terapia com inibidores de pontos de controlo poderia tornar-se mais importante num futuro próximo.
Até agora, a terapia inibidora de pontos de controlo para o cancro gástrico só tem sido aprovada na Suíça para casos muito avançados. Por exemplo, a aprovação para o nivolumab é limitada à terapia de terceira linha e a do pembrolizumab ao tratamento de tumores metastáticos com elevada instabilidade por microssatélite (MSI-H) ou reparação de desajustes de DNA defeituosos (dMMR) sem opções terapêuticas alternativas [2]. Os resultados de vários estudos dão agora razão para esperar que estas indicações sejam em breve alargadas.
Estado de coisas
Até agora, o cancro gástrico de fase IV tem sido o domínio da quimioterapia (Fig. 1) . Embora a quimioterapia possa melhorar o tempo de sobrevivência em comparação com o tratamento meramente de apoio, apenas melhora a sobrevivência em cerca de 6,7 meses [3]. Um mês adicional pode ser ganho usando combinações de quimioterapia, mas estas também implicam um aumento de toxicidade [3]. As quimioterapias duplas baseadas em platina e uma fluoropyrimidina são o padrão recomendado, o benefício das combinações triplas é avaliado de forma controversa [4].
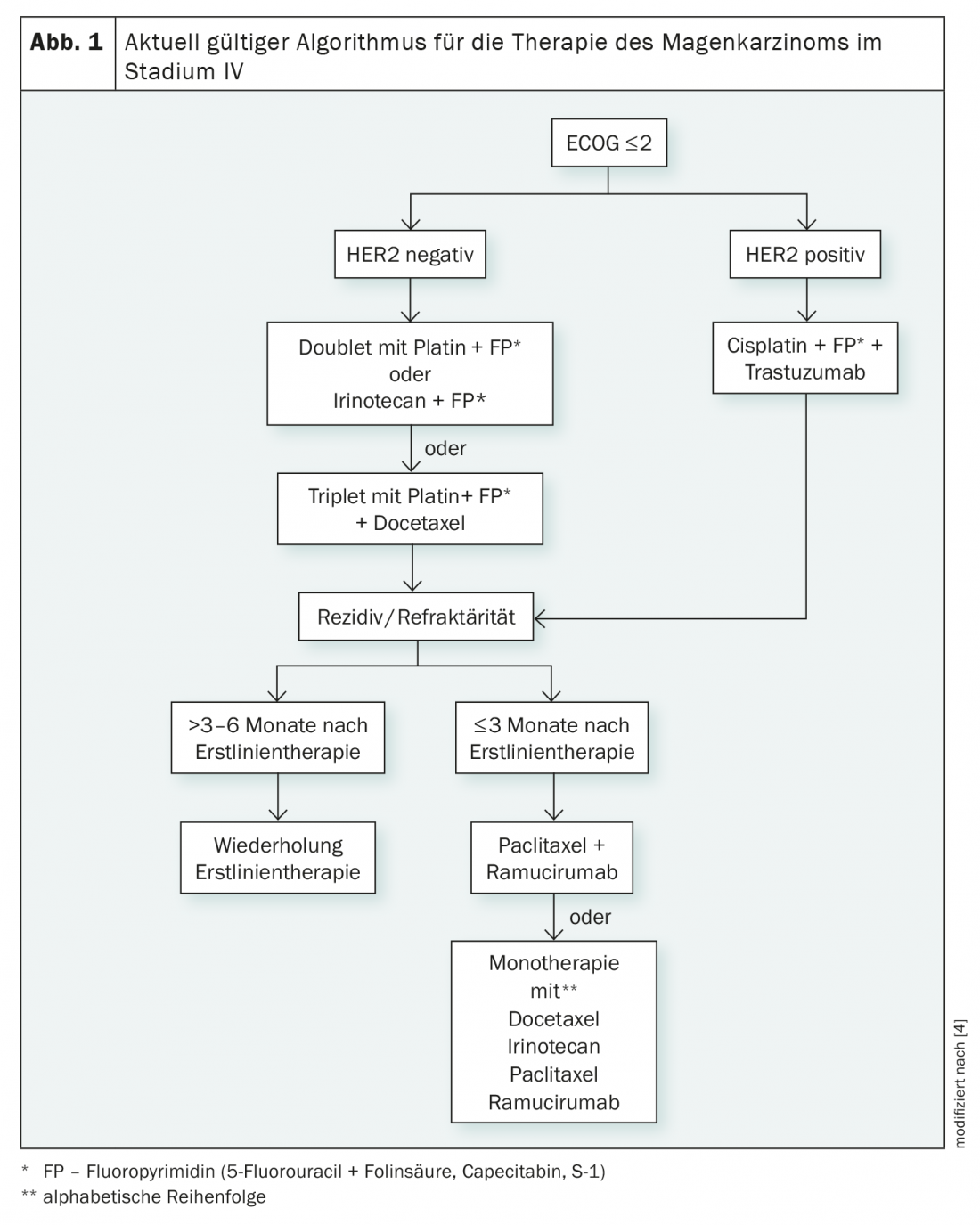
Embora estejam disponíveis terapias específicas para tumores HER2-positivos, esta opção não existe actualmente para casos HER2-negativos. A adição de trastuzumab à quimioterapia leva a um aumento da taxa de resposta e de sobrevivência global e sem progressão nos tumores HER2 positivos, que representam 10-15% dos cancros gástricos. O efeito é detectável, com um aumento da mediana de sobrevivência de pouco mais de dois meses, mas é pequeno [5]. Portanto, estamos longe de ser uma cura, independentemente do estatuto HER2.
Se a quimioterapia de primeira linha com ou sem trastuzumab falhar, o anticorpo ramucirumab dirigido contra VEGFR-2 (receptor do factor de crescimento endotelial vascular 2) pode ser utilizado. Isto causa um prolongamento da sobrevivência por cerca de 1,5 meses em comparação com o placebo [6]. Alternativamente, a quimioterapia também é possível na segunda linha. Os seus resultados são comparáveis aos do tratamento com ramucirumab. Os melhores resultados podem ser alcançados com combinações de paclitaxel e o anticorpo anti-VEGFR-2 [4].
Em relação a todas as outras linhas de terapia, não existem actualmente directrizes claras. As opções incluem ramucirumab, quimioterapia, trifluridina/tipiracil (TAS-102) e vários inibidores de pontos de controlo. Para além de melhorar as opções terapêuticas para o tratamento da primeira e segunda linha do cancro gástrico da fase IV, é portanto importante estabelecer um padrão terapêutico para a terceira linha ao longo dos próximos anos.
Inibidores de pontos de controlo como opção
Não só para um tal padrão de cuidados na terceira linha, os inibidores de pontos de controlo poderão em breve desempenhar um papel de apoio, mas também para complementar as opções em fases anteriores do tratamento. Estão actualmente em curso vários estudos que testam o uso do nivolumab, pembrolizumab e outros em todas as linhas de terapia (Tab. 1). Os resultados até agora indicam que o tratamento com inibidores de pontos de controlo não é, pelo menos, inferior à quimioterapia. Por exemplo, o ensaio KEYNOTE-062 relatou uma eficácia comparável do bloqueador PD-1 pembrolizumab como monoterapia de primeira linha, com uma tolerabilidade significativamente melhor [7]. Parece importante considerar diferentes subgrupos na análise da eficácia. Com uma expressão elevada de PD-L1, havia uma tendência clara para uma sobrevivência global mais longa com o tratamento pembrolizumab.
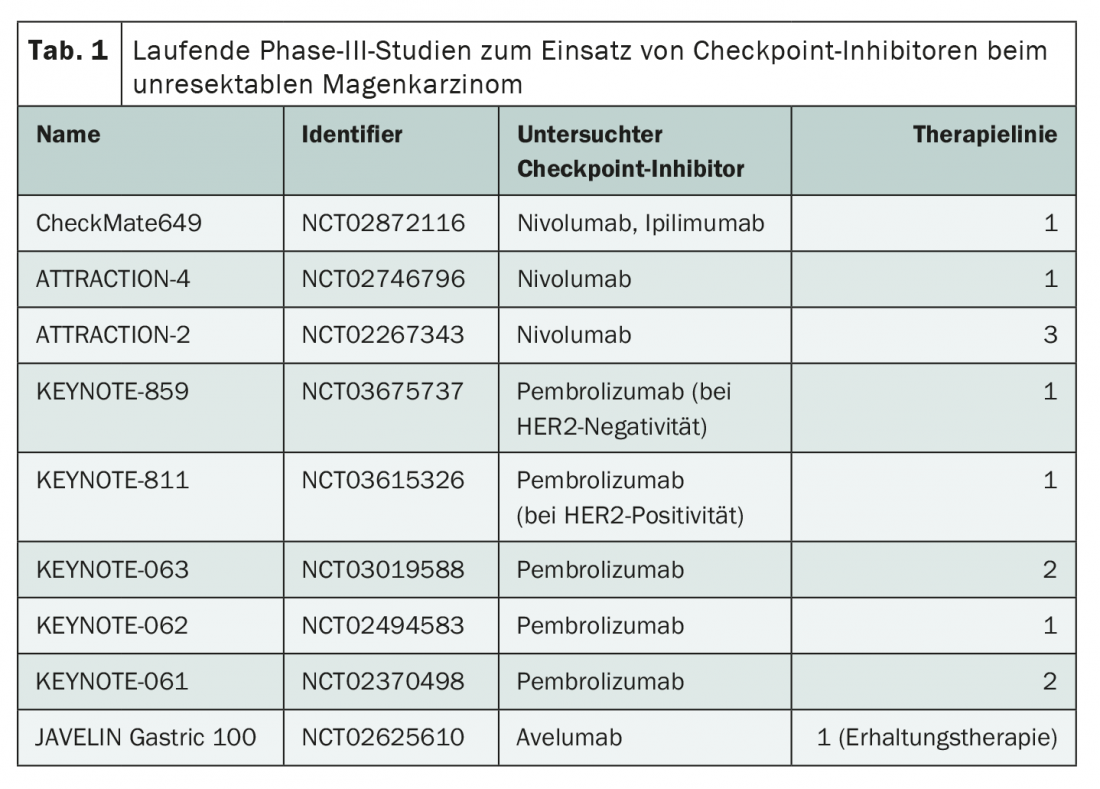
Os resultados de numerosos outros estudos sobre a utilização de inibidores de pontos de controlo na terapia de primeira linha estão pendentes, mas foram fornecidos conhecimentos interessantes em vários congressos em 2020. No Congresso da Sociedade Europeia de Oncologia Médica (ESMO), Markus Moehler apresentou os primeiros dados promissores do estudo CheckMate649, que inclui 1581 doentes [8]. Em comparação apenas com a quimioterapia, a expressão PD-L1 com a adição de nivolumabe mostrou uma melhoria significativa na sobrevivência global e na sobrevivência sem progressão. Um efeito menor – também significativo – também esteve presente no grupo total.
Além disso, foram apresentadas as primeiras conclusões do ensaio ATTRACTION-4, que também investiga a administração adicional de nivolumab na primeira linha, mas em 724 pacientes exclusivamente asiáticos [9]. Narikazu Boku relatou um aumento significativo na taxa de sobrevivência e resposta sem progressão com a adição de nivolumab à quimioterapia. No entanto, a sobrevivência global não foi significativamente prolongada de acordo com esta primeira análise.
Enquanto a administração adicional de imunoterapêutica é normalmente investigada para a terapia de primeira linha, a terapia inibidora de pontos de controlo por si só também está a ser discutida em linhas posteriores. No estudo ATTRACTION-2, por exemplo, já foi observada uma melhoria significativa no prognóstico com a utilização de nivolumab na terapia de terceira linha. A sobrevivência média foi aumentada de 4,14 para 5,26 meses [10].
Um olhar sobre o futuro
Mesmo que ainda seja necessário esperar por dados a longo prazo, o uso de imunoterapêutica no carcinoma gástrico avançado é uma opção válida. Entretanto, estão em curso numerosos grandes estudos sobre esta abordagem, alguns dos quais já produziram resultados – alguns dos quais são esperançosos. A administração de inibidores de pontos de controlo poderá em breve ser rotina na terapia de primeira linha do carcinoma gástrico não-resectável, especialmente em casos de expressão de PD-L1 e como coadjuvante da quimioterapia padrão. Em linhas de tratamento posteriores, está também em discussão o uso exclusivo de imunoterapêutica, que se tem mostrado superior à administração de placebo. Globalmente, a tolerabilidade parece ser superior à da quimioterapia.
A identificação de biomarcadores adequados facilitaria a selecção dos pacientes certos para a imunoterapia. Este tópico, que também afecta numerosas doenças para além do carcinoma gástrico, estará provavelmente connosco durante muito tempo. Os candidatos promissores são actualmente a expressão da PD-L1 em tumores e estroma (pontuação de positividade combinada), associação do vírus Epstein-Barr e instabilidade por microsatélite [11,12]. Estão actualmente em curso vários estudos também sobre este assunto.
Muitas questões permanecem sem resposta, tais como a aplicação exacta, a selecção ideal do paciente e também a própria eficácia. No entanto, poderá ser impossível imaginar em breve um tratamento para o carcinoma gástrico sem imunoterapia, desde que a aprovação seja prolongada. Com base nos dados disponíveis até agora, não se pode esperar um grande avanço, mas pequenos passos na direcção certa estão ao nosso alcance.
Literatura:
- Smyth EC, et al: Gastric cancer: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Anais de Oncologia. 2016; 27: v38-v49.
- Informação sobre medicamentos swissmedic. www.swissmedicinfo.ch (último acesso em 17.01.2021)
- Wagner AD, et al: Quimioterapia para o cancro gástrico avançado. Cochrane Database Syst Rev. 2017; 8: CD004064.
- Lordick F, et al.: Onkopedia – Carcinoma gástrico. www.onkopedia.com/de/onkopedia/guidelines/magenkarzinom (último acesso 17.01.2021)
- Bang YJ, et al: Trastuzumab em combinação com quimioterapia versus quimioterapia apenas para o tratamento do cancro de junção gástrico ou gastro-esofágico avançado HER2-positivo (ToGA): uma fase 3, rótulo aberto, ensaio controlado aleatório. Lanceta. 2010; 376(9742): 687-697.
- Fuchs CS, et al: monoterapia Ramucirumab para adenocarcinoma de junção gástrico ou gastro-esofágico avançado previamente tratado (REGARD): um ensaio internacional, randomizado, multicêntrico, controlado por placebo, fase 3. Lanceta. 2014; 383(9911): 31-39.
- Shitara K, et al: Eficácia e Segurança do Pembrolizumab ou Pembrolizumab Plus Quimioterapia vs Quimioterapia Sozinha para Pacientes com Cancro Gástrico de Primeira Linha, Avançado: O ensaio clínico aleatório KEYNOTE-062 Fase 3. JAMA Oncol. 2020; 6(10): 1571-80.
- Moehler M, et al.: Nivolumab (nivo) mais quimioterapia (quimioterapia) versus quimioterapia como tratamento de primeira linha (1L) para cancro gástrico avançado/câncer de junção gastroesofágica (GC/GEJC)/adenocarcinoma esofágico (EAC): Primeiros resultados do estudo CheckMate 649. Anais de Oncologia. 2020; 31: S1142-1215.
- Boku N, et al: Nivolumab mais quimioterapia versus quimioterapia apenas em pacientes com junção gástrica/gastroesofágica avançada ou recorrente (G/GEJ) cancro: estudo ATTRACTION-4 (ONO-4538-37) não tratada anteriormente. Anais de Oncologia. 2020; 31: S1142-1215.
- Chen L-T, et al: Um estudo fase 3 de nivolumab em cancro de junção gástrico ou gastroesofágico avançado previamente tratado (ATTRACTION-2): dados actualizados de 2 anos. Cancro gástrico: jornal oficial da Associação Internacional do Cancro Gástrico e da Associação Japonesa do Cancro Gástrico. 2020; 23(3): 510-519.
- Shitara K, et al: Pembrolizumab versus paclitaxel para cancro de junção gástrica ou gastro-esofágica avançada previamente tratada (KEYNOTE-061): um ensaio aleatório, de rótulo aberto, controlado, fase 3. Lanceta. 2018; 392(10142): 123-133.
- Kim ST, et al: Caracterização molecular abrangente das respostas clínicas à inibição do PD-1 no cancro gástrico metastásico. Nat Med. 2018; 24(9): 1449-1458.
- ClinicalTrials.gov. www.clinicaltrials.gov (último acesso em 17.01.2021)
InFo ONCOLOGy & HEMATOLOGy 2021; 9(1): 18-19