Em processos inflamatórios de doenças dermatológicas, pró…As citocinas inflamatórias desempenham um papel central. Por conseguinte, estão em foco abordagens terapêuticas quando se trata de quebrar caminhos de sinalização críticos. Para além dos anticorpos monoclonais, são cada vez mais utilizados medicamentos de pequenas moléculas dirigidos contra Janus kinases (JAK). Os primeiros inibidores JAK já foram aprovados para dermatite atópica e psoríase, mas os dados até à data também são promissores para outras doenças inflamatórias da pele, tais como vitiligo e alopecia areata.
Os inibidores JAK são uma adição valiosa às estratégias de tratamento sistémico de doenças de pele inflamatórias. “A via de sinalização JAK-STAT é uma chave essencial no tratamento de doenças imunológicas e inflamatórias crónicas. Se conseguirmos parar as cascatas de citocinas pró-inflamatórias, isto tem um efeito imediato na resposta inflamatória”, explica o Prof. Dr. med. Michael Hertl, presidente interino da Sociedade Alemã de Dermatologia (DDG) e director da Clínica de Dermatologia e Alergologia, Universidade Philipps e Hospital Universitário Marburg [1]. Ao ocupar os locais de atracagem do STAT, os inibidores JAK inibem a via de sinalização JAK-STAT e, portanto, a cascata de sinalização pró-inflamatória (Fig. 1).
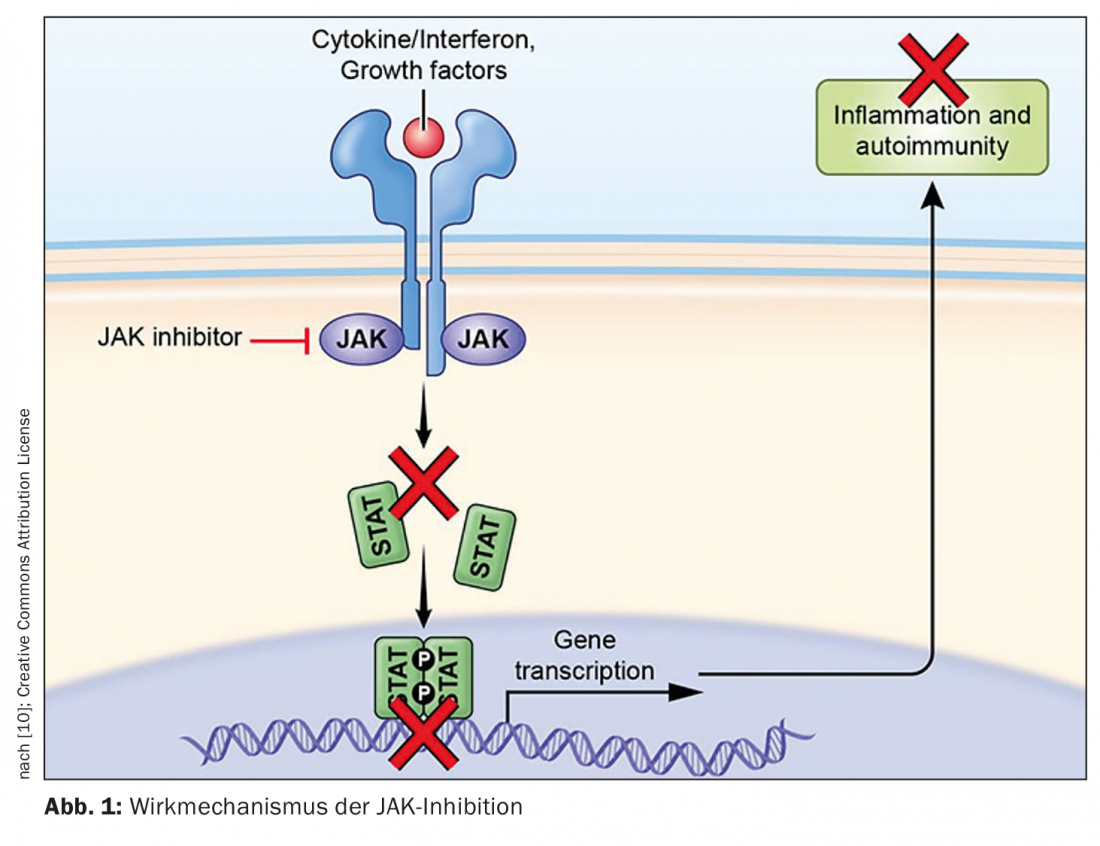
Vias específicas de sinalização intracelular são moduladas
A via desregulada e activada de Janus kinase (JAK)-signal transdutor e activador de transcrição (STAT) desempenha um papel fundamental na patogénese de muitas dermatoses inflamatórias. Quatro subunidades das Janus kinases (JAKs) ocorrem em células humanas: JAK1, JAK2, JAK3 e TYK2. A transdução de sinal intracelular de numerosas citocinas pró-inflamatórias é mediada por Janus kinases. Após a dimerização e auto-fosforilação, as proteínas STAT são recrutadas e fosforiladas, que controlam a transcrição dos genes alvo no núcleo. Janus kinases formam homo- ou heterodímeros, sendo que JAK2 também ocorre como homodímero [2]. A inibição farmacológica das JAK pode diminuir a actividade da via de sinalização JAK-STAT, impedindo a sinalização intracelular de várias citocinas pró-inflamatórias [1,2].
Os inibidores JAK conquistam diversas áreas de indicação dermatológica
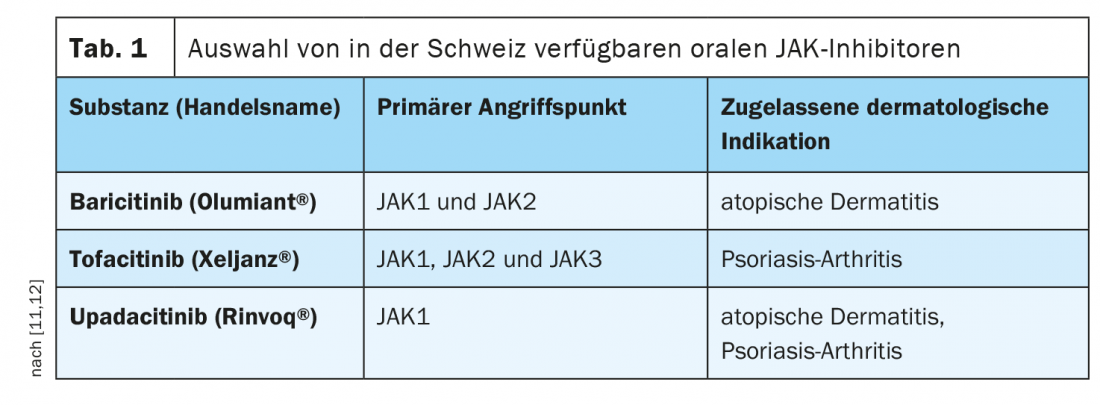
Para o tratamento de pacientes adultos com dermatite atópica moderada a grave, o baricitinibe (Olumiant®) foi aprovado na Suíça no primeiro trimestre do ano passado como primeiro representante do grupo de inibidores orais JAK, e em Novembro o upadacitinib (Rinvoq®) também eliminou o obstáculo à aprovação [4]. O Baricitinib em particular mostra uma elevada potência e selectividade para os subtipos JAK1 e JAK2, enquanto que com o upadacitinib JAK1 é o alvo principal (Tabela 1) . Com abrocitinibe, um terceiro representante dos inibidores de Janus kinase já foi aprovado na UE para esta indicação [5]. Para o tratamento de adultos com artrite psoriásica activa, o tofacitinibe (Xeljanz®) é aprovado na Suíça em combinação com um DMARD sintético convencional. Além disso, a eficácia da inibição de TYK2 com deucravacitinib-BMS986165 foi demonstrada num estudo de fase II em comparação com placebo [6].
Os dados para inibidores JAK também parecem promissores no que diz respeito à sua utilização em areata de alopecia. Numa meta-análise de 30 pequenos ensaios de inibidores JAK em alopecia areata, 72,4% dos doentes responderam à terapia, dos quais 45,7% tiveram uma boa resposta (50-100% de recrescimento capilar) e 21,4% tiveram uma resposta parcial (5-50% de recrescimento capilar) [7]. O ensaio ALLEGRO duplo-cego, controlado aleatoriamente, também investigou a eficácia dos inibidores JAK em mulheres e homens com alopecia areata. Todos os participantes tinham mais de 50% de queda de cabelo no couro cabeludo no início. O tratamento durante 24 semanas foi eficaz e bem tolerado: em comparação com o grupo placebo, os participantes no grupo verum tiveram queda de cabelo de 20% ou menos [8]. O perfil do efeito secundário dos inibidores JAK é claro, explica o Prof. Hertl. As infecções podem ocorrer mais frequentemente, por exemplo na zona do nariz e da garganta ou nas vias respiratórias. Foram também observadas infecções do tracto urinário, queixas gastrointestinais e acne. “Se uma infecção for aguda, a terapia com inibidores JAK deve evidentemente ser pausada”, diz o presidente do DDG. No entanto, isto funciona muito bem devido à aplicação oral e à curta meia-vida dos fármacos, acrescenta o perito [1]. Os últimos desenvolvimentos incluem inibidores JAK topicamente aplicáveis. Um inibidor JAK 1/2 administrado por creme melhorou a pele facial doente (repigmentação das lesões vitiligo) em cerca de 50% dos doentes contra 3% com placebo no tratamento do vitiligo auto-imune [9]. “Estes são resultados promissores que sugerem que este creme poderia ser uma opção terapêutica eficaz para pacientes com vitiligo”, sublinha o Prof. Hertl e acrescenta: “Os efeitos secundários conhecidos das pomadas de cortisona não foram observados” [1].
Congresso: Dermatologia compacta e prática
Literatura:
- “Pequenas moléculas contra neurodermatite, psoríase, vitiligo e queda de cabelo circular: inibidores JAK em doenças inflamatórias da pele expandem o espectro do tratamento”, Deutsche Dermatologische Gesellschaft e. V. (DDG), 31.01.2022
- Schwartz DM, et al: A inibição JAK como estratégia terapêutica para doenças imunitárias e inflamatórias. Nat Rev Drug Discov 2017; 16: 843-862.
- Damsky W, et al: O papel emergente dos inibidores de Janus kinase no tratamento de doenças auto-imunes e inflamatórias. J Allergy Clin Immunol 2021; 147: 814-826.
- Informação sobre drogas, www.swissmedicinfo.ch, (último acesso 07.03.2022)
- Klein B, Treudler R, Simon JC: inibidores JAK em dermatologia – pequenas moléculas, grande efeito? Visão geral do mecanismo de acção, resultados de estudos e possíveis efeitos adversos. J Dtsch Dermatol Ges 2022; 20(1): 19-25.
- Papp K, et al: Fase 2 do ensaio de inibição selectiva da tirosina kinase 2 na psoríase. N Engl J Med 2018; 379: 1313-1321.
- Phan K, Sebaratnam DF: inibidores JAK para a alopecia areata: uma revisão sistemática e meta-análise. J Eur Acad Dermatol Venereol 2019; 33: 850-856.
- King B, et al: Um estudo fase 2a randomizado, controlado por placebo para avaliar a eficácia e segurança dos inibidores orais de Janus kinase ritlecitinib e brepocitinib em alopecia areata: resultados de 24 semanas. J Am Acad Dermatol 2021; 85(2): 379-387.
- Rosmarin D, et al: creme de Ruxolitinibe para tratamento do vitiligo: um ensaio aleatório, controlado, fase 2. Lanceta 2020; 396: 110-120.
- Alexander M, et al: Jakinibs of All Trades: Inhibiting Cytokine Signaling in Immune-Mediated Pathologies. Farmacêuticos 2022; 15(1): 48.
- Bonnekoh H, Butze M, Metz M: Caracterização dos efeitos das novas terapias para o tratamento da dermatite atópica no prurido. J Dtsch Dermatol Ges 2022; 20(2): 150-156,
- Karonitsch T: Importância dos inibidores JAK (“pequeno é bonito”). J Metabolismo Mineiro Doenças Musculoesqueléticas 2021; 28: 78-83.
DERMATOLOGIE PRAXIS 2022; 32(2): 30-31 (publicado 20.4.22, antes da impressão).