Cerca de 2-4% da população em geral é afectada por rinossinusite crónica com pólipos nasais (CRSwNP) [1]. As opções de tratamento foram muito limitadas durante muito tempo, mas desde a aprovação da biologia para esta indicação, novos horizontes terapêuticos se abriram.
Os sintomas do CRSwNP podem afectar significativamente a qualidade de vida e levar a um elevado nível de sofrimento. A extensão das limitações é quase equivalente à insuficiência cardíaca ou asma [2]. Os factores de influência negativa incluem a asma, sensibilidade ao ácido acetilsalicílico e analgésicos não esteróides, colonização com Staphylococcus aureus e doenças alérgicas [2]. Até recentemente, o leque de opções terapêuticas era pequeno: o tratamento com corticosteróides intranasais representa a terapia medicamentosa permanente e básica. No entanto, na ausência de sucesso, a única opção era a escalada com esteróides sistémicos [3]. A terapia contínua em alta dose com esteróides sistémicos aumenta o risco de osteoporose, diabetes, eventos cardiovasculares e infecções [3]. Se o paciente não respondeu à terapia, a alternativa era a cirurgia. No entanto, a cirurgia endoscópica dos seios nasais está associada a taxas de recidiva muito elevadas, especialmente para os pólipos nasais, particularmente nos pacientes que se submetem a cirurgia para estes pólipos [4]. Quase uma em cada cinco (18,6%) requereu pelo menos mais uma intervenção cirúrgica [4]. Ainda não existe um padrão de ouro para avaliar o controlo de doenças na rinossinusite crónica, mas isto seria desejável tanto do ponto de vista clínico como do ponto de vista da investigação [2]. Entretanto, os biólogos encontraram o seu caminho para o tratamento do CRSwNP. Em Setembro de 2021, o mepolizumab (Nucala®) tornou-se o primeiro e único anticorpo anti-interleucina (IL)-5 a ser aprovado como terapia adicional aos corticosteróides intranasais para rinossinusite crónica grave com pólipos nasais [5].
IL-5 com um papel decisivo
No CRSwNP, há geralmente infiltração de mastócitos e polarização Th2 na mucosa das vias aéreas, para além da eosinofilia [7]. Os eosinófilos desempenham um papel particularmente importante nos pólipos nasais refratários ao tratamento [1,8–10]. Até 90% dos casos de pólipos nasais recorrentes são o resultado de inflamação eosinofílica [8,11,12]. IL-5 é a principal citocina para promover o crescimento, diferenciação, sobrevivência e recrutamento de eosinófilos em pólipos nasais [9,10,13]. Os doentes com níveis elevados de eosinófilos eram 3Å~ mais propensos a ter uma recidiva após a cirurgia do pólipo nasal do que os doentes com níveis mais baixos de eosinófilos [8]. O CRSwNP é uma comorbidade comum na asma eosinofílica grave (SEA) e cerca de 40% dos doentes com asma grave são afectados por pólipos nasais comorbidos [1,14]. Da mesma forma, a ocorrência de CRSwNP está associada à gravidade da asma: Na asma ligeira, apenas 10-30% têm CRSwNP, enquanto nos casos graves, 70-90% dos doentes são afectados [15]. A partir de uma análise de Howarth et al. mostra que o mepolizumabe de anticorpos anti-IL-5 melhorou a eficácia como terapia adicional em doentes com AAE e pólipos nasais comorbidos [16]. Neste grupo de pacientes, a taxa de exacerbação foi reduzida em 80% em comparação com placebo (vs. 49% em pacientes sem pólipos nasais). Um estudo recentemente publicado conseguiu provar que a inibição da IL-5 reduz a inflamação eosinofílica, bem como o tamanho dos pólipos nasais [1]. Em doentes refractários em que a terapia anterior, incluindo a cirurgia, não conseguiu melhorar os sintomas, o anticorpo monoclonal mepolizumab como terapia adicional mostrou uma melhoria sintomática com boa tolerabilidade [1]. Estes resultados baseiam-se no estudo SYNAPSE fase III (StudY em pacientes com NAsal Polyp para avaliar a Segurança e Eficácia do mepolizumab), que investigou a eficácia do mepolizumab vs. placebo como terapia adicional ao furo de mometasona intranasal durante um período de 52 semanas [1]. Os pacientes incluídos tiveram de ter sintomas graves de CRSwNP (pontuação VAS* >7) e foram submetidos a pelo menos uma cirurgia de pólipo nasal nos últimos 10 anos. Os pontos finais primários foram o escore endoscópico do pólipo nasal e o escore de obstrução nasal do VAS [1].
Melhorias significativas
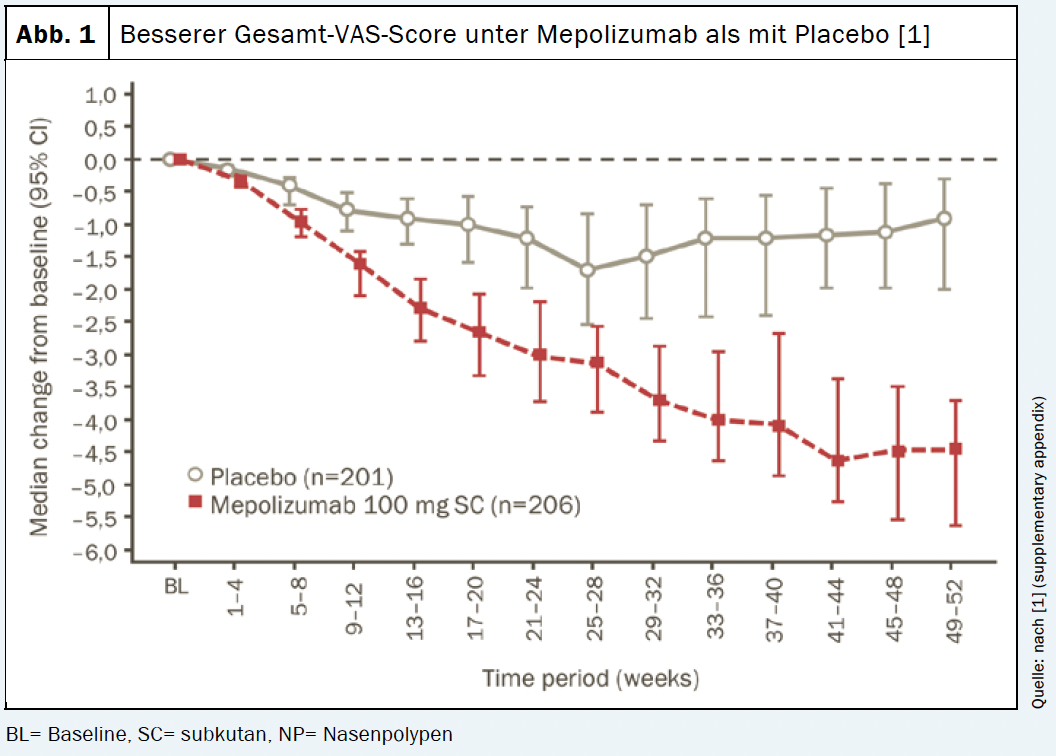
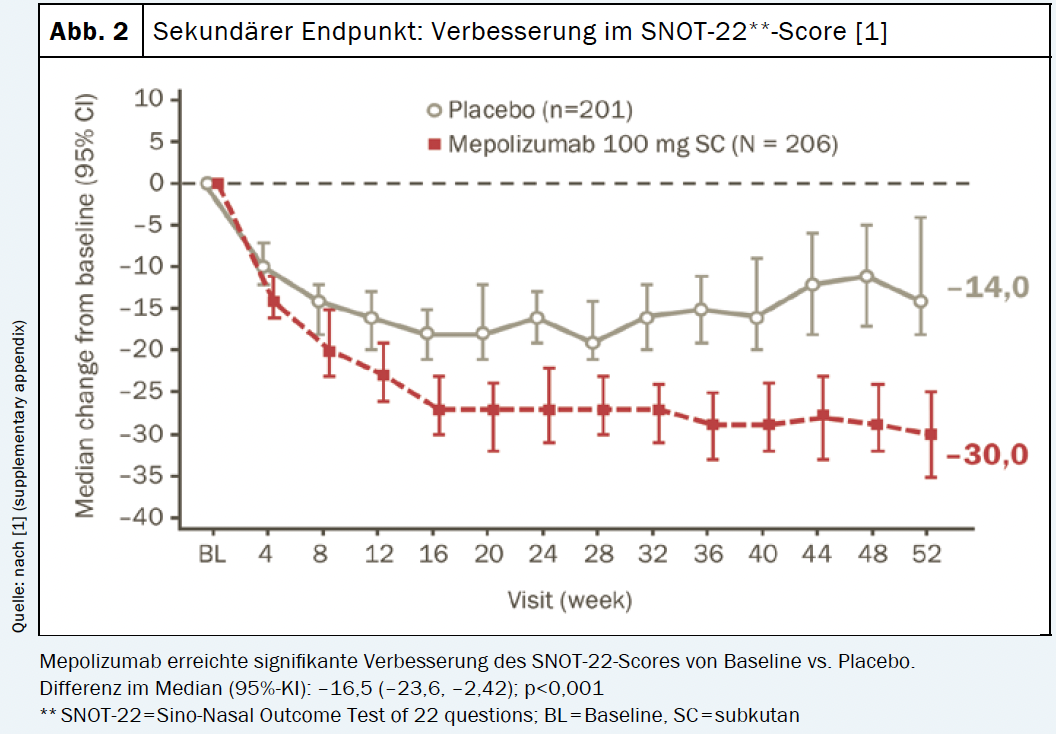
Foram atingidos tanto os pontos finais primários como secundários do estudo. O braço mepolizumab (n=206) mostrou melhorias significativamente maiores na pontuação total de pólipo nasal endoscópico na semana 52 e pontuação de VAS para obstrução nasal nas semanas 49-52 em comparação com placebo (n=201) [1]. Da mesma forma, o tempo para a primeira cirurgia de pólipo nasal provou ser significativamente mais longo com tratamento mepolizumab vs. tratamento placebo. O risco de necessitar de cirurgia durante o período de estudo de 12 meses foi reduzido em 57% em comparação com o grupo placebo [1]. 145 pacientes (70%) do braço mepolizumab alcançaram uma melhoria de >1 ponto na pontuação VAS para o total de sintomas em comparação com 99 pacientes (49%) do grupo placebo. A resposta com o anticorpo IL-5 persistiu durante todo o período de estudo (Fig. 1). Da mesma forma, foi observada uma melhoria significativa na pontuação de SNOT†-22 com uma redução de 30 pontos em relação à linha de base (Fig. 2). Além disso, o uso de esteróides sistémicos foi significativamente reduzido sob mepolizumab [1]. Em resumo, para pacientes com CRSwNP, o mepolizumab oferece uma opção de tratamento adicional direccionada para melhorar os sintomas clínicos e reduzir o uso de corticosteróides sistémicos. Além disso, em pacientes refractários, pode ser conseguida uma redução na necessidade de cirurgia de polipo nasal repetida [1].

Os profissionais podem solicitar as referências mencionadas à GSK AG.
Impressão
Texto/Editorial: Jens Dehn, Mirjam Peter
Fonte: Hopkins C: Mepolizumab para pólipos nasais – Evidência actual no contexto da prática clínica. Workshop Interlaken, 12 de Novembro de 2021. Exoneração de Responsabilidade de Marcas: As marcas comerciais são propriedade do grupo de empresas GSK ou estão licenciadas a este grupo.
©2021 Grupo de empresas GSK ou o seu licenciador. GlaxoSmithKline AG, Talstrasse 3-5, 3053 Münchenbuchsee, Suíça
Este artigo foi escrito com o apoio financeiro da GlaxoSmithKline Schweiz AG.
© Prime Public Media AG, Zurique 2021
Breve informação técnica NUCALA
®
:
Nucala (liofilizado para a preparação de uma solução de injecção para administração de s.c., solução de injecção numa caneta pronta a usar para s.c.) administração, solução de injecção numa caneta pré-cheia para administração de s.c., solução de injecção numa seringa pré-cheia para administração de s.c. (liofilizado para a preparação de uma solução de injecção para administração de s.c., solução de injecção numa seringa pronta a encher para administração de s.c.). administração). T: Mepolizumab. I: Asma eosinófila grave: Terapia adjunta em adultos e adolescentes com 12 anos ou mais, com os seguintes critérios Pelo menos. 2 exacerbações nos últimos 12 meses na terapia padrão (ICS de alta dose e terapia de manutenção adicional) e/ou necessidade de corticosteróides sistémicos, e contagem de eosinófilos sanguíneos ≥ 0,15 G/l no início do tratamento ou ≥ 0,3 G/l nos últimos 12 meses. Rinossinusite crónica com pólipos nasais (CRSwNP): terapia adjunta aos corticosteróides intranasais em adultos com 18 anos ou mais com CRSwNP grave que não pode ser adequadamente controlada com corticosteróides sistémicos intermitentes e/ou intervenção cirúrgica (caneta pré-carregada, seringa pré-carregada). Granulomatose eosinofílica com poliangite (EGPA): Terapia adjunta em adultos com 18 anos ou mais, com os seguintes critérios: EGPA recorrente ou refractária, estabilização prévia da doença com corticosteróides sistémicos, ou tratamento de manutenção necessária com corticosteróides sistémicos e possivelmente imunossupressores com esteróides. Síndrome de Hipereosinofilia (HES): terapia adjunta para o tratamento de adultos e adolescentes com 12 anos ou mais com HES sem fusão FIP1L1-PDGFRα (F/P HES negativa). D: Asma eosinófila grave e CRSwNP: 100 mg Nucala s.c. 1Å~ cada 4 semanas. EGPA e HES: 300 mg Nucala s.c. 1Å~ de 4 em 4 semanas. KI: Hipersensibilidade a um ingrediente. C/V: Não deve ser utilizado para o tratamento da asma aguda exacerbações. Em caso de asma persistente descontrolada ou de agravamento, contactar o médico. Sem descontinuação abrupta dos corticosteróides. Podem ocorrer reacções de hipersensibilidade local e sistémica (tipo imediato e retardado) sob Nucala. Tratar qualquer infestação de helmintos antes de dar Nucala. IA: Não existem estudos sobre as interacções com outros medicamentos. S/S: Gravidez: Não utilizar a menos que seja claramente necessário. Amamentação: Interromper a amamentação ou terapia com Nucala durante a amamentação. UW: Muito comum: dor de cabeça. Comum: reacções locais (incluindo dor, eritema, prurido, ardor), eczema, febre, congestão nasal, faringite, infecções do tracto respiratório inferior, infecções do tracto urinário, dor abdominal superior, dores nas costas. Estudo HES: muito comum: infecções. Experiência pós-comercialização: rara: Hipersensibilidade (incluindo anafilaxia). P: Liofilizado para a preparação de uma solução de injecção para uso s.c. Administração: frasco de 100 mg Å~1. Solução de injecção para administração de s.c. Administração: 100 mg Å~1 caneta pré-cheia, 100 mg Å~1 seringa pré-cheia. AK: B. Kassenzul.ssig (Lim). Estado da informação: Novembro de 2020 (liofilizado), Outubro de 2021 (caneta pronta a usar, seringa pronta a encher). GlaxoSmithKline AG, 3053 Münchenbuchsee. Informação detalhada pode ser encontrada em www.swissmedicinfo.ch. É favor comunicar reacções adversas aos medicamentos em pv.swiss@gsk.com. Abreviaturas: CRSwnP, rinossinusite crónica grave com polipose nasal; EGPA, granulomatose eosinófila com poliangite; HES, síndrome de hipereosinofilia; SEA: asma eosinófila grave; VAS, Visual Analogue Scale Referências: 1. SmPC Nucala 10/2021. www.swissmedicinfo.ch. 2. cintura. C et al. Mepolizumab numa população com grave asma eosinofílica e dependência de corticosteróides resulta de um programa francês de acesso precoce. Eur Respir J 2020; 55 :11. Han JK, Bachert C, Fokkens W et al. Mepolizumab para rinossinusite crónica com pólipos nasais (SYNAPSE): um ensaio aleatório, duplo-cego, controlado por placebo, fase 3. Lancet Respir Med. 2021; publicado online a 16 de Abril. 4 Roufosse F, Kahn JE, Rothenberg ME, et al. Eficácia e segurança do mepolizumab na síndrome hipereosinofílica: um ensaio fase III, aleatório, controlado por placebo. J Allergy Clin Immunol. 2020. 5 Wechsler ME, et al. Mepolizumab ou Placebo para Granulomatose Eosinófila com Poliangite. N Engl J Med 2017; 376:1921-1932. Os profissionais podem solicitar as referências mencionadas à GlaxoSmithKline AG. As marcas comerciais pertencem ao grupo de empresas GSK ou são licenciadas a este grupo. ©2021 Grupo de empresas GSK ou o seu licenciador. GlaxoSmithKline AG, Talstrasse 3-5, 3053 Münchenbuchsee, Suíça PM-CH-MPL-ADVT-210005-11/2021
Literatura:
Han JK, Bachert C, Fokkens W, et al: Mepolizumab para rinossinusite crónica com pólipos nasais (SYNAPSE): um ensaio aleatório, duplo-cego, controlado por placebo, fase 3. Lancet Respir Med 2021; 10: 1141-1153.
Fokkens WJ, Lund VJ, Hopkins C et al: European Position Paper on Rhinosinusitis and Nasal Polyps 2020. Rhinology 2020; Suppl 29: 1-464.
3 Stuck BA, Beule A, Jobst D et al. Guia para a “rinossinusite” – versão longa: Guia S2k do Colégio Alemão de Clínicos Gerais e Médicos de Família e da Sociedade Alemã de Oto-Rhino-Laryngologia, Cirurgia da Cabeça e do Pescoço. ENT 2018; 66 (1): 38-74; doi: 10.1007/s00106-017-0401-5.
Loftus CA, Soler ZM, Koochakzadeh S, et al: Taxas de cirurgia de revisão em rinossinusite crónica com pólipos nasais: meta-análise dos factores de risco. Int Forum Allergy Rhinol 2020; 10 (2): 199-207.
5. informação especializada Nucala, 10/2021, www.swissmedicinfo.ch
6 Gleich GJ: Mecanismos da inflamação associada ao eosinofil. J Allergy Clin Immunol 2000; 105(4): 651-663.
7ª Directriz S2k Rinossinusite, AWMF Nº de registo. 017 /049 e 053-012, www.awmf.org/uploads/tx_szleitlinien/017-049_und_053-012l_S2k_Rhinosinusitis_2019-04.pdf
Tosun F, et al: Relação entre a taxa de recorrência pós-operatória e a densidade eosinófila dos pólipos nasais. Ann Otol Rhinol Laryngol. 2010; 119(7): 455-459.
9 Bachert C, Gevaert P, Holtappels G, et al: A IgE total e específica nos pólipos nasais está relacionada com a inflamação eosinofílica local. J Allergy Clin Immunol 2001; 107(4): 607-614.
10 Bachert C, Wagenmann M, Hauser U, Rudack C: a síntese de IL-5 não está impregnada em tecido de pólipo nasal humano. J Allergy Clin Immunol 1997; 99(6.1): 837-842.
11 Lou H, Meng Y, Piao Y, et al: Fenotipagem celular da rinossinusite crónica com pólipos nasais. Rinologia 2016; 54: 150-159.
12 Fujieda S, Imoto Y, Kato Y, et al: Eosinophilic chronic rhinosinusitis. Allergol Int. 2019;68(4): 403-412.
13 Hulse KE, et al: Patogénese da polipose nasal. Clin Exp Allergy 2015; 45(2): 328-346.
14 Harrison T, et al: Real-world mepolizumab in the prospective severe asthma REALITI-A study: initial analysis. Eur Respir J 2020; 56(4): 200015.
15. Klimek L, Förster-Ruhrmann U, Becker S, et al.: Position Paper: Application of Biologics in Chronic Rhinosinusitis with Polyposis nasi (CRSwNP) in the German Health Care System – Recommendations of the Association of German Allergists (AeDA) and the WG Clinical Immunology, Allergology and Environmental Medicine and Rhinology and Rhinosurgery of the German Society of otolaryngology, Head and Neck Surgery (DGHNOKHC). Laryngorhinootology 2020; 99(08): 511-527.
16 Howarth P, Chupp G, Nelsen LM et al: Severe eosinophilic asthma with nasal polyposis: Um fenótipo para melhores resultados sinonasais e asmáticos com terapia de mepolizumab. J Allergy Clin Immunol 2020; 145: 1713-1715.












