O Atezolizumab permite a sobrevivência a longo prazo de alguns doentes com cancro do pulmão pré-tratados. O Alectinib também ajuda os pacientes a viver uma vida diária mais tolerável, reduzindo os sintomas da doença a longo prazo. Estes são os resultados de dois estudos ELCC.
O ensaio da fase II denominado POPLAR randomizou 287 pacientes de um total de 13 países. Todos eles sofriam de uma forma avançada de cancro de pulmão de células não pequenas (NSCLC) e já tinham recebido tratamento para o mesmo. Uma parte foi submetida a imunoterapia com o anticorpo anti-PD-L1 atezolizumab, a outra quimioterapia com docetaxel.
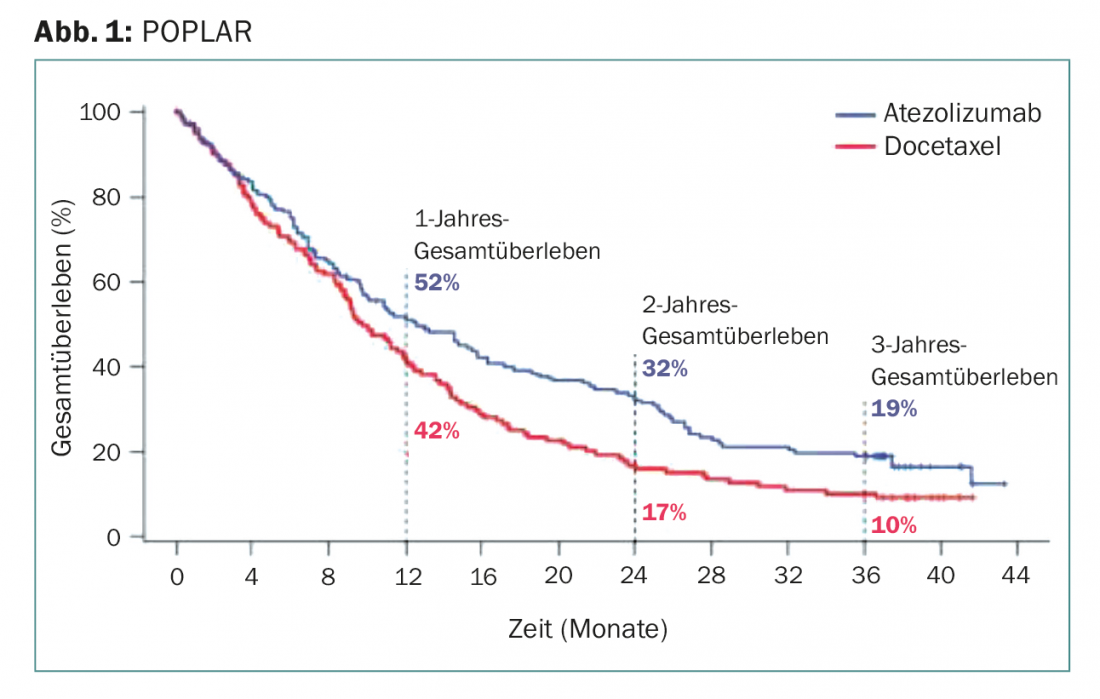
Após dois e três anos – o seguimento mais longo da imunoterapia PD-L1 neste contexto até à data – o atezolizumab foi significativamente superior ao docetaxel (Fig. 1):
- Cerca de um terço do primeiro grupo ainda estava vivo após dois anos. No grupo do docetaxel, a taxa de sobrevivência foi uma boa metade mais baixa (16,6%).
- Mesmo após três anos, a imunoterapia ainda aumentou duas vezes a sobrevivência, de 10% com docetaxel para 18,7% com atezolizumab.
- O benefício foi independente da expressão e histologia PD-L1 prospectivamente avaliada (carcinoma escamoso de células ou não). Mesmo os doentes com expressão PD-L1 em menos de 1% das células tumorais e imunitárias ainda beneficiaram.
Além disso, há um triplo aumento da duração da resposta (com a mesma elevada taxa de resposta global de 15%) e menos eventos adversos com imunoterapia. A substância em estudo foi bem tolerada (o suficiente) para ser administrada durante vários anos. Assim, com a imunoterapia, alguns pacientes são agora considerados “sobreviventes do cancro do pulmão de longa duração”, estão de volta ao trabalho e têm uma qualidade de vida mais ou menos boa.
Os dados de eficácia do POPLAR foram confirmados no ensaio da fase III chamado OAK [1].
Que conclusões podem ser tiradas do POPLAR?
Com base nas análises de subgrupos do POPLAR, o atezolizumab parece ser uma opção para todos os pacientes com NSCLC avançado. No entanto, isto também torna difícil prever quais os pacientes que beneficiarão do medicamento a longo prazo. Não se sabe exactamente quem é este quinto dos pacientes que ainda estão vivos após três anos e como se caracterizam a si próprios. A definição de biomarcadores preditivos continua assim a ser um desafio.
Ao mesmo tempo, o número de aproximadamente um quinto dos sobreviventes de 3 anos representa um resultado extremamente bom neste colectivo. O Atezolizumab é assim elevado às fileiras de agentes com as mais altas taxas de sobrevivência de sempre em doentes com cancro do pulmão previamente tratados. Antes da imunoterapia, não havia praticamente sobreviventes a longo prazo com o NSCLC. Agora, à luz de novos dados de estudo, isto é possível pela primeira vez. Os resultados POPLAR são ladeados e apoiados pelas taxas de sobrevivência comparáveis de 3 e 5 anos de estudos com os anticorpos anti-PD1 pembrolizumab e nivolumab [2]. Sob esta última, cerca de 15% dos pacientes ainda estavam vivos após cinco anos (fase I), que normalmente já é considerada “curada” no cancro. POPLAR tem relevância crítica como um grande ensaio aleatório que agora confirma o benefício de sobrevivência a longo prazo para a abordagem PD-L1.
Se olharmos para toda a situação de estudo, há muito a dizer hoje em dia a favor de cada paciente NSCLC com formulários avançados que recebem imunoterapia. Finalmente, a hipótese de sobrevivência de 5 anos parece ser de cerca de 1:6. Infelizmente, como tantas vezes em tempos recentes, as questões financeiras permanecem em aberto. Como poderia o nosso sistema de saúde sustentar uma prescrição mais ampla de imunoterapia? Provavelmente só se fosse possível identificar pacientes que certamente não beneficiariam de tal estratégia. Agora, porém, a expressão PD-L1 no POPLAR provou mais uma vez ser um biomarcador inadequado. Mesmo que indivíduos com níveis de expressão extremamente baixos continuem a beneficiar da sobrevivência – só isso não pode servir para os excluir. Actualmente, a investigação de biomarcadores está em pleno andamento. No futuro, é provável que um “pacote” de biomarcadores seja cada vez mais utilizado, possivelmente incluindo a carga de mutação tumoral. Contudo, no que diz respeito à combinação de biomarcadores, há necessidade de estudos realizados em populações semelhantes às dos estudos do atezolizumabe, pembrolizumabe e nivolumabe acima mencionados. Os sobreviventes a longo prazo teriam portanto de ser definidos com precisão (demograficamente, história do tabagismo, carga de mutação tumoral, resposta imunitária, nível de expressão, etc.) e, numa próxima etapa, quais os biomarcadores (juntos) que são mais preditivos.
O Atezolizumab (Tecentriq®) está actualmente aprovado na Suíça para o tratamento de pacientes com NSCLC localmente avançado ou metastásico, após quimioterapia prévia. O tratamento requer a aprovação dos custos pela seguradora de saúde após consulta prévia com o médico legista.
Notícias sobre o ALEX
O ensaio ALEX [3], publicado em Agosto do ano passado, investigou o inibidor selectivo ALK e RET kinase alectinib na fase III. Este é considerado um inibidor da “próxima geração” de tirosina quinase. Numa amostra de 303 pacientes NSCLC com doença avançada anteriormente não tratada e mutação oncogénica do condutor (ALK), o agente de investigação mostrou eficácia e segurança/tolerabilidade superiores em comparação com o anterior inibidor padrão de tirosina quinase crizotinibe. Globalmente, cerca de 4% de todos os pacientes do NSCLC são ALK-positivos e, portanto, mais susceptíveis às metástases do SNC. Entre outras coisas, o risco de progressão ou morte foi significativamente reduzido em mais de 50% no estudo cabeça a cabeça, e a progressão do SNC foi significativamente menos frequente (12% vs. 45%, HR 0,16, p<0,001).
No ELCC em Genebra, o foco estava agora nos resultados do ALEX que podiam ser avaliados pelos próprios pacientes, ou seja, o peso da doença, a tolerabilidade dos sintomas e a qualidade de vida relacionada com a saúde. Para este fim, foi utilizado o questionário validado QLQ-C30 da EORTC com o apêndice modular QLQ-LC13, que foi especificamente desenvolvido para doentes com cancro do pulmão. Os sintomas de doença correspondentes podem assim ser apurados num questionário de 13 partes. As características de base dos doentes avaliáveis (cerca de dois terços cada um dos grupos de alectinibe e crizotinibe) eram comparáveis. Os pacientes completaram os questionários na linha de base e depois mensalmente, e no prazo de um mês após a saída do estudo (embora o tratamento raramente tenha sido interrompido devido ao agravamento dos sintomas) e após a progressão da doença.
Ambos os agentes conduziram a uma melhoria significativa dos sintomas da doença. Olhando para o complexo de sintomas de tosse, dispneia e dor no peito (que é normalmente um fardo elevado para os doentes avançados com cancro do pulmão), o tempo médio de agravamento dos sintomas foi mais ou menos o mesmo para ambos os agentes. No entanto, em média, os pacientes constataram que os seus sintomas de base melhoraram durante um período mais longo quando receberam alectinibe em vez de crizotinibe (consistente com os dados benéficos de PFS com alectinibe). A tosse, por exemplo, melhorou clinicamente de forma significativa numa média de 96 semanas (em comparação com 84 semanas no grupo de comparação), dores no peito durante 96 vs. 80 semanas, dores noutros locais ou fadiga durante 96 vs. 68 semanas em cada caso.
A qualidade de vida foi clinicamente significativamente melhorada em ambos os grupos, mas durante um período mais longo com alectinibe, 88 semanas contra 68 semanas. Um agravamento significativo em termos de sintomas associados ao tratamento, tais como náuseas, vómitos, diarreia, perda de apetite, disfagia, neuropatia periférica, etc., ocorreu em menos doentes com alectinibe do que em doentes com crizotinibe. Globalmente, os dados documentados pelos próprios pacientes eram consistentes com os dados de segurança previamente publicados e confirmam a melhor tolerância com o alectinib. São também bem compatíveis com os dados de eficácia: ambos os braços tinham mostrado taxas de resposta comparáveis, embora com uma duração de resposta mais longa sob alectinibe. Do mesmo modo, a qualidade de vida e os sintomas do cancro do pulmão foram melhorados em ambos os braços, mas as melhorias duraram mais tempo com o alectinibe.
Os pacientes com ALK-positivo NSCLC têm um risco particularmente elevado de desenvolver múltiplas metástases cerebrais, como mencionado acima. As opções de radiação são limitadas para esta sintomatologia angustiante, e as funções cognitivas também podem ser prejudicadas. O Alectinib está associado a um elevado nível de protecção contra as metástases cerebrais, reduz a probabilidade de que uma metástase cerebral existente progrida. Os mecanismos por detrás disto estão actualmente a ser investigados [4]. Se apenas os pacientes com metástases do SNC na linha de base fossem considerados na sub-análise dos dados dos pacientes apresentados no ELCC, o alectinib também era superior: As vantagens no que diz respeito à progressão resp. a forte actividade do SNC com a substância activa reflectiu-se consequentemente na vida quotidiana dos pacientes. Por um lado, a qualidade de vida diminuiu menos frequentemente, por outro lado, cerca de metade do número de pessoas afectadas referiu uma deterioração cognitiva (17,9% vs. 34,6% na semana 32).
Por conseguinte, há muito a dizer sobre um novo padrão de tratamento na primeira linha de tratamento de pacientes NSCLC positivos ALK em fases avançadas. Para este último grupo, a Alecensa® é actualmente também aprovada na Suíça, mas de acordo com o Limitatio apenas após a progressão sob crizotinibe ou no caso de intolerância ao crizotinibe e após aprovação de custos pela seguradora de saúde após consulta prévia com o oficial médico.
O facto de os dados dos doentes serem sistematicamente recolhidos e avaliados num grande ensaio de fase III é de importância central. A qualidade de vida e o peso da doença são possivelmente ainda mais importantes na situação paliativa do que a sobrevivência prolongada per se (e “a qualquer preço”). As substâncias activas que não só prolongam o tempo de vida restante, mas também fazem com que valha a pena viver, são por isso altamente bem-vindas.
Fonte: ELCC 2018 (European Lung Cancer Congress), 11-14 de Abril de 2018, Genebra
Literatura:
- Rittmeyer A, et al: Atezolizumab versus docetaxel em doentes com cancro do pulmão não-celular (OAK) previamente tratado: uma fase 3, rótulo aberto, ensaio multicêntrico randomizado e controlado. Lancet 2017 21 de Janeiro; 389(10066): 255-265.
- Vokes EE, et al: Nivolumab versus docetaxel em cancro do pulmão avançado de células não pequenas previamente tratadas (CheckMate 017 e CheckMate 057): actualização de 3 anos e resultados em doentes com metástases hepáticas. Ann Oncol 2018 Fev 2. DOI: 10.1093/annonc/mdy041 [Epub ahead of print].
- Peters S, et al: Alectinib versus crizotinib em Câncer de Pulmão Não-Positivo de Pequenas-Células ALK não tratado. N Engl J Med 2017 Ago 31; 377(9): 829-838.
- Kodama T, et al: Actividade antitumoral do inibidor selectivo ALK alectinib em modelos de metástases intracranianas. Cancer Chemother Pharmacol 2014 Nov; 74(5): 1023-1028.
InFo ONCOLOGY & HEMATOLOGY 2018; 6(3) – publicado 8.6.18 (antes da impressão).