As doenças glomerulares são causas importantes de insuficiência renal em fase terminal. Patogenicamente, os processos imuno-mediados estão em primeiro plano. Graças ao avanço do conhecimento da fisiopatologia e dos métodos modernos de engenharia genética, há esperança de uma terapia que seja tão direccionada quanto possível e que tenha poucos efeitos secundários. As novas abordagens de tratamento das doenças glomerulares são brevemente destacadas neste artigo e algumas substâncias são apresentadas como exemplos.
As glomerulopatias (GP) são uma causa importante de insuficiência renal crónica e terminal. Nos EUA, a nefropatia diabética ocupa o primeiro lugar e o GP não diabético o terceiro lugar na etiologia da insuficiência renal terminal (TNV). A patogénese deste grupo heterogéneo de doenças é maioritariamente imuno-mediada. Os princípios gerais da terapia incluem a terapia de apoio, bem como a terapia específica em certos casos. Isto consiste geralmente em imunossupressores relativamente sem alvo, com toxicidade por vezes cumulativa, o que se revela problemático no GP, que muitas vezes recai. Graças à crescente elucidação dos processos patogénicos de diferentes GP nas últimas décadas, bem como dos métodos modernos de engenharia genética, há esperança de uma terapia orientada para o patomecanismo.
Esta panorâmica destina-se a nomear novos desenvolvimentos na terapia de doenças glomerulares sem pretender ser completa. Serão destacados temas relevantes para a prática, bem como abordagens e conceitos terapêuticos inovadores.
Terapia de apoio
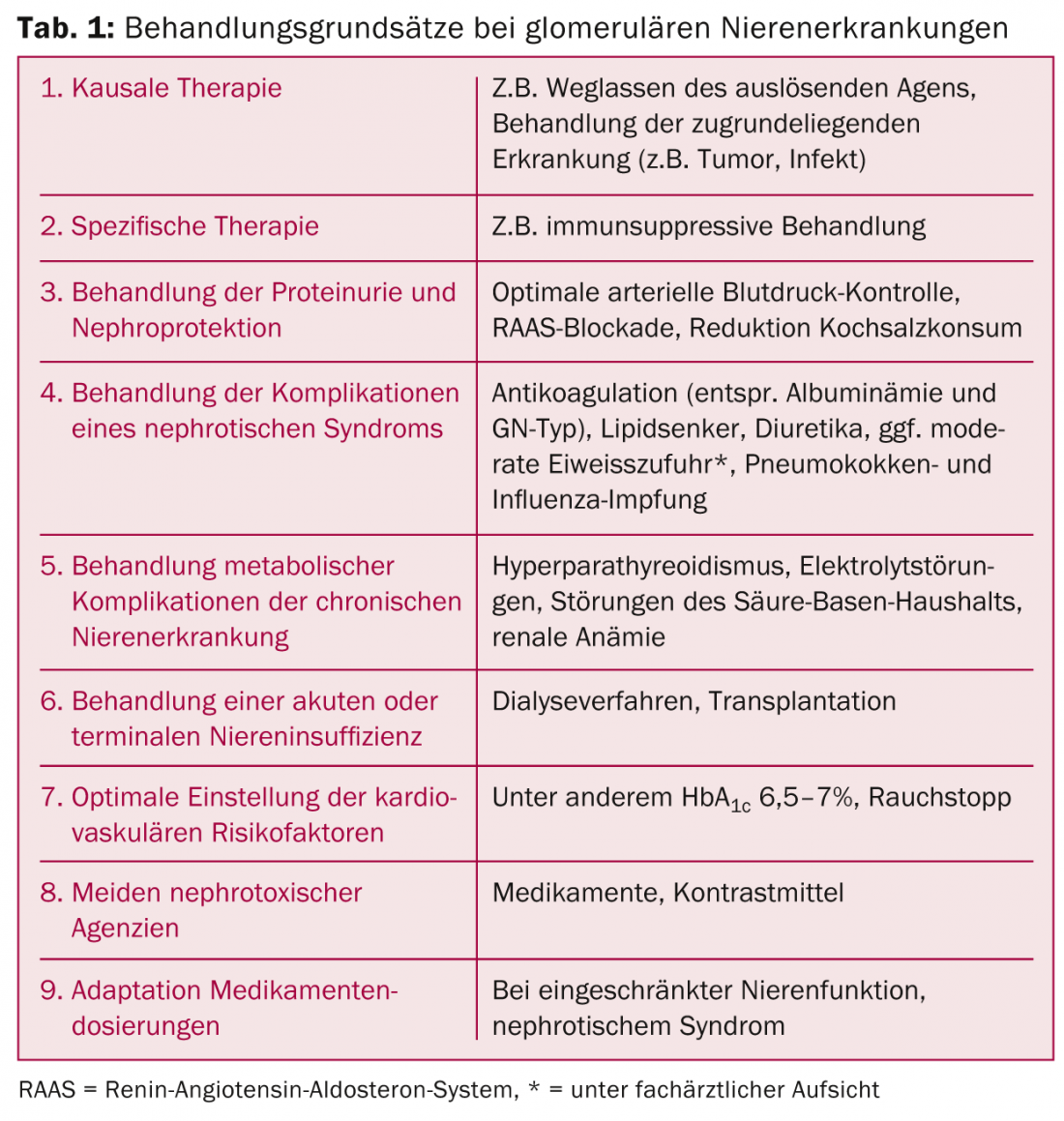
Como com todas as doenças renais crónicas, é essencial uma terapia de apoio óptima. Em alguns casos, os tratamentos imunossupressores podem ser evitados e o prognóstico renal e/ou global pode ser melhorado. É aqui que o prestador de cuidados primários tem um papel fundamental a desempenhar. As pedras angulares terapêuticas podem ser encontradas no Quadro 1.
No tratamento da proteinúria, para além do controlo rigoroso dos valores da tensão arterial (<130/90 mmHg para não diabéticos, <130/ 85 mmHg para diabéticos) [1] e consumo limitado de sal (5-6 g/d), está indicada a inibição de drogas do sistema renina-angiotensina-aldosterona (RAAS). Os inibidores da ECA e os sartans são maximizados após a tolerância (dose máxima mais elevada do que para o tratamento de hipertensão). As provas dos últimos anos têm questionado o valor do bloqueio duplo RAAS [2,3]. De facto, os diabéticos em particular mostram riscos mais elevados de hipercalemia e insuficiência renal aguda com um prognóstico cardiovascular concomitante não melhorado, apesar de um efeito aditivo sobre a proteinúria. A nova introdução de tais medicamentos em doentes renais já não pode, portanto, ser geralmente recomendada. A combinação de um inibidor da ECA ou sartan com antagonistas de aldosterona tem um efeito sinérgico na proteinúria, mas aumenta o risco de episódios graves de hipercalemia, especialmente em funções renais deficientes.
Terapia dirigida às células B
Devido ao seu papel central na patogénese das doenças auto-imunes (produção de auto-anticorpos patogénicos, apresentação antigénica, produção de citocinas pró-inflamatórias), os linfócitos B têm sido explorados como alvo terapêutico em vários GP nos últimos anos.
Rituximab
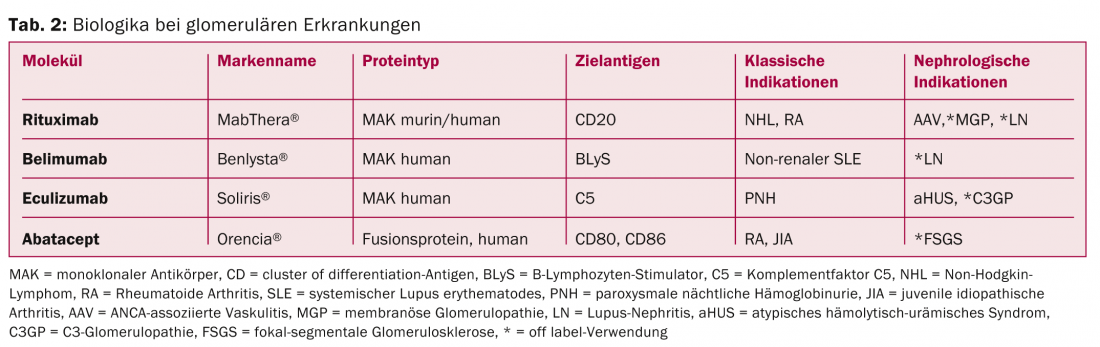
O Rituximab (RTX) é um anticorpo monoclonal quimérico (rato/humano) dirigido contra o antigénio de superfície CD20 dos linfócitos B (Tab. 2) . A ligação a este antigénio induz a lise celular e leva ao esgotamento das células B no sangue periférico. Desde a sua introdução no tratamento do linfoma não-Hodgkin em 1997, a utilização de RTX foi alargada a doenças auto-imunes como a artrite reumatóide e a medicina de transplante. RTX tem sido utilizado no tratamento de vários GPs [4]. As indicações mais importantes actualmente em investigação são vasculite associada à ANCA, nefrite lupus e glomerulopatia membranosa idiopática.
Vasculite associada à ANCA (AAV): A terapia de AAV com RTX foi aprovada na Suíça em 2012. A aprovação baseia-se em dois ensaios controlados aleatorizados (TCR), incluindo doentes com envolvimento renal de AAV; os ensaios mostraram uma eficácia comparável (possivelmente uma eficácia ainda maior nas recidivas) com taxas de efeitos secundários (inesperadamente) comparáveis às da terapia padrão com ciclofosfamida e esteróides de dose elevada [5,6]. De acordo com directrizes internacionais, esta terapia pode ser considerada uma alternativa à terapia padrão. Devido à falta de dados a longo prazo, a substância é actualmente utilizada na prática especialmente em contra-indicações para a terapia convencional (por exemplo, desejo de crianças), em recaídas ou casos refractários.
Lupus nephritis (LN): RTX tem sido utilizado com sucesso no tratamento do LN em numerosos estudos de observação e séries de casos (especialmente em recidivas graves, recaídas, em situações refractárias e em contra-indicações à terapia convencional). Dois TCR com RTX como terapia adicional em pacientes com lúpus eritematoso sistémico activo ou extrarrenal mostram taxas de remissão comparáveis à terapia com placebo [7,8]. Apesar destes resultados decepcionantes, que os peritos atribuem à concepção do estudo, entre outras coisas, e encorajados pelos dados de acompanhamento e pela experiência prática, muitos clínicos continuam a tratar fora do âmbito do estudo com RTX, especialmente nas situações mencionadas. Estão previstos outros estudos de avaliação de RTX para o tratamento de LN com base em diferentes regimes imunossupressores.
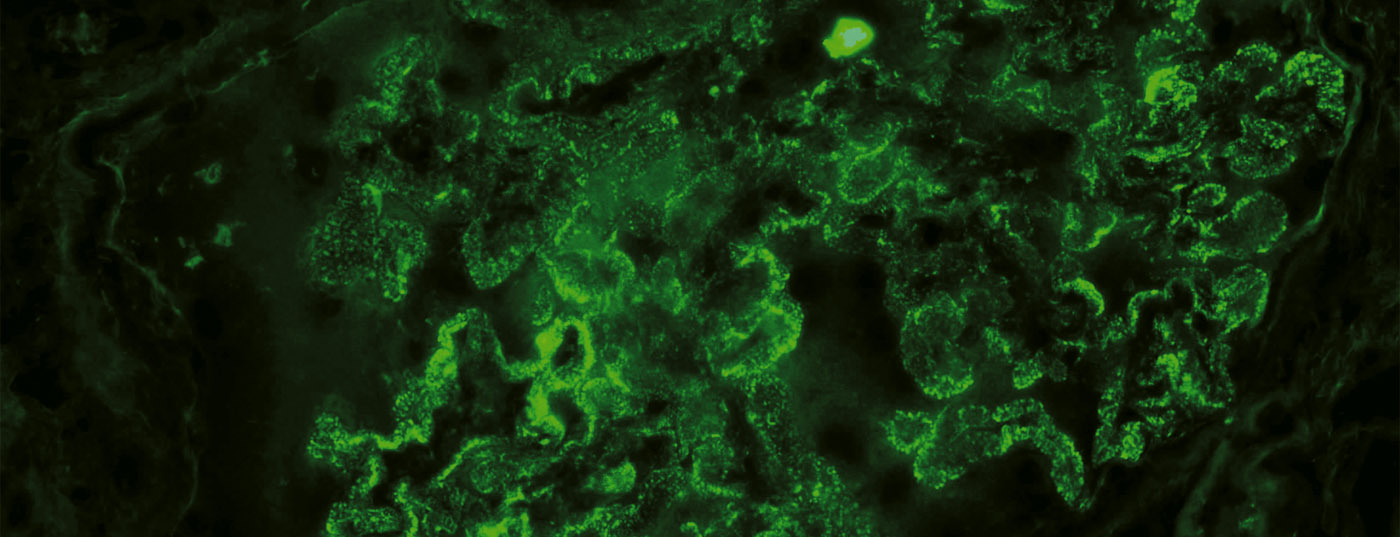
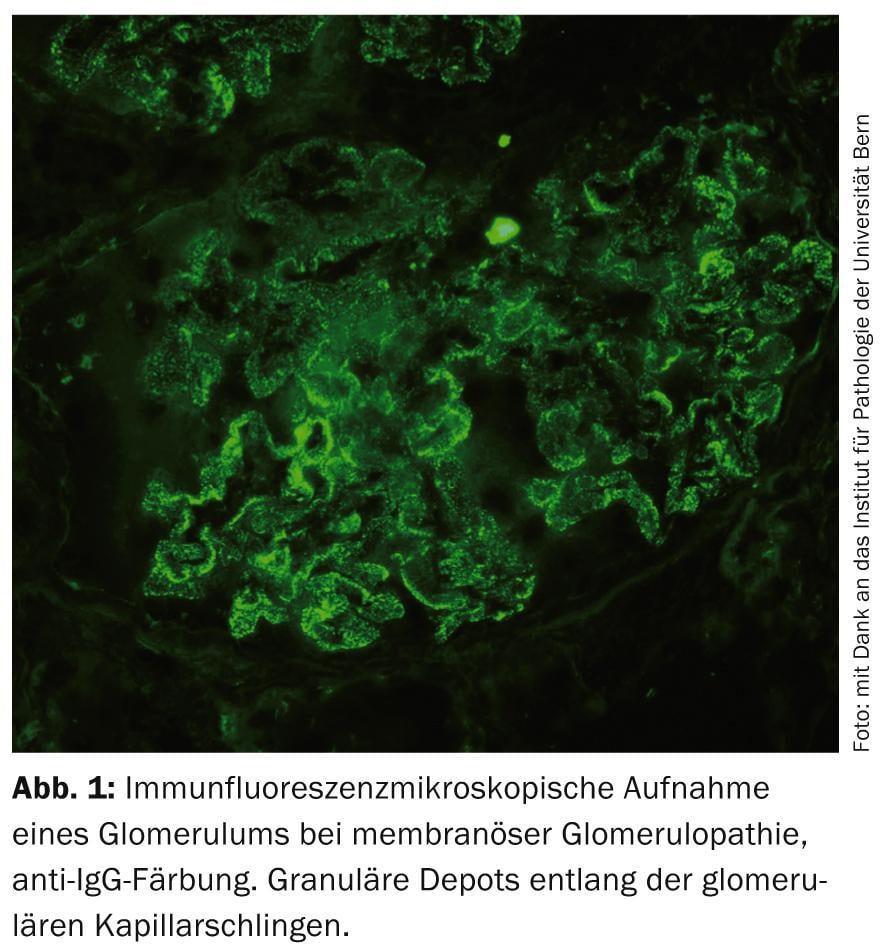
Glomerulopatia membranosa idiopática (MGP): O MGP é um dos GP primários mais comuns (Fig. 1) . Descobertas de investigação inovadoras na última década forneceram provas de que o MGP é uma doença auto-imune com a formação de auto-anticorpos contra antigénios podocíticos [9]. Contra este pano de fundo, uma terapia com RTX é patofisiologicamente interessante. RTX tem sido até agora utilizada com sucesso em numerosos estudos observacionais com uma grande variedade de regimes de administração para tratar principalmente casos refractários [10]. Faltam actualmente dados controlados e a longo prazo, mas vários RCTs estão em curso comparando esta substância com terapias de apoio ou outras imunossupressoras. Na prática, RTX é actualmente utilizado fora do rótulo no MGP, principalmente em casos de autoanticorpos detectados.
A utilização generalizada de RTX mostra geralmente uma boa tolerabilidade. Os efeitos secundários mais frequentes incluem reacções de infusão (sendo portanto necessária a administração de pré-medicação), neutropenia, hipogamaglobulinemia, bem como infecções; foram descritos casos individuais de leucoencefalopatia multifocal progressiva.
As células plasmáticas não são esgotadas por RTX, as células B derivadas de tecidos só podem ser parcialmente esgotadas. Há ainda um efeito limitado na síndrome nefrótica, nos polimorfismos do receptor Fc-γ e nos níveis elevados do factor de estimulação das células B (BLyS). Além disso, uma pequena parte das células B, células B reguladoras com efeitos anti-inflamatórios, estão também a esgotar-se.
Belimumab
Belimumab (BEL) é um anticorpo monoclonal humanizado que se liga ao BLyS solúvel, inibindo a sobrevivência das células B e a diferenciação em plasmócitos. A BEL foi recentemente aprovada para o tratamento de LES extrarrenais. Análises post-thoc dos dados mostram uma taxa possivelmente reduzida de recorrência renal em doentes tratados com BEL [11]. Estudos em LES renal com ou sem administração de RTX (como imunomodulação sinérgica de células B) ajudarão a definir o papel da BEL para os nefrologistas.
Eculizumab
Eculizumab (ECU) é um anticorpo monoclonal humanizado contra o factor complementar C5, que se encontra no fim comum da cascata de activação do complemento. Inicialmente utilizada para o tratamento da hemoglobinúria paroxística nocturna, a preparação tem sido aprovada desde 2011 para o tratamento da síndrome hemolítico-uraémica atípica. Outra entidade patológica baseada na desregulação da via alternativa do complemento são as glomerulopatias C3 (C3GP), que foram recentemente distinguidas das glomerulonefríticas membranoproliferativas clássicas mediadas pelo complexo imunitário (por exemplo, em infecções, neoplasias), graças a descobertas recentes [12]. Neste contexto, a utilização bem sucedida do ECU foi documentada nas descrições de casos. Devido aos danos frequentemente causados pela complementação, o ECU também foi testado noutros GN como a nefropatia IgA, LN e MGP. As esperanças de utilização generalizada são actualmente atenuadas pelos custos extremamente elevados de uma tal terapia potencialmente vitalícia.
Abatacept
A proteína de fusão Abatacept (ABT) liga-se ao antigénio CD80 em células T, inibindo assim a estimulação da célula T por células que apresentam antigénio. Até agora, os dados existem principalmente em LN (RCT, negativo) e AAV (observacional, positivo). Curiosamente, a indução de moléculas de superfície CD80 em podócitos foi recentemente demonstrada no caso de doença renal proteinúrica. O ABT foi assim utilizado com sucesso em cinco pacientes com glomerulosclerose segmentar focal primária (FSGS), bem como FSGS recorrente após transplante renal [13]. Estes dados promissores aguardam confirmação em estudos futuros.
Esteróides tópicos para a nefropatia IgA
A nefropatia IgA (IgA-NP) é o GP mais comum a nível mundial. Depósitos mesangianos de anticorpos IgA insuficientemente glicosilados juntamente com auto-anticorpos induzidos levam à inflamação glomerular. Assume-se que a causa é uma desregulação do sistema imunitário da mucosa, o que leva a uma tolerância imunitária defeituosa de, por exemplo, antigénios alimentares ou bacterianos. Num estudo sueco de prova de princípio, a budesonida numa nova formulação com libertação na região ileocecal foi utilizada para tratar pacientes com IgA-NP e observou-se uma redução na proteinúria. Para além do novo conceito terapêutico, é interessante a minimização dos efeitos sistémicos induzidos por esteróides [14]. Está actualmente em curso um ensaio de fase II.
Hormona adrenocorticotrófica
A hormona adrenocorticotrópica (ACTH) foi utilizada para tratar a síndrome nefrótica já nos anos 50, mas foi depois abandonada em favor dos glicocorticóides orais mais fáceis de administrar. Graças a uma redescoberta acidental num estudo lipídico em doentes com MGP nefrótico, tem sido cada vez mais utilizado em GP proteinúrico nos últimos anos (ACTH sintético na Europa, ACTH derivado de animais na forma de gel nos EUA). O mecanismo de acção parece ir além de uma indução da produção de cortisol e ser mediado através da ligação a receptores de melanocortina em podócitos. Existem dados observacionais para a doença de alteração mínima e FSGS primário, e existe um RCT piloto com resultados promissores para o MGP [15]. Foram descritos efeitos secundários semelhantes aos dos esteróides. Também aqui, os elevados custos da terapia são um factor limitativo.
Eprodisate
A amiloidose AA é uma doença multissistémica que pode ocorrer em infecções crónicas ou doenças inflamatórias e é caracterizada por depósitos fibrilares de amilóide sérico A, uma proteína de fase aguda. O envolvimento renal frequente é manifestado pela proteinúria e insuficiência renal. Além de tratar a doença subjacente, um novo alvo terapêutico são os depósitos fibrilares. O eprodisado é uma molécula sulfonada com semelhança estrutural com o sulfato de heparan que se liga aos sítios de ligação dos glicosaminoglicanos na proteína amilóide A do soro e inibe a polimerização das fibrilhas. Um RCT recente mostrou um abrandamento do declínio da função renal [16].
Outros estudos precisam de confirmar estes resultados.
Conclusão para a prática
- Não há indicação geral de duplo bloqueio de RAAS para o tratamento da proteinúria.
- O Rituximab é aprovado para a terapia de indução da vasculite associada à ANCA e é utilizado fora do rótulo na nefrite por lúpus e na glomerulopatia membranosa idiopática.
- Eculizumab está aprovado para o tratamento da síndrome hemolítica uraémica, e os ensaios iniciais para utilização em glomerulopatias C3 estão em curso.
- A utilização bem sucedida do abatacept em glomerulosclerose segmentar focal primária e da hormona adrenocorticotrópica em glomerulopatias proteinúricas foi recentemente descrita.
- Existem resultados interessantes de estudos iniciais sobre a administração de esteróides tópicos na nefropatia IgA.
Literatura:
- Mancia G, et al: 2013 ESH/ESC Orientações Práticas para a Gestão da Hipertensão Arterial. Blood Press 2014; 23(1): 3-16.
- Mann JF, et al: resultados renais com telmisartan, ramipril, ou ambos, em pessoas de alto risco vascular (o estudo ONTARGET): um ensaio multicêntrico, aleatório, duplo-cego, controlado. Lancet 2008; 372(9638): 547-553.
- Parving HH, et al: Cardiorenal end points in a trial of aliskiren for type 2 diabetes. N Engl J Med 2012; 367(23): 2204-2213.
- Mani LY, et al: [Rationale and clinical evidence for the use of rituximab in glomerular diseases]. Rev Med Suisse 2011; 7(290): 819-824.
- Specks U, et al: Eficácia dos regimes de indução de remissão para a vasculite associada à ANCA. N Engl J Med 2013; 369(5): 417-427.
- Jones RB, et al: Rituximab versus ciclofosfamida na vasculite renal associada à ANCA. N Engl J Med 2010; 363(3): 211-220.
- Rovin BH, et al: Eficácia e segurança do rituximab em doentes com lúpus nefrite proliferativa activa: o estudo Lupus Nephritis Assessment with Rituximab. Arthritis Rheum 2012; 64(4): 1215-1226.
- Merrill JT, et al: Eficácia e segurança do rituximab na erupção do lúpus sistémico moderadamente a severamente activo: a avaliação aleatória, duplo-cego, fase II/III SLE do ensaio de rituximab. Arthritis Rheum 2010; 62(1): 222-233.
- Beck LH, et al: Receptor de fosfolipase tipo M A2 como antigénio alvo na nefropatia idiopática membranosa. N Engl J Med 2009; 361(1): 11-21.
- Ruggenenti P, et al: Rituximab em nefropatia membranosa idiopática. J Am Soc Nephrol 2012; 23(8): 1416-1425.
- Dooley MA, et al: Effect of belimumab treatment on renal outcomes: results from the phase 3 belimumab clinical trials in patients with SLE. Lúpus 2013; 22(1): 63-72.
- Fakhouri F, et al: C3 glomerulopatia: uma nova classificação. Nat Rev Nephrol 2010; 6(8): 494-499.
- Yu CC, et al: Abatacept em B7-1-positivo de doença renal proteinúrica. N Engl J Med 2013; 369(25): 2416-2423.
- Smerud HK, et al.: Novo tratamento para a nefropatia IgA: budesonida entérica orientada para a região ileocecal ameliorates proteinuria. Nephrol Dial Transplant 2011; 26(10): 3237-3242.
- Ponticelli C, et al: Um ensaio piloto aleatório comparando a etilprednisolona mais um agente citotóxico versus hormona adrenocorticotrópica sintética em nefropatia membranosa idiopática. Am J Kidney Dis 2006; 47(2): 233-240.
- Dember LM, et al: Eprodisato para o tratamento de doenças renais em amiloidose AA. N Engl J Med 2007; 356(23): 2349-2360.
CARDIOVASC 2015; 14(1): 9-12