Existem várias novas opções de tratamento para o cancro da mama metastásico positivo de RH. O objectivo da conferência anual de oncologia em St. Gallen era classificar e avaliar estas substâncias. Como poderia ser um algoritmo terapêutico moderno?
“Quando falamos de novas terapias nesta área, referimo-nos principalmente ao everolimus (Afinitor®), palbociclib (Ibrance®), ribociclib (Kisqali®) e abemaciclib (ainda não aprovado na Suíça) – até certo ponto, também completo, que apareceu no mercado no início dos anos 2000″, diz o Dr. Müller. “Os estudos sobre os inibidores da aromatase letrozol e anastrozol exemplificam o que conseguimos com os fármacos mais antigos na primeira linha pós-menopausa: Em comparação com o tamoxifen, prolongaram significativamente a sobrevivência sem progressão e resultaram numa resposta comparável ou superior [1–3]”.
No ensaio FALCON [4], o fulvestrant demonstrou ser superior ao anastrozol no cenário de primeira linha. Após cerca de seis meses, as curvas PFS divergiram. A resposta foi comparável. Uma análise de subgrupo mostrou que os pacientes sem envolvimento visceral em particular viviam mais tempo sem progressão (HR 0,59), enquanto que aqueles com envolvimento visceral não beneficiavam do anastrozol (HR 0,99).
Actualmente, a terapia endócrina é a opção preferida para os carcinomas mamários avançados receptores de estrogénios, mesmo para as metástases viscerais (apenas não em casos de “crise visceral” ou suspeita de resistência endócrina – para estes casos, a quimioterapia primária deve ser escolhida). Mas que substâncias activas e combinações são preferidas na terapia endócrina moderna?
Problema: Resistência
“O desenvolvimento da resistência às terapias endócrinas é inevitável na situação metastática”, disse o orador. Fala-se de “resistência primária” se o tumor progredir em menos de meio ano sob terapia endócrina, enquanto se fala de “resistência secundária” se só progredir após este período. Isto aplica-se à situação metastática primária.
Na situação adjuvante inicial, “principalmente resistente” significa uma recaída precoce até dois anos após o início da terapia endócrina adjuvante. Os “secundários resistentes” são tumores que só se repetem após dois a cerca de seis anos (sob terapia adjuvante prolongada), e os “sensíveis” são aqueles que só se repetem pelo menos um ano após o fim da terapia adjuvante.
Os mecanismos de resistência são múltiplos. As mutações ER (activando a mutação ESR-1) são comuns, por exemplo. Estes são adquiridos, ocorrem em 15-30% dos anteriormente tratados com terapia endócrina e levam à resistência ao tamoxifeno, aos inibidores da aromatase e ao fulvestrante (possivelmente não fulvestrante-HD [5]). Outros mecanismos de resistência incluem as vias de transdução de sinal de bypass celular.
Solução: Novas substâncias activas
Para algumas destas vias de desvio, os novos medicamentos acima mencionados estão agora disponíveis.
Everolimus, por exemplo, visa o desvio através da via PI3K/AKT/mTOR através da inibição do mTOR. Como kinase serina-treonina, o mTOR tem uma função chave nesta via de sinalização, que é conhecida por ser perturbada em muitos tumores malignos humanos. BOLERO-2 [6] mostrou uma superioridade significativa no ponto final primário do PFS na segunda linha em combinação com o exemestane, em comparação com o exemestane apenas. As curvas divergiram após cerca de um mês e meio e a resposta também reflectiu o benefício. Não foi possível demonstrar qualquer efeito significativo no parâmetro secundário, a sobrevivência global, embora o estudo tenha sido, evidentemente, principalmente alimentado por PFS. Uma toxicidade problemática e comum da droga é a estomatite, que – como o ensaio SWISH mostrou – pode ser controlada pelo menos em certa medida com o elixir bucal de dexametasona quatro vezes por dia. Além disso, pode ocorrer pneumonite, que requer uma interrupção da terapia em caso de sintomas moderados e graves. Globalmente, a qualidade de vida não parece ser afectada de forma relevante pela substância activa, mas não parece ser melhorada em comparação com o isestano-somente.
Outro modo de acção é a inibição CDK4/6. O complexo ciclina D-CDK4/6 regula a progressão do ciclo celular através da fosforilação da proteína do retinoblastoma (Rb). A resistência endócrina está associada à expressão persistente da ciclina D e à fosforilação Rb. Os inibidores de cinase CDK4/CDK6 selectivos visam precisamente este ponto. No ensaio PALOMA-3 [7], que foi apresentado na ASCO 2015 e noutros locais, o palbociclib revelou-se superior ao fulvestrant sozinho na segunda linha, em combinação com o fulvestrant. Também aqui, as curvas PFS separaram-se muito cedo (após cerca de um mês e meio). Se observar a toxicidade, o perfil com neutropenia e alopecia pode lembrá-lo da quimioterapia no início. “No entanto, a alopecia é quase sempre de grau 1 e a neutropenia é claramente diferente da da quimioterapia”, explicou o orador. As células estaminais hematopoiéticas e os primeiros progenitores de neutrófilos dependem da actividade da ciclina D-CDK4/6 para entrar, progredir e proliferar no ciclo celular. Enquanto que com os inibidores CDK4/CDK6 da cinase, a neutropenia resulta assim da paragem do ciclo celular e assim a recuperação é geralmente rápida no curso (não cumulativa), os danos do ADN e a apoptose de precursores proliferantes na quimioterapia levam a uma recuperação retardada. As neutropenias de grau 3/4 com palbociclib são controláveis, na medida em que mais de dois terços dos eventos ocorrem no primeiro ciclo, e após a redução da dose o risco de neutropenias graves é baixo [8].
E a primeira linha?
MONALEESA-2 [9] demonstrou a superioridade do ribociclibe com letrozol sobre o letrozol apenas na primeira linha (redução do risco no ponto final primário PFS de mais de 40% e melhor resposta). Os resultados foram ladeados por PALOMA-2 (palbociclib) [10] e MONARCH-3 (abemaciclib) [11] – o efeito dos diferentes inibidores da cinase CDK4/CDK6 é comparável. As diferenças são observadas principalmente no perfil de toxicidade. Os acontecimentos adversos graves mais comuns foram a neutropenia em PALOMA-2 e MONALEESA-2, juntamente com a alopecia, fadiga e anemia em palbociclib e adicionalmente náuseas em ribociclib. Em MONARCH-3, era principalmente diarreia, juntamente com fadiga e também neutropenia e alopecia.
“As análises dos subgrupos correspondentes mostram que até agora não foi possível identificar claramente nenhum grupo clínico ou molecular de doentes que não beneficie dos novos medicamentos. Portanto, também ainda não há biomarcadores de previsão estabelecidos”, explicou o Dr. Müller. “A eficácia parece ser a mesma nas mulheres idosas com mais de 70 anos de idade. A tolerância é, contudo, – como esperado – significativamente pior aqui”. A qualidade de vida com palbociclib na primeira linha não é pior, mas também não é melhor do que com o letrozol sozinho [12]. Na segunda linha, contudo, a combinação com o inibidor CDK4/6 é superior à monoterapia com fulvestrante em termos de qualidade de vida [13].
Como decidir?
Para além de biomarcadores válidos, ainda faltavam na altura da apresentação – tal como os estudos sobre a sequência óptima – dados sobre os novos agentes alvo no cancro da mama metastásico receptor de hormonas.
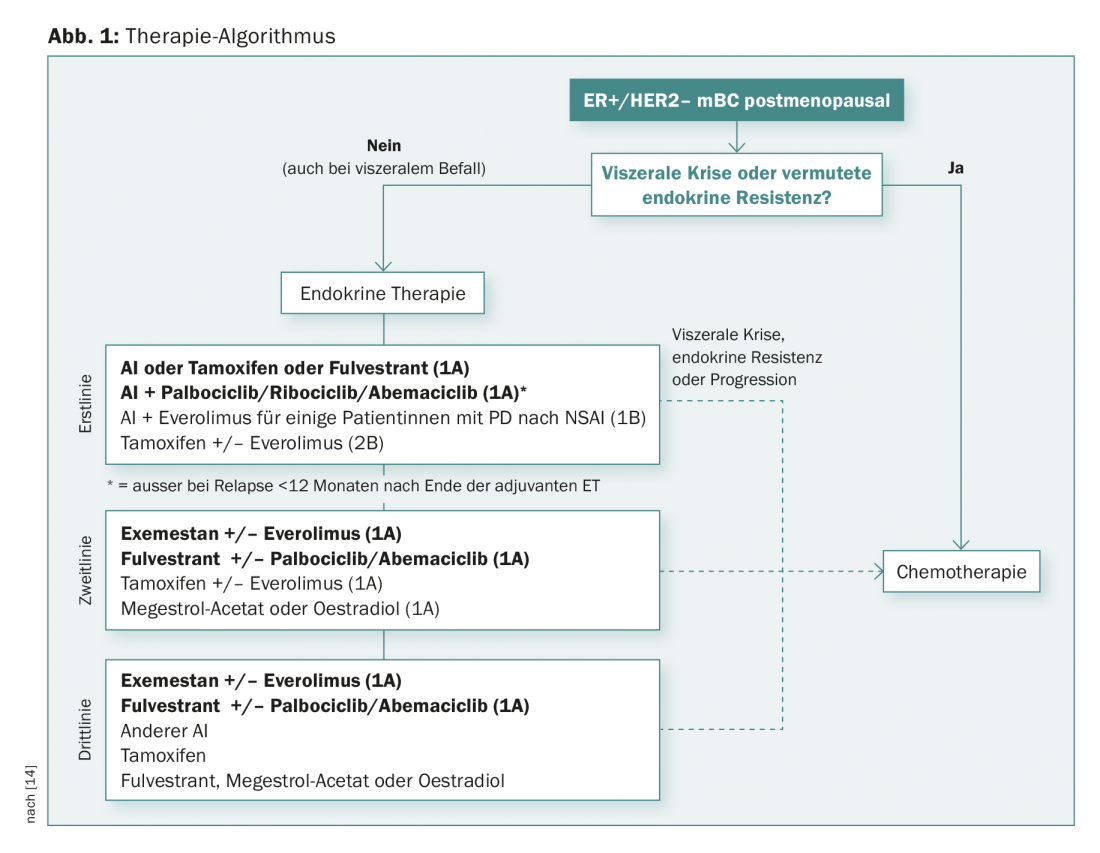
A figura 1 mostra um possível algoritmo para doentes pós-menopausa com ER+/HER2- doença metastática. “A terapia endócrina por si só é uma boa opção em baixa pressão de remissão. A combinação com a inibição CDK4/CDK6 é eficaz na primeira linha e também mais tarde. É uma opção importante na pressão de remissão (embora também nos idosos com mais toxicidade). Everolimus e o isento são eficazes após falha da terapia endócrina. Eficaz” com as novas substâncias ainda significa actualmente uma melhoria em PFS e resposta (e ainda não em OS)”, resumiu o Dr. Müller.
Fonte: 28º Curso de Formação Contínua de Médicos em Oncologia Clínica, 22-24 de Fevereiro de 2018, St.
Literatura:
- Mouridsen H, et al: Estudo de fase III do letrozol versus tamoxifeno como terapia de primeira linha do cancro da mama avançado em mulheres na pós-menopausa: análise da sobrevivência e actualização da eficácia do Grupo Internacional do Cancro da Mama Letrozol. J Clin Oncol 2003 Jun 1; 21(11): 2101-2109.
- Nabholtz JM, et al: Anastrozole (Arimidex) versus tamoxifen como terapia de primeira linha para o cancro da mama avançado em mulheres na pós-menopausa: análise de sobrevivência e resultados de segurança actualizados. Eur J Cancer 2003 Ago; 39(12): 1684-1689.
- Nabholtz JM, et al: Anastrozole é superior ao tamoxifeno como terapia de primeira linha para o cancro da mama avançado em mulheres na pós-menopausa: resultados de um ensaio multicêntrico randomizado norte-americano. Grupo de Estudo Arimidex. J Clin Oncol 2000 Nov 15; 18(22): 3758-3767.
- Robertson JFR, et al: Fulvestrant 500 mg versus anastrozol 1 mg para o cancro da mama com receptor hormonal avançado positivo (FALCON): um ensaio internacional, aleatório, duplo-cego, fase 3. Lancet 2016 Dez 17; 388(10063): 2997-3005.
- Fribbens C, et al: Plasma ESR1 Mutations and the Treatment of Estrogen Receptor-Positive Advanced Breast Cancer. J Clin Oncol 2016 Set 1; 34(25): 2961-2968.
- Baselga J, et al: Everolimus em cancro da mama avançado pós-menopausa – receptores de hormonas positivas. N Engl J Med 2012 Fev 9; 366(6): 520-529.
- Cristofanilli M, et al: Fulvestrant plus palbociclib versus fulvestrant plus placebo para o tratamento do cancro da mama com hormonas-receptor-positivo, HER2-negativo metastásico que progrediu na terapia endócrina anterior (PALOMA-3): análise final do ensaio controlado multicêntrico, duplo-cego, fase 3 aleatorizado. Lancet Oncol 2016; 17(4): 425-439.
- Verma S, et al: Palbociclib em combinação com Fulvestrant em Mulheres com Receptor Hormonal-Positivo/HER2-Negativo Câncer de Mama Metástático Avançado: Análise de Segurança Detalhada de um Estudo Multicêntrico, Aleatório, Controlado por Placebo, Fase III (PALOMA-3). Oncologista 2016 Out; 21(10): 1165-1175.
- Hortobagyi GN, et al: Ribociclib como Terapia de Primeira Linha para o Câncer de Mama Avançado, HR-Positivo. N Engl J Med 2016; 375: 1738-1748.
- Finn RS, et al: Palbociclib e Letrozole em Advanced Breast Cancer. N Engl J Med 2016 17 de Novembro; 375(20): 1925-1936.
- Goetz MP, et al: MONARCH 3: Abemaciclib As Initial Therapy for Advanced Breast Cancer. J Clin Oncol 2017 Nov 10; 35(32): 3638-3646.
- Rugo HS, et al: Impact of Palbociclib Plus Letrozole on Patient Reported Health-Related Health-Related Quality of Life: Results from the PALOMA-2 Trial. Ann Oncol 2018 Jan 19. doi: 10.1093/annonc/mdy012 [Epub ahead of print].
- Harbeck N, et al: Qualidade de vida com palbociclib plus fulvestrant em receptor hormonal previamente tratado – positivo, HER2-negativo – cancro da mama metastásico: resultados relatados pelos pacientes do ensaio PALOMA-3. Ann Oncol 2016 Jun; 27(6): 1047-1054.
- Cardoso F, et al: 3rd ESO-ESMO International Consensus Guidelines for Advanced Breast Cancer (ABC 3). Ann Oncol 2017 Jan 1; 28(1): 16-33.
InFo ONCOLOGY & HEMATOLOGY 2018; 6(2): 38-40.