O tratamento da hipertensão arterial pulmonar (HAP) inclui medidas não específicas (terapia básica) e medicamentos específicos (vasodilatadores pulmonares selectivos). Uma terapia básica bem desenvolvida, incluindo anticoagulação oral, controlo do ritmo, medidas de reabilitação e apoio psicossocial para sintomas depressivos, é essencial. Os vasodilatadores específicos reduzem a morbilidade e mortalidade de HAP. Actualmente, estão disponíveis várias substâncias que influenciam uma das três vias de sinalização de HAP: Endotelin, NO ou prostacyclin em cascata. As substâncias que influenciam o mesmo caminho de sinalização (por exemplo, riociguat e sildenafil ou macitentan e bosentan) não devem ser combinadas.
A hipertensão arterial pulmonar (HAP) é uma doença da vasculatura pulmonar periférica que, se não for tratada, leva a um aumento progressivo da resistência vascular pulmonar e a uma redução do tamanho da circulação pulmonar. O prognóstico é determinado pela capacidade do ventrículo direito de tolerar este aumento de pós-carga.
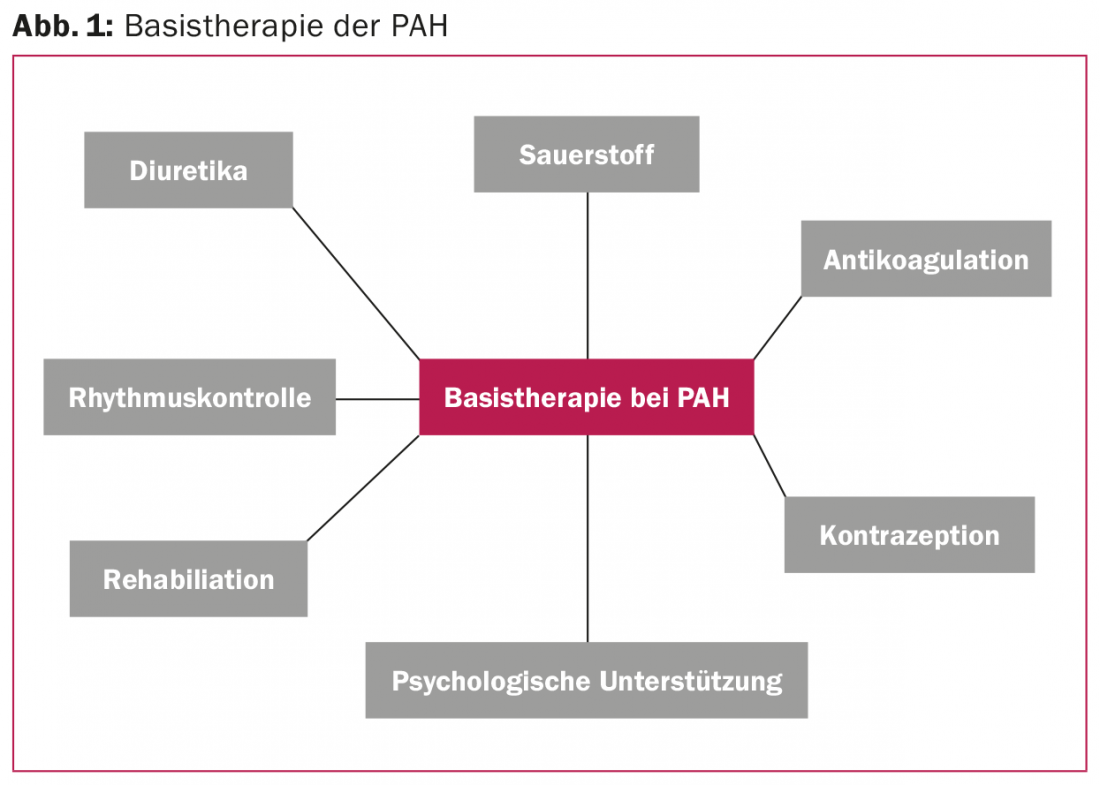
Há cerca de 30 anos, a sobrevida mediana após o diagnóstico de “hipertensão pulmonar primária” foi de 2,8 anos [1]. Desde as primeiras abordagens terapêuticas com antagonistas do cálcio e anticoagulação oral, as opções terapêuticas têm-se multiplicado. Enquanto no início o foco estava em medidas não específicas como o tratamento da insuficiência cardíaca direita com diuréticos e digoxina, entretanto foram desenvolvidos medicamentos que influenciam selectivamente várias vias de sinalização da vasoconstrição pulmonar e inibem a progressão da doença. Dez substâncias estão agora aprovadas para o tratamento de HAP [2]. No entanto, para além desta vasodilatação pulmonar selectiva, a terapia básica adaptada individualmente não perdeu a sua importância e deve complementar qualquer terapia específica de HAP (fig. 1).
Vasodilatadores pulmonares selectivos
A disfunção endotelial e o desequilíbrio resultante de vasoconstritores versus vasodilatadores é um aspecto importante na patogénese da HAP. A disfunção endotelial afecta a remodelação vascular da circulação pulmonar, bem como a hemostasia e a coagulação, que por sua vez contribuem para a progressão da HAP. As drogas HAP utilizadas hoje em dia visam uma das três vias de sinalização conhecidas que influenciam a pressão pulmonar: Prostaciclina (PGI2) [3], Nitrogénio (NO) [4] e a via Endothelin-1 [5] (Fig. 2).
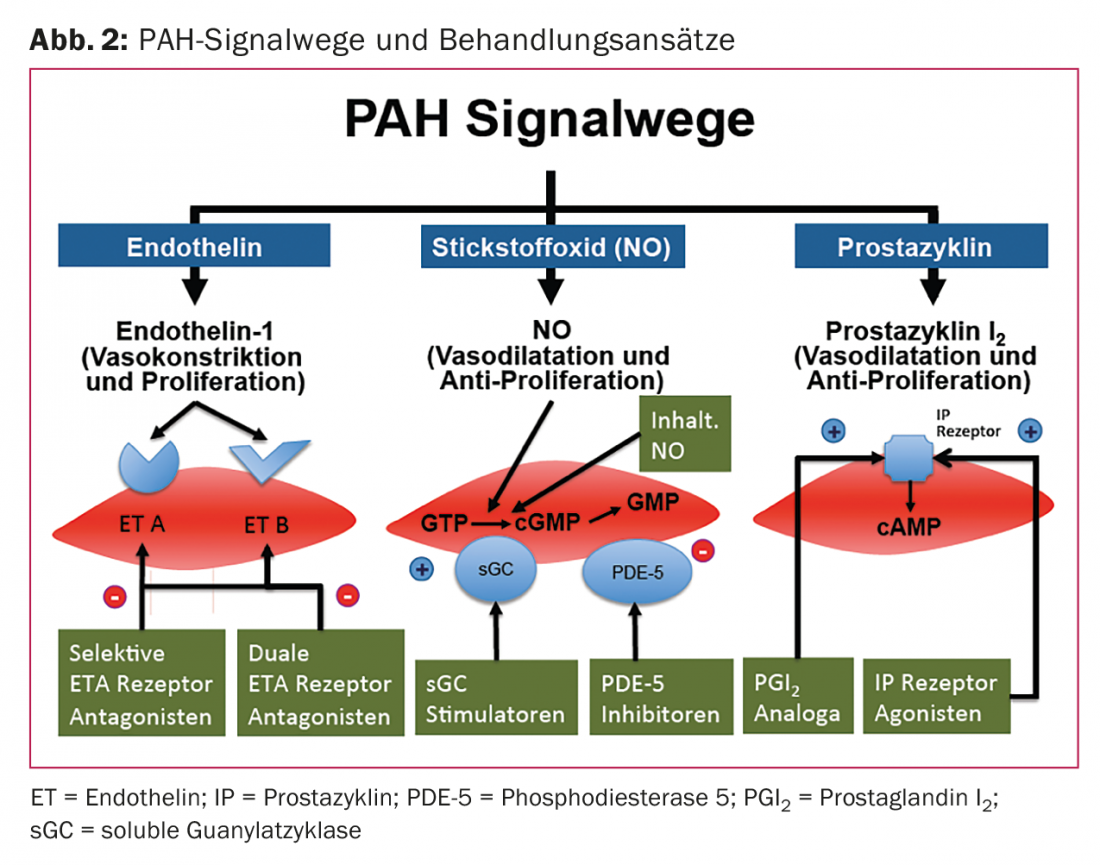
A HAP caracteriza-se por uma upregulação de vasoconstritores (por exemplo, endotelina-1) e uma redução de vasodilatadores (por exemplo, PGI2 e NO).
Desde 2004, os vasodilatadores pulmonares das três vias têm estado à nossa disposição. Nos últimos anos, foram testados fármacos que ou são novos desenvolvimentos de moléculas existentes (p. ex. macitentan), ou visam novos pontos na cascata de sinalização (p. ex. riociguat) ou contêm uma molécula nova que se pode ligar a receptores idênticos aos existentes (p. ex. selexipag). Espera-se que estes novos agentes tenham propriedades farmacocinéticas melhoradas que simplifiquem a administração, aumentem a eficácia e/ou sejam associados a um perfil de efeitos secundários mais baixo.
Macitentan
Macitentan (Opsumit®) é a mais recente substância activa do grupo de antagonistas dos receptores de endotelina. Outros antagonistas dos receptores de endotelina aprovados na Suíça são bosentan (Tracleer®) e ambrisentan (Volibris®). Endothelin-1 tem um potencial vasoconstritivo pronunciado e efeitos estimulantes dos leucócitos. A ligação às isoformas A (ETA) e B (ETB) das células musculares lisas medeia a vasoconstrição das artérias pulmonares. Tal como o bosentan, o macitentan actua através de um bloqueio de duplo receptor. Devido a metabolitos activos mais longos e a uma dissociação retardada do receptor, é postulado um melhor efeito de diminuição da pressão para o macitentan [6].
A eficácia do macitentan foi investigada num ensaio de fase III (ensaio SERAPHIN) em 742 doentes [7]. Receberam placebo, macitentan 3 mg/dia ou macitentan 10 mg/dia numa proporção de 1:1:1. Além disso, poderia ser utilizada terapia com prostanóides ou inibidores de fosfodiesterase. SERAPHIN é o maior estudo duplo-cego, randomizado, controlado por placebo, a longo prazo em doentes com HAP até à data e apresenta uma abordagem de estudo inovadora como um estudo de resultados orientado por eventos. Com base nestes dados, demonstrou-se que o macitentan reduz o ponto final combinado de morbilidade e/ou mortalidade em 45% em doentes com HAP em comparação com placebo.
A figura 3 mostra os gráficos de Kaplan-Meier do efeito a longo prazo em termos de morbilidade e mortalidade em pacientes com e sem terapia combinada com outros vasodilatadores pulmonares.
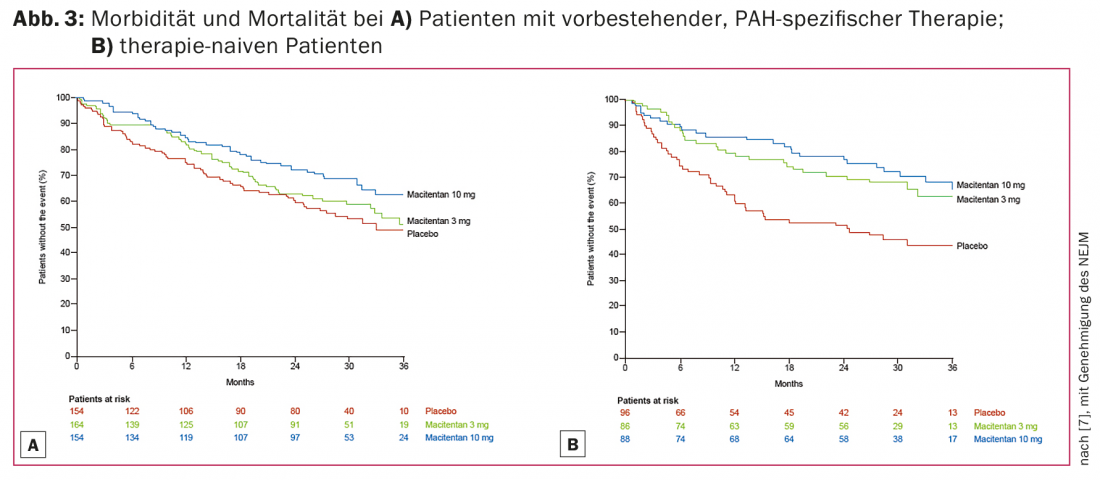
Com base nestes dados de estudo, o macitentan 10 mg diários foi aprovado desde Fevereiro de 2014 para o tratamento de HAP com uma classe funcional II-III, de acordo com a definição da OMS. Em comparação com o bosentano estabelecido, induz menos interacções medicamentosas e tem menos efeitos secundários; em particular, as transaminases não precisam de ser controladas mensalmente. Os efeitos secundários mais comuns são nasofaringite, anemia e dores de cabeça.
Macitentan é principalmente decomposto no fígado através do citocromo P450 3A4 (CYP3A4). Deve portanto notar-se que os indutores de CYP3A4 (erva de São João, anticonvulsivos, rifampicina, etc.) e inibidores de CYP3A4 (sumo de toranja, antibióticos macrolídeos, metronidazol, antifúngicos, HAART, etc.) podem levar à alteração dos níveis de drogas.
Riociguat
Riociguat pertence a uma nova classe de terapia de HAP de medicamentos. Tal como os inibidores convencionais de fosfodiesterase-5 (PDE-5), funciona através da via de sinalização de óxido nítrico vasodilatador (NO). Riociguat estimula a guanilato ciclase independentemente do NO, levando a um aumento da guanosina monofosfato cíclico intracelular (cGMP). O GMPc por sua vez influencia a concentração de cálcio e, portanto, a contratilidade das células musculares lisas das artérias pulmonares. Os inibidores convencionais de PDE-5 inibem a degradação do cGMP. O seu efeito requer assim uma produção de cGMP basal, NÃO mediada. Como a HAP está associada à redução da produção endógena de NO, isto poderia limitar o perfil de eficácia dos inibidores de PDE-5. Esta desvantagem teórica é contornada com o riociguat.
Grandes ensaios controlados por placebo demonstraram a eficácia do riociguat em melhorar a distância percorrida a pé no ensaio de 6 minutos de caminhada para doentes com HAP (ensaio PATENTE) [8] e para doentes com hipertensão pulmonar tromboembólica crónica inoperável ou persistente/recorrente após tromboendarterectomia (ensaio CHEST) [9]. Ambos os estudos da fase III confirmaram um bom perfil de segurança, com hemorragia pulmonar a ocorrer em alguns casos.
A dosagem do riociguat deve ser determinada individualmente; a dose máxima é de 2,5 mg três vezes por dia. Os efeitos secundários mais comuns são hipotensão, dor de cabeça, tonturas e desconforto gastrointestinal incl. Dispepsia. A combinação com inibidores de PDE-5 ou NO preparações está contra-indicada, e as combinações com agentes antiplaquetários devem ser bem avaliadas caso a caso.
Selexipag
Selexipag é o primeiro agonista receptor de prostaglandina I2 disponível na forma de comprimidos que não consiste de uma molécula de prostacyclin. Até agora, só podiam ser utilizados análogos de prostaciclina, que tinham de ser administrados continuamente por via intravenosa ou subcutânea ou inalados de três em três horas devido a uma meia-vida muito curta.
A via de sinalização da prostacyclin tem um papel especial no tratamento da HAP, na medida em que apenas o epoprostenol (análogo da prostaglandina I2 para administração intravenosa contínua) foi documentado para reduzir directamente a mortalidade num ensaio controlado por placebo [10]. As prostaciclinas de administração contínua são o tratamento de escolha para a HAP descompensada.
O efeito do selexipag foi investigado pela primeira vez num pequeno estudo de fase II de 43 pacientes já em terapia de HAP com antagonistas dos receptores de endotelina ou inibidores de PDE-5 (ou ambos) [11]. Com selexipag, foi alcançada uma redução na resistência pulmonar de >30%, independentemente de os pacientes já terem sido ou não pré-tratados.
No estudo Griphon fase III com mais de 1100 pacientes e um desfecho clínico combinado (mortalidade e morbilidade), o benefício do selexipag mostrou-se novamente independente do sexo, da medicação pré-existente, da gravidade da deficiência de desempenho, da idade e da causa da HAP. O ponto final primário foi atingido por 42% dos pacientes com placebo vs. 27% dos pacientes com selexipag após uma média de 70 semanas [12].
Assumindo que a densidade dos receptores de prostaciclina varia de paciente para paciente e que, por conseguinte, são necessárias doses diferentes individualmente para o bloqueio máximo, foi fornecida uma filtração da dose de selexipag (400-3200 µg/d). Se ocorressem efeitos secundários (dor de cabeça, diarreia, náuseas ou dores na mandíbula), a dose inferior seguinte era escolhida como dose de manutenção. Como não foi observada qualquer diferença entre pacientes com doses altas e baixas na análise dos parâmetros, supõe-se que este conceito está provado (Fig. 4).
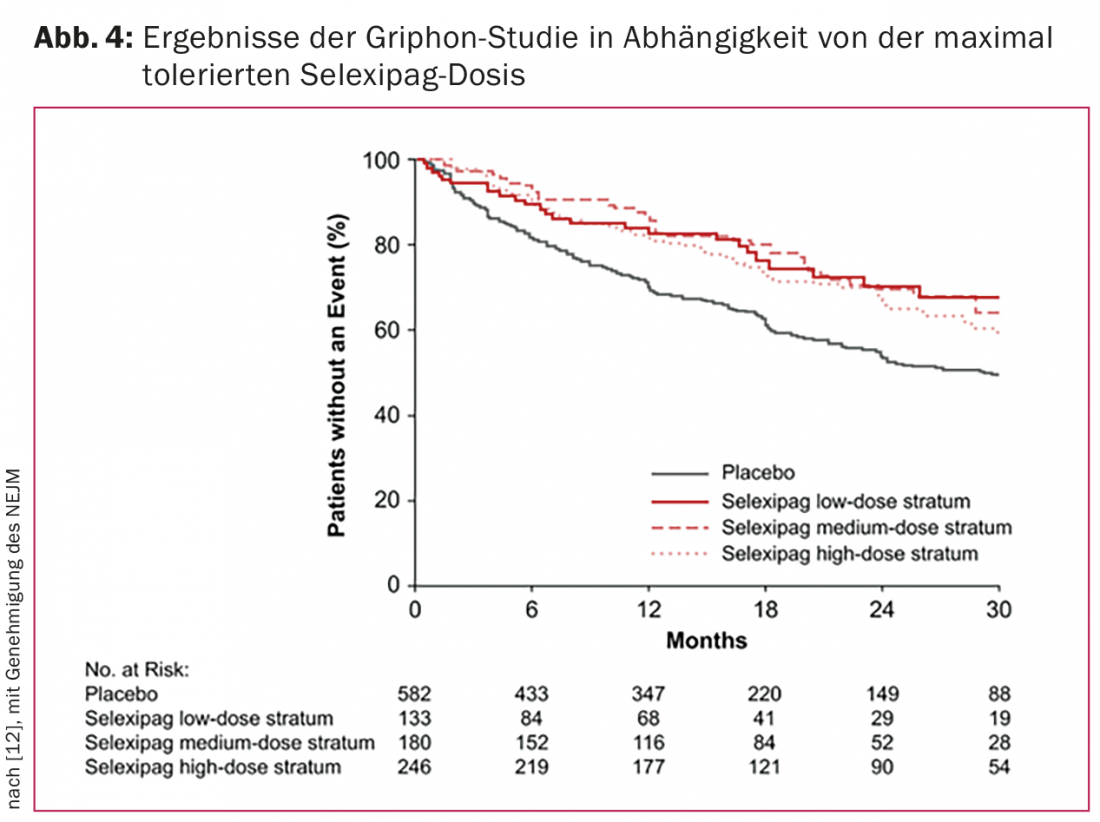
A Selexipag será aprovada na Suíça a partir de meados de 2016. Semelhante à droga riociguat, será outra droga PAH que não é prescrita numa dose fixa, mas que tem de ser titulada individualmente. Como todas as outras substâncias, só deve ser prescrito por médicos com experiência em tratamento de HAP, idealmente através de centros de HAP estabelecidos.
Literatura:
- Rich S, et al: Hipertensão pulmonar primária. Um estudo prospectivo nacional. Ann Intern Med 1987; 107(2): 216-223.
- Humbert M, et al: Avanços em Intervenções Terapêuticas para Pacientes com Hipertensão Arterial Pulmonar. Circulação 2014; 130(24): 2189-2208.
- Giaid A, Saleh D: Redução da expressão de óxido nítrico sintase endotelial nos pulmões de pacientes com hipertensão pulmonar. N Engl J Med 1995; 333(4): 214-221.
- Christman BW, et al: Um desequilíbrio entre a excreção de metabolitos de tromboxano e prostaciclina na hipertensão pulmonar. N Engl J Med 1992; 327(2): 70-75.
- Giaid A, et al: Expressão da endotelina-1 nos pulmões de pacientes com hipertensão pulmonar. N Engl J Med 1993; 328(24): 1732-1739.
- Iglarz M, et al.: Comparação da actividade farmacológica de macitentan e bosentan em modelos pré-clínicos de hipertensão sistémica e pulmonar. Life Sci 2014; 118(2): 333-339.
- Pulido T, et al: Macitentan e morbidade e mortalidade na hipertensão arterial pulmonar. N Engl J Med 2013; 369(9): 809-818.
- Ghofrani HA, et al: Riociguat para o tratamento da hipertensão arterial pulmonar. N Engl J Med 2013; 369(4): 330-340.
- Ghofrani HA, et al: Riociguat para o tratamento da hipertensão pulmonar tromboembólica crónica. N Engl J Med 2013; 369(4): 319-329.
- Barst RJ, et al: Uma comparação do epoprostenol intravenoso contínuo (prostacyclin) com a terapia convencional para a hipertensão pulmonar primária. O Grupo de Estudo da Hipertensão Pulmonar Primária. N Engl J Med 1996; 334(5): 296-302.
- Simonneau G, et al: Selexipag: um agonista receptor de prostaciclina oral e selectivo para o tratamento da hipertensão arterial pulmonar. Eur Respir J 2012; 40(4): 874-880.
- Sitbon O, et al: Selexipag para o Tratamento da Hipertensão Arterial Pulmonar. N Engl J Med 2015; 373(26): 2522-2533.
CARDIOVASC 2016; 15(2): 6-10