Mesmo na era do VEGF e dos inibidores de pontos de controlo, o prognóstico para o carcinoma avançado de células renais continua pobre. A utilização de terapias específicas e abordagens imunoterapêuticas é difícil devido à falta de alvos claros e à baixa imunogenicidade. No entanto, existem alguns novos conceitos de tratamento que poderão moldar a gestão desta doença nos próximos anos e suscitar ligeiras esperanças para o futuro.
Actualmente, os inibidores de ponto de controlo e VEGF (factor de crescimento endotelial vascular) estão em primeiro plano no tratamento do carcinoma metastático das células renais. Assim, combinações anti-VEGF/imunoterapia tais como axitinib/pembrolizumab ou a combinação de imunoterapia nivolumab/ipilimumab são normalmente utilizadas na primeira linha. Embora a utilização destas substâncias tenha melhorado o prognóstico, ainda há margem para melhorias. Com o desenvolvimento de novas abordagens terapêuticas tais como o bloqueio do factor induzível de hipoxia 2α (HIF-2α), estão actualmente a ser dados passos importantes que poderiam já contribuir para uma gestão mais bem sucedida num futuro próximo. Para além da inibição da HIF-2α, o foco é a utilização de interleucina-2 modificada (IL-2) e de conjugados antidrogativos bem como sobre conceitos terapêuticos que intervêm no metabolismo das células malignas.
Um olhar para trás
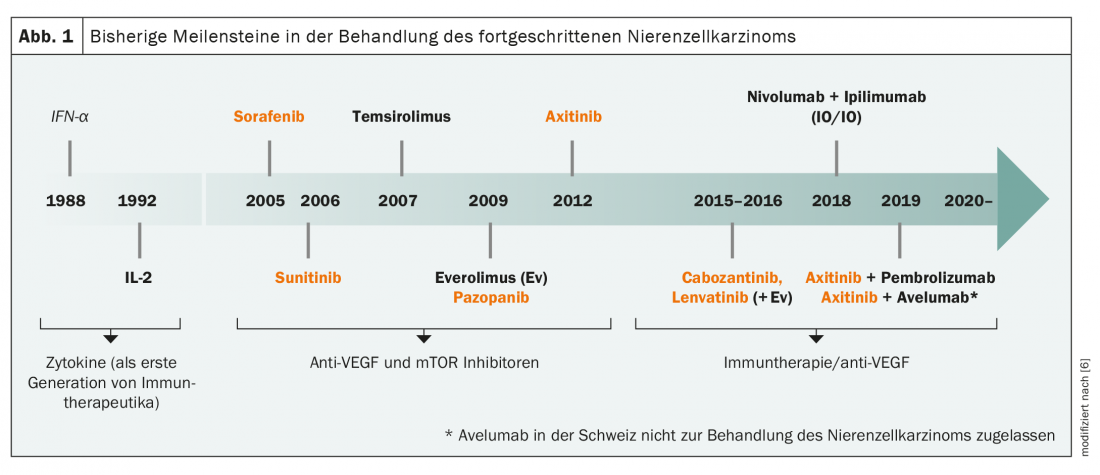
A história da imunoterapia no carcinoma de células renais remonta aos anos 80, quando citocinas como o interferon-α e a interleucina-2 foram utilizadas como forma precoce de imunoterapia (Fig. 1) . Depois foi silencioso durante muito tempo sobre novas opções terapêuticas até 2005, quando o sorafenibe entrou no mercado como o primeiro inibidor VEGF. Com sunitinibe, axitinibe e pazopanibe, seguiram-se rapidamente outros representantes desta classe de medicamentos, que foram complementados por inibidores de mTOR, como o everolimus. Na década de 2010, a segunda era da imunoterapia para o carcinoma avançado de células renais começou finalmente com os inibidores do pembrolizumab, nivolumab e ipilimumab, de modo que hoje em dia um grande número de agentes activos em várias combinações são aprovados para o seu tratamento. No entanto, a baixa imunogenicidade da maioria dos tumores e a falta de alvos claros levam a dificuldades na utilização de diferentes abordagens imunoterapêuticas e terapias orientadas. Quase não há casos em que a instabilidade por microsatélite ou um aumento da carga mutativa tumoral (TMB) – ambos marcadores preditivos para abordagens imunoterapêuticas – possam ser detectados. Há também uma falta de mutações conhecidas do condutor que são adequadas como alvos terapêuticos. No entanto, alguns ensaios clínicos de terapias específicas estão actualmente em curso, incluindo conjugados de anti-corpos e o protooncogene MET.
Terapias orientadas: Conjuntos anticorpos-fármacos e MET protooncogene
O protooncogene MET poderia ganhar importância no futuro, especialmente no tratamento do raro carcinoma de células renais papilares. No entanto, a monoterapia com savolitinibe e crizotinibe não foi convincente em estudos anteriores. Actualmente, as preparações estão a ser testadas em tratamentos combinados.
Tendo em conta os desenvolvimentos actuais, também é necessário ter cautela no que diz respeito aos chamados conjugados antifármacos. Estes medicamentos consistem em três componentes: Um anticorpo com elevada especificidade para antigénios associados a tumores, um ligante que é estável na corrente sanguínea mas que liberta o medicamento na célula alvo, e o próprio medicamento. Três estudos sobre tais conjugados anti-corpos tiveram de ser interrompidos num passado recente devido à falta de eficácia. Por outro lado, duas preparações que estão ainda a ser investigadas em ensaios clínicos são BA-3021 e DS-6000a. Este último medicamento tem o princípio activo Deruxtecan, que já é utilizado com sucesso para o carcinoma da mama.
HIF-2α inibição promissora
Mais encorajadores e já um pouco mais maduros são os dados sobre o bloqueio do factor induzível de hipoxia 2α (HIF-2α). Isto acumula-se nas pessoas afectadas que têm uma mutação do gene supressor do tumor de von Hippel-Lindau– e isto afinal é 90% de todos os doentes que sofrem de carcinoma claro de células renais. A superprodução de HIF-2α cria um sinal enganador que sinaliza escassez de oxigénio, levando a um aumento no fornecimento de sangue e a um crescimento mais rápido do tumor.
O mecanismo patogénico desencadeado pela HIF-2α pode ser interrompido pelo inibidor selectivo de pequenas moléculas belzutifan. Isto está actualmente a ser diligentemente investigado em ensaios clínicos (Tab. 1) . Até agora, a substância tem-se mostrado prometedora tanto como monoterapia como como parte de tratamentos combinados. Por exemplo, num ensaio da fase I/II com 55 participantes, foi observada uma redução do tamanho do tumor em 64%, e a taxa de resposta objectiva foi de 25%. Deve ter-se em conta que se tratava de uma população de estudo fortemente pré-tratada; o número médio de pacientes já tinha sido submetido a três linhas de terapia. A duração da resposta excedeu seis meses em 71% dos participantes, e 19 dos 55 pacientes continuaram o tratamento após um ano [1].
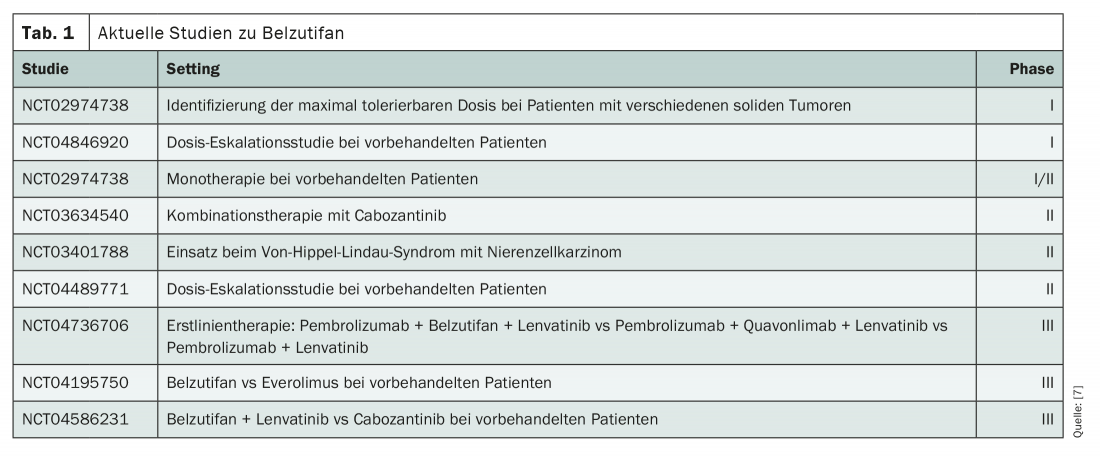
Em combinação com o cabozantinibe, foram vistos resultados semelhantes num ensaio recentemente apresentado na fase II [2]. Assim, 88% do total de 41 pacientes pré-tratados experimentaram uma redução do seu tumor, a taxa de resposta objectiva foi de 22% e a sobrevida mediana sem progressão (PFS) foi de 16,8 meses. Após um ano, 81% dos pacientes ainda estavam vivos. Os ensaios da Fase III estão a investigar a utilização do próprio Belzutifan na primeira linha. Aqui, a substância activa está a ser testada em combinação com pembrolizumab e lenvatinibe. Em linhas posteriores de terapia, Belzutifan está actualmente em julgamento como monoterapia contra o everolimus e em combinação com lenvatinib contra o cabozantinibe. Até agora, a anemia desencadeada por Belzutifan, causada por uma redução da eritropoietina, parece ser dose-limitante.
Metabolismo de tumores-alvo
Para além da HIF-2α, o metabolismo das células malignas também oferece um novo alvo potencial. Assim, a sobreactivação do crescimento celular das células tumorais leva a um metabolismo anormal da glucose. Este fenómeno, conhecido como o “efeito Warburg”, leva a uma falta de metabolitos e a um aumento da formação de lactato. A fim de assegurar um abastecimento suficiente, as células malignas aumentam o seu metabolismo de glutamina. Isto pode ser perturbado pela droga telaglenastat, que está actualmente a ser testada em combinação com cabozantinibe num ensaio de fase I [3]. Até agora, o complexo tem demonstrado uma actividade encorajadora com respostas sustentadas em casos avançados.
Além disso, o telaglenastat está a ser investigado no ensaio CANTATA de fase II, que está a testar a adição do composto ao cabozantinibe na segunda e terceira linhas de terapia. Estão incluídos 444 pacientes sem tratamento prévio de cabozantinibe, com conclusão esperada em 2022. Infelizmente, numa análise publicada em Janeiro de 2021, o ponto final primário PFS não foi cumprido. No entanto, se o perfil de segurança for bom, o ensaio continuará, especialmente para testar o telaglenastat noutras entidades, tais como o cancro do pulmão de células não pequenas.
Voltar às Raízes: Interleukin-2
A Interleukin-2 (IL-2) está actualmente a experimentar um renascimento como uma potencial opção terapêutica no carcinoma das células renais. Mesmo nos estudos originais sobre aldesleukin dos anos 80, foi frequentemente demonstrada uma duração de resposta impressionantemente longa. Contudo, as taxas de resposta ao tratamento foram baixas e a substância provou ser tóxica. A taxa de mortalidade foi de 4%, devido em particular à síndrome de fuga capilar desencadeada pela IL-2 [4]. Várias modificações da IL-2 devem agora evitar estes efeitos negativos e aumentar a taxa de resposta. Por exemplo, a ligação em cadeia α pode ser evitada, resultando em menos efeitos secundários e numa maior proliferação de células T effector, enquanto que são produzidas menos células T reguladoras.
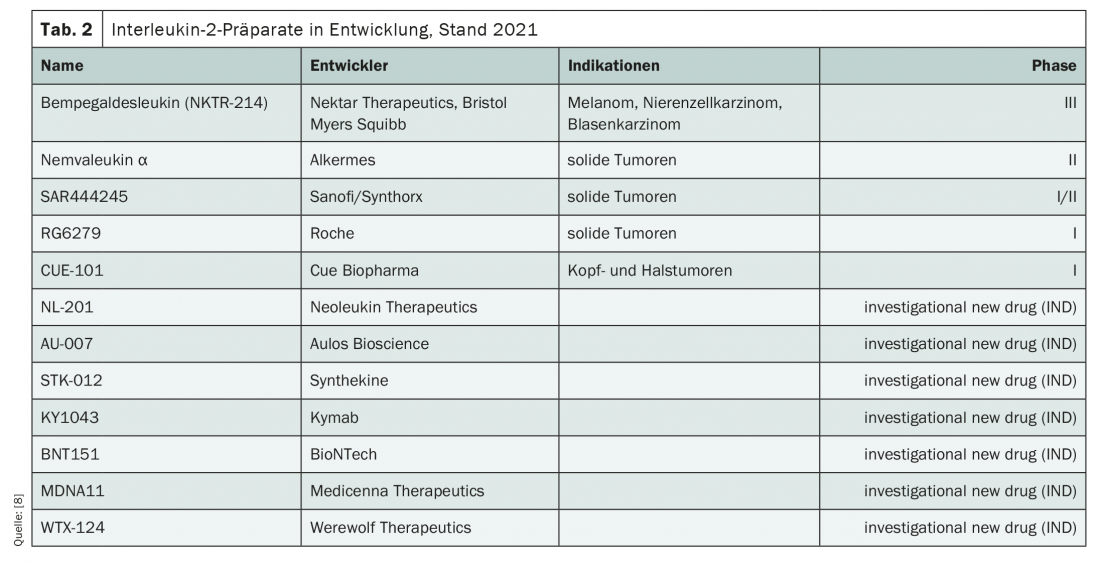
Actualmente, está em desenvolvimento um bouquet colorido de candidatos IL-2 de várias empresas (Tab. 2) . A Bempegaldesleukin, que está actualmente a ser investigada no estudo da fase III PIVOT-09, tem o maior número de dados. Destina-se a ser utilizado em melanoma, carcinoma de células renais e cancro da bexiga. Em combinação com nivolumab, a taxa de resposta em estudos iniciais num ensaio de fase I foi de 71,4% na primeira linha de terapia, enquanto ainda era de 28,6% na segunda linha [5]. Outros exemplos de modificações químicas da IL-2 incluem nemvaleukin α e SAR444245, que estão a ser testados em ensaios de fase II para utilização em tumores sólidos.
Quintessência
Embora dados a longo prazo sobre a utilização de inibidores HIF2α, IL-2, conjugados de anti-corpos e inibidores do metabolismo da glutamina no carcinoma de células renais claras ainda estejam por ver e ainda haja alguns obstáculos a ultrapassar antes de uma utilização clínica generalizada, algo está a acontecer no pipeline. Em particular, o bloqueio de HIF2α mostrou ser prometedor nos ensaios clínicos. No entanto, estes sucessos não podem esconder o facto de ainda faltarem opções específicas, especialmente para os subtipos papilares, cromófobos e medulares de acordo com , e é necessário identificar alvos adequados.
Fonte: Apresentação “Novel Targets and Promising New Therapies for Renal Cancer”, Howard Burries, reunião anual da Associação Americana para a Investigação do Cancro (AACR), 09.-14.04.2021, realização virtual
Literatura:
- Bauer TM: O inibidor oral HIF-2 α inibidor MK-6482 em doentes com carcinoma de células renais claras avançadas (RCC): Acompanhamento actualizado de um estudo fase I/II2021; Apresentação, American Society of Clinical Oncology (ASCO) Genitourinary Cancers Symposium, 11-13.02.2021.
- Choueiri TK: Estudo da fase 2 do factor induzível de hipoxia oral 2α (HIF-2α) inibidor MK-6482 em combinação com cabozantinibe em doentes com carcinoma de células renais claras avançadas (ccRCC); apresentação, American Society of Clinical Oncology (ASCO) Genitourinary Cancers Symposium, 11-13 Fev 2021.
- Meric-Bernstam F, et al.: CB-839, um inibidor da glutaminase, em combinação com cabozantinibe em doentes com cancro de células claras e de células renais metastáticas papilares (mRCC): Resultados de um estudo da fase I. Journal of Clinical Oncology. 2019; 37(7_suppl): 549.
- Fyfe G, et al: Resultados do tratamento de 255 doentes com carcinoma metastático de células renais que receberam terapia com altas doses de interleucina-2 recombinante. J Clin Oncol. 1995; 13(3): 688-696.
- Diab A, et al: Bempegaldesleukin (NKTR-214) mais Nivolumab em Pacientes com Tumores Sólidos Avançados: Estudo da Fase I da Dose-Escalação da Segurança, Eficácia e Activação Imune (PIVOT-02). Descoberta do cancro. 2020; 10(8): 1158-1173.
- Choueiri T: Advanced Kidney Cancer Update – “A Glimpse into the Future” (Um Vislumbre do Futuro). Apresentação, SOCIEDADE DA ONCOLOGIA UROLÓGICA (SUO) 21ª REUNIÃO ANUAL; Washington, DC, Dezembro de 2020.
- www.clinicaltrials.gov (último acesso 16.04.2021)
- Mullard A: Restaurando a IL-2 à sua glória de imunoterapia contra o cancro. Nat Rev Drug Discov. 2021; 20(3): 163-165.
InFo ONCOLOGY & HEMATOLOGY 2021; 9(3): 18-21 (publicado 17.6.21, antes da impressão).