A doença hepática gorda não alcoólica é a doença hepática mais comum em todo o mundo. A diretriz alemã S2k, actualizada em 2022, recomenda o rastreio dos doentes em risco. O algoritmo de rastreio proposto inclui a avaliação da fibrose e a deteção da esteatose como elementos principais e está em grande medida em conformidade com as recomendações da EASL. Os principais pilares da terapia são a modificação do estilo de vida e o controlo das comorbilidades.
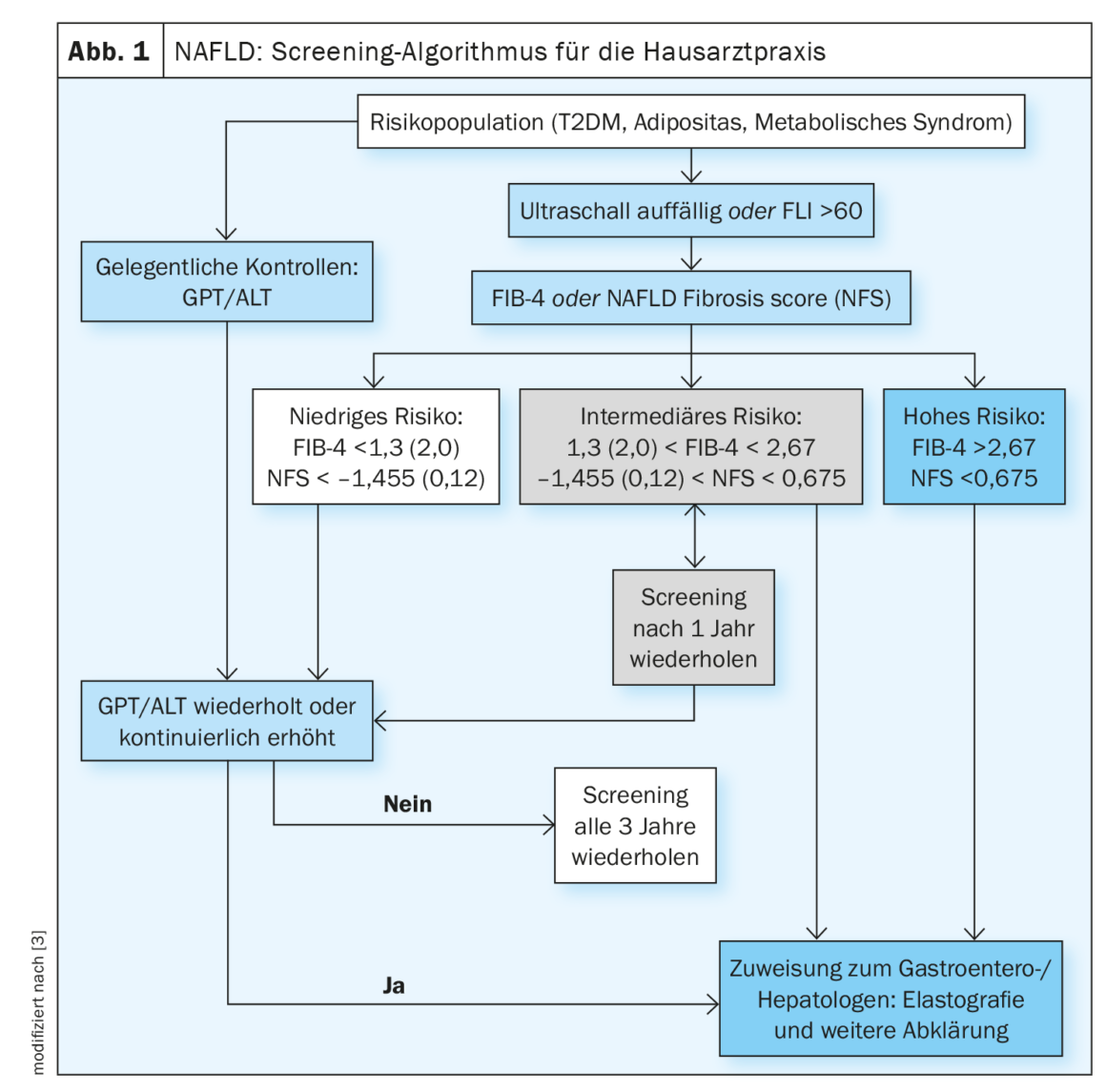
A doença hepática gorda não alcoólica é uma das principais causas de complicações associadas ao fígado e de morte. Um nível de fibrose elevado está associado a um risco acrescido de complicações. É possível a regressão da remodelação cirrótica [1]. Num estudo publicado em 2022, foi demonstrado que a melhoria da fibrose hepática reduz o risco de complicações em 10 vezes (HR, 0,08; 95% CI: 0,02-0,32) [2]. O algoritmo de rastreio da NAFLD proposto para os cuidados primários (Fig. 1) inclui pontuações como o quociente AST/ALT ou o FIB-4 [3]. Os doentes que têm um ou mais factores de risco para fibrose avançada devem ser rastreados: Idade >45-55 anos, diabetes tipo 2 (T2DM), síndrome metabólica, obesidade (IMC >30 kg/m²), hipertensão arterial [2,3]. A DMT2 e a obesidade são factores de risco independentes para o desenvolvimento de fibrose relacionada com a NASH [4]. Em doentes com suspeita de NAFLD, a ecografia transabdominal actua como a principal modalidade de imagem no rastreio.
Dependendo do estádio da fibrose, os doentes com DHGNA têm uma mortalidade relacionada com o fígado e uma mortalidade por todas as causas mais elevada do que os controlos saudáveis [5,6]. As causas de morte cardiovasculares estão no topo da lista [7,8].
Numa análise retrospetiva de 619 doentes com NAFLD durante o período de 1975-2005 e um seguimento médio de 12,6 anos, a doença cardiovascular foi a causa mais comum de morte (38%), seguida de doença tumoral não hepática (19%) e complicações da cirrose hepática (8%) [9]. Dois estudos prospectivos da Suécia, com um seguimento de até 33 anos, apresentam dados semelhantes: causas de morte cardiovasculares 43% e 48%, tumores não hepáticos 23% e 22% e mortalidade relacionada com o fígado 9% e 10% [10,11].
Rastreio da progressão da fibrose em doentes de alto risco
As directrizes s2k sugerem o rastreio de doentes em risco a cada 2-3 anos, utilizando um algoritmo que é largamente consistente com o das Directrizes de Prática Clínica da Associação Europeia para o Estudo do Fígado (EASL) e outras recomendações de consenso para médicos de clínica geral e diabetologistas, mas que é mais simples de utilizar (Fig. 1) [3,12]. O FLI (fatty liver index) pode ser utilizado para a determinação não invasiva do teor de gordura do fígado. Os instrumentos habitualmente utilizados para a previsão não invasiva da fibrose são o FIB-4 e o NAFLD Fibrosis Score (NFS).
O FIB-4 é fácil de calcular a partir dos valores de AST, ALT, plaquetas e da idade do doente. A avaliação baseia-se em dois valores de corte: os doentes com um valor <1,45 haben ein geringes Fibroserisiko, während Patienten mit einem Wert>2,67 têm um risco elevado de fibrose avançada [13].
O NAFLD Fibrosis Score (NFS) é fácil de calcular a partir de valores laboratoriais padrão através de uma máscara de introdução em linha. Para o cálculo, são introduzidos os seguintes parâmetros: Idade, IMC, diabetes sim/não, AST, ALT, plaquetas e albumina. Um valor inferior a -1,455 exclui a fibrose avançada com uma sensibilidade de 90%. Um NFS >0,676 diagnostica fibrose avançada com 97% de especificidade e 67% de sensibilidade.
Uma vez que ambas as pontuações se baseiam em grande medida em parâmetros de rotina, são adequadas para utilização no rastreio. Outras pontuações de fibrose não invasivas, como a relação AST/plaquetas (APRI) ou a pontuaçãoBARD (IMC, relação AST/ALT e diabetes), apresentam bons valores preditivos negativos, pelo que são adequadas para excluir a fibrose avançada.
A sequência de FLI (Fatty Liver Index) e FIB-4 foi estudada numa população de risco de diabéticos de tipo 2 para rastreio [14].
A utilização de valores de corte ajustados à idade pode ser útil para reduzir a elevada proporção de indivíduos com testes intermédios. A gestão dos doentes de risco intermédio é uma questão de discussão e pode ser organizada de forma diferente (novo rastreio ou encaminhamento direto para um hepatologista). Estudos futuros devem mostrar se novos marcadores de substituição (por exemplo, NIS4, pontuação FAST) ou técnicas de imagiologia como a elastografia por RM ou a MR-PDFF podem também ser utilizados para avaliar a progressão da fibrose individual e o curso da NASH [15].
Os dados do registo da NAFLD fornecem conclusões esclarecedoras
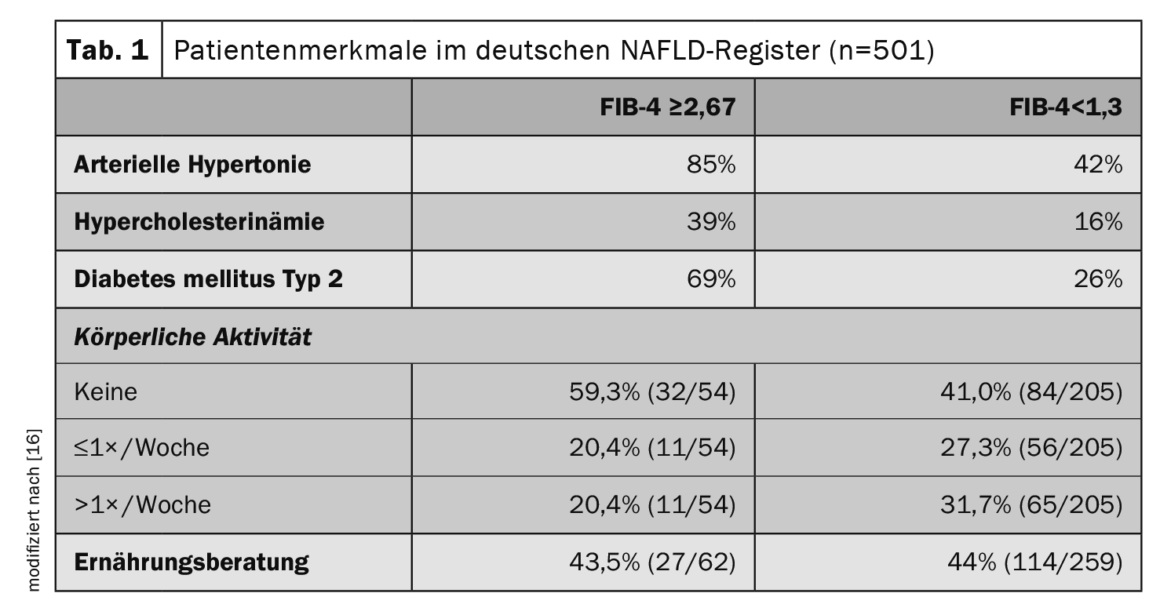
Para saber mais sobre os marcadores de risco e os factores significativos para o prognóstico associados à NAFLD, os dados dos registos são informativos. O Registo Alemão de NAFLD é um estudo prospetivo não interventivo da Fundação Alemã do Fígado para descrever as características clínicas e a evolução da doença dos doentes com NAFLD em estruturas de cuidados secundários e terciários [16]. Dos 501 doentes com NAFLD (idade média de 54 anos, 48% mulheres), 13% apresentavam um risco elevado de fibrose avançada (índice FIB-4 ≥2,67) e 10% tinham um diagnóstico clínico de cirrose. As estatinas foram utilizadas em 22% da população total do estudo, enquanto que, entre os diabéticos, a metformina, os agonistas do GLP-1 e os inibidores do SGLT2 foram utilizados em 65%, 17% e 17%, respetivamente. Entre os doentes com fibrose avançada (FIB-4 ≥2,67), 85% tinham hipertensão arterial, 69% tinham diabetes tipo 2 e 39% tinham hipercolesterolemia (tab. 1). O controlo das comorbilidades metabólicas e as alterações do estilo de vida (perda de peso e exercício físico) são a base do tratamento da NAFLD.
Congresso: Praxis Update
Literatura:
- «Leber», Gastroenterologie, Prof. Dr. med. Andreas Stallmach, Praxis Update, Berlin, 28-29.04.2023.
- Sanyal AJ, et al.: Cirrhosis regression is associated with improved clinical outcomes in patients with nonalcoholic steatohepatitis. Hepatology 2022; 75: 1235–1246.
- Roeb E, et al.; Collaborators: Aktualisierte S2k-Leitlinie nicht-alkoholische Fettlebererkrankung der Deutschen Gesellschaft für Gastroenterologie, Verdauungs- und Stoffwechselkrankheiten (DGVS) – April 2022 – AWMF-Registernummer: 021–025. Z Gastroenterol 2022; 60(9): 1346–1421.
- Jarvis H, et al.: Metabolic risk factors and incident advanced liver disease in non-alcoholic fatty liver disease (NAFLD): A systematic review and meta-analysis of population-based observational studies. PLoS Med 2020; 17: e1003100
- Dulai PS, et al.: Increased risk of mortality by fibrosis stage in nonalcoholic fatty liver disease: Systematic review and meta-analysis. Hepatology 2017; 65: 1557–1565.
- Vilar-Gomez E, et al.: Fibrosis Severity as a Determinant of Cause-Specific Mortality in Patients With Advanced Nonalcoholic Fatty Liver Disease: A Multi-National Cohort Study. Gastroenterology 2018; 155: 443–457.
- Younossi ZM, et al.: Global epidemiology of nonalcoholic fatty liver disease-Meta-analytic assessment of prevalence, incidence, and outcomes. Hepatology 2016; 64: 73–84.
- Kim D, et al.: Association between noninvasive fibrosis markers and mortality among adults with nonalcoholic fatty liver disease in the United States. Hepatology 2013; 57: 1357–1365.
- Angulo P, et al.: Liver Fibrosis, but No Other Histologic Features, Is Associated With Long-term Outcomes of Patients With Nonalcoholic Fatty Liver Disease. Gastroenterology 2015; 149: 389-397.e310
- Nasr P, et al: História natural da doença hepática gordurosa não alcoólica: um estudo prospetivo de acompanhamento com biópsias em série. Hepatol Commun 2018; 2: 199-210.
- Ekstedt M, et al.: Fibrosis stage is the strongest predictor for disease-specific mortality in NAFLD after up to 33 years of follow-up. Hepatology 2015; 61: 1547–1554.
- Berzigotti A, et al.: EASL Clinical Practice Guidelines (Cpgs) On Non-Invasive Tests For Evaluation Of Liver Disease Severity And Prognosis- 2020 Update. J Hepatol 2021; DOI: 10.1016/j.jhep.2021.05.025.
- Kaswala DH, Lai M, Afdhal NH: Fibrosis Assessment in Nonalcoholic Fatty Liver Disease (NAFLD) in 2016. Dig Dis Sci 2016; 61: 1356–1364.
- Ciardullo S, et al.: Screening for non-alcoholic fatty liver disease in type 2 diabetes using non-invasive scores and association with diabetic complications. BMJ Open Diabetes Res Care 2020; 8.
DOI: 10.1136/bmjdrc-2019-000904. - Loomba R, et al.: Multicenter Validation of Association Between Decline in MRI-PDFF and Histologic Response in NASH. Hepatology 2020;
DOI: 10.1002/hep.31121. - Geier A, et al.: Clinical characteristics of patients with nonalcoholic fatty liver disease (NAFLD) in Germany – First data from the German NAFLDRegistry. Zeitschrift für Gastroenterologie 2023; 61: 60–70.
| Titelbild: Micrograph of non-alcoholic fatty liver disease (NAFLD). Masson’s trichrome & Verhoeff stain. Autor: Nephron, wikimedia |
HAUSARZT PRAXIS 2023; 18(7): 28–29