A opção de tomografia computorizada sequencial PET (PET) abre novas possibilidades no tratamento do linfoma de Hodgkin. A terapia padrão actual para pacientes de baixo risco consiste em dois ciclos de ABVD e 20 Gy de radiação. A terapia primária guiada por PET, sem radioterapia, está também a ser testada. Os regimes terapêuticos guiados por PET também se estão a estabelecer cada vez mais em doentes com doenças de risco intermédio ou avançadas. A esperança de melhores taxas de sobrevivência reside também em novas substâncias tais como brentuximab vedotin ou nivolumab.
Devido à singularidade da biologia e da ocorrência, o linfoma de Hodgkin continua a ser a entidade linfoma mais bem caracterizada. De acordo com o Global Burden of Cancer Working Group, a incidência diminuiu entre 1990 e 2013. No mesmo período, a incidência de linfoma não-Hodgkin aumentou significativamente. Este artigo centra-se nas opções de tratamento para o linfoma de Hodgkin.
Redução da intensidade da terapia graças ao PET
Até recentemente, a pletora de estudos centrava-se em maximizar o índice terapêutico de uma terapia de primeira linha. O foco estava em alcançar as mais altas taxas possíveis de libertação de doenças e de sobrevivência global. A opção de tomografia computorizada sequencial PET (PET) abre novas possibilidades. Os resultados PET têm não só um prognóstico, mas também, cada vez mais, um valor preditivo. Com o PET provisório, a dose citostática total pode ser potencialmente reduzida e a radioterapia parcialmente omitida. O que é bastante novo é que isto é feito em parte à custa de uma menor eficiência da terapia inicial. Se a terapia inicial falhar, o efeito da terapia intensiva de salvamento é confiado.
Qual é a opinião dos pacientes? Um colega afectado há 50 anos escreveu: “Penso que a maioria das pessoas escolherá uma maior certeza de cura em vez da incerteza dos efeitos futuros. Se viverem o tempo suficiente para terem sequelas, ainda pode parecer a escolha certa” [1]. Esta declaração corresponde à realidade de hoje? Não é bem assim: cada vez mais pacientes com fases iniciais de tumores de células germinativas estão agora a optar por uma abordagem de “esperar e observar”. Estes pacientes aceitam um risco e, no pior dos casos, aceitam quimioterapia mais intensiva. O médico e o paciente devem estar absolutamente convencidos de que a sobrevivência global é idêntica a ambas as estratégias terapêuticas.
A seguinte discussão das opções de tratamento para o linfoma clássico de Hodgkin é dedicada a três grupos de doentes: Pacientes de baixo risco, pacientes de risco intermédio e pacientes com doença avançada. O tratamento do linfoma não clássico, CD20-positivo, linfocitopredominante de Hodgkin segue o tratamento do linfoma clássico de Hodgkin, especialmente nas fases avançadas. Os 10-20 pacientes que recebem este diagnóstico todos os anos na Suíça devem ser apresentados em conferências regionais sobre tumores.
Linfoma de baixo risco de Hodgkin
Para a preparação do linfoma de Hodgkin, é necessário um PET mas não um exame de medula óssea de acordo com o Sistema Ann Arbor 2014 revisto [2]. As fases baixas devem ter baixa sedimentação sanguínea, nenhum volume (ver secção sobre risco intermédio para definição), um máximo de duas estações de gânglios linfáticos e nenhuma lesão extranodal (E), de acordo com as directrizes do Grupo Alemão de Estudo Hodgkin (GHSG) utilizadas na Suíça. A terapia padrão actual foi estabelecida no estudo HD10 [3]. Com dois ciclos de ABVD e 20 Gy de radiação, após um período de observação de cinco anos, mais de 90% dos pacientes estão livres de doenças e mais de 95% sobrevivem. A toxicidade a longo prazo deste regime ainda não é conhecida. Em estudos pediátricos, 20 Gy também mostram toxicidade.
A terapia primária isenta de radioterapia com doses maioritariamente aumentadas de quimioterapia tem sido testada há já algum tempo. O exame PET parece trazer um avanço aqui. O estudo H10 do EORTC/Lysa e o estudo RAPID dos britânicos [4] mostram a mesma imagem. Se um PET for ABVD negativo após alguns ciclos, a radiação pode ser omitida. No ensaio RAPID, a sobrevivência sem progressão após três anos foi de 95% no grupo de radioterapia e 92% no grupo só de quimioterapia. O ensaio H10 foi interrompido cedo após um ano de observação devido a uma diferença PFS de 97,3% vs. 94,7%. Em ambos os estudos, no entanto, não houve absolutamente nenhuma diferença na sobrevivência. No estudo RAPID, 25% dos pacientes eram PET positivos. Receberam radioterapia local e 88% estavam livres de doenças após cinco anos.
Deve ser oferecida aos pacientes esta terapia guiada por PET para o linfoma de baixo risco de Hodgkin hoje em dia? O tempo de observação não é demasiado curto? Quantos ciclos de quimioterapia são necessários? Quatro, como sugerido pelo Grupo de Vancouver ou pela National Comprehensive Cancer Network (NCCN)? Três como no estudo RAPID? Dois como no estudo HD16 recentemente concluído (Fig. 1) do Grupo de Estudo Hodgkin Alemão (GHSG)? O HD16 incluía mais de 1000 pacientes e não foi parado prematuramente. Portanto, o conceito de dois ciclos não pode estar muito longe dos limites. O facto é que actualmente na América do Norte apenas metade dos pacientes de baixo risco de Hodgkin recebem radioterapia!
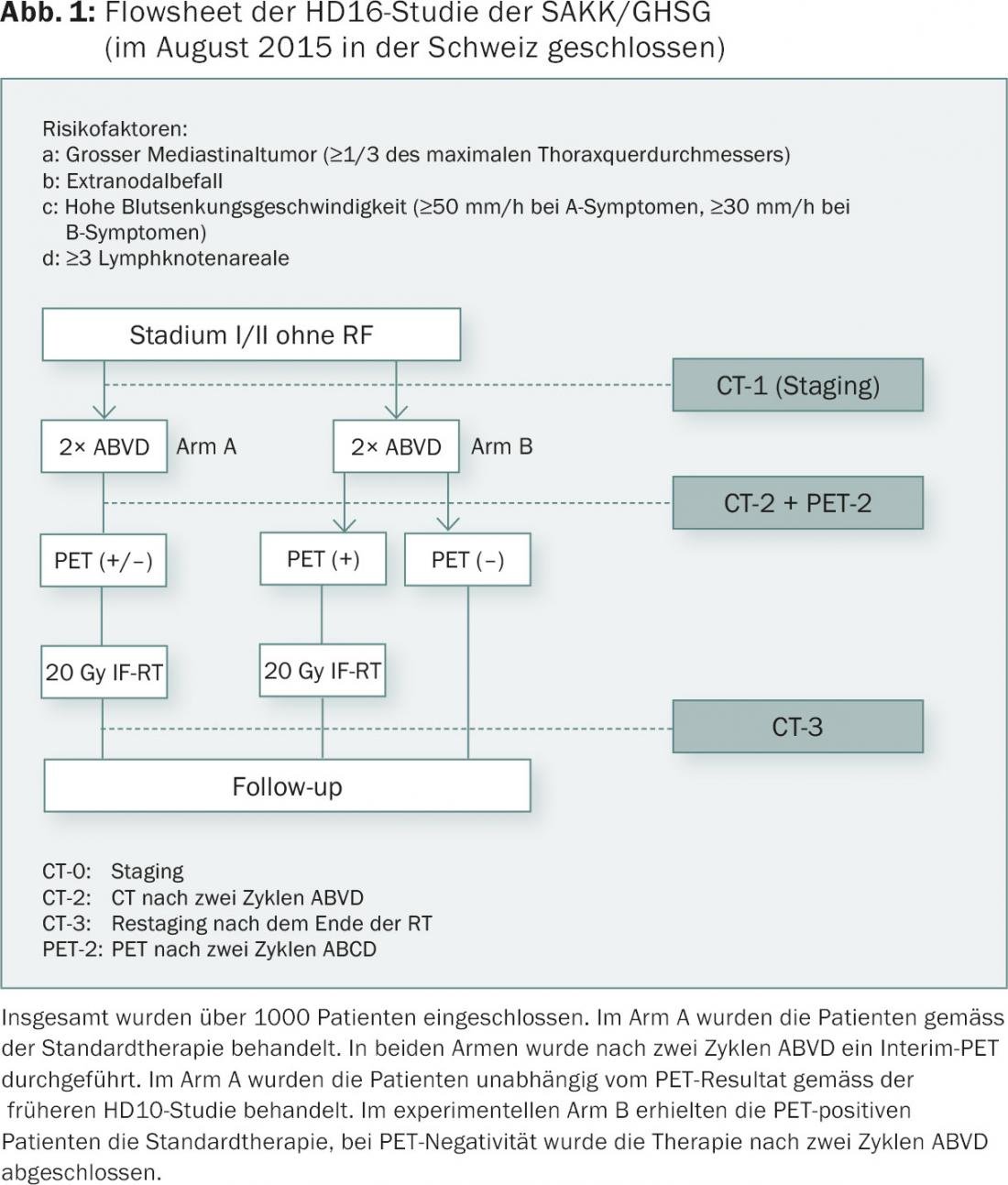
O que significa PET-positivo em PET provisório?
A avaliação de um PET provisório deve ser feita de acordo com a escala de 5 pontos da pontuação de Deauville. Os pontos 1 e 2 são normalmente considerados remissão completa. No Hodgkin’s, segundo Barrington, isto é independente da remissão morfológica [5]. As pontuações de Deauville de 4 e 5 são consideradas insuficientes para a remissão. Cada nova lesão é considerada uma progressão até prova em contrário. As rebiopsias são frequentemente necessárias. Uma pontuação de 3 é tratada de forma diferente. Nos estudos RAPID e H10, uma pontuação de 3 foi considerada PET-positivo; no estudo RATHL mencionado mais tarde, os pacientes com um Deauville 3 foram considerados PET-negativo.
Linfoma de Hodgkin de risco intermédio
Um risco intermédio é definido de forma ligeiramente diferente. Basicamente, trata-se de pacientes com doença locoregionalmente avançada, mas ainda confinados a um lado do diafragma. Um volume é comum e é relatado como >10 cm ou superior a um terço do diâmetro transtorácico, de acordo com os critérios revistos de Ann Arbor. Para isso já não é necessária uma radiografia de tórax convencional. Estes critérios estão em contraste com a definição de um volume no estudo HD17 do SAKK/GHSG (Fig. 2). Um volume é aqui definido como >5 cm na TC, um volume mediastinal como mais de um terço do diâmetro do tórax medido numa radiografia de tórax convencional.
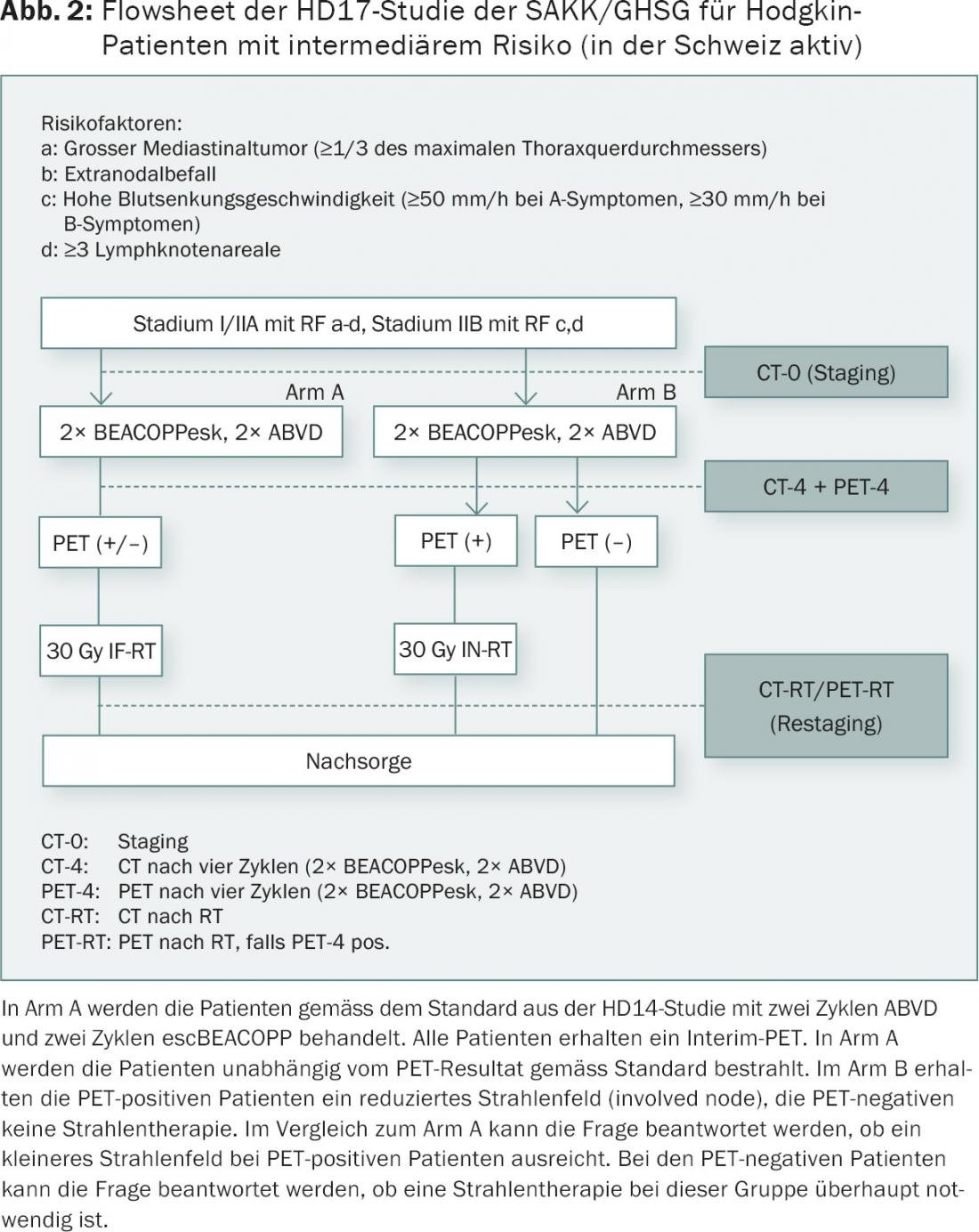
O estudo HD17 está a ser realizado com doentes em fase intermédia (AA fase I, II com volume, alta subsidência, envolvimento extranodal, três ou mais estações de gânglios linfáticos). Está a ser testado se a radioterapia pode ser omitida no caso de PET negativo e se o campo de radiação pode ser reduzido nos pacientes com PET positivo. O regime 2+2 (2 ABVD+2 escBEACOPP) de acordo com o estudo HD14 do GHSG é utilizado como quimioterapia de base. A utilização do regime escBEACOPP neste contexto é controversa. No entanto, a fertilidade e os tumores secundários são susceptíveis de ser menos problemáticos em comparação com seis ciclos. No ensaio EORTC H10, pacientes em fase intermédia – 40% com volume mediastinal – foram programados para PET após dois ciclos de ABVD. Os pacientes PET-negativos receberam quatro ciclos adicionais de ABVD, os pacientes PET-positivos receberam escBEACOPP duas vezes e radiação. O estudo foi terminado prematuramente devido a critérios pré-definidos. Resultados sólidos só podem ser esperados em 2016/17.
Linfoma de Hodgkin avançado
As Fases III e IV da AA são geralmente consideradas avançadas. O GHSG também inclui aqui fases IIB com grandes mediastino ou lesões E. A controvérsia ABVD/escBEACOPP tem sido discutida longamente noutros locais. Todos os ensaios aleatorizados mostraram uma sobrevivência significativamente melhor sem doenças, e o ensaio HD15 é sem dúvida o melhor resultado de tratamento alguma vez publicado no linfoma avançado de Hodgkin [6]. Contudo, as provas do benefício de sobrevivência do escBEACOPP sobre o ABVD só foram mostradas indirectamente no ensaio HD9 ou num modelo matemático, numa análise Cochrane.
Com o PET sequencial, esta discussão está a tornar-se cada vez mais obsoleta. Os resultados iniciais do ensaio HD15 estabeleceram a radioterapia guiada por PET com uma tomografia PET no final da quimioterapia. No total, apenas 10% de todos os pacientes foram ainda irradiados. Os resultados do estudo britânico RATHL foram mostrados no 13º Congresso do ICML em Lugano 2015. Pela primeira vez, estão disponíveis dados provisórios significativos de PET de um grande ensaio de fase III. Um PET negativo após dois ciclos de ABVD permite a omissão de bleomicina para os quatro ciclos seguintes com redução significativa da toxicidade da bleomicina. É discutível se uma sobrevivência livre de doenças de 84% após três anos com negatividade PET é uma boa referência. Mesmo com uma PET negativa, quase um em cada seis pacientes teve de se submeter a uma segunda terapia. No estudo HD15, que não foi orientado por PET em relação ao BEACOPP, apenas um em cada dez pacientes tinha recebido uma segunda terapia após cinco anos de observação. Vários grupos de investigação estão a estudar a escalada terapêutica da ABVD para o escBEACOPP em doentes com PET provisório positivo. Estes dados ainda não estão maduros.
No tratamento do linfoma de Hodgkin avançado, encontramo-nos actualmente num dilema na Suíça. O HD18 está fechado. O novo estudo Hodgkin (HD21) com implementação do brentuximab vedotin está à espera até 2016. O conceito de Viviani de realizar geralmente terapia baseada em ABVD e tratar todos os “fracassos” com uma terapia de salvamento em altas doses, se possível, soa tentador [7]. Isto significaria que pelo menos 20% dos doentes teriam de receber quimioterapia de alta dose no prazo de cinco anos após o diagnóstico. Na realidade, nestes casos, um terço dos doentes decide contra a quimioterapia de alta dose e o facto é que a quimioterapia de alta dose é curativa em apenas metade dos casos. Muita esperança reside em novas substâncias tais como brentuximab vedotin, nivolumab, etc. Aqui ainda é necessária muita paciência.
Conclusão
Em resumo, todas as evidências sugerem que cerca de 80% dos pacientes de Hodgkin irão experimentar uma toxicidade significativamente menor com terapia baseada principalmente em ABVD e PET-guia em comparação com os padrões actuais. Os restantes 20% necessitarão de terapias mais intensivas. Os pacientes e clínicos só aceitarão tal conceito se a sobrevivência for maximizada.
Literatura:
- Bispo G: Terapia PET-Directada para Linfoma de Hodgkin (correspondência). Novo Engl J Med 2015; 373: 392.
- Cheson BD, et al: Recomendações para avaliação inicial, encenação, e avaliação da resposta do linfoma Hodgkin e não Hodgkin: A Classificação de Lugano. J Clin Oncol 2014; 32: 3059-3067.
- Engert A, et al: Redução da intensidade do tratamento em doentes com linfoma de Hodgkin em fase inicial. N Engl J Med 2010; 363: 640-652.
- Radford J, et al: Resultados de um ensaio de terapia orientada por PET para o linfoma de Hodgkin em fase inicial. N Engl J Med 2015; 372: 1598-1607.
- Barrington SF, et al: Role of imaging in the staging and response assessment of lymphoma: Consensus of the international conference on malignant lymphomas imaging working group. J Clin Oncol 2014; 32: 3048-3058.
- Engert A, et al: quimioterapia de intensidade reduzida e radioterapia guiada por PET em doentes com linfoma de Hodgkin em fase avançada (ensaio HD15): um ensaio aleatório, aberto, fase 3 de não-inferioridade.Lancet 2012; 379: 1791-1799.
- Viviani S, et al: ABVD versus BEACOPP para o linfoma de Hodgkin quando está planeada uma dose elevada de salvamento. Engl J Med 2011; 365: 203-212.
InFo ONCOLOGY & HEMATOLOGY 2015; 14(5): 18-21











