Na preparação do seu roadshow nacional de 6 a 8 de Outubro de 2020, Andreas Pinter, MD, Hospital Universitário Frankfurt/Main, explicou a importância da interleucina (IL)-23 inibidores para a terapia moderna da psoríase e relatou as suas experiências com esta opção de tratamento, bem como os desejos e expectativas dos seus pacientes.

Andreas Pinter, MD Consultor Dermatologista,
Chefe da Investigação Clínica e Chefe da Consulta para Dermatoses Crónicas Inflamatórias,
Clínica de Dermatologia, Venereologia e Alergologia, Hospital Universitário de Frankfurt/Main
Desde a descoberta da IL-23 na viragem do milénio, o papel desta citocina pró-inflamatória como regulador principal no desenvolvimento da psoríase tem sido identificado [1, 2]. O que significa esta descoberta para a terapia moderna da psoríase?
Com a descoberta da IL-23, foi adquirida uma visão muito mais detalhada da fisiopatologia da psoríase. IL-23 é uma citocina pró-inflamatória muito precoce. Ao bloqueá-la, é possível intervir relativamente cedo na fisiopatologia. A IL-23 é correctamente chamada de “regulador principal”, porque ao inibi-la, muitas outras citocinas são subsequentemente suprimidas, o que por sua vez pode ter um efeito muito bom e duradouro no combate à psoríase.
2) Como diferem os diferentes inibidores de IL-23 risankizumab, guselkumab e tildrakizumab em termos dos seus mecanismos de acção?
Embora o modo de acção seja o mesmo para os três inibidores de IL-23, existem certas diferenças farmacológicas e clínicas. Assim, nem todos os anticorpos têm o mesmo sítio de ligação na citocina, razão pela qual a inibição de IL-23 pelos diferentes inibidores de IL-23 pode variar em força. Embora não estejam disponíveis dados frente a frente, podem ser observadas diferenças na eficácia. Por exemplo, a resposta PASI 75, PASI 90 ou PASI 100 do tildrakizumab em estudos de fase III é um pouco menos pronunciada do que a do risankizumab ou do guselkumab [3-5]. Existem também pequenas diferenças na meia-vida dos anticorpos, o que por sua vez se reflecte em diferentes intervalos de injecção. Guselkumab tem de ser injectado de oito em oito semanas na fase de manutenção, tildrakizumab e risankizumab apenas de doze em doze semanas – esta é uma grande vantagem [3-5].
3. Qual é a sua experiência prática no tratamento de doentes com psoríase em placas moderada a grave com o inibidor selectivo IL-23 risankizumab em termos de eficácia e tolerabilidade [3]?
Risankizumab já está no mercado há pouco mais de um ano. Até agora, pude observar um efeito muito bom, por vezes até excelente, mesmo fora dos ensaios clínicos, e todos os meus pacientes em risankizumab responderam à terapia. Uma grande proporção de pacientes está mesmo completamente ou quase completamente livre de sintomas. Portanto, o efeito é muito convincente. Além disso, nenhum doente se queixa de efeitos secundários relevantes, tais como infecções respiratórias. Globalmente, posso observar uma baixa taxa de efeitos secundários na prática, como já acontecia nos ensaios clínicos [3]. Assim, em resumo, a minha experiência com Risankizumab tem sido muito boa – é muito bem tolerada e muito eficaz.
4. O que esperam actualmente os seus pacientes da terapia da psoríase e, com base na comunicação com os seus pacientes, como avalia a gestão da terapia num tratamento com risankizumab?
Naturalmente, os pacientes querem uma terapia sem complicações que seja eficaz e tenha poucos efeitos secundários. Risankizumab é uma das drogas que combinam estas propriedades. O intervalo de três meses de injecção na terapia de manutenção torna-a muito fácil para os pacientes, uma vez que entretanto não têm de lidar de todo com a terapia. Também em termos de eficácia, como vemos tanto nos ensaios clínicos como na prática clínica, os pacientes podem beneficiar grandemente do tratamento. Podem tornar-se livres de sintomas com risankizumab, que é o que a maioria dos doentes espera da sua terapia. E a taxa de efeito secundário também é baixa, como já foi mencionado [3].
5. O que faz a diferença entre uma ausência completa e uma ausência quase completa de aparência para o paciente e o que é que isto significa para o médico?
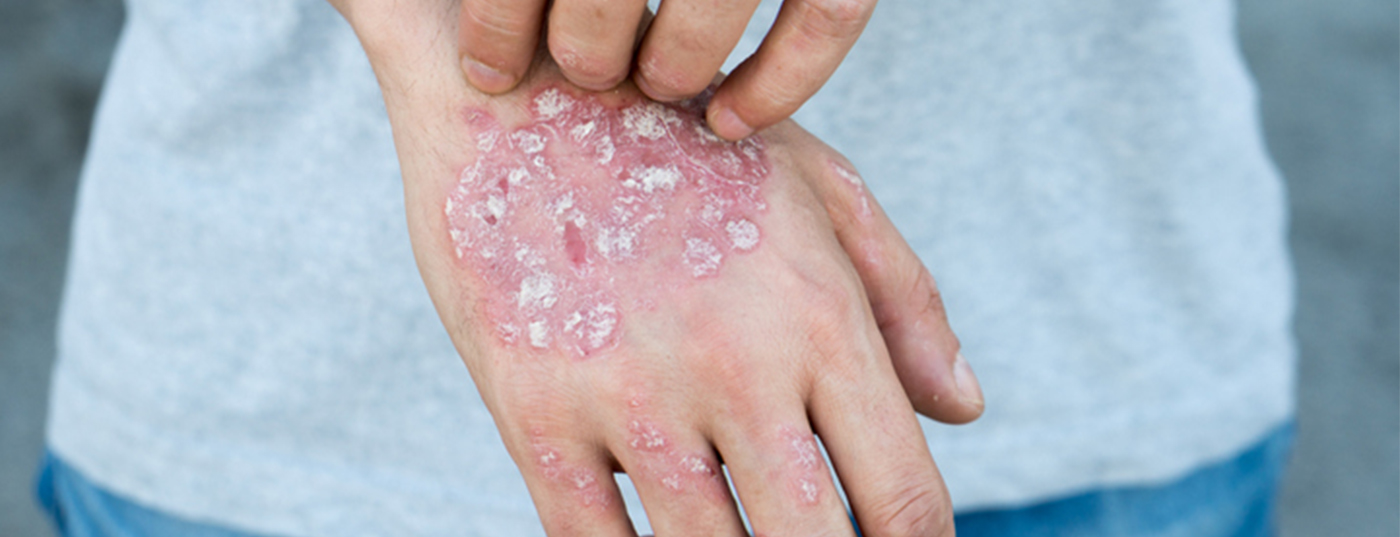
Se a pele sarou completamente ou só quase completamente faz a diferença em qualquer caso [6]. Porque se nem todos os sintomas desapareceram, o doente não tem a certeza de que a sua psoríase está completamente sob controlo. Especialmente quando há uma pretensão de completa liberdade de aparência, os sintomas residuais da pele são perturbadores, mesmo que sejam apenas placas menores. Também importa se as placas fazem comichão ou queimam e se estão em áreas visíveis, tais como o couro cabeludo ou as mãos [7]. Neste caso, é ainda mais desconfortável para os pacientes se não for alcançada uma completa ausência de sintomas, e estes podem começar a cremar ou esconder novamente as áreas afectadas. E é exactamente isso que os doentes não querem, porque querem uma vida sem psoríase [8]! Esquecer a doença é melhor alcançado com um Cicatrização da pele.
6. deve mudar o tratamento de um paciente com um PASI absoluto > 3 que está satisfeito com a sua terapia actual e como lida com tal paciente?
Tal situação deve ser discutida individualmente com o doente. Porque a forma de lidar com ela depende, entre outras coisas, do quanto o doente foi afectado quando a pré-terapia foi iniciada. Se alguém foi muito severamente afectado, com um PASI 30 ou superior, e ainda pode ser bem reduzido, não se tem necessariamente de apontar para um PASI < 3. Tais casos especiais são certamente também bem ajustados com um PASI < 5 ou <8. Em geral, contudo, deve-se sempre verificar novamente se o objectivo da terapia pode ser alcançado e o grau de satisfação do paciente. Se não estiver satisfeito, por exemplo, as terapias locais tópicas, por exemplo, cremes ou pomadas, podem ser adicionadas ao tratamento para se conseguir um PASI < 3. Se tais terapias adicionais, bastante convencionais, não conduzirem ao sucesso desejado, esperar pouco tempo é certamente também uma boa opção, pois a psoríase também tem um curso naturalmente flutuante. Contudo, se a psoríase não puder ser adequadamente controlada a longo prazo após um máximo de seis meses de uma determinada terapia, deve ser considerada uma mudança para um medicamento com eficácia comprovadamente maior. Contudo, não se deve alterar a terapia demasiado cedo, mas dar a cada medicamento pelo menos três meses para desenvolver o seu efeito. Porque apesar de muitos medicamentos estarem agora disponíveis, as opções de tratamento esgotam-se muito rapidamente. Globalmente, seria desejável que o médico procurasse discutir com o paciente e, dependendo da terapia actual, apontar-lhe que pode haver mais substâncias activas potentes entretanto disponíveis. Isto poderia aumentar a motivação para uma possível mudança.
Pode encontrar aqui a continuação da entrevista.
Literatura
CH-SKZD-210046_08/2021
Este artigo foi escrito com o apoio financeiro da AbbVie AG, Cham.