No primeiro simpósio suíço sobre malignidades peritoneais e HIPEC em St. Gallen, peritos falaram sobre os temas do carcinoma ovariano e do carcinoma colorrectal metastático. Tratava-se de opções de tratamento actuais e potenciais futuras. Qual é o valor correctivo de bevacizumab? Onde estão as possibilidades de terapia individualizada? E quais são os marcadores preditivos confirmados que devem orientar as decisões de tratamento?
Os mesmos princípios aplicam-se ao tratamento oncológico do carcinoma ovariano e aos carcinomas tubáricos e peritoneais. Segundo o Prof. Dr. med. Beat Thürlimann do Hospital Cantonal St. Gallen, existem padrões bem estabelecidos, mas quase não existem padrões de ouro. Tais são:
- Cirurgia óptima com descascamento
- Quimioterapia de primeira linha: à base de platina
- Quimioterapia de segunda linha: terapia combinada à base de platina
- Cirurgia paliativa.
As tendências relativamente novas são bevacizumab após o descascamento primário como adjunto da quimioterapia (disponível) e cediranibe e olaparibe (disponível em breve) para formas progressivas sensíveis à platina.

Bevacizumab (anti-VEGF): O estudo ICON7 (fase III) investigou a segurança e eficácia do bevacizumab como coadjuvante da quimioterapia padrão com carboplatina e paclitaxel em 1528 mulheres com cancro de ovário recentemente diagnosticado (FIGO fase I-IIA [klarzellig oder Grad 3] ou FIGO fase IIB-IV). Após a análise primária [1] da sobrevivência sem progressão já ter demonstrado um benefício da adição, especialmente nas mulheres em alto risco de progressão, os resultados finais relativos à sobrevivência global foram apresentados no Congresso da CCE de 2013: Embora não tenha sido possível mostrar uma diferença significativa entre os grupos de controlo e de estudo em toda a população, o subgrupo com um elevado risco de progressão (doentes “descascados” subaproveitados da fase III, da fase IV e doentes não operados) beneficiou particularmente: Aqui, a sobrevivência global melhorou significativamente.
O estudo AURELIA foi o primeiro ensaio randomizado para analisar a adição de bevacizumab à quimioterapia numa população de cancro dos ovários resistente à platina. Os participantes já tinham sido submetidos a duas ou mais terapias do cancro. Foram randomizados para receberem quimioterapia (paclitaxel, topotecan, “peguylated liposomal doxorubicin” [PLD]) ou bevacizumab plus quimioterapia, até à progressão ou toxicidade insustentável. Como resultado, a adição de bevacizumab prolongou significativamente a sobrevivência sem progressão por cerca de três meses. O benefício na sobrevivência global (também aproximadamente três meses), por outro lado, não alcançou significado estatístico, como ficou claro noutra apresentação no Congresso da CCE de 2013.
Cediranibe (anti-VEGF): O estudo ICON6 (fase III) investigou o cediranibe no tratamento do cancro do ovário sensível à platina, recidivado. Os participantes já tinham recebido quimioterapia de primeira linha à base de platina e, após uma nova recidiva, ou tomaram quimioterapia sozinhos (Braço A) ou quimioterapia mais cediranibe (braços B e C). Além disso, foi dada uma fase de manutenção com cediranibe no terceiro grupo de estudo (braço C) e uma fase de manutenção com cediranibe nos outros dois (braços A e B) um iniciado com placebo.
Foi demonstrado que a quimioterapia mais cediranibe seguida de manutenção de cediranibe proporcionou um benefício de sobrevivência significativo para esta população (em comparação com a quimioterapia apenas). Há também fortes evidências de um efeito do cediranibe na sobrevivência sem progressão durante e após a quimioterapia.
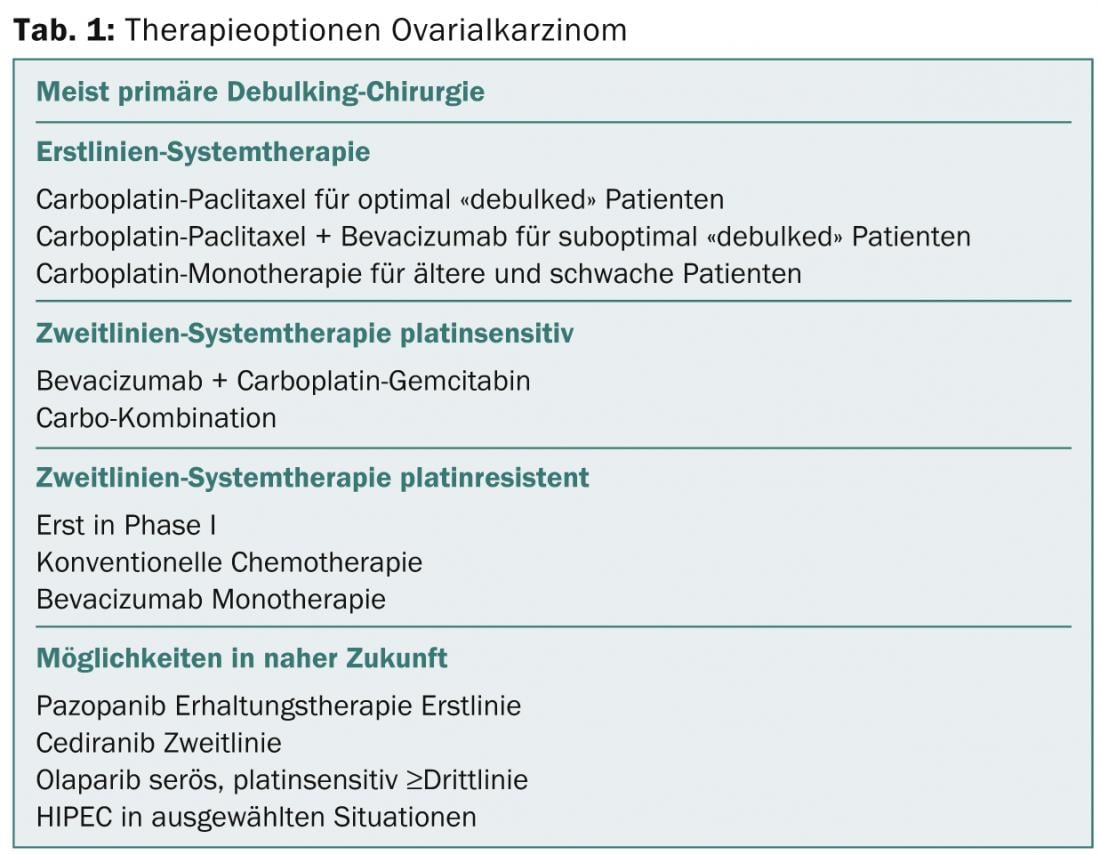
“Assim, há muitas opções para o tratamento do carcinoma primário dos ovários. As opções terapêuticas estão a aumentar, mas em última análise é sempre uma questão de custo”, conclui o Prof. Thürlimann. O quadro 1 fornece uma visão geral.
CRC peritoneal metastásico
O progresso no cancro colorrectal metastático (mCRC) deve-se principalmente a uma cirurgia mais agressiva, a uma melhor terapia sistémica e a uma colaboração mais estreita entre a oncologia e a cirurgia.
Prof. Dr. med. Ulrich Güller, Hospital Cantonal St. Gallen, discutiu pela primeira vez o tratamento sistémico: “A quimioterapia convencional é hoje realizada com sucesso como tratamento mono ou combinado com a ajuda das substâncias activas 5-fluorouracil (5-FU), capecitabina (preparação oral 5-FU), irinotecan e oxaliplatina. No entanto, precisamos sempre de novos alvos, e só os encontraremos se aprendermos a compreender melhor e com mais pormenor a proliferação de células tumorais.
Por exemplo, um novo medicamento que demonstrou um benefício de sobrevivência num ensaio de fase III como terapia de segunda linha é aflibercept [2]. Bloqueia a actividade de três factores de crescimento pró-angiogénicos: VEGF-A, VEGF-B e o chamado “factor de crescimento placentário” (PIGF). Impede que estes factores de crescimento se liguem aos receptores das células cancerosas e, assim, suprime o crescimento de novos vasos sanguíneos.
Os anticorpos utilizados actualmente no mCRC são bevacizumab (anti-VEGF-A), cetuximab (anti-EGFR) e panitumumab (anti-EGFR). Vários estudos mostraram que estes agentes podem melhorar as taxas de resposta e de sobrevivência.

Além disso, o regorafenibe [3], um inibidor oral multiquinase com actividade intracelular, é aprovado. Especificamente, bloqueia várias quinases envolvidas na angiogénese/oncogénese tumoral (incluindo VEGFR1, VEGFR2, VEGFR3, KIT, RET, PDGF).
“Portanto, esta é a nossa situação hoje: Temos quimioterapia convencional, aflibercept, três anticorpos e um inibidor da tirosina quinase”, explicou o Prof Güller. “Nos próximos anos, espera-se que os inibidores BRAF, PIK3, MEK e mTOR ganhem importância no mCRC. Além disso, o objectivo no futuro é administrar um tratamento adaptado ao paciente individual”, disse o Prof. Güller. “A determinação do estado do SAR (KRAS/NRAS) é um primeiro passo para uma tal terapia individualizada: Foi demonstrado que apenas os doentes com SAR de tipo selvagem beneficiam de anticorpos EGFR [4, 5]. A determinação do estado RAS é portanto necessária em qualquer caso antes de iniciar o tratamento com um anticorpo EGFR, pois o estado RAS tem um claro valor preditivo”.
Isto foi confirmado mais recentemente pelo ensaio FIRE-3, onde numa análise post-hoc o benefício global de sobrevivência da adição de cetuximab ao FOLFIRI (em oposição ao bevacizumab/FOLFIRI) foi ainda significativamente maior para os doentes do tipo selvagem RAS em comparação com a população original do tipo selvagem KRAS.
Fonte: 1º Simpósio Suíço sobre Malignidades Peritoneais e HIPEC, 23 de Janeiro de 2014, St.
Literatura:
- Perren TJ, et al: Um ensaio de fase 3 de bevacizumab no cancro dos ovários. N Engl J Med 2011 Dez 29; 365(26): 2484-2496. doi: 10.1056/NEJMoa1103799.
- Van Cutsem E, et al: A adição de aflibercept ao fluorouracil, leucovorina, e irinotecan melhora a sobrevivência num ensaio aleatório fase III em doentes com cancro colorrectal metastático previamente tratados com um regime à base de oxaliplatina. J Clin Oncol 2012 Oct 1; 30(28): 3499-3506. Epub 2012 Set 4.
- Grothey A, et al: monoterapia Regorafenib para cancro colorrectal metastásico previamente tratado (CORRECT): um ensaio internacional, multicêntrico, randomizado, controlado por placebo, fase 3. Lancet 2013 Jan 26; 381(9863): 303-312. doi: 10.1016/S0140-6736(12)61900-X. Epub 2012 22 de Novembro.
- Van Cutsem E, et al: Cetuximab mais irinotecan, fluorouracil, e leucovorin como tratamento de primeira linha para o cancro colorrectal metastático: análise actualizada da sobrevivência global de acordo com o estado de mutação do tumor KRAS e BRAF. J Clin Oncol 2011 20 de Maio; 29(15): 2011-2019. doi: 10.1200/JCO.2010.33.5091. epub 2011 abr 18.
- Douillard JY, et al: Tratamento Panitumumab-FOLFOX4 e mutações RAS no cancro colorrectal. N Engl J Med 2013 Set 12; 369(11): 1023-1034. doi: 10.1056/NEJMoa1305275.
InFo Oncologia & Hematologia 2014; 2(2): 18-21