Estudos como o CESAR ou SHOCK II, mas também o desenvolvimento posterior de bombas, oxigenadores e tubos de perfusão contribuíram para que a terapia com ECMO e ECLS se tenha tornado muito mais importante. Estes procedimentos são um desafio para a equipa de tratamento interdisciplinar.
ECMO significa “extracorporeal membrane oxygenation” e refere-se a uma bomba centrífuga extracorpórea com um oxigenador que está ligado à circulação do paciente através de um sistema de tubos. É feita uma distinção entre o ECMO venoso, que é utilizado na insuficiência respiratória aguda, e o ECMO veno-arterial, que é utilizado em pacientes em choque cardiogénico agudo. Recentemente, a nomenclatura foi especificada na designação ECMO para a configuração veno-venosa (vv) e ECLS (“Extracorporeal Life Support”) para a configuração veno-arterial (va).
A terapia com ECMO/ECLS ganhou rapidamente em importância nos últimos anos. Isto deveu-se inicialmente aos resultados publicados no estudo CESAR, que mostrou que os pacientes com síndrome do desconforto respiratório agudo (SDRA) tratados com ECMO venoso tinham uma vantagem em termos de sobrevivência e qualidade de vida em comparação com os pacientes que receberam apenas terapia de ventilação orientada para a SDRA [1]. A implantação de vaECLS em choque cardiogénico também experimentou uma extraordinária ascensão. Por um lado, isto deveu-se aos avanços técnicos nas bombas, oxigenadores e tubos de perfusão. Por outro lado, o ensaio SHOCK II, que não demonstrou um benefício de sobrevivência em choque cardiogénico com a utilização da bomba de balão intra-aórtica (IABP) [2], abriu o caminho para a utilização de vaECLS.
A gestão de pacientes em vvECMO ou vaECLS é particularmente desafiante. A implantação do sistema e o subsequente tratamento do paciente requer uma equipa interdisciplinar e multiprofissional, incluindo intensivistas, cirurgiões cardíacos, cardiologistas e pneumologistas, bem como perfusionistas e enfermeiros de cuidados intensivos.
Canulação e configuração de vvECMO e vaECLS
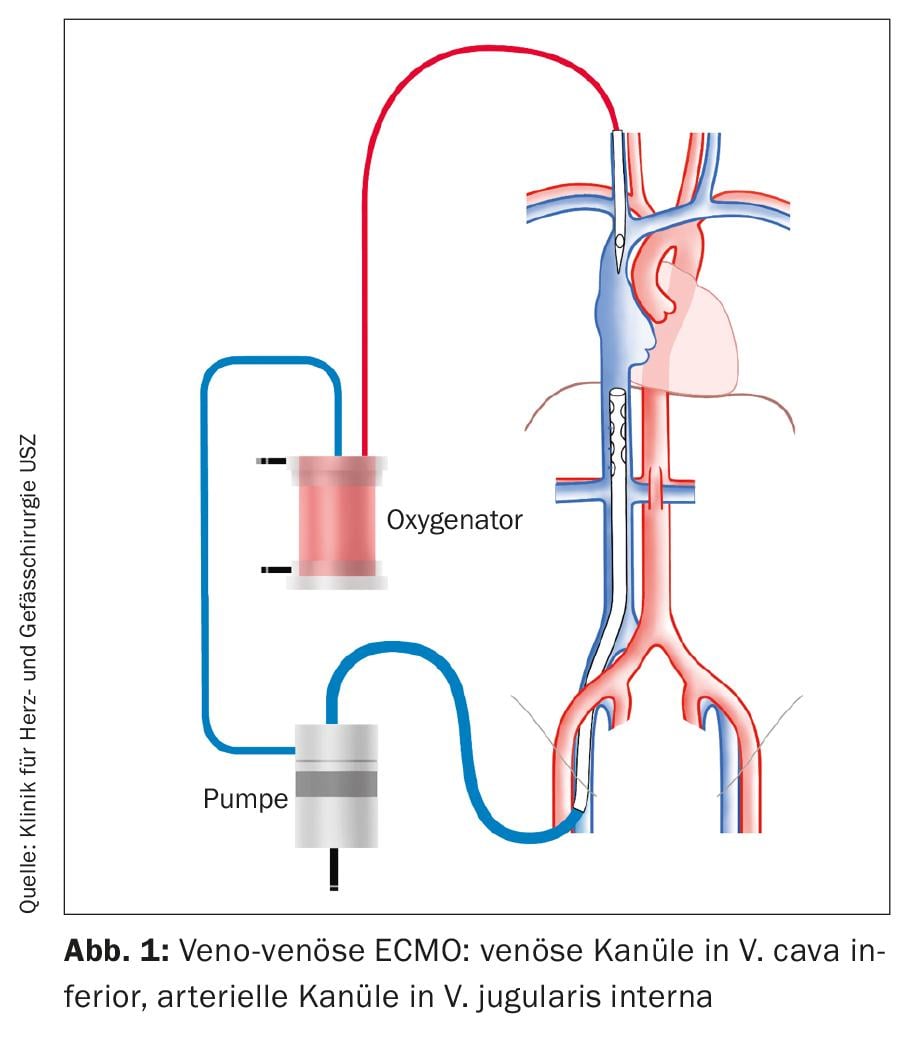
Como um procedimento para insuficiência respiratória aguda, ECMO é implantado numa configuração veno-venosa (Fig. 1). Para drenagem venosa, uma cânula é inserida na veia femoral comum (VFC). A ponta da cânula é colocada sob controlo ecocardiográfico para que fique à entrada da veia cava inferior (VCI) no átrio direito. Uma cânula é inserida na veia jugular interna (VJI) para fornecer o sangue oxigenado. A ponta da cânula encontra-se na veia cava superior (VCS).
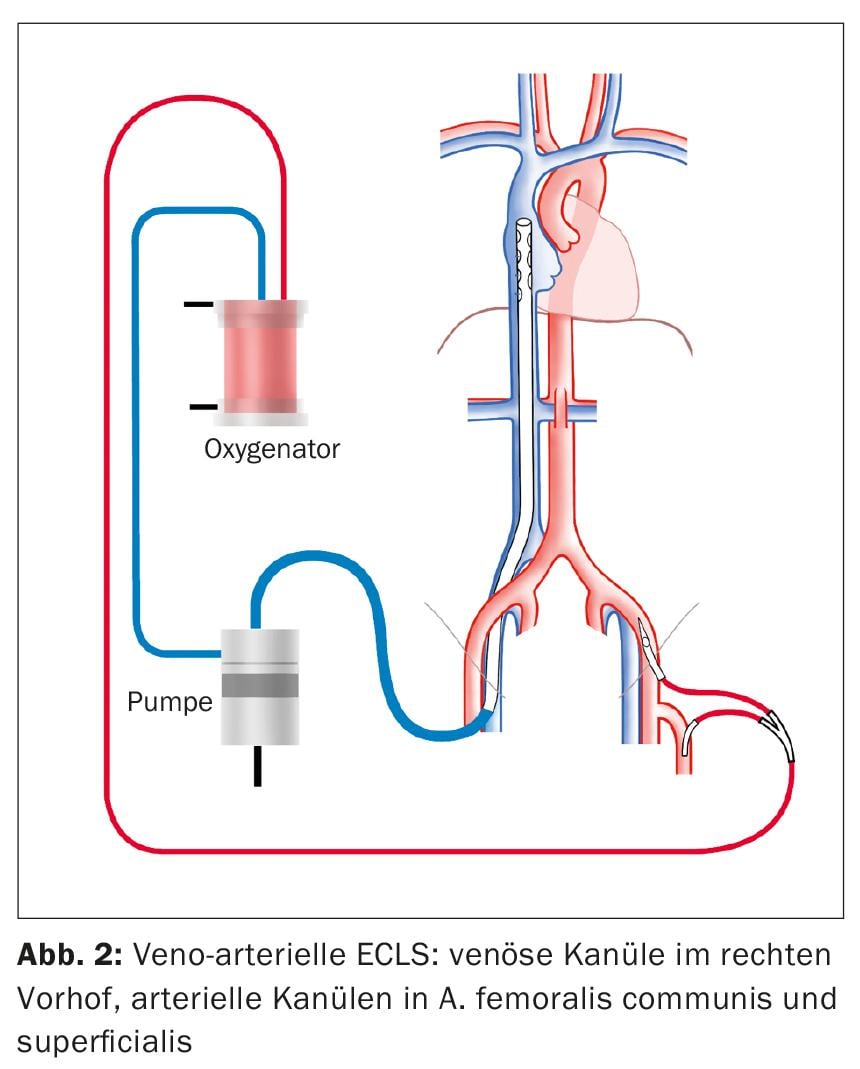
ECLS como procedimento para choque cardiogénico é implantado numa configuração veno-arterial (Fig. 2). Semelhante ao vvECMO, uma cânula é inserida no VFC correcto para drenagem venosa. Também sob controlo ecocardiográfico, a ponta da cânula é colocada de modo a que fique 1-2 cm na veia cava superior para conseguir uma drenagem óptima da metade superior e inferior do corpo. O acesso padrão para o fornecimento arterial é o A. femoralis communis (AFC). A cânula é inserida proximalmente na artéria ilíaca externa. Além disso, uma perna de perfusão é colocada distalmente na artéria femoral superficial para prevenir a isquemia da perna.
Em primeiro lugar, todas as cânulas são implantadas por via percutânea. É colocado um sistema de fecho percutâneo do recipiente antes da inserção da cânula AFC para conseguir o fecho do orifício de perfuração durante a subsequente remoção percutânea da cânula. Se a punção percutânea do AFC não for bem sucedida, a cânula deve ser implantada abertamente cirurgicamente. Este procedimento pode ser necessário quando se implanta em condições de reanimação. Não é necessário qualquer sistema de fecho vascular percutâneo para a remoção de cânulas venosas do VFC e da VJI. O buraco de perfuração pode ser fechado com uma sutura.
Estratégias de tratamento
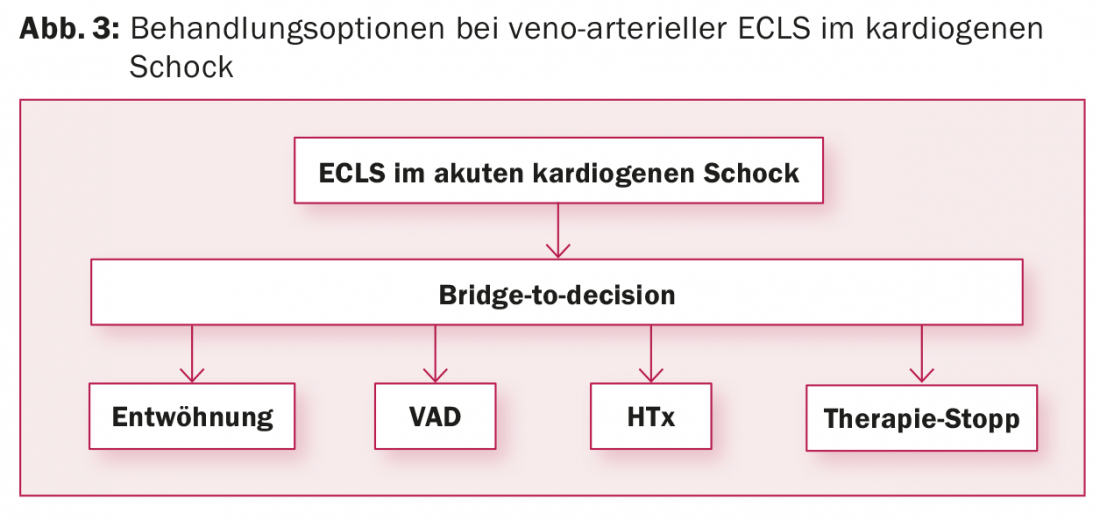
vaECLS: A implantação do vaECLS ocorre frequentemente numa situação de emergência que não dá tempo de avaliar a estratégia de tratamento após o vaECLS. As comorbilidades e o ambiente psicossocial do paciente são geralmente desconhecidos. Contudo, isto é um pré-requisito para determinar o conceito de tratamento seguindo o vaECLS. Portanto, o vaECLS é geralmente implantado como uma “ponte para a decisão” para ganhar tempo para determinar a situação do paciente. Além de clarificar as doenças concomitantes e a situação de vida do paciente, é necessária a avaliação da situação neurológica, especialmente se o vaECLS foi implantado em condições de ressuscitação. Para este efeito, para além da TAC craniana e do EEG, deve ser realizado um teste de despertar no ECMO para poder avaliar clinicamente-neurologicamente o paciente. Após a conclusão dos exames, há quatro opções de terapia adicional à escolha (Fig. 3):
- Desmame do paciente do vaECLS se a função cardíaca se recuperar.
- Se a função cardíaca não recuperar: Mudar o paciente de vaECLS para um dispositivo de assistência cardíaca como “ponte para transplante”, se o paciente for candidato a um transplante cardíaco, ou como “terapia de destino”, se o paciente não for candidato a um transplante cardíaco.
- Transplante cardíaco, se a mudança para um sistema de suporte cardíaco não parecer razoável, não há contra-indicações para o transplante cardíaco e está disponível um coração doador adequado dentro de um prazo máximo de duas a três semanas. Para tal, o paciente é incluído urgentemente na lista de espera. Se um coração doador adequado não estiver disponível dentro deste período, o paciente será implantado com um dispositivo de assistência ventricular, caso contrário, a taxa de complicações no vaECLS aumentará.
- Encerramento do vaECLS com morte consecutiva do paciente se a função cardíaca do paciente não recuperar e as contra-indicações não permitirem o implante de um dispositivo de assistência cardíaca ou transplante cardíaco.
De acordo com as actuais directrizes da Sociedade Europeia de Cardiologia de 2016 para insuficiência cardíaca aguda e crónica [3], o implante de um vaECLS pode ser considerado em choque cardiogénico refractário, tendo em conta a idade do paciente, comorbilidades e função neurológica (recomendação IIb, nível de evidência C).
vvECMO: A implantação do vvECMO é geralmente urgente e raramente de emergência. Há três opções de tratamento após o vvECMO:
- Desmame da vvECMO em caso de recuperação da função pulmonar.
- Transplante pulmonar se a função pulmonar não recuperar e não houver contra-indicações.
- Terminação da vvECMO com morte subsequente do paciente se a função pulmonar não recuperar e o paciente não for um candidato a transplante pulmonar.
Mortalidade e morbidez
vaECLS: A taxa de sobrevivência dos pacientes que receberam vaECLS em choque cardiogénico à alta hospitalar é de aproximadamente 40%. Este é o resultado de uma análise de 3846 pacientes no registo internacional da Organização de Apoio à Vida Extracorpórea (ELSO), de 2003 a 2013 [4]. Com base nos seus resultados, os autores desenvolveram uma pontuação de risco, a chamada “pontuação SAVE”, que permite a estimativa da taxa de sobrevivência dos pacientes em vaECLS, dependendo dos factores de risco presentes. Uma meta-análise de 1199 pacientes de 22 estudos observacionais de 2000 a 2014 confirma a análise do registo ELSO com uma taxa de sobrevivência de 40% dos pacientes vaECLS a alta hospitalar [5]. A taxa de sobrevivência parece baixa no início, cerca de 40%. Sem o vaECLS, no entanto, 0% teria sobrevivido. A baixa taxa de sobrevivência apesar da restauração de uma circulação suficiente por vaECLS deve-se pelo menos em parte aos complexos processos de choque cardiogénico com o desenvolvimento de uma reacção inflamatória sistémica e de uma síndrome de multiorgandysfunction. O estabelecimento de perfusão suficiente de órgãos apenas através de vaECLS nem sempre é obviamente suficiente para quebrar estes processos.
As taxas de sobrevivência a longo prazo dos pacientes após a implantação de um vaECLS são esparsas na literatura. Na meta-análise acima mencionada, a sobrevivência de 3 anos é dada como 42,7% [5]. Isto corresponde aproximadamente à taxa de sobrevivência até à alta do hospital. Isto significa que a mortalidade só é baixa depois de os pacientes terem tido alta do hospital.
As complicações no ECMO têm geralmente um impacto desfavorável na sobrevivência dos pacientes. Mais de metade de todos os doentes desenvolvem uma ou mais complicações [5]. As complicações vasculares podem ocorrer em 10-20% dos pacientes [5,6]. Dependendo da extensão da obstrução vascular pela cânula no AFC, pode ocorrer isquemia da perna. Para evitar isto, é agora prática corrente inserir uma cânula de perfusão distal no AFS no momento da implantação do vaECLS. As complicações hemorrágicas ocorrem em 26-41% dos pacientes [5,6]. São favorecidos pela doença de coagulação intravascular disseminada frequentemente presente no choque cardiogénico, produção insuficiente de factores de coagulação na insuficiência hepática, trombocitopenia e a diluição do sangue necessária no vaECLS.
As complicações neurológicas incluem o AVC isquémico ou hemorrágico em 6-8% dos doentes [5,6]. Resultam de um fluxo sanguíneo cerebral insuficiente em choque cardiogénico ou durante a ressuscitação antes da implantação do vaECLS. A complexa desordem de coagulação resultante do choque cardiogénico, que nem sempre pode ser detectada pela química de laboratório, pode favorecer o desenvolvimento destas complicações no vaECLS. As complicações infecciosas são comuns (25-49%) e incluem infecções locais nos locais de canulação (17%) e infecções sistémicas incluindo pneumonia e sepsis. As normas de esterilidade que nem sempre podem ser cumpridas durante a implantação de vaECLS de emergência e o sistema imunitário comprometido em choque cardiogénico favorecem o desenvolvimento de infecções [5–7]. A insuficiência renal aguda resulta de uma perfusão reduzida no choque cardiogénico e ocorre em 47-55% dos doentes [5,6]. A substituição renal é necessária em 40-46% dos pacientes [6,7]. Também foram desenvolvidas pontuações de risco para a terapia vvECMO para estimar a probabilidade de sobrevivência, como a pontuação PRESERVE ou PRESET [9,10].
vvECMO: Mais de 60% dos pacientes que recebem vvECMO por insuficiência pulmonar refractária sobrevivem à alta hospitalar, tal como demonstrado numa meta-análise recentemente publicada de 1042 pacientes [8]. A idade do paciente e o tamanho insuficiente da cânula com o consequente potencial de oxigenação insuficiente são factores de risco.
As complicações ocorrem em 40,2%. A hemorragia é a mais comum, com 29,3%. As hemorragias intracerebrais ocorrem em 5,4% dos casos. A hemorragia nos locais de canulação venosa não desempenha um papel significativo a 10%, em contraste com o maior risco de hemorragia nas cânulas arteriais em vaECLS. As infecções locais nos locais de canulação desenvolvem-se em pouco menos de 10% de todos os pacientes. Mas apenas 7% das complicações levam à morte.
Transporte de doentes ECMO
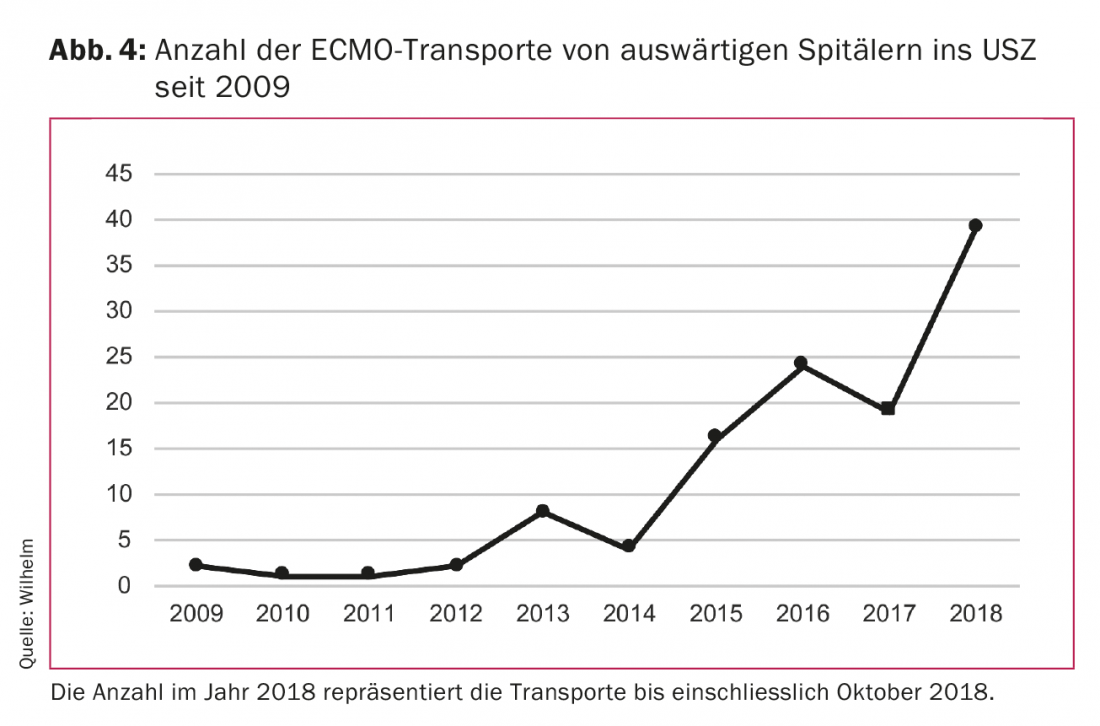
O desenvolvimento técnico das bombas centrífugas e oxigenadores levou a uma redução significativa da dimensão dos sistemas. Como resultado, podem agora ser facilmente transportados numa ambulância ou helicóptero. Isto tornou possível transportar pacientes de hospital para hospital no vaECLS ou vvECMO. Isto deu origem a um novo conceito de tratamento. Os pacientes em hospitais fora da cidade com insuficiência respiratória aguda ou em choque cardiogénico que não são transportáveis devido ao seu estado crítico podem ser tratados no local com o vaECLS ou vvECMO e subsequentemente transportados neste sistema para o hospital central para tratamento posterior. A nossa equipa da Clínica de Cirurgia Cardiovascular do Hospital Universitário de Zurique (USZ) tem sido capaz de efectuar tais transportes com sucesso, em segurança e sem problemas técnicos, quer em terra, quer de helicóptero. A necessidade deste tipo de tratamento tem aumentado significativamente nos últimos anos (Fig. 4). A equipa, constituída por um cirurgião cardíaco e um perfusionista, é levada com o equipamento para o hospital fora da cidade onde implantam o vaECLS ou vvECMO. O paciente é então transportado para a USZ no sistema. Os nossos resultados mostram que a taxa de sobrevivência de tais pacientes é absolutamente comparável à dos pacientes que recebem vaECLS ou vvECMO no nosso hospital central.
O desafio mantém-se
A utilização de vaECLS em choque cardiogénico e vvECMO em insuficiência respiratória refractária permite o tratamento de doentes críticos que teriam morrido antes de este tratamento estar disponível. No entanto, esta terapia ainda não é tão bem sucedida como gostaríamos que fosse. Isto é devido à complexidade desta população de doentes. Tendo em conta o esforço humano, material e financeiro envolvido, a utilização de vaECLS ou vvECMO deve ser examinada criticamente em cada caso individual do ponto de vista ético e socioeconómico. A utilização de pontuações pode ser aqui uma ajuda para a avaliação de risco. Os ensaios controlados aleatórios, que podem fornecer orientação noutras áreas da medicina, ainda não estão disponíveis neste campo e podem nunca estar disponíveis.
Mensagens Take-Home
- O ECMO venoso é utilizado em insuficiência respiratória refractária.
- O ECLS veno-arterial é implantado em choque cardiogénico agudo.
- ECMO veno-venoso e ECLS veno-arterial servem como “ponte para a decisão”.
- A taxa de sobrevivência à alta hospitalar é de 40% para o vaECLS e 60% para o vvECMO.
- Os pacientes podem ser transportados em segurança de um hospital fora da cidade para o hospital central no vaECLS ou no vvECMO.
Literatura:
- Peek GJ, et al: Eficácia e avaliação económica do apoio ventilatório convencional versus oxigenação extracorporal da membrana para insuficiência respiratória grave de adultos (CESAR): um ensaio controlado multicêntrico randomizado. Lancet 2009; 374(9698): 1351-1363.
- Thiele H, et al: Contrapulsação intra-aórtica por balão em enfarte agudo do miocárdio complicado por choque cardiogénico (IABP-SHOCK II): resultados finais de 12 meses de um ensaio aleatório, de marca aberta. Lancet 2013; 382(9905): 1638-1645.
- Ponikowski P, et al.: 2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure: The Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC) Developed with the special contribution of the Heart Failure Association (HFA) of the ESC. Eur Heart J 2016; 37(27): 2129-2200.
- Schmidt M, et al: Previsão de sobrevivência após ECMO para choque cardiogénico refractário: a sobrevivência após a pontuação veno-arterial-ECMO (SAVE). Eur Heart J 2015; 36(33): 2246-2256.
- Xie A, et al: Oxigenação da membrana extracorpórea venoarterial para choque cardiogénico e paragem cardíaca: Uma meta-análise. J Cardiothorac Vasc Anesth 2015; 29(3): 637-645.
- Cheng R, et al: Complicações da oxigenação extracorporal da membrana para o tratamento do choque cardiogénico e da paragem cardíaca: uma meta-análise de 1.866 pacientes adultos. Ann Thorac Surg 2014; 97(2): 610-616.
- Bermudez CA, et al: Oxigenação extracorporal da membrana para choque refractário avançado em cardiomiopatia aguda e crónica. Ann Thorac Surg 2011; 92(6): 2125-2131.
- Vaquer S, et al: Revisão sistemática e meta-análise de complicações e mortalidade da oxigenação da membrana extracorpórea veno-venosa para a síndrome do desconforto respiratório agudo refractário. Ann Cuidados Intensivos 2017; 7(1): 51.
- Schmidt M, et al: O escore de risco de mortalidade PRESERVE e análise dos resultados a longo prazo após oxigenação extracorporal da membrana para a síndrome do desconforto respiratório agudo grave. Intensive Care Med 2013; 39(10): 1704-1713.
- Hilder M, et al: Comparação de modelos de previsão de mortalidade na síndrome de angústia respiratória aguda submetida a oxigenação extracorporal da membrana e desenvolvimento de uma nova pontuação de previsão: a PREdição de Sobrevivência em ECMO Therapy-Score (PRESET-Score). Critérios Cuidados 2017; 21: 301.
CARDIOVASC 2018; 17(6): 4-7