Uma terapia precoce adequada da artrite reumatóide (AR) é de importância central para todo o curso futuro da doença, de acordo com a conclusão das actuais directrizes. Após o diagnóstico, a indicação de terapia modificadora de doenças deve ser avaliada no prazo de três meses. Para além dos DMARD sintéticos convencionais, encontra-se hoje disponível uma vasta gama de produtos biológicos e pequenas moléculas.
A artrite reumatóide (AR) é a mais comum das cerca de 400 doenças reumatológicas. Os sintomas típicos da artrite reumatóide são dor, rigidez articular e movimentos restritos. O diagnóstico baseia-se na história, nos critérios de classificação ACR/EULAR e noutros resultados da inspecção, laboratório, ultra-sons e exames de raios X [1]. “O padrão de infestação é importante”, diz Konstantinos Triantafyllias, MD, Hospital de Reumatismo Agudo, Brad Kreuznach e Universidade de Medicina Mainz (D) [2]. Quanto mais pequenas forem as articulações afectadas, mais pontos há de acordo com os critérios de classificação ACR/EULAR, com uma pontuação total de ≥6 fala-se de artrite reumatóide. O critério temporal são as queixas existentes há mais de 6 semanas.
Factor reumatóide frequentemente negativo
Os resultados laboratoriais indicativos para AR incluem [3]: ESR elevado, CRP elevado, detecção de factores reumatóides e/ou detecção de anticorpos contra peptídeos citrullinated (ACPA/CCP-AK). Contudo, em 50% dos pacientes com artrite reumatóide incipiente, o factor reumatóide é indetectável. Pelo contrário, um factor reumatóide positivo ocorre com o aumento da idade em até 20% das pessoas saudáveis. “O factor reumatóide é frequentemente negativo mesmo nas fases iniciais da artrite reumatóide, e é por isso que precisamos de mais marcadores”, resume o Dr. Triantafyllias [2]. Os anticorpos CCP, também chamados ACPA, são um marcador adicional importante que tem uma elevada especificidade para a artrite reumatóide. Considerando que estudos recentes relataram uma incidência crescente de RA ACPA-negativa [4,5].
“Tecnologia de Transmissão Óptica Espectral” – novo processo
As erosões visíveis na imagem de raio X só são normalmente visíveis numa fase posterior da doença, disse o orador. Deve-se pensar também na coluna cervical, que também é referida como o quinto membro do reumático. A instabilidade da articulação atlantoaxial ameaça a medula espinal.
Os exames ultrassonográficos também desempenham um papel importante. Pode perfurar o líquido e fazer testes laboratoriais para determinar com maior precisão a actividade da doença. Também importante é a RM com ou sem meio de contraste, tanto para diagnóstico inicial como para avaliação de seguimento. Além disso, existem alguns novos desenvolvimentos interessantes no campo do diagnóstico por imagem, tais como a “Tecnologia de Transmissão Óptica Espectral”. Esta é uma técnica de imagem não invasiva baseada em laser que visualiza o fluxo sanguíneo na área das articulações inchadas, explica o Dr. Triantafyllias [2]. Além disso, a quantificação é possível. Num estudo, foram demonstradas correlações com clínica (DAS28-CRP), marcadores inflamatórios (CRP) e achados artroscópicos [6].
A terapia sintomática é importante, mas não modifica a doença.
Num ataque agudo, os NSAIDs/ coxibs e/ou preparados de cortisona são frequentemente utilizados primeiro para a terapia sintomática. Embora estas substâncias sejam uma parte importante do tratamento na medida em que têm efeitos analgésicos e/ou anti-inflamatórios, não influenciam o curso da doença ou a destruição da articulação. De acordo com as directrizes da EULAR, as preparações de cortisona não devem geralmente ser utilizadas durante mais de três a seis meses na artrite reumatóide.
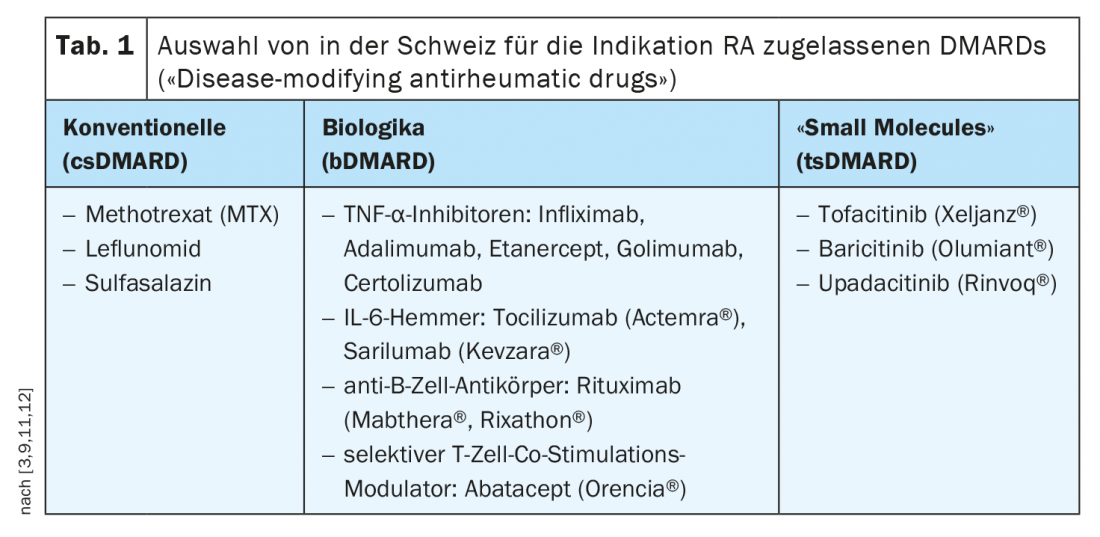
Em contraste, os DMARD são medicamentos que têm uma influência positiva a longo prazo no curso da artrite reumatóide ou outras doenças inflamatórias crónicas reumáticas, parando ou pelo menos retardando a progressão da doença. Os medicamentos modificadores de doenças dividem-se em substâncias convencionais, sintéticas (csDMARD), biológicas (bDMARD) e medicamentos básicos sintéticos (tsDMARD).
Conclusão das directrizes: Não perca a janela de oportunidade para DMARDs
Estudos recentes mostraram que o controlo rápido da actividade da doença através do início precoce da terapia com substâncias modificadoras da doença é crucial para o prognóstico futuro [7,8]. A fim de aproveitar esta janela de oportunidade, tanto a directriz “Therapy of rheumatoid arthritis with disease modifying drugs” como a “Interdisciplinary guideline Management of early rheumatoid arthritis” recomendam o início da terapia de modificação da doença (DMARD) no prazo de três meses após o diagnóstico [3,9]. O lema é que a utilização precoce de DMARD tem um efeito favorável sobre o prognóstico, tendo em conta as características individuais do paciente e factores situacionais. Para a implementação destas recomendações de tratamento, é necessário um cuidado interdisciplinar coordenado em que os primeiros sinais de doença sejam correctamente interpretados, a indicação de uma terapia modificadora da doença seja examinada e os afectados sejam prontamente encaminhados para um reumatologista.
Quando mudar de csDMARD para biólogos ou pequenas moléculas?
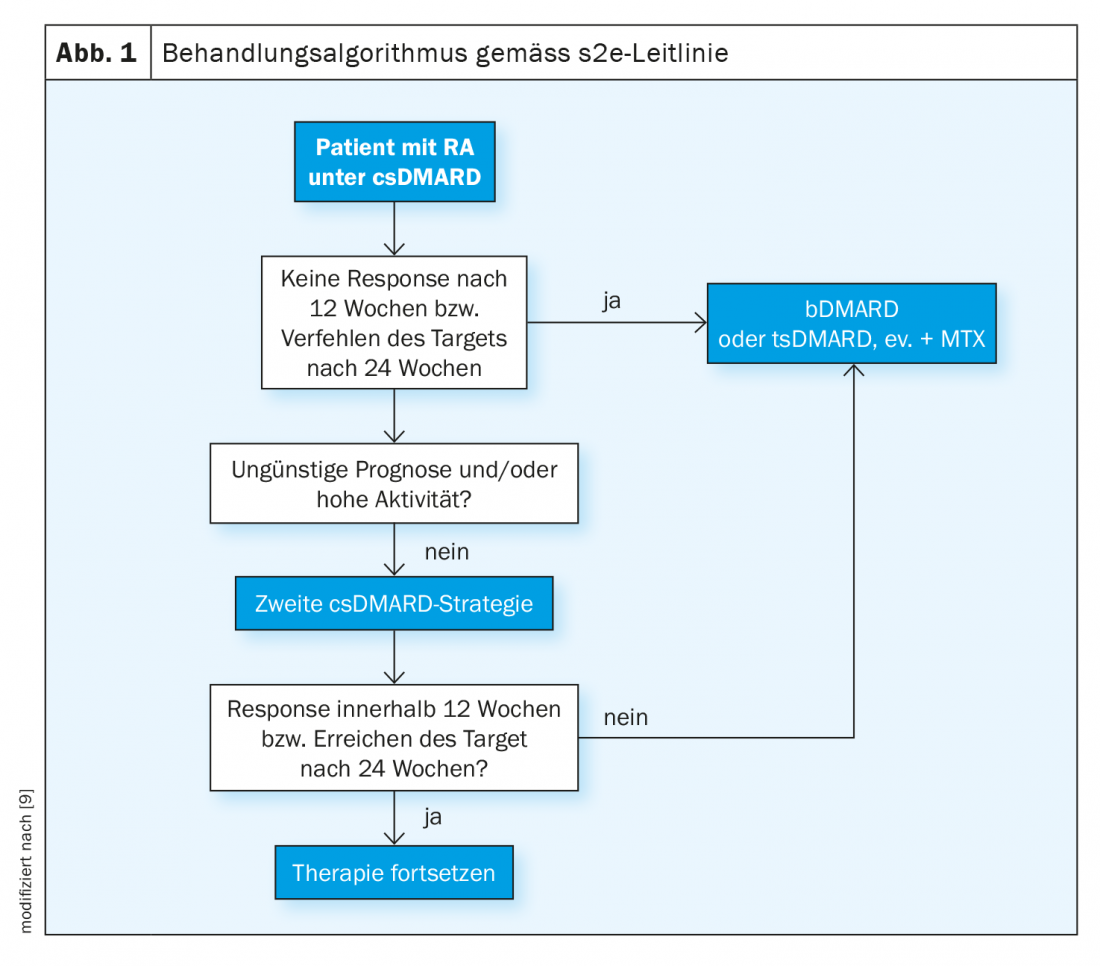
A directriz s2e recomenda a utilização de metotrexato primeiro se não houver contra-indicações (por exemplo, insuficiência renal). Em alternativa, pode ser utilizada leflunomida e sulfasalazina [9]. É melhor combinar inicialmente os csDMARD com glicocorticóides, uma vez que por vezes leva 6-12 semanas para se obter uma resposta terapêutica. O objectivo é até 30 mg de equivalente de prednisolona diariamente, com uma redução de dose para “dose baixa” (por exemplo, 5 mg ou 7,5 mg) no prazo de 8 semanas. Paralelamente à terapia de indução, deve ser realizado um acompanhamento. Quando é que alguém responde? De acordo com a directriz, se a pontuação composta da actividade da doença (por exemplo, DAS28) melhorar em 50% três meses após o início da terapia. A DAS28 regista o número de articulações dolorosas e inchadas sob pressão, bem como a actividade subjectiva da doença e os valores da inflamação. Se for observada uma redução de 50% na DAS28, a terapia pode ser continuada com o objectivo de obter uma remissão (0-1 inchaço ou articulações dolorosas). “Se isto não for conseguido, a terapia deve ter lugar”, explica o orador [2]. Neste caso, isto significa mudar para uma terapia biológica (Fig. 1) . Isto é especialmente verdade se estiverem presentes factores prognósticos desfavoráveis, tais como erosões, elevada actividade da doença e resultados seropositivos. “Então não se deve perder muito tempo com um segundo DMARD sintético convencional”, disse o orador. Após 3-6 meses, a resposta à terapia é verificada.
“Treat-to-target” é o lema
Se houver resposta insuficiente ou intolerância à primeira terapia bDMARD, recomenda-se uma mudança para uma bDMARD alternativa com o mesmo ou diferente modo de acção ou para uma bDMARD tsDMARD. Se a terapia após csDMARD for iniciada com um tsDMARD em vez de um bDMARD, deve ser feita, se possível, uma mudança para uma biologia se não houver resposta. Os medicamentos de base sintéticos específicos (tsDMARD, medicamentos de base sintéticos específicos que modificam os medicamentos anti-reumáticos) são o mais recente subgrupo de medicamentos de base. Ao contrário dos biólogos, os tsDMARD não interceptam substâncias pró-inflamatórias mensageiras no sangue, mas actuam dentro das células e interrompem o caminho de sinalização que aí promove a inflamação. A eficácia dos inibidores JAK na artrite reumatóide é comparável à da biologia.
Congresso: Conferência Anual da DGIM 2021
Literatura:
- Aletaha D, et al: 2010 Rheumatoid Arthritis Classification Criteria, Arthritis & Rheumatism 2010; 62(9): 2569-2581.
- Triantafyllias K: Diagnóstico e terapia primária para o internista em artrite reumatóide. Konstantinos Triantafyllias, MD, Reunião Anual da DGIM, 19.04.2021.
- Schneider M, et al.: S3-Leitlinie: Interdisziplinäre Leitlinie Management der frühen rheumatoiden Arthritis, 2019, AWMF-Register Nr. 060/002.
- Myasoedova E, et al: A epidemiologia da artrite reumatóide está a mudar? Resultados de um estudo de incidência populacional, 1985-2014. Annals of the Rheumatic Diseases 2020; 79: 440-444.
- Matthijssen XME, et al: O aumento da incidência de AR autoanticorpos negativos é replicado e é parcialmente explicado por uma população envelhecida. Ann Rheum Dis 2020, doi: 10.1136/annrheumdis-2020-217609.
- Triantafyllias K, et al. Valor Diagnóstico da Transmissão Óptica Espectral na Artrite Reumatóide: Associações com Características Clínicas e Comparação com Ultrassonografia Articulada. J Rheumatol. 2020; 47(9): 1314-1322.
- Combe B, et al: 2016 actualização das recomendações eulares para a gestão da artrite precoce. Anais das doenças reumáticas 2017; 76: 948-959.
- van Nies JA, et al: Avaliação das relações entre a duração dos sintomas e a persistência da artrite reumatóide: Existe uma janela de oportunidade? Resultados da primeira clínica de artrite precoce e coortes de espoirismo. Anais das doenças reumáticas 2015; 74: 806-812.
- Fiehn C, et al.: S2e-Leitlinie: Therapie der rheumatoiden Arthritis mit krankheitsmodifizierenden Medikamenten, 2018, AWMF Register Nummer: 060-004.
- Deutsche Rheuma-Liga Bundesverband e.V., www.rheuma-liga.de/rheuma/therapie/medikamententherapie/schmerzmedikamente (último acesso 16.06.2021)
- Rheumaliga Schweiz: Artrite reumatóide: viver com uma doença crónica, www.rheumaliga.ch/assets/doc/ZH_Dokumente/Broschueren-Merkblaetter/Krankheitsbilder/RA.pdf, (último acesso 16.06.2021)
- Sociedade Suíça de Reumatologia: Recomendação de Terapia Básica 2021.
HAUSARZT PRAXIS 2021; 16(7): 26-27 (publicado 27.6.21, antes da impressão).