Os tumores de células germinativas são globalmente raros, mas ao mesmo tempo os tumores mais comuns nos homens jovens. A gestão difere em função do estágio e do grupo de prognóstico. A terapia adequada e adequada ao estágio de tumores de células germinativas metastasisadas é um desafio neste contexto.
O tumor de células germinativas é uma entidade rara em geral, mas ao mesmo tempo o tumor mais comum nos homens jovens. A terapia adequada e adequada ao estágio de tumores de células germinativas metastasisadas é um desafio neste contexto. A seguir, a terapia de primeira linha de tumores metastáticos primários, bem como a terapia de recorrência, são explicadas com mais detalhe.
Introdução
Os tumores de células germinativas representam cerca de 2% de todos os tumores malignos e representam a neoplasia mais comum em homens com idades compreendidas entre os 15-45 anos. Na Suíça, cerca de 400 homens adoecem todos os anos, e cerca de 14 morrem todos os anos. Graças à aplicação de conceitos terapêuticos adequados ao estágio, pode ser alcançada uma taxa de cura superior a 90% em todas as fases. Histologicamente, os seminomas distinguem-se dos tumores de células germinais não sinomatosas. Enquanto 95% dos tumores testiculares nos homens ocorrem nos testículos, aproximadamente 5% estão localizados principalmente extragonadalmente. Os factores de risco conhecidos incluem o criptorquidismo, história de cancro testicular, história familiar positiva, infertilidade e síndrome de Klinefelter.
O sintoma mais comum é um aumento ou inchaço não doloroso do testículo. Em casos raros, os pacientes também notam sinais de doenças mais avançadas, tais como dores nas costas, dispneia, perda de peso ou sintomas neurológicos. Diagnóstico, exame clínico com palpação dos testículos, sonografia de ambos os testículos, e determinação laboratorial suplementar dos marcadores tumorais HCG, AFP e LDH são obrigatórios. Os marcadores tumorais já podem muitas vezes provar a neoplasia e servem também para a monitorização terapêutica e controlo de seguimento. É sempre realizada uma tomografia computorizada do tórax, abdómen e pélvis. A imagem da cabeça e dos ossos só é obrigatoriamente recomendada em caso de metástases extensivas, especialmente pulmonares, marcadores de tumores muito elevados, provas de sintomas clínicos ou em recidiva. Se o paciente desejar ter filhos, uma análise de esperma e subsequente criopreservação deve ser sempre realizada antes de se iniciar a terapia.
A orquiectomia é frequentemente a primeira e também já curativa etapa terapêutica na fase I localizada. No caso de tumores de células germinativas com uma elevada carga tumoral, constelação marcadora de tumores muito elevada ou com metástases sintomáticas pronunciadas, por outro lado, a orquiectomia só é realizada após a conclusão da terapia do sistema.
A classificação correcta das fases do tumor é relevante para a selecção da terapia e para a avaliação do prognóstico e optimiza as hipóteses de cura. Neste contexto, o uso de quimioterapia, cirurgia e radioterapia, a selecção dos medicamentos necessários e o tipo e duração da sua aplicação são precisamente definidos por recomendações e orientações consensuais internacionais.
No caso de tumores de células germinativas gonadal, a doença limita-se ao testículo na fase I. Muitas vezes, neste caso, a orquiectomia é seguida apenas de vigilância (“vigilância activa”) para seminomas e não seminomas. Contudo, se determinados factores de risco estiverem presentes, a quimioterapia ou radioterapia adjuvante pode também ser necessária na fase localizada, e raramente a ressecção cirúrgica dos gânglios linfáticos retroperitoneais (RPLND).
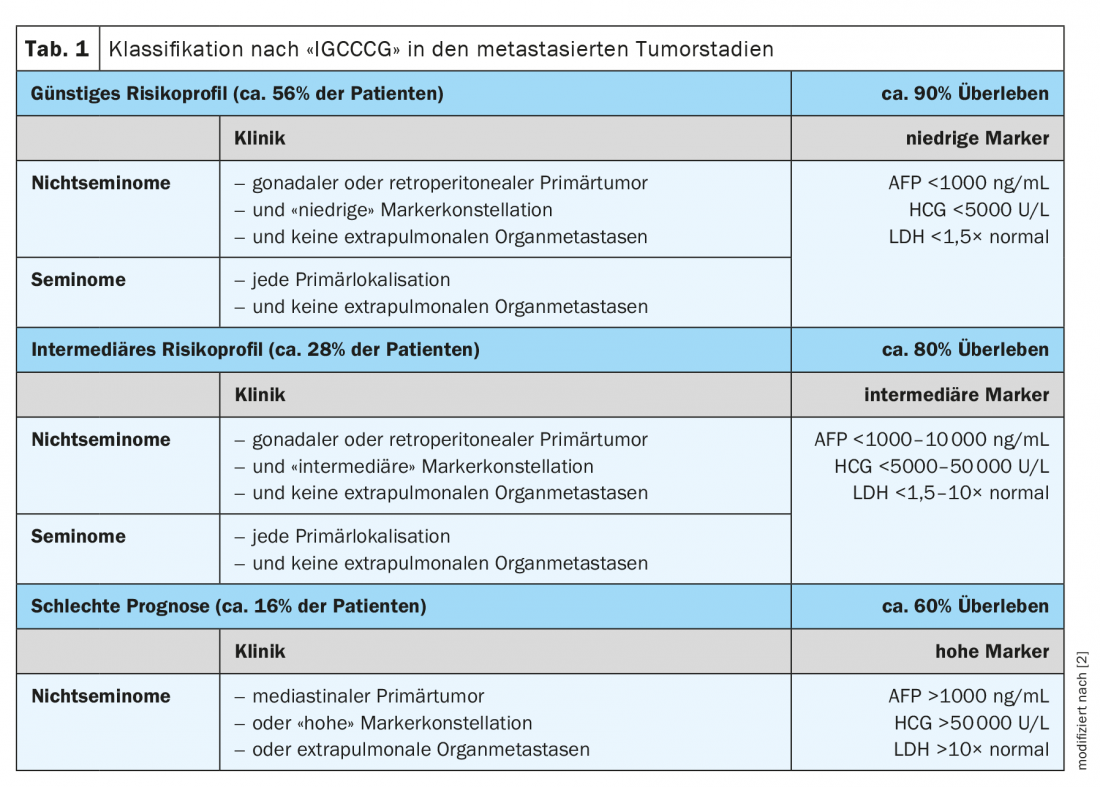
A partir da fase II, fala-se de uma doença metastasisada. Todos os pacientes com uma fase tumoral >IIB e III requerem quimioterapia primária e são também atribuídos a um grupo de risco específico de acordo com a chamada classificação de risco IGCCCG (International Germ Cell Cancer Collaborative Group) (Tabela 1) . Após terapia sistémica, os não-seminomas com um tumor residual de >1 cm, uma chamada ressecção de tumor residual (RTR) é obrigatória.
Cerca de 5-10% de todos os pacientes e 30% dos pacientes que já metástasearam sofrem uma recidiva no decurso do tratamento. Neste contexto clínico, como na situação primária, é importante uma abordagem adaptada ao risco com base em factores prognósticos.
A negligência dos padrões terapêuticos pode levar a uma maior taxa de fracasso terapêutico com a necessidade de terapias de seguimento ou mesmo à morte, tanto na terapia primária como na de recidiva. Por conseguinte, os doentes, especialmente na situação metastática e recaída ou na presença de cenários de doenças raras (envolvimento do SNC, recaídas tardias, etc.), devem ser apresentados a clínicas com elevada perícia para aconselhamento.
Terapia de primeira linha na fase II
Na fase rara do seminoma IIA, a radioterapia ( radioterapia de campo envolvida) permanece a primeira opção de tratamento fora dos ensaios clínicos. Todas as fases de seminoma a partir da fase IIB são tratadas principalmente com três ciclos de quimioterapia combinada com os fármacos cisplatina, etoposida e -leomicina (PEB) a cada 21 dias ou, em alternativa, com quatro ciclos de cisplatina/etoposida (PE) (Tab. 2) . A radioterapia também pode ser discutida [1,2].

Actualmente, os pacientes na Suíça também podem ser inscritos num ensaio clínico de fase III (SAKK 01/18). Os pacientes recebem quimioterapia combinada (1 ciclo de carbo-platina AUC 7 seguido de radioterapia de nó envolvido com 24 Gy em II A ou 1 ciclo de PE e subsequente radioterapia de nó envolvido com 30 Gy em II B). Outros ensaios da fase II na Alemanha ou
nos EUA estão actualmente a investigar a cirurgia sozinhos sem terapia adjuvante (PRIMETEST, NCT 02797626).
Os doentes com constelação de marcadores tumorais normais e gânglios linfáticos retroperitoneais imagino-morfológicos suspeitos (a maioria com 1-2 cm de diâmetro) representam uma subpopulação especial. Nestes pacientes, recomenda-se um acompanhamento por imagem a curto prazo 6-8 semanas mais tarde, com acompanhamento próximo de marcadores concorrentes. A RPLND pode ser procurada em doentes com não-seminomas cujos gânglios linfáticos (LK) se mantêm inalterados, permanecendo os marcadores tumorais normais para excluir o teratoma. Em alternativa, é efectuado um maior controlo. Todos os pacientes com marcadores tumorais que aumentam durante o curso da doença e/ou gânglios linfáticos de crescimento rápido em imagens requerem o início imediato da quimioterapia de acordo com a estratificação do risco para tumores avançados [3].
O tratamento de todos os seminomas metastáticos da fase IIC consiste na quimioterapia de acordo com o regime PEB (cisplatina, etoposida, bleomicina) [1,2]. A duração e intensidade são baseadas na classificação de risco IGCCCG. Se o grupo de prognóstico for bom, os pacientes são tratados com um total de três ciclos de PEB a intervalos de 21 dias. O grupo intermediário ou de mau prognóstico é tratado com quatro ciclos no mesmo intervalo. Se houver uma contra-indicação à bleomicina, quatro ciclos de PE (cisplatina, etoposida) equivalem a três ciclos de PEB num grupo de bom prognóstico. No grupo de prognóstico intermédio e pobre, são aplicados quatro ciclos de PEI (cisplatina, etoposida, ifosfamida) em vez de quatro ciclos de PEB.
Os não-seminomas da fase II com marcadores tumorais elevados são tratados de acordo com a sua classificação IGCCCG, de acordo com o algoritmo terapêutico para fases tumorais avançadas [2].
Terapia de primeira linha na fase III
A terapia padrão é de acordo com a estratificação de risco de acordo com a classificação de risco IGCCCG, independente da histologia. Consiste em quimioterapia com três (para grupo de bom prognóstico) ou quatro ciclos (para grupo de prognóstico intermédio ou mau) de PEB a intervalos de 21 dias (alternativamente 4 ciclos de PE para bom prognóstico ou 3 – 4 ciclos de PEI para prognóstico intermédio/pobre) [2].
Nos últimos anos, têm sido investigadas estratégias de quimioterapia intensificadas especialmente para os grupos intermediários e de mau prognóstico. Pela primeira vez, um estudo prospectivo randomizado (GETUG13) por um grupo de investigação francês foi capaz de mostrar uma vantagem na sobrevivência sem progressão em pacientes com um declínio inadequado dos marcadores no primeiro ciclo através da intensificação subsequente da terapia [4].
Dados americanos para o regime TIP com paclitaxel, ifosfamida e cisplatina, que até agora só tem sido utilizado em terapia de salvamento, também mostraram resultados muito bons a longo prazo nesta população de doentes num estudo de fase II, mas sem vantagem significativa em comparação com a terapia padrão [5]. A adição de paclitaxel à PEB no grupo de doentes de risco intermédio num ensaio EORTC mostrou uma melhoria significativa de 12% na sobrevivência sem progressão, mas sem um prolongamento significativo da sobrevivência global com aumento da toxicidade [6].
Também tem sido feita muita investigação sobre o valor da quimioterapia primária de alta dose (HDCT) com suporte de células estaminais autólogas na terapia primária, especialmente no grupo de pacientes com características de mau prognóstico de acordo com IGCCCG. Num estudo multicêntrico da fase II do Grupo Alemão de Estudo do Tumor Testicular, foi investigada a HDCT sequencial com cisplatina, etoposida e ifosfamida (HD-PEI), tendo sido demonstrada uma taxa de sobrevivência a longo prazo de 75%. Um ensaio aleatório de fase III dos EUA comparando a administração de quatro ciclos de PEB contra dois ciclos de PEB seguidos de dois ciclos de quimioterapia de alta dose com carboplatina, etoposida e ciclofosfamida (CEC) não pôde mostrar uma vantagem geral a favor da HDCT. Apenas os pacientes cujos marcadores tumorais não tinham diminuído adequadamente ao longo do tempo beneficiaram mais do tratamento no braço de alta dose. O ensaio EORTC fase III publicado comparando quatro ciclos de PEB com administração sequencial de alta dose de PEI também não mostrou nenhum benefício estatisticamente significativo em favor do HDCT [7,8]. A utilização de HDCT na terapia primária para pacientes com factores de prognóstico desfavoráveis ainda não é, por isso, padrão no presente.
O HDCT primário pode, no entanto, ser útil em casos individuais, especialmente em pacientes com declínio inadequado dos marcadores após o primeiro ciclo terapêutico dosado convencionalmente, em pacientes com não-seminoma essencialmente mediastinal, e em pacientes com metástases do SNC ou metástases hepáticas ou ósseas extensas. Este procedimento só deve ser decidido em consulta com centros experientes e, se possível, os dados devem ser registados num registo.
Ressecção de tumor residual (RTR) após terapia de primeira linha
Em doentes com seminoma e resíduos de tumores pós-quimioterapia, o RTR não é obrigatório. No caso de resíduos >3 cm, um PET-CT pode ser discutido no mínimo oito semanas após a conclusão da quimioterapia. Apenas nesta constelação o PET é uma indicação que vale a pena considerar. Em pacientes com PET positivo, o exame deve ser primeiro repetido no intervalo por meio de controlos do progresso da TC ou, se necessário, uma biopsia deve ser avaliada a fim de excluir de forma fiável possíveis resultados falsos positivos com uma constelação de marcadores simultaneamente normal [9].
Em todos os pacientes não-seminoma com resíduos tumorais >1 cm, deve ser realizado um RTR antecipadamente, cerca de quatro a um máximo de oito semanas após a conclusão da quimioterapia, com o objectivo de remoção completa de todos os resíduos tumorais. Esta intervenção muitas vezes complexa só deve ter lugar num centro interdisciplinar com os conhecimentos adequados. Se forem detectadas células tumorais vitais na ressecção, o procedimento seguinte não está claramente definido. No caso de uma percentagem de células tumorais vitais no tecido ressecado de >10%, tanto a terapia renovada com dois ciclos de quimioterapia como os cuidados de seguimento podem ser discutidos apenas [10].
Terapia de salvados
O tratamento de pacientes com seminoma ou não-seminoma e recidiva de uma fase I é análogo aos algoritmos de tratamento para pacientes com doença metastática primária [1].
Os pacientes que desenvolvem uma recaída após quimioterapia primária com pelo menos três ciclos de terapia com cisplatina recebem um tratamento quimioterápico intensivo renovado. Isto é complementado por um RTR subsequente em pacientes não-seminoma. As opções de tratamento são, em princípio, a terapia de salvamento convencional à base de cisplatina (CDCT) ou quimioterapia sequencial de alta dose com transplante de células estaminais autólogas (HDCT). Em certos cenários, só a cirurgia de salvamento é também indicada (por exemplo, Growing Teratoma) [11].
O tratamento considerado para o paciente individual depende principalmente do momento da ocorrência da recaída da doença, bem como de certos factores de risco. Em função dos factores de risco, é feita uma distinção entre cinco categorias de prognóstico. O PFS estimado de 2 anos de acordo com Kaplan-Meier é de 75% para pacientes no grupo de risco muito baixo, 51% no grupo de risco baixo, 40% no grupo de risco médio, 26% no grupo de risco alto e 6% no grupo de risco muito alto [12].
Terapia convencional com cisplatina contendo salvamento
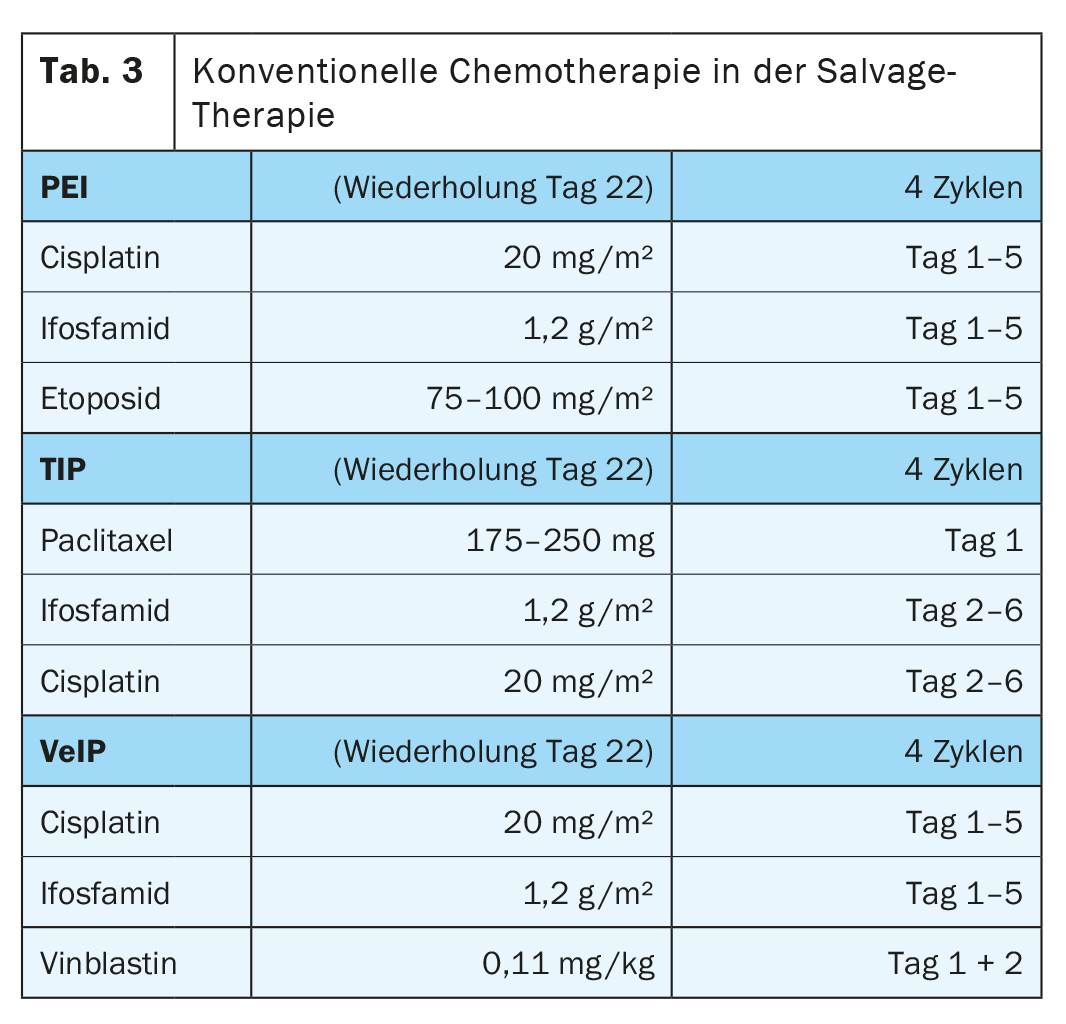
Os regimes combinam cisplatina (que não pode ser substituída por carboplatina) e ifosfamida com etoposida (PEI), com vinblastina (VeIP) ou com paclitaxel (TIP) sem superioridade clara de uma determinada combinação terapêutica (Tab. 3) . O padrão da quimioterapia combinada é a administração de quatro ciclos em intervalos de 21 dias [3].
Quimioterapia sequencial de alta dose com transfusão de células estaminais autólogas (HDCT)
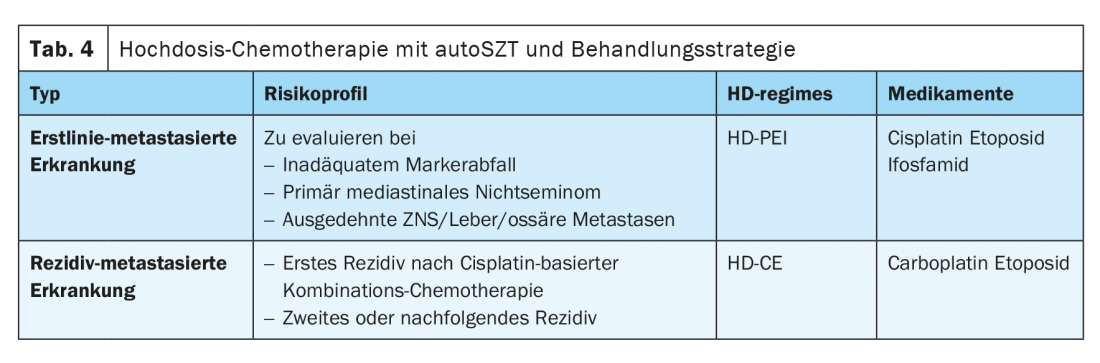
A combinação de carboplatina e etoposida (CE) forma o quadro básico do HDCT. Actualmente, isto é realizado em quase todos os centros em todo o mundo sob a forma de uma terapia sequencial com dois a três ciclos de alta dose de EC. (Tab. 4). Uma melhor terapia de suporte e a utilização de células estaminais autólogas do sangue periférico (PBSC) reduziram significativamente os tempos de reconstituição hematopoiética e assim reduziram a mortalidade inicialmente elevada relacionada com o tratamento de mais de 10% para menos de 3%.
O significado do HDCT como a primeira terapia de salvamento ainda é controverso e o tema das discussões actuais. A análise subgrupo de um estudo retrospectivo de quase 1600 registos de pacientes com terapia de recuperação primária foi capaz de mostrar uma vantagem a favor da HDCT em comparação com a CDCT no primeiro tratamento de recidiva. Estes resultados são contrários aos dados de um ensaio aleatório prospectivo que não demonstrou um benefício claro para o HDCT na primeira recidiva [13,14].
Um ensaio global fase III aleatorizado comparando o regime convencional com a TIP e quimioterapia sequencial de alta dose (CE) (ensaio TIGER) está actualmente a validar prospectivamente o benefício da HDCT na primeira recidiva. Os pacientes também podem ser incluídos na Suíça.
Na segunda ou subsequente recaída, a HDCT pode ainda alcançar uma remissão a longo prazo numa pequena proporção de doentes. Contudo, também aqui, a pequena dimensão e heterogeneidade dos colectivos de doentes estudados dificulta a interpretação dos resultados disponíveis do estudo [15].
Ressecção de tumores residuais após terapia de salvamento
A proporção de pacientes com histologia vital e indiferenciada é globalmente mais elevada após quimioterapia de recidiva. Após a conclusão da terapia sistémica, todos os pacientes com não-seminomas e resíduos detectáveis devem, portanto, ser avaliados para RTR. Em pacientes individuais sem normalização de marcadores ou múltiplas recidivas quimioterápicas-refractárias, a ressecção no sentido da chamada “cirurgia do desespero” ainda pode levar à remissão em casos excepcionais, especialmente na presença de manifestações tumorais singulares e facilmente ressecáveis e elevação de AFP única [3,16].
Recidivas tardias
As recidivas que ocorrem pelo menos dois anos após a última quimioterapia com cisplatina são chamadas recidivas tardias. Na doença ressecável, a remoção cirúrgica primária é o tratamento de escolha. No caso de achados não ressecáveis e/ou marcadores tumorais muito elevados (especialmente HCG), a terapia sistémica deve ser dada em primeiro lugar (quer sob a forma de CDCT ou HDCT) e a ressecção deve ser realizada após a conclusão da quimioterapia. Mais frequentemente, em recidivas tardias, as histologias desfavoráveis com transformação em sarcomas ou adenocarcinomas, entre outros, encontram-se no resectate [16].
Infestação do SNC
As metástases do SNC raramente ocorrem. Estes podem ocorrer de forma síncrona no diagnóstico primário ou na recorrência. A recidiva cerebral isolada é encontrada em apenas cerca de 2% dos pacientes. Para além de identificar factores prognósticos, um estudo retrospectivo comparou as modalidades de tratamento individual de quimioterapia, radioterapia e ressecção e investigou a sobrevivência do paciente tanto no diagnóstico primário como na recidiva. Por exemplo, foi demonstrado que após o diagnóstico, a radioterapia e/ou a ressecção não têm necessariamente de ser realizadas para além da quimioterapia. Em contraste, na situação de recaída, a utilização máxima de todas as formas de terapia, incluindo a HDCT, parece melhorar significativamente a sobrevivência do paciente [17].
Recorrência após HDCT e autoSCT
Os pacientes com recidivas múltiplas ou pacientes com recidivas após quimioterapia de alta dose raramente são mais curados. Contudo, através do uso bem coordenado de quimioterapia paliativa, ressecção de tumores paliativos se necessário, ou mesmo radiação paliativa, é muitas vezes possível alcançar um alívio dos sintomas e, assim, uma melhor qualidade de vida.
Além do paclitaxel, as substâncias oxaliplatina e gemcitabina também demonstram eficácia e são utilizadas como substâncias isoladas ou em várias combinações. O regime GOP, que combina oxaliplatina com gemcitabina e paclitaxel, é particularmente bem sucedido e pode provocar remissões a longo prazo em pacientes individuais, mesmo em recidivas após HDCT anteriores. A eficácia paliativa também foi demonstrada para a utilização de etoposídeos orais. Infelizmente, até agora não existe alternativa eficaz à quimioterapia; em particular, a tirosina quinase e os inibidores de pontos de controlo não demonstraram qualquer eficácia nos ensaios clínicos [2,3,18].
Mensagens Take-Home
- O tumor de células germinativas é o tumor mais comum nos homens jovens.
- Na fase metastática, a classificação é feita em três grupos de prognóstico: bom, intermédio e pobre, dependendo do nível do marcador e do envolvimento visceral.
- A quimioterapia com PEB é a terapia padrão para tumores em fase avançada, em alternativa pode ser usada PE ou PEI.
- O número de ciclos na terapia primária depende do grupo de prognóstico.
- Para nãoeminomas, a ressecção do tumor residual é obrigatória para os resíduos >1 cm.
- Na situação de salvamento, é realizada quimioterapia convencional ou de alta dose com suporte de células estaminais autólogas.
- Os pacientes com SNC e recaídas tardias representam uma forma especial.
Literatura:
- Honecker F, et al: Conferência de Consenso da ESMO sobre cancro de células germinais testiculares: diagnóstico, tratamento e seguimento. Ann Oncol. 2018; 29(8): 1658-1686.
- International Germ Cell Consensus Classification: um sistema de estadiamento baseado em factores prognósticos para cancros de células germinativas metastásicas. Grupo Colaborativo Internacional sobre o Câncer de Células Alemãs. J Clin Oncol. 1997; 15: 594-603.
- Directrizes Onkopedia Tumores de células germinativas do macho. www.onkopedia.com (último acesso: 20/0321)
- Fizazi K, et al: Quimioterapia personalizada baseada no declínio de marcadores tumorais em tumores de células germinais de mau prognóstico (GETUG 13): um ensaio fase 3, multicêntrico, aleatório. Lancet Oncol. 2014; 15: 1442-1450.
- Feldman DR, et al: Paclitaxel, Ifosfamide, and Cisplatin Efficacy for First-Line Treatment of Patients with Intermediate- or Poor-Risk Germ Cell Tumors. J Clin Oncol. 2016; 34(21): 2478-2483.
- de Wit R, et al: Estudo aleatório fase III comparando paclitaxel-bleomicina, etoposídeo e cisplatina (BEP) com BEP padrão no cancro de células germinais de prognóstico intermédio: estudo intergrupos EORTC 30983. J Clin Oncol. 2012; 30(8): 792-799.
- Motzer RJ, et al: Fase III de ensaio aleatório de quimioterapia de dose convencional com ou sem quimioterapia de alta dose e resgate autólogo de células estaminais hematopoiéticas como tratamento de primeira linha para pacientes com tumores de células germinais metastáticas de mau prognóstico. J Clin Oncol. 2007; 25: 247-256.
- Daugaard G, et al.: Um estudo aleatório da fase III comparando a dose padrão BEP com cisplatina, etoposídeo e ifosfamida (VIP) e suporte de células estaminais em homens com cancro de células germinais de mau prognóstico. Um estudo intergrupo da EORTC, GTCSG, e Grupo Germinal (EORTC 30974). Ann Oncol. 2011; 22: 1054-1061.
- Cathomas R, et al: Questioning the Value of Fluorodeoxyglucose Positron Emission Tomography for Residual Lesions After Chemotherapy for Metastatic Seminoma: Results of an International Global Germ Cell Cancer Group Registry. J Clin Oncol. 2018. DOI: 10.1200/JCO.18.00210.
- Heidenreich A: Ressecção de tumor residual após quimioterapia indutiva em cancro testicular avançado. Eur Urol. 2007; 51: 299-301.
- Lorch A, et al.: Quimioterapia sequencial versus dose única de alta dose em doentes com tumores de células germinativas recaídas ou refractárias: resultados a longo prazo de um ensaio aleatório prospectivo. J Clin Oncol. 2012; 30: 800-805.
- Lorch A, et al: Factores Prognósticos em Pacientes com Tumores de Células Germatóticas Metástases que Sofriram Falha no Tratamento com Quimioterapia de Primeira Linha Baseada em Cisplatina. J Clin Oncol. 2010; 28: 4906-4911.
- Lorch A, et al.: Dose convencional versus quimioterapia de alta dose como primeiro tratamento de salvamento em pacientes do sexo masculino com tumores de células germinativas metastáticas: evidência de uma grande base de dados internacional. J Clin Oncol. 2011; 29: 2178-2184.
- Pico JL, et al: Um ensaio aleatório de quimioterapia de alta dose no tratamento de recuperação de pacientes que falham na quimioterapia de primeira linha de platina para tumores avançados de células germinativas. Ann Oncol. 2005; 16: 1152-1159.
- Adra N, et al: Quimioterapia de alta dose e transplante de células estaminais periféricas autólogas para tumores de células germinativas metástases: The Indiana University Experience. J Clin Oncol. 2017; 35(10): 1096-1102.
- Albers P, et al: Guidelines on Testicular Cancer: 2015 Update. Eur Urol. 2015; 68(6): 1054-1068.
- Feldman DR, et al: Metástases cerebrais em doentes com tumores de células germinativas: Factores prognósticos e opções de tratamento – Análise do grupo global de cancro de células germinativas. J Clin Oncol. 2016; 34: 345-351.
- Bokemeyer C, et al.: Combinação de quimioterapia com gemcitabina, oxaliplatina, e paclitaxel em pacientes com tumores cisplato-refractários ou multiplicados de células germinativas recaídas: um estudo do Grupo Alemão de Estudo do Cancro Testicular. Ann Oncol. 2008; 19: 448-453.
InFo ONCOLOGy & HEMATOLOGy 2022; 10(5): 6-10