A segurança dos medicamentos tem a ver com a investigação antes e depois da aprovação de um medicamento, com o conhecimento de médicos e grupos especiais de pacientes, mas também com a integração da tecnologia na vida quotidiana dos hospitais. Os erros terapêuticos e as interacções perigosas podem assim ser evitados.
Antes de mais nada, falemos de medicamentos. As “fases de vida” do desenvolvimento clínico de um fármaco são suficientemente bem conhecidas. Desde a pré-comercialização, que inclui ensaios das fases I a III, até à submissão à autoridade reguladora de medicamentos relevante (por exemplo, a FDA nos EUA) e aprovação – se o medicamento sobreviver à revisão. Embora nos últimos anos populações de estudos especiais, isto é, pessoas de idade avançada, com doenças renais/fígadas, de diferentes ascendência, etc., tenham cada vez mais encontrado o seu caminho para a fase de pré-comercialização, isto não cobre, naturalmente, todos os grupos e situações de tratamento a longo prazo. Por exemplo, as mulheres grávidas e as crianças são frequentemente excluídas por razões éticas.
A fim de poder avaliar melhor a segurança de um medicamento, a aprovação é seguida de pós-comercialização (fase IV), que envolve a monitorização a longo prazo dos acontecimentos adversos, monitorização sistemática e estudos farmacoepidemiológicos de segurança. Desde o final dos anos 90, esta “fase de vida” dos medicamentos tem sido cada vez mais sistematizada e mais activamente integrada no conceito global de marketing. Hoje em dia, já é normalmente considerado ou integrado de forma proactiva no desenvolvimento de novas substâncias (ou seja, estudos sistemáticos, populacionais e epidemiológicos de segurança são normalmente negociados ao mesmo tempo que é apresentada uma autorização de introdução no mercado).
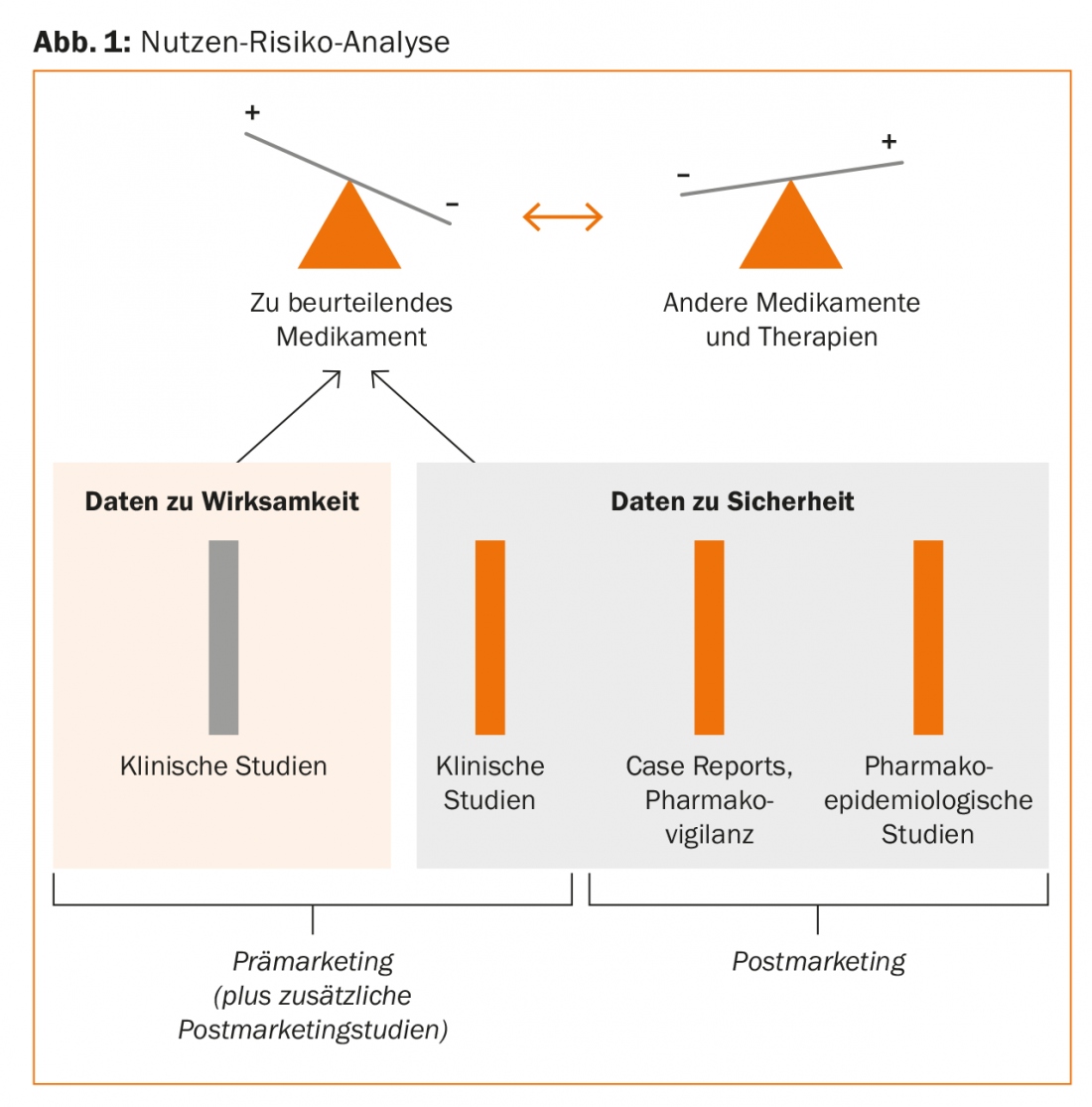
Uma análise racional de risco-benefício de medicamentos com a mesma indicação assenta assim nos seguintes pilares:
- Estudos clínicos (Fase I, II, III)
- Relatórios de casos/farmacovigilância (relatórios espontâneos)
- Estudos farmacoepidemiológicos (Fig. 1).
A área da farmacovigilância ou relatórios de casos pode ser muito bem avaliada qualitativamente e tem um efeito de sinalização (geração de hipóteses), mas é pouco adequada para a quantificação dos riscos relativos. O maior conjunto de provas provém de estudos farmacoepidemiológicos sistemáticos. “Esta área é agora altamente especializada e os estudos são muito extensos e exigentes. Mas o que também podemos fazer muito bem na vida quotidiana com as novas possibilidades técnicas são avaliações utilizando sistemas de informação clínica. Publicámos estudos correspondentes sobre as interacções medicamentosas em 2011 [1]. Os nossos dados sobre neurolépticos de segunda geração de 2016 [2] também mostram que isto também é possível localmente, no vosso próprio hospital, e que faz sentido melhorar a segurança das receitas médicas”, explicou o orador.
Fases da vida dos médicos
No que respeita a erros terapêuticos, Ashcroft et al. há dois anos atrás, ilustram bem que os médicos jovens e inexperientes cometem o dobro de erros no primeiro e segundo anos do que os médicos mais velhos, mas que estes últimos de modo algum “escapam” sem erros de medicação e que os erros – se é que cometem algum – são tão graves. Isto significa que as intervenções são indicadas não só para os médicos em formação mas também para os médicos seniores, para evitar erros de medicação potencialmente graves [3]. A vontade de continuar a aprender e a aprender ao longo da vida (também mais velho de mais novo), bem como a integração de tecnologia moderna (por exemplo, iPad em rondas) na tomada de decisões são pré-requisitos para tal.
“Será que aderimos realmente ao princípio Hipocrático ‘Primum non nocere’ (ou em alemão: Primeiro não fazer mal)? Eis um exemplo: para uma doença de outro modo fatal, prescreve-se o medicamento 1, que cura 75% dos pacientes mas acarreta o risco de um efeito secundário fatal agudo de 1:10.000 casos, ou o medicamento 2 com uma taxa de cura de 80% e um risco correspondente de 1:100?”, perguntou o Prof. Russmann à audiência. “Bastantes poucos escolheriam a droga 1. No entanto, isto causa 421 mais mortes do que a droga 2. O cálculo correspondente é muito simples:
Medicamento 1: Um paciente em 10.000 morre, dos restantes 9999, 7499 são curados. Assim, 7499 de um total de 10.000 sobrevivem.
Medicamento 2: 100 pacientes em 10.000 morrem, dos restantes 9900, 7920 são curados. 7920 de um total de 10.000 sobrevivem.
A “tomada de decisão defensiva”, ou seja, uma atitude auto-protectora por parte do médico, combinada com uma falsa avaliação intuitiva das probabilidades, pode assim terminar perigosamente para o doente. Para ficar com o exemplo acima: O facto de o paciente ter morrido da doença em vez da medicação prescrita pela sua própria mão é um pouco mais fácil de suportar pelo médico.
Um resumo de como melhorar a segurança dos medicamentos por parte dos médicos é apresentado na visão geral 1.
Fases da vida da prova
Os seguintes princípios são aqui relevantes:
- Usar medicamentos com um perfil de segurança bem documentado
- Mantendo-se “actualizado”, educação contínua
- Permanecer crítico de novas provas, examinar cuidadosamente
- Preocupações: “Sempre que uma nova droga chega ao mercado, algo de louco acontecerá”.
Fases da vida dos hospitais
Com análises sistemáticas e sistemas de informação clínica, combinações de medicamentos perigosos ou mesmo contra-indicados podem ser detectadas e indicadas a tempo. As verificações de interacção são possíveis, por exemplo, através de www.mediq.ch. Russmann, como farmacologista clínico e epidemiologista, está ele próprio intensamente envolvido com este tópico e tem co-desenvolvido e implementado o chamado programa “farmacoepidemiologia interventiva”. No processo, um grande número de prescrições são registadas através de um sistema electrónico de informação clínica e é criada uma base de dados hospitalar farmacoepidemiológica local. Através do programa “farmacoepidemiologia interventiva”, os erros de medicação nos hospitais podem ser identificados, quantificados e a sua relevância clínica avaliada num período de tempo muito curto. Desta forma, os alertas automáticos direccionados podem ser integrados na prescrição electrónica de medicamentos (em “tempo real”). Além disso, são obtidos dos dados estudos de coorte/case-controlo e estudos longitudinais com declarações sobre padrões de prescrição, efeitos secundários e aspectos económicos. Duas publicações dos últimos anos mostram que este trabalho funciona [4,5].
A gestão proactiva da qualidade, bem como os investimentos em TI e nos sistemas acima mencionados que reconhecem potenciais problemas em farmacoterapia, avaliam a relevância clínica e alertam atempadamente para situações críticas são, assim, centrais. Para além da estabilidade da mão-de-obra e da baixa rotatividade do pessoal, ajudam um hospital a melhorar a segurança dos medicamentos de forma sustentável e a longo prazo.
Fases da vida dos pacientes
Finalmente, algumas palavras sobre os doentes na fase final das suas vidas”. Nos idosos, devido à multimorbilidade e portanto à polifarmácia, o exame das interacções entre drogas (“Drug-drug-interaction”) é central. No entanto, as interacções entre drogas e doenças (“Drug-disease interaction”) não devem ser esquecidas. Um inventário da função renal e possíveis ajustes de dose, visitas clínicas regulares e monitorização de vários parâmetros tais como pressão arterial, ECG, etc., também fazem parte de uma prática clínica que visa melhorar a segurança dos medicamentos. “Para a população pediátrica, ou seja, os pacientes no início da sua vida, o website/base de dados de conhecimento kinderdosierungen.ch fornece informações valiosas”, disse ele.
Fonte: 15ª Reunião Anual da SGAMSP, 28 de Setembro de 2017, Wil
Literatura:
- Haueis P, et al.: Avaliação das interacções medicamentosas numa grande amostra de pacientes internados psiquiátricos: uma interface de dados para análise em massa com software de apoio à decisão clínica. Clin Pharmacol Ther 2011 Oct; 90(4): 588-596.
- Low DF, et al: Antipsicóticos de segunda geração num hospital de cuidados terciários: padrões de prescrição, perfis metabólicos, e interacções medicamentosas. Int Clin Psychopharmacol 2016 Jan; 31(1): 42-50.
- Ashcroft DM, et al: Prevalência, Natureza, Severidade e Factores de Risco para Prescrição de Erros em Hospitais Internados: Estudo Prospectivo em 20 Hospitais do Reino Unido. Drug Saf 2015 Set; 38(9): 833-843.
- Niedrig D, et al.: Desenvolvimento, implementação e análise de resultados de alertas semi-automatizados para ajuste da dose de metformina em doentes hospitalizados com insuficiência renal. Pharmacoepidemiol Drug Saf 2016 Oct; 25(10): 1204-1209.
- Niedrig D, et al: overdosing de Paracetamol num hospital de cuidados terciários: implementação e análise dos resultados de um programa de alerta preventivo. Journal of Clinical Pharmacy and Therapeutics 2016; 41(5): 515-518.
Leitura adicional:
- Gigerenzer G: Risco: Como tomar as decisões certas. Munique: Random House GmbH 2013.
InFo NEUROLOGIA & PSYCHIATRY 2017; 15(6): 39-41