Sendo a doença de coagulação hereditária mais comum, a síndrome de Von Willebrand afecta cerca de uma em cada mil pessoas. Com novas possibilidades de diagnóstico e descobertas no campo da genética molecular, a questão do significado clínico da análise genética está cada vez mais a ser levantada. Este foi também um tema muito debatido na 63ª Reunião Anual da Sociedade Americana de Hematologia (ASH).
Testes genéticos na síndrome de von Willebrand (Doença de von Willebrand, vWD) é como o amor, todos falam dele, mas ninguém o entende exactamente – com estas palavras Emmanuel Favaloro, um famoso investigador australiano do Institutos de Patologia Clínica e Investigação Médica em Hospital Westmead em Sydney, a sua palestra sobre Reunião Anual da ASH 2021. E de facto, existe alguma incerteza sobre a melhor maneira de proceder. Embora a análise genética não faça sentido na maioria dos casos de síndrome de tipo 1 de von Willebrand, é recomendada para doentes de tipo 2 e 3 nas novas directrizes publicadas em 2021 [2].
Síndrome de von Willebrand: O básico
A síndrome de Von Willebrand foi descrita pela primeira vez em 1926 como “pseudohaemofilia” numa jovem mulher que sangrou até à morte durante um dos seus primeiros períodos. O descobridor – nomen est omen – é o Dr. Erik von Willebrand. A doença hereditária autossómica é definida por anomalias quantitativas ou qualitativas do factor von Willebrand (vWF), a prevalência sintomática é de cerca de 1/1000. Embora homens e mulheres sejam formalmente afectados igualmente, as mulheres são diagnosticadas duas a três vezes mais frequentemente devido às complicações ginecológicas. Na maioria dos casos, a síndrome de von Willebrand manifesta-se como aumento da hemorragia mucosa; em casos graves, também pode ocorrer hemorragia músculo-esquelética.
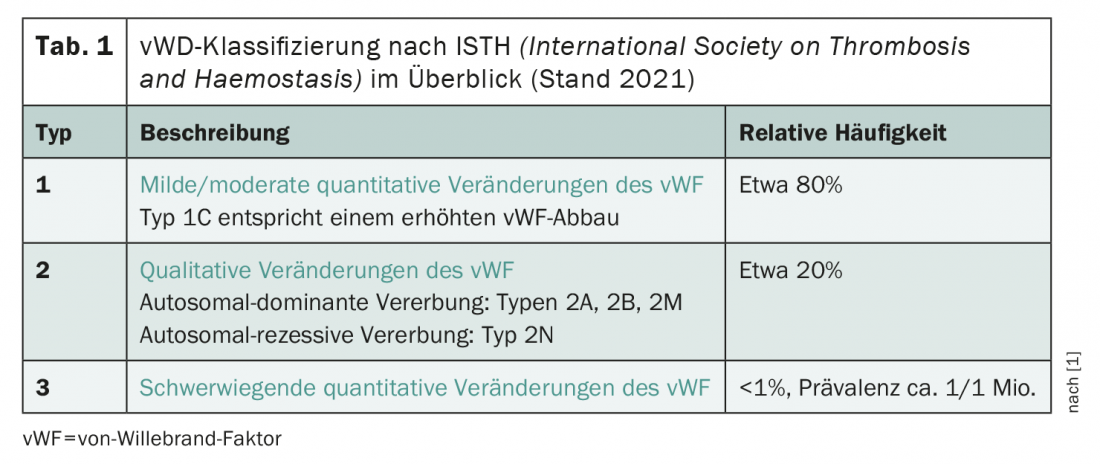
De acordo com a classificação recentemente revista da Sociedade Internacional de Trombose e Hemostasia (ISTH), o quadro clínico está dividido aproximadamente em três tipos (tab. 1) . Em princípio, é feita uma distinção entre qualitativa (tipo 2) e alterações quantitativas (tipos 1 e 3) do vWF. Em 2021, o subtipo 1C foi adicionado à classificação, que é definida pelo aumento da degradação do vWF. O tipo 1 Síndrome de von Willebrand – ou seja, alterações quantitativas leves a moderadas na vWF – é de longe a mais frequentemente diagnosticada, seguida pelo tipo 2. A ausência quase completa de vWF na síndrome de von Willebrand tipo 3 é extremamente rara e afecta cerca de uma em cada milhão de pessoas.
Além da terapia sintomática com medicamentos anti-fibrinolíticos como o Cyklokapron e a pílula em pacientes do sexo feminino, existem também opções de tratamento que visam directamente o vWF. Estes consistem em desmopressina (DDAVP), que promove a libertação de vWF a partir de células endoteliais, e vWF recombinante ou derivado do plasma sanguíneo. Em princípio, a terapia para todos os tipos de síndrome de von Willebrand é semelhante e depende da gravidade. Em casos mais graves, o vWF tem normalmente de ser substituído, uma vez que o efeito do DDAVP já diminui rapidamente após um curto período de tratamento.
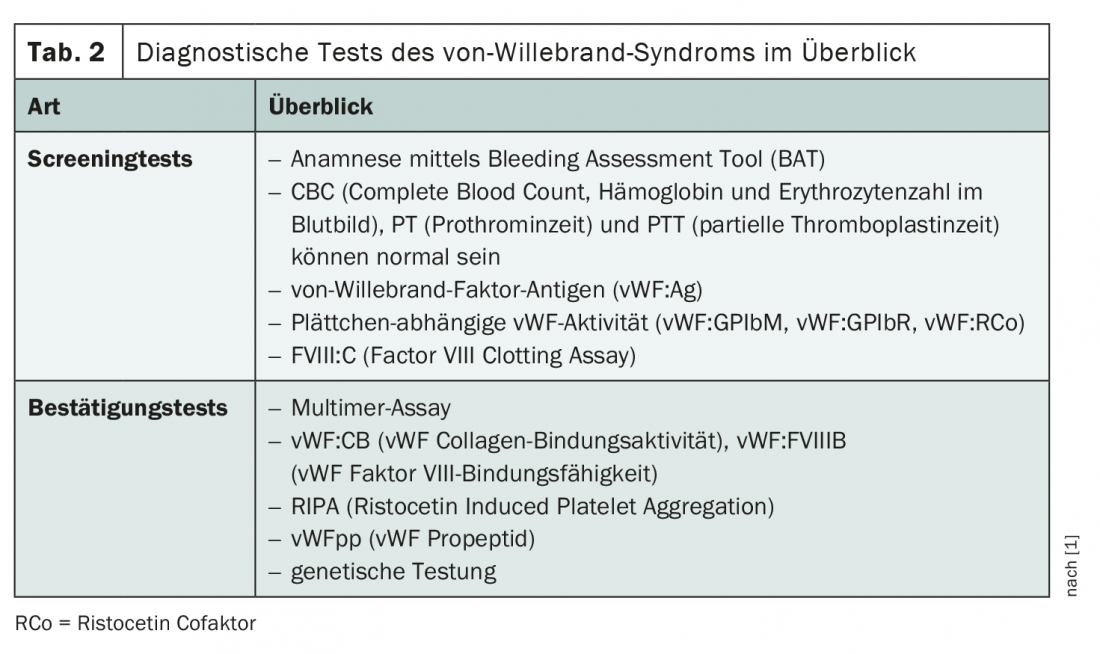
Vários testes de rastreio e de confirmação são utilizados para fazer o diagnóstico (tab. 2) . A história médica também desempenha um papel decisivo. Como o hemograma, o tempo de protrombina e o tempo parcial de tromboplastina podem ser normais, são necessários procedimentos de rastreio mais específicos. Um painel de três ferramentas de diagnóstico é normalmente realizado para detectar antigénios vWF, actividade vWF dependente de plaquetas e actividade de factor VIII. Se a suspeita de síndrome de von Willebrand for confirmada durante estas investigações, são utilizados outros testes para confirmar e identificar o subtipo vWD.
Testes genéticos controversos
No contexto de novos testes, a análise genética também desempenha um papel até agora controverso. Uma vez que a terapia não varia entre os subtipos e alternativa, estão disponíveis métodos mais favoráveis para classificar a doença, coloca-se a questão da utilidade da caracterização genética. A sua disponibilidade varia, mas está a aumentar. Quaisquer efeitos negativos sobre as pessoas em questão não devem ser negligenciados, porque os testes genéticos podem levar a problemas de seguro e estigmatização, por exemplo. O resultado final é que a análise genética do subtipo mais comum de vWD, tipo 1, não é geralmente útil, de acordo com os peritos na Reunião Anual ASH – entre outras coisas, porque uma variante genética correspondente só pode ser detectada em cerca de 65% dos casos e isto não tem impacto na gestão.
Mesmo que muito tenha sido feito no que diz respeito à caracterização genética da doença, o que foi conseguido pela primeira vez em 1984, a base de dados ainda está cheia de erros e lacunas. Por exemplo, existem algumas das chamadas “variantes de significado clínico incerto” e certas alterações genéticas ainda não puderam ser claramente atribuídas aos seus fenótipos correspondentes. No entanto, uma vantagem dos testes genéticos é a sua viabilidade centralizada e, portanto, boas possibilidades de normalização. O gene vWF está localizado no braço curto do cromossoma 12.
Quando é que a análise genética é útil?
Apesar de todas as reservas, existem algumas situações em que os testes genéticos na síndrome de von Willebrand já são hoje em dia altamente valorizados. Especialmente no caso dos subtipos vWD 2B, 2N e 3, pode fornecer informação adicional importante e clinicamente relevante – por um lado para diferenciação de outras perturbações de coagulação e por outro lado para aconselhamento genético e avaliação do risco terapêutico. As mutações podem ser detectadas em cerca de 90% dos casos do tipo 2 síndrome de von Willebrand, e em cerca de 85% dos casos do tipo 3. No que respeita ao procedimento de diagnóstico óptimo, incluindo análises genéticas, foram publicadas novas directrizes em 2021 [2].
Estes recomendam testes genéticos para os subtipos suspeitos de vWD 2A, 2B, bem como 2N [2]. A principal questão aqui é a demarcação a partir do chamado “Tipo placa síndrome de von Willebrand” (também conhecida como “pseudotipo”) e hemofilia A. Isto porque a síndrome de von Willebrand tipo 2B – tipicamente caracterizada por uma afinidade acrescida para as plaquetas, uma análise multimer conspícua e trombocitopenia – assemelha-se muito à Do tipo placa. No entanto, enquanto a mutação desencadeadora neste último está localizada no gene plaquetário, na síndrome de tipo 2B von Willebrand está localizada no gene vWF. Isto tem implicações importantes para a gestão: a síndrome “real” de von Willebrand é tratada por substituição de vWF, o pseudotipo por administração de plaquetas. O tipo de placa é herdado de uma forma autossómica dominante. A causa é uma mutação de ganho de funçãoda glicoproteína que liga o vWF. Isto leva a uma interacção excessiva e desnecessária entre plaquetas e vWF com consumo consecutivo de ambos os componentes – e a um quadro clínico que muitas vezes se assemelha ao mais comum tipo “verdadeiro” de síndrome de von Willebrand 2B está confuso. Estima-se que cerca de 15% do tipo 2B diagnostica na verdade uma síndrome de von Willebrand do tipo plaquetário [3].
Há também um importante diagnóstico diferencial para a síndrome de tipo 2N (“Normandia”) von Willebrand: a hemofilia A. Neste subtipo, os níveis do factor VIII são classicamente inferiores aos níveis vWF – uma constelação que na síndrome de von Willebrand ocorre apenas no tipo 2N ocorre e está associado à hemofilia A pode ser confundido. Assim, as novas directrizes recomendam que, nos casos de tipo suspeito 2N vWD os testes genéticos direccionados e/ou a determinação da capacidade de ligação do factor VIII vWF [2]. Só identificando correctamente a doença subjacente é que se pode garantir uma terapia adequada – quer através do factor VIII ou da substituição do vWF.
Ao contrário do tipo 2 da síndrome de von Willebrand, o diagnóstico do tipo 3 geralmente esclarecido antes dos testes genéticos. No entanto, pode fazer sentido nesta rara e autossómica forma recessiva da doença – embora a localização da mutação desencadeadora varie mais do que nos tipos geneticamente mais claramente caracterizados. 2A, B e N. Por um lado, a análise genética pode desempenhar um papel importante no aconselhamento genético das pessoas afectadas e dos seus familiares, por outro, fornece informações valiosas para a avaliação do risco de uma terapia que utiliza vWF exógena. Assim, grandes supressões predispõem a formação de aloanticorpos durante a terapia. Os doentes com mutações no propéptido vWF também parecem ter um maior risco de sangramento do que aqueles com mutações em outros locais.
O resultado final é que o benefício dos testes genéticos em tipo 1 Síndrome de von Willebrand – e portanto em mais de 70% de todas as pessoas afectadas – é actualmente questionável. Para além da correlação genótipo-fenótipo insuficientemente caracterizada, falta também a consequência terapêutica de tais análises. Para os tipos 2 e 3, por outro lado, a análise genética pode ser bastante útil e já é altamente valorizada no diagnóstico diferencial, avaliação de riscos e aconselhamento genético.
Congresso: 63ª Conferência Anual da ASH
Fonte/Literatura:
- Sessão em Destaque “Testes Genéticos para a Doença de von Willebrand”, Paula James e Emmanuel Favaloro, 13.12.2021, 63ª Reunião Anual da ASH, Atlanta, EUA.
- James PD, et al: ASH ISTH NHF WFH 2021 guidelines on the diagnosis of von Willebrand disease. Blood Adv. 2021; 5(1): 280-300.
- Othman M: doença de Platelet-type von Willebrand: uma doença rara, muitas vezes mal diagnosticada e subdiagnosticada, com hemorragia. Semin Thromb Hemost. 2011; 37(5): 464-469.
InFo ONCOLOGy & HEMATOLOGy 2022; 10(1): 38-40