Se a colonização do biofilme persistir em feridas crónicas apesar do melhor tratamento possível da doença subjacente, a cicatrização da ferida estagnará. O desbridamento mecânico é muito importante, mas não é suficiente como única medida e, em alguns casos, também não é prático. Para que as soluções de irrigação de feridas antimicrobianas e os pensos sejam eficazes contra o biofilme, é fundamental que consigam penetrar a substância polimérica extracelular. Por conseguinte, a eficácia das diferentes preparações varia.
As feridas que ainda estão abertas após 30 dias são consideradas crónicas, independentemente da sua causa, e são propensas a infecção devido a uma série de factores [1]. Assim, o ambiente quente e húmido da ferida é um terreno ideal para a reprodução de bactérias e fungos e o encerramento retardado da ferida aumenta o risco de exposição contínua a agentes patogénicos com o risco de formação de biofilme. Por ocasião do Congresso de Feridas deste ano em Nuremberga, a Prof. Dra. med. Ewa Klara Stürmer, Directora Médica do Centro Integral de Feridas e Chefe da Investigação Translacional de Feridas, Centro Médico Universitário Hamburg-Eppendorf, falou sobre a prática clínica e novas descobertas no tratamento do biofilme de feridas [2].

O biofilme é encontrado em mais de três quartos de todas as feridas crónicas
Um biofilme desenvolve-se quando a colonização bacteriana na ferida leva a colónias ou associações bacterianas nas quais as bactérias amadurecem e se espalham (caixa) [16]. Segundo uma meta-análise, cerca de 78% de todas as feridas crónicas são colonizadas com microrganismos patogénicos sob a forma de biofilmes [3]. O biofilme da ferida fornece uma resposta imunitária mais ou menos pronunciada ou inflamação local [4]. Se o biofilme não for quebrado e eliminado, a cicatrização da ferida estagna, resultando na persistência da cronicidade de uma ferida – apesar do melhor tratamento possível da doença subjacente [2,4,5]. As principais espécies bacterianas em biofilmes de feridas, utilizando o exemplo de úlceras de perna, são (Resumo 1) : Staphylococcus aureus, a sua variante resistente à meticilina (MRSA), Pseudomonas aeruginosa, Enterobacteriaceae e Proteus mirabilis [6].

Substância polimérica extracelular como ponto crítico de aderência
A comunidade simbiótica e interespécies de microrganismos a partir dos quais se formam os biofilmes produz uma substância polimérica extracelular (EPS) na qual eles próprios “murais” [2,4]. O EPS consiste essencialmente em polissacarídeos, bem como numa variedade de proteínas, lípidos, glicoproteínas e glicolípidos, o que o faz aderir firmemente ao leito da ferida [7]. Esta mistura de açúcar-proteína representa um “escudo protector” bacteriano contra antissépticos e antibióticos [2]. Após 2-4 dias, fala-se de “biofilme maduro”. Um biofilme da ferida ou uma forte colonização bacteriana da ferida pode ser tornado visível ao olho humano com luz UV (por exemplo MolecuLight®, MolecuLight Corp., Toronto, Canadá) [4].
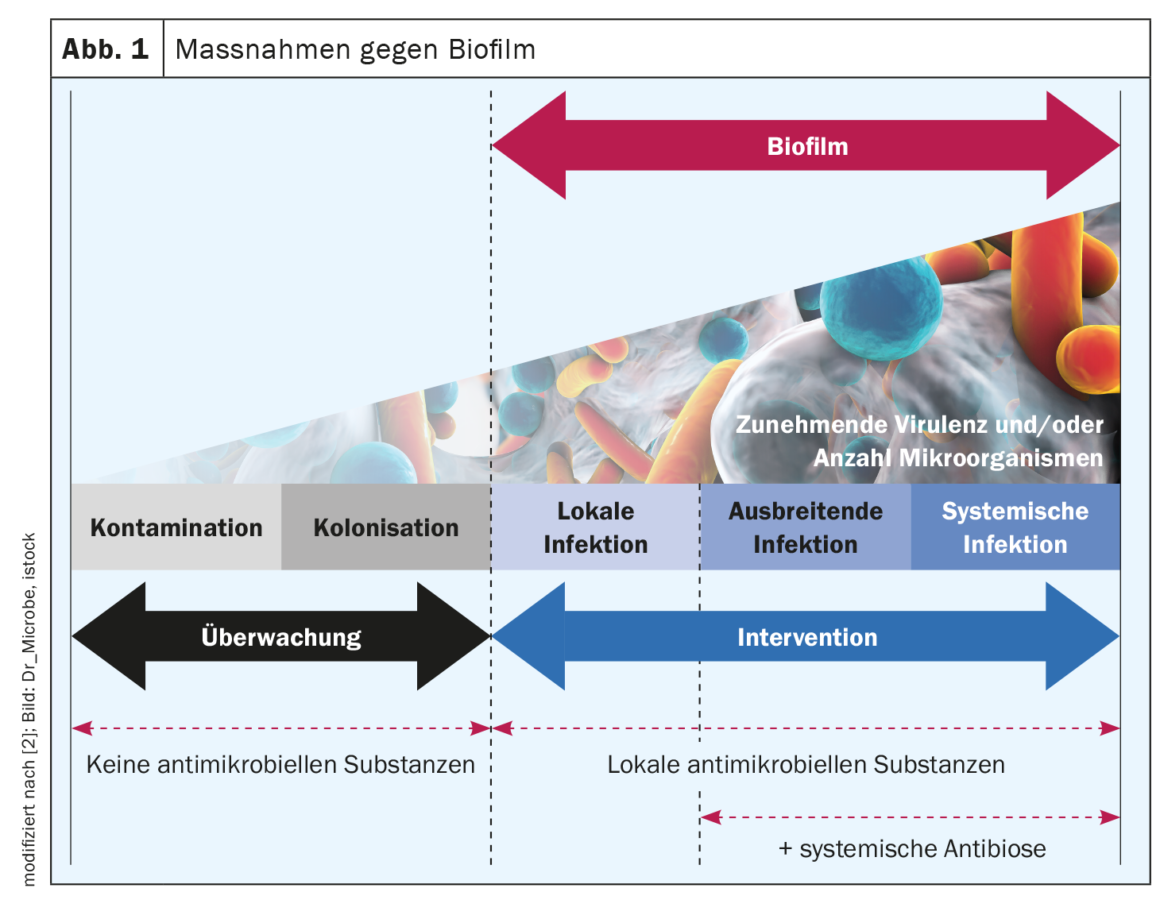
Eficiência das irrigações e curativos de feridas antimicrobianas
O desbridamento mecânico é actualmente o único tratamento para o biofilme de feridas recomendado por consenso de especialistas, mas, por um lado, o desbridamento por si só não remove todo o biofilme e, por outro lado, nem sempre é uma opção viável no contexto dos cuidados domiciliários (por exemplo, higiene limitada, pacientes em anticoagulação terapêutica com medicamentos) [4,8]. As soluções antimicrobianas de irrigação de feridas abordam e destroem as paredes bacterianas, membranas e proteínas de transporte bacteriano ou inibem a sua função [4]. Se não conseguirem quebrar o EPS – que funciona como uma barreira bioquímica contra o sistema imunitário do hospedeiro e especialmente contra agentes antimicrobianos – não podem funcionar eficazmente. Consequentemente, a eficácia das diferentes soluções de irrigação de feridas contra biofilmes bacterianos varia [4]. Os testes translacionais sistemáticos utilizando o modelo de biofilme humano hpBIOM mostra que Octenisept® é capaz de clivar os biofilmes e matar as bactérias dentro deles em 72 h [4,9,10,17]. PHMB tem um sucesso limitado no mesmo período, mas a erradicação completa não é alcançada mesmo após 72 horas. As soluções de irrigação de feridas hipoclorosas e a clorexidina não conseguem eliminar eficazmente as bactérias do biofilme [4,10].

No que diz respeito à importância dos pensos para feridas, é um pouco difícil derivar recomendações terapêuticas diferenciadas da pequena base de evidências de estudos clínicos comparativos com pensos para feridas (antimicrobianos), uma vez que não só as substâncias activas (iões de prata, prata nanocristalina, PHMB, derivados de iodo, etc.) e as suas concentrações variam, mas também a respectiva base dos pensos para feridas (espuma de PU, alginatos, fibras, etc.). [4,11]. Mas vários testes in vitro utilizando um modelo de biofilme humano mostraram que um produto combinado de iodo e amido (Cadexomer iodine) foi capaz de erradicar completamente as bactérias do biofilme no prazo de seis dias [2,4]. Outros pensos para feridas contendo PHMB ou prata apenas reduziram a carga bacteriana [12]. As análises correspondentes foram efectuadas após um período de seis dias sem mudança de penso e pode assumir-se que se pode conseguir uma maior eficácia para todos os pensos de ferida testados com mudanças diárias ou de dois em dois dias [4].
O mecanismo de acção do produto combinado de iodo e amido (Iodosorb™) baseia-se em microesferas de Cadexomer, que destroem a estrutura do biofilme ou a substância polimérica extracelular bacteriana por desidratação como pré-requisito para que o iodo elimine facilmente as bactérias assim expostas no biofilme [12,18].
Congresso: Wound Congress Nuremberga
Literatura:
- Hunt S, Elg F: A eficácia clínica do spray de hemoglobina como terapia adjuvante no tratamento de feridas crónicas. J Wound Care 2017; 26(9): 558-568.
- “Biofilm – Die Herausforderung des Jahrzehntes in der Wundversorgung – Wundbiofilm erkennen, verstehen und nachhaltig beseitigen”, Prof. Dr. med. Stürmer, Industriesymposium Smith & Nephew GmbH, Wundkongress Nürnberg, 1.12.2022.
- Malone M, et al: A prevalência de biofilmes em feridas crónicas: uma revisão sistemática e uma meta-análise dos dados publicados. J Wound Care 2017; 26(1): 20-25.
- Stürmer EK, Rembe J-D: Reconhecer e compreender o biofilme da ferida: As possibilidades terapêuticas e os seus limites. CME educação contínua, DERMATOLOGIE PRAXIS 2/2022, 6-11.
- James GA, et al: Biofilmes em feridas crónicas. Wound Repair Regen 2008; 16(1): 3-44.
- Jockenhofer F, et al.: Bacteriological pathogen spectrum of chronic leg ulcers: Resultados de um ensaio multicêntrico em centros de tratamento dermatológico de feridas diferenciados por regiões. J Dtsch Dermatol Ges 2013; 11(11): 1057-1063.
- Flemming HC, Wingender J: A matriz do biofilme. Nat Rev Microbiol 2010; 8(9): 623-633.
- Schwartz JA, et al: O desbridamento cirúrgico por si só não reduz adequadamente a bioburden planctónica nas feridas crónicas das extremidades inferiores. J Tratamento de feridas. 2014 Set; 23(9): S4, S6, S8 passim. doi: 10.12968/jowc.2014.23.Sup9.S4.
- Besser M, et al.: Eficácia dos anti-sépticos num novo modelo tridimensional de biofilme de plasma humano (hpBIOM). Rep. Sci 2020; 10(1): 4792.
- Rembe JD, et al: Antimicrobiano Hipoclorous Wound Irrigation Solutions Demonstram Baixa Eficácia Anti-biofilme Contra Biofilme Bacteriano num Modelo de Biofilme de Plasma Humano Complexo in-vitro (hpBIOM) do que os Antimicrobianos de Feridas Comuns. Microbiol frontal 2020; 11: 564513.
- Schwarzer S, et al: A eficácia dos agentes tópicos utilizados em feridas para gerir infecções crónicas de biofilme: Uma revisão sistemática. J Infect 2020; 80(3): 261-270.
- Stuermer EK, et al: Actividade in vitro de curativos antimicrobianos de feridas em biofilme de P. aeruginosa. Microbiol frontal 2021; 12: 664030.
- Stuermer EK, et al: Infiltração bacteriana em feridas colonizadas por biofilme: Análises no modelo de ferida ex vivo hpBIOM e possível impacto no esfregaço e desbridamento. Int Wound J 2022 (em revisão)
- 14. “Principles of wound care, wound cleansing/debridement techniques”, www.bk-trier.de/media-bkt/docs/Bildung/Handouts-Wundmanagement/Basisseminar-Handouts/03_Debridement.pdf,(último acesso 20.01.2023).
- Rembe JD, Stürmer EK: Modern wound antisepsis – indicações e limitações, entre conhecimento, desejo e incerteza. Cirurgia Vascular 2020; 25, 272-276.
- Percival SL, McCarty SM, Lipsky B: Biofilmes e Feridas: Uma Visão Geral das Evidências. In: Advances in wound care 2015; 4(7): 373-381.
- Compêndio Suíço de Drogas,
https://compendium.ch,(último acesso 20.01.2023) - Iodosorb™ Dressing, www.smith-nephew.com/switzerland/fachgebiete/wundmanagement/iodosorb-dressing,(último acesso 20.01.2023).
DERMATOLOGIE PRAXIS 2023; 33(1): 32-33 (publicado 16.2.23, antes da impressão).











