Apesar dos grandes avanços no tratamento da artrite reumatóide, muitos pacientes não respondem satisfatoriamente (ou adequadamente) aos tratamentos disponíveis [1]. Dados de ensaios clínicos de um medicamento anti-reumático modificador de doenças-alvo mostram que com opções terapêuticas adicionais eficazes, cada vez mais pacientes de AR podem também alcançar o objectivo de remissão a longo prazo [2, 3].
A artrite reumatóide (AR) é uma das doenças inflamatórias crónicas mais comuns – só na Suíça, cerca de 85.000 pessoas são afectadas [1, 4]. A AR caracteriza-se pela inflamação progressiva das articulações afectadas, que pode levar à perda de cartilagem, à erosão irreversível dos ossos e à incapacidade [1]. Além disso, as manifestações extra-articulares ocorrem em cerca de metade dos doentes, o que contribui para o aumento da mortalidade na AR [1,5].
Tratamento atempado e direccionado da AR [1].
Um tratamento atempado e orientado é essencial para contrariar as consequências consideráveis da doença e para permitir aos doentes alcançar a remissão ou, pelo menos, uma baixa actividade da doença [1]. Se o objectivo terapêutico não for alcançado através da utilização de um medicamento anti-reumático convencional modificador de doenças sintéticas (csDMARD), como o metotrexato (MTX), e se existirem factores de prognóstico deficiente, o tratamento deve ser alargado para incluir um medicamento do grupo dos DMARD biológicos ou alvo, de acordo com as Recomendações EULAR 2020 [6]. Estes últimos incluem também os inibidores de Janus kinase (JAK), que interferem especificamente com o transdutor de sinal pró-inflamatório JAK de activação (STAT) em cascata, suprimindo assim os processos inflamatórios típicos da AR [1].
Upadacitinib inibidor JAK como uma opção terapêutica eficaz a longo prazo [7].
O inibidor reversível e selectivo JAK upadacitinib (RINVOQ®) foi aprovado em Janeiro de 2020 para o tratamento de adultos com AR activa moderada a grave que tiveram uma resposta inadequada, ou não toleraram o tratamento com um ou mais csDMARD [7, 8]. Upadacitinib pode ser tomado como monoterapia ou em combinação com MTX, bem como outros csDMARD uma vez por dia sob a forma de comprimidos (15 mg), com ou sem alimentos [7]. Os custos de tratamento são cobertos pelas companhias de seguros de saúde [9]. O factor decisivo para a aprovação do upadacitinib foram os resultados do programa de estudo RA-SELECT com um total de mais de 4.380 pacientes adultos com AR activa em cinco estudos fulcrais [7]. O Upadacitinib demonstrou ser uma opção terapêutica eficaz tanto em combinação com MTX como como monoterapia [2, 3].
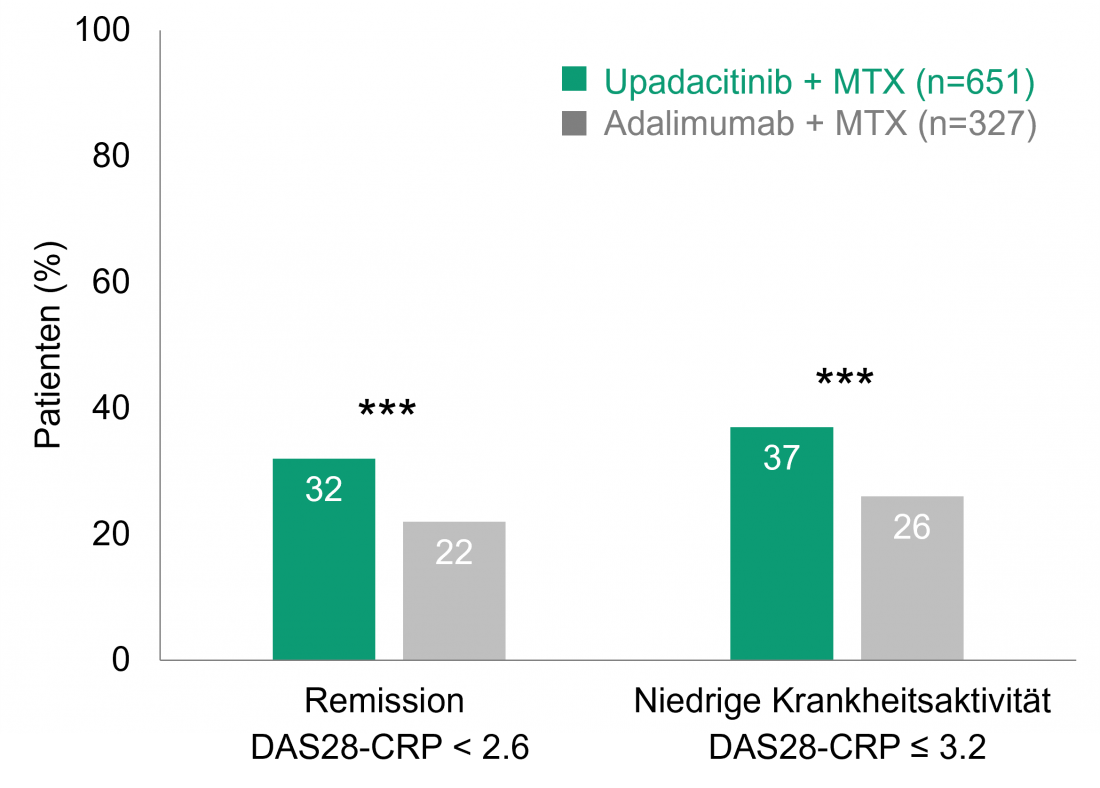
Upadacitinib + MTX versus adalimumab + MTX: taxas de remissão mais elevadas mesmo após 156 semanas [2].
O ensaio de fase III SELECT-COMPARE, controlado por placebo, comparou a eficácia e segurança do upadacitinib e do inibidor de TNF-alfa adalimumab, ambos em combinação com o MTX. Para este fim, 1.629 pacientes que tinham respondido inadequadamente ao MTX receberam 15 mg de upadacitinib (uma vez por dia), 40 mg de adalimumab (quinzenalmente) ou placebo, todos eles + MTX [10]. Se os doentes reagissem inadequadamente à terapia que lhes foi atribuída, seriam trocados de placebo para upadacitinib, de upadacitinib para adalimumab ou de adalimumab para upadacitinib ao fim de 14 a 26 semanas; todos os doentes restantes com placebo receberam upadacitinib [11] a partir da semana 26. A primeira fase de 48 semanas, duplo-cego, foi seguida por uma extensão de rótulo aberto com 1.403 doentes [2]. Já após 12 e após 48 semanas, um número significativamente maior de doentes atingiu a remissão (índice de actividade da doença para 28-joints C-Reactive Protein, DAS28-CRP < 2.6) ou baixa actividade da doença (DAS28-CRP ≤ 3.2) sob upadacitinib + MTX do que sob adalimumab + MTX [10, 11]. Esta melhor eficácia do upadacitinib + MTX em comparação com o adalimumab + MTX permaneceu durante todo o período de observação da extensão do rótulo aberto(Figura 1): Após 156 semanas, 32% dos pacientes com upadacitinib + MTX estavam em remissão, contra 22% no grupo adalimumab + MTX (p < 0,001). A baixa actividade da doença foi observada em 37% tomandoadacitinib + MTX e 26% tomando adalimumab + MTX (p < 0,001). Também em relação aos parâmetros relacionados com a dor e o funcionamento físico do paciente (Health Assessment Questionnaire-Disability Index, HAQ-DI), foram observadas melhorias significativamente maiores no braço upadacitinib + MTX após 156 semanas do que no grupo de comparação (p < 0,001 para a dor e p < 0,01 para HAQ-DI) [2].
O desafio da polifarmácia [12]A polifarmácia, definida como a utilização simultânea de cinco ou mais medicamentos, é – mesmo entre pessoas de meia idade – um fenómeno crescente associado à multimorbilidade. Assim, está associado a consequências negativas tais como quedas, hospitalização e mesmo a morte. A utilização inflacionista de medicamentos não essenciais deve assim ser evitada. No entanto, descobrir que medicamentos adicionais beneficiarão os doentes mais do que os danos é um grande desafio [12]. |
O Upadacitinib também é eficaz como monoterapia [3].
A questão de saber se podem ser alcançados melhores resultados com o upadacitinib do que apenas com o MTX, mesmo sem o uso adicional de csDMARD, foi o foco do ensaio aleatório duplo-cego fase III SELECT-MONOTHERAPY. Para este fim, a eficácia e segurança do upadacitinib como monoterapia após uma mudança do MTX em comparação com o tratamento MTX continuado foram investigados em 648 pacientes com resposta inadequada ao tratamento MTX inicial. Após 14 semanas, um número significativamente maior de pacientes atingiu o ponto final primário, uma resposta de 20% de acordo com os critérios do American College of Rheumatology (ACR), em monoterapia upadacitinib do que em MTX (68% vs. 41%, p ≤ 0,0001). Além disso, uma proporção significativamente maior de doentes do grupo upadacitinib estava em remissão ou apresentava baixa actividade da doença do que com MTX (DAS28-CRP < 2,6: 28% vs. 8%; DAS28-CRP ≤ 3,2: 45% vs. 19%; ambos p ≤ 0,0001) [3].
Perfil de segurança a longo prazo do upadacitinib [13]
A Agência Europeia de Medicamentos (EMA) iniciou actualmente uma avaliação da segurança no tratamento de doenças inflamatórias crónicas para todas as JAKi aprovadas [14]. O perfil de segurança do upadacitinib em RA a longo prazo em comparação com o MTX e o adalimumab foi avaliado numa análise integrada dos cinco estudos da fase III do programa experimental SELECT. Isto incluiu 2.630 pacientes com pelo menos uma dose de 15 mg de upadacitinib; mais de metade dos pacientes tomaram upadacitinib durante pelo menos 48 semanas. No total, isto corresponde a uma análise de 4.020,1 anos-paciente. Os efeitos secundários que levaram à interrupção do tratamento ocorreram com frequência comparável entre o upadacitinib, MTX e adalimumab (upadacitinib 8,4; MTX 9,5; adalimumab 11,1 por 100 pacientes-ano). A incidência de infecções graves foi semelhante nos grupos upadacitinib e adalimumab, mas mais elevada do que no grupo MTX. Infecções oportunistas, tromboembolismo venoso, complicações cardíacas graves (MACE) e malignidades ocorreram com frequência comparável nos três grupos. O herpes zoster era mais comum com upadacitinibe do que com adalimumabe e MTX (upadactinibe: 3,7; MTX: 1,4; adalimumabe: 1,3 por 100 pacientes-ano), mas não era grave em 96% dos casos. Globalmente, não foram observados novos sinais de segurança com upadacitinib na análise integrada a longo prazo [13].
Conclusão
Upadacitinib (RINVOQ®) oferece uma opção de tratamento eficaz com um perfil favorável de risco-benefício em AR activa moderada a grave e resposta inadequada ou intolerância a pelo menos um csDMARD [7, 16]. Como mostra a análise a longo prazo do estudo SELECT COMPARE, a ingestão diária do inibidor de JAK reversível e selectivo durante um período de mais de 3 anos pode permitir que mais de 30% dos doentes tratados atinjam o objectivo terapêutico de remissão (DAS28-CRP < 2.6) [2]. Além disso, a maioria dos pacientes de AR preferem tratamento sob a forma de comprimidos e sem o uso adicional de MTX, pelo que a opção de terapia oral (mono)com upadacitinib está potencialmente associada a uma melhor aderência e pode contrariar a polifarmácia [12, 16].
Literatura
As referências podem ser solicitadas por profissionais em medinfo.ch@abbvie.com.
Breve informação técnica RINVOQ®
Este texto foi produzido com o apoio financeiro da AbbVie AG, Alte Steinhauserstrasse 14, 6330 Cham.
CH-RNQR-220045_04/2022
Contribuição online desde 15.04.2021
Publicação actualizada 30.05.2022