Actualmente, a psoríase é considerada uma doença sistémica inflamatória na qual as citocinas pró-inflamatórias desempenham um papel importante. Vários circuitos inflamatórios estão envolvidos na patogénese da psoríase. As citocinas das famílias IL-23 e IL-17 são alvos comprovados, mas estão também a ser pesquisados outros alvos terapêuticos.
A eficácia e segurança da imunoterapia sistémica melhorou significativamente nos últimos anos com a introdução de novos agentes das classes de inibidores de IL-17 e IL-23. “Temos testemunhado um rápido aumento no número de preparações nos últimos anos”, diz a Dra. med. Sylvie Haase, especialista em doenças de pele e venéreas numa prática de grupo dermatológico em Constance [2]. Uma vasta gama de agentes sistémicos está agora disponível, dirigidos contra diferentes alvos, e como os patomecanismos moleculares continuam a ser decifrados, espera-se que esta tendência se mantenha no futuro (Fig. 1). Cada vez mais, o desafio é adequar os pacientes às opções de tratamento adequadas. Acontece que entre os doentes com psoríase moderada a grave, há aqueles que respondem muito bem à primeira opção de terapia sistémica e permanecem no mesmo tratamento durante anos, mas também alguns em que a psoríase se revela refratária à terapia, explicou o orador.
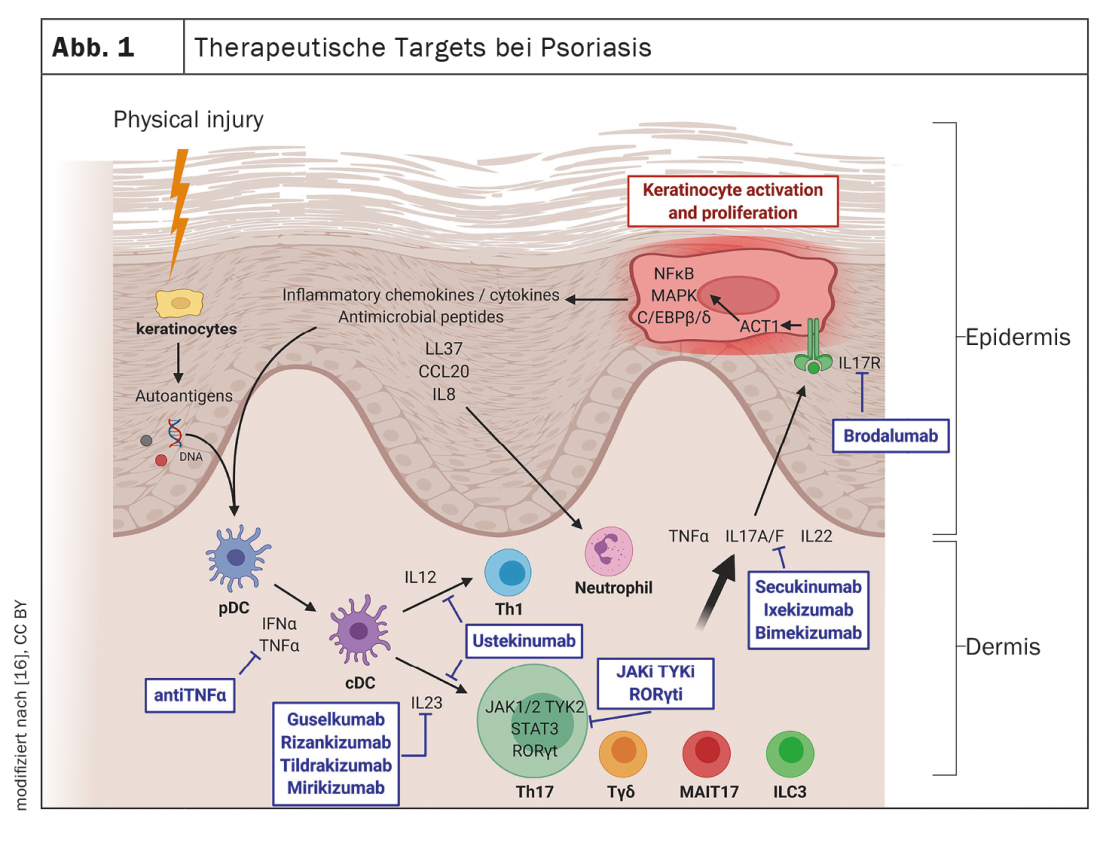
Análises de resposta à biologia: O que se pode deduzir delas?
A principal característica patológica da psoríase é considerada como uma inflamação cutânea crónica, que leva a uma proliferação descontrolada e diferenciação disfuncional dos queratinócitos. A nível molecular, o papel fisiopatológico central do eixo TNF-α-IL-23-Th17 é muito bem caracterizado. Os anticorpos monoclonais actualmente aprovados na Suíça para o tratamento da psoríase são dirigidos contra as seguintes citocinas: TNF-α, interleukin(IL)-12/IL-23, IL-23, IL-17A, ou IL-17A/F [1]. Segundo as meta-análises de rede, os grupos inibidores da IL-17 (IL-17-i) e IL-23 (IL-23-i) mostram uma eficácia mais elevada em termos de PASI*-90 e PASI-100 em comparação com TNF-α-i [8]. Relativamente à IL-23-i, o Dr. Haase explica: “O efeito ocorre um pouco mais lentamente em comparação com os inibidores da IL-17, mas os preparados não têm um espectro específico de efeitos secundários”. Na Suíça, o IL-17A-i secukinumab e ixekizumab estão actualmente aprovados, assim como recentemente o IL17A/F-i bimekizumab, e entre os IL-23-i, guselkumab, risankizumab e tildrakizumab estão no mercado.
* PASI = Área de Psoríase e Índice de Severidade
Num estudo de coorte, uma equipa de investigação da Dinamarca analisou a resposta a diferentes biólogos [3]. Os resultados de 2022 publicados no Journal of the European Academy of Dermatology and Venereology mostram que do total de 3280 pacientes incluídos (idade média de 45,0 anos, 37% do sexo feminino), 6,3% foram classificados como super-respondedores e 6,5% como refractários ao tratamento. Este último tinha um IMC médio mais elevado em comparação com os outros pacientes (32,2 vs. 29,4, p<0,0001), enquanto que os super-respondedores tinham menos comorbilidades e um estatuto socioeconómico mais elevado.
IL-17A/F inibidor bimekizumab é um novo jogador
Que a IL-17A desempenha um papel central na patogénese da psoríase foi provado várias vezes pela utilização bem sucedida dos correspondentes anticorpos inibidores. No entanto, a IL-17F é também sobreexpressa na pele e no tecido sinovial das pessoas que sofrem de psoríase [4]. Bimekizumab, um anticorpo monoclonal IgG1 que inibe selectivamente a interleucina IL-17F e IL-17A, tornou-se recentemente disponível na Suíça. Nos três estudos centrais, bimekizumab mostrou boa eficácia e teve melhor desempenho do que o antagonista da IL-12/IL-23 ustekinumab e o inibidor TNF-α adalimumab nos parâmetros co-primários PASI-90 e IGA# 0/1 na semana 16 [5–7]. O perfil de segurança do bimekizumab é caracterizado por efeitos de classe conhecidos de inibição da IL-17, os efeitos secundários comuns incluem a candidíase oral. Um novo nanobody trivalente contra IL-17A e IL-17F que está actualmente a ser investigado para uso na psoríase é o sonelokimab. Foram alcançados resultados promissores nos estudos das fases I e II [4]. Os nanocorpos são recombinados, anticorpos específicos de antigénios que consistem apenas no domínio variável necessário para a ligação de antigénios e são assim comparativamente pequenos.
# IGA=Investigator’s Global Assessment: Pacientes com IGA: 0 = pele sem aspecto, 1 = sintomas cutâneos ligeiros.
Vários agentes aplicados oralmente ou por via tópica estão também em fase de preparação
A investigação de novos agentes antipsoriásicos é um campo de investigação em rápido desenvolvimento. Os seguintes agentes sistémicos foram recentemente aprovados para a psoríase em placas pela US Food and Drug Administration (FDA) este ano (Quadro 1):
- Deucravacitinib (BMS-986165) é um inibidor altamente selectivo do TYK2 em forma de dosagem oral para uso diário em psoríase de placa moderada a severa (aprovação da FDA 09/09/22) [9,10].
- Roflumilast (ARQ-151) é um inibidor de PDE-4 tópico para o tratamento da psoríase em placas em doentes ≥12 anos de idade (aprovação da FDA 07/29/22) [11–13].
- Tapinarof-Crème 1% (Vtama) é um modulador de receptor de hidrocarbonetos arilo para o tratamento da psoríase em placas em adultos (aprovação da FDA 05/24/22) [18,19].
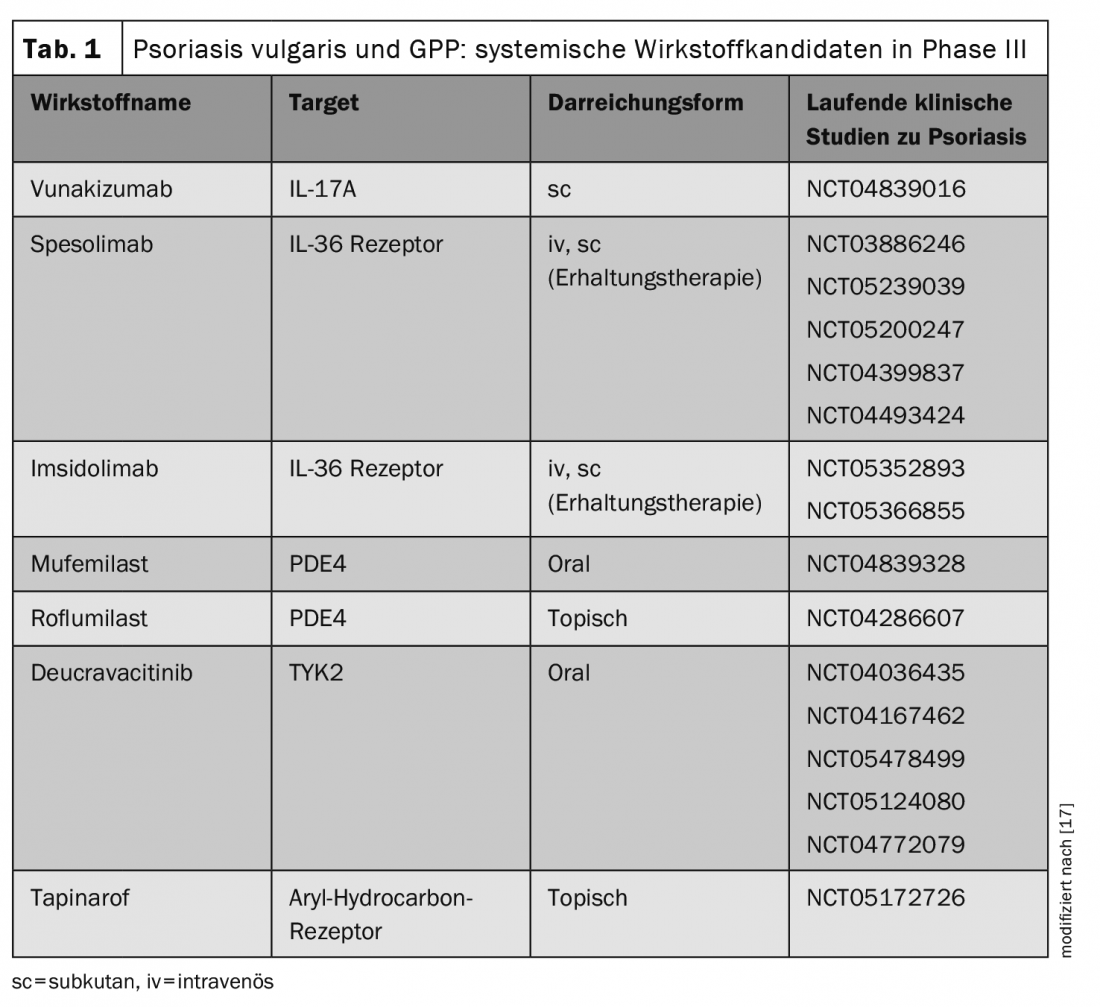
Além disso, o spesolimab, um anticorpo monoclonal humanizado contra a IL36-R foi aprovado pela FDA para o tratamento das crises de GPP (Psoríase Pustular Generalizada) (aprovação da FDA 01.09.22). A decisão de aprovação é baseada no estudo da fase II Effisayil-1 [14,15]. Outros agentes sistémicos inovadores estão actualmente em fases avançadas de desenvolvimento clínico (Tab. 1) [17]. Por conseguinte, é possível que o espectro do tratamento também possa ser alargado na Europa num futuro não muito distante para incluir mais terapias de sistema. Especialmente para pacientes refractários, são bem-vindas novas alternativas de tratamento. No que diz respeito aos perfis de efeitos secundários, o Dr. Haase salienta que os efeitos conhecidos da classe de substâncias dos inibidores JAK incluem um número ligeiramente maior de infecções do tracto respiratório superior e herpes simples, e que o exantema semelhante ao acne pode ocasionalmente ocorrer. São necessários dados a longo prazo para compreender melhor as diferenças entre as várias opções de tratamento e para poder fazer uma escolha orientada para o paciente.
Congresso: Bodensee Dermaconsil
Literatura:
- Lauffer F, et al: Citoquinas da família IL-17 na psoríase. JDDG; 1610-0379/2020/1807
- “Psoríase – há algo de novo?”, Dr. med. Sylvie Haase, 3rd Bodensee Dermaconsil, 22.10.2022.
- Loft N, et al: Prevalência e caracterização da psoríase refratária ao tratamento e super-respondedores ao tratamento biológico: um estudo de âmbito nacional. J Eur Acad Dermatol Venereol 2022; 36(8): 1284-1291.
- Iznardo H, Puig L: Dupla inibição da IL-17A e da IL-17F na doença psoriásica. Ther Adv Chronic Dis 2021 Ago 12;12:20406223211037846
- Warren RB, et al: Bimekizumab versus adalimumab na psoríase em placas. N Engl J Med 2021; 385: 130-141.
- Reich K, et al: Bimekizumab versus ustekinumab para o tratamento da psoríase de placa moderada a grave (BE VIVID): eficácia e segurança de um ensaio de 52 semanas, multicêntrico, duplo-cego, comparador activo e placebo controlado fase 3. Lancet 2021; 397: 487-498.
- Gordon KB, et al: Bimekizumab eficácia e segurança na psoríase de placa moderada a grave (BE READY): um ensaio multicêntrico, duplo-cego, controlado por placebo, fase 3 de retirada aleatória. Lancet 2021; 397: 475-486.
- Yasmeen N, et al: Terapias direccionadas para doentes com psoríase moderada a grave: uma revisão sistemática e meta-análise em rede da resposta à PASI a 1 ano. J Dermatolog Treat 2022; 33(1): 204-218.
- Boerner LK. Reunião híbrida divulga estruturas de candidatos a drogas [Internet]. Notícias Químicas e de Engenharia. 2022. Disponível em: https://cen.acs.org/acs-news/acs-meeting-news/Hybrid-meeting-divulges-st…,(último acesso em 15.11.2022)
- Chimalakonda A, et al.: Perfil de selectividade do inibidor deucravacitinibe de tirosina kinase 2 em comparação com os inibidores de Janus kinase 1/2/3. Dermatol Ther (Heidelb) 2021; 11(5): 1763-1776.
- Lebwohl MG, et al: Ensaio de creme de roflumilast para psoríase crónica em placas. N Eng J Med 2020; 383(3): 229-239.
- Bioterapêutica de Arcutis. A FDA aprova o Creme ZORYVE (roflumilast) da Arcutis 0,3% Para o tratamento da psoríase em placas em indivíduos com 12 anos ou mais [Internet]. 2022. Disponível a partir de: www.arcutis.com/fda-approves-arcutis-zoryve-roflumilast-cream-0-3-for-th…,(último acesso em 15.11.2022)
- Lebwohl M, et al.: Segurança e eficácia do creme uma vez por dia roflumilast Cream 0,3%, um potente inibidor de fosfodiesterase 4 para o tratamento da psoríase nos ensaios DERMIS-1 e DERMIS-2 fase 3. Poster apresentado em:30º Congresso da EADV, 29 de Setembro – 2 de Outubro de 2021; virtual
- Boehringer Ingelheim. A FDA aprova a primeira opção de tratamento para as crises de psoríase pustulosa generalizada em adultos [Internet]. 2022. Disponível em: www.boehringer-ingelheim.us/press-release/fda-approves-first-treatment-o….,(último acesso em 15.11.2022)
- Bachelez H, et al: Ensaio de espesolimab para psoríase pustulosa generalizada. N Engl J Med 2021; 385(26): 2431-2440.
- Bugaut H, Aractingi S: Papel Principal do Eixo IL17/23 na Psoríase Apoia o Desenvolvimento de Novas Terapias Orientadas. Front Immunol 2021;12:621956. www.frontiersin.org,(último acesso 15 Nov 2022).
- Drakos A, Vender RA: Revisão da Paisagem dos Ensaios Clínicos em Psoríase: Uma Actualização para os Clínicos. Dermatol Ther (Heidelb) 2022, https://doi.org/10.1007/s13555-022-00840-9,(último acesso 15 Nov 2022).
- Keam SJ: Tapinarof creme 1%: primeira aprovação. Drogas 2022; 82(11): 1221-1228.
- Lebwohl MG, et al: Ensaios de fase 3 de creme de tapinarofo para psoríase em placas. N Engl J Med 2021; 385(24): 2219-2229.











