O ferro é essencial para várias funções bioquímicas e fisiológicas. A deficiência de ferro é generalizada e uma das principais causas de anemia. Como profilaxia, é importante um fornecimento adequado de ferritina através da dieta. Na presença de deficiência de ferro, pode ser utilizada a substituição oral ou intravenosa, em que a eficácia e a tolerabilidade variam de indivíduo para indivíduo.
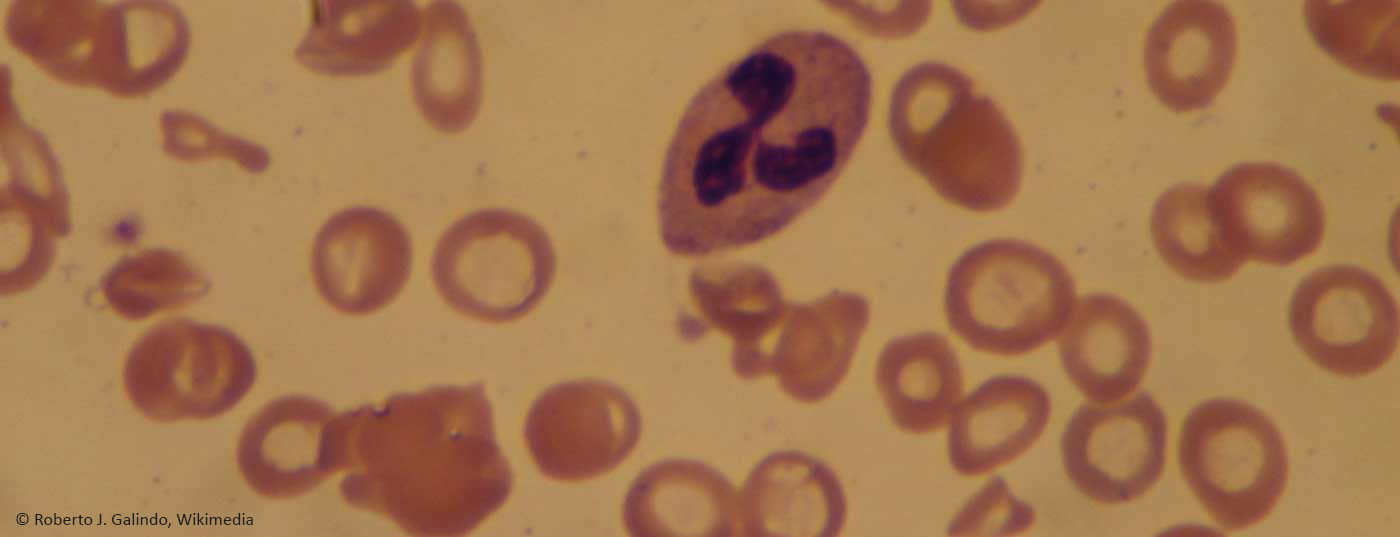
O ferro é um dos quatro elementos mais comuns na crosta terrestre. É um importante elemento vestigial para todos os seres vivos – incluindo os humanos. Deve o seu papel essencial em biologia à sua capacidade de transportar e ligar electrões de forma reversível. Em hemoglobina, por exemplo, é responsável por assegurar que o oxigénio altamente electronegativo possa ser transportado eficazmente. Pela mesma razão, o ferro é um componente central de numerosos sistemas enzimáticos que assumem muitas funções bioquímicas e fisiológicas.
Mais de 1,2 mil milhões de pessoas em todo o mundo sofrem de deficiência de ferro [1]. Esta é uma das principais causas de anemia [2]. Na Europa, as recolhas de dados entre mulheres em idade fértil mostram uma prevalência de deficiência de ferro de 10-32%, com uma prevalência estimada de anemia de 2-5%. A percentagem de mulheres com armazéns de ferro baixos é estimada em 40-55% [3]. As prevalências de deficiência de ferro em crianças pequenas foram registadas localmente e mostraram valores de 4-48%. Assim, as crianças pequenas representam outro grupo de risco de deficiência de ferro [4].
Porque é um dos elementos mais difundidos ao mesmo tempo responsável por uma deficiência global de peso? A razão reside na capacidade do ferro de promover a formação de radicais reactivos tóxicos. Além disso, o ferro é praticamente insolúvel na sua forma livre a pH fisiológico (ou seja, em qualquer parte do corpo excepto no ácido gástrico). A absorção do ferro é, portanto, naturalmente limitada. Para que possa ser utilizado, deve ser tomado de forma vinculada: associado a proteínas que o possam ligar de forma forte mas reversível.
Metabolismo e absorção do ferro
Até à data, nenhum mecanismo activo de excreção do ferro é conhecido; a excreção renal é irrelevante para o equilíbrio do ferro. O equilíbrio do ferro humano deve portanto ser regulado activamente durante a absorção dos alimentos no intestino delgado, onde os enterócitos desempenham um papel fundamental.
O ferro nos alimentos existe em duas formas principais: Ferro Haeme (em produtos de origem animal) e ferro não haeme (em produtos de origem animal e não animal). É absorvido principalmente no intestino delgado, onde o pH do conteúdo intestinal sobe sucessivamente ao longo de um gradiente até quase neutralidade. O ferro não-hidratado dos alimentos torna-se mais insolúvel ao longo deste gradiente, razão pela qual a absorção no intestino distal desempenha provavelmente um papel subordinado. A solubilidade do ferro no intestino delgado é um factor importante na absorção do ferro dos alimentos e pode ser significativamente influenciada pela composição de uma refeição.
A nível celular, o ferro em hémen e o ferro não em hémen são tomados por diferentes transportadores. Ambos contribuem para a concentração de ferro em enterócitos, o que é crucial para a regulação do ferro celular. Tem uma influência directa na conformação das proteínas de resposta do ferro (IRPs), que controlam a síntese das proteínas de transporte celular. Assim, o ferro intervém directamente na síntese dos mecanismos de transporte que o importam ou exportam para a célula. Isto é particularmente importante para o controlo do equilíbrio sistémico de ferro em enterócitos, macrófagos e hepatócitos.
Um segundo componente regulador, de acção sistémica, é a hepcidina hormonal, que é sintetizada no fígado. A Hepcidina é regulada por diferentes sinais: O aumento da eritropoiese ou hipoxia leva a baixas concentrações, enquanto os estímulos inflamatórios/infecciosos (interleucina-6) e o próprio estado do ferro do organismo (saturação da transferrina) aumentam a síntese. A Hepcidina liga-se ao único exportador de ferro celular conhecido, a ferroportina, levando à sua degradação. Assim, o ferro permanece nas células e já não pode entrar na corrente sanguínea, o que, por sua vez, afecta os IRPs e a sua cascata de reacção. Uma vez que este processo é sistemicamente regulado, isto afecta todos os tipos de células. Um balanço equilibrado do ferro é assim o resultado dos processos de todos os balanços celulares individuais do ferro e da sua orquestração sistémica por hepcidina [5]. A descoberta desta hormona nos anos 2000 expandiu grandemente a compreensão da regulação do ferro: a elevação crónica da hepcidina leva a uma anemia marcada que não pode ser corrigida, ou só pode ser parcialmente corrigida, pela ingestão oral de ferro; por exemplo, a anemia causada por doenças inflamatórias ou infecciosas crónicas.
Recuperação do ferro através da reciclagem
O conteúdo de ferro em adultos é ≈4 g e encontra-se principalmente nos glóbulos vermelhos (≈2.8 g). 90% das necessidades diárias são cobertas pela recuperação de glóbulos vermelhos antigos. Este ciclo de reciclagem tem lugar entre medula óssea, glóbulos vermelhos e macrófagos. Na medula óssea, são produzidos os eritrócitos (≈300 mg), os macrófagos absorvem os antigos eritrócitos, decompõem-nos e libertam o ferro de volta para a corrente sanguínea, onde pode ser utilizado novamente pela medula óssea (≈600 mg). As reservas de ferro variam individualmente e encontram-se principalmente no fígado. O ferro a ser transportado na corrente sanguínea está ligado à transferrina, que constitui uma proporção dinâmica mas pequena (3-4 mg) do teor total de ferro. Esta fracção é responsável pelo transporte entre células e tecidos e é, portanto, de grande importância funcional.
10-20% das necessidades diárias de ferro (1-2 mg) devem ser ingeridas através dos alimentos para compensar as perdas diárias naturais de ferro (por exemplo, através de pequenas hemorragias, através das membranas mucosas, etc.). Como a quantidade a ser absorvida por dia é muito pequena em comparação com o conteúdo do corpo, a deficiência de ferro só pode resultar de um défice de ferro a longo prazo. As mulheres jovens, grávidas ou crianças são mais frequentemente afectadas, uma vez que a perda de sangue durante a menstruação e o crescimento leva a um aumento das necessidades de ferro.
A anemia aumenta o risco de complicações na gravidez e pode levar a um parto prematuro. A deficiência de ferro pode ser crónica e assintomática. Sintomaticamente, manifesta-se em fadiga, falta de concentração, irritabilidade, tolerância reduzida ao frio, falta de ar durante a actividade física, síndrome de pica e síndrome das pernas inquietas. Outros sintomas incluem pele e palidez conjuntival, estomatite e koilonychia.
Biomarcador para deficiência de ferro
As medidas bioquímicas do estado do ferro reflectem o tamanho relativo dos diferentes compartimentos e, ao mesmo tempo, informam sobre o estado geral do ferro do organismo. O padrão de ouro é a medição do teor de ferro na medula óssea. Se este for demasiado baixo, muito pouco ferro é reciclado na circulação do corpo. este défice não pode ser compensado por dieta ou reservas de fígado, resultando na redução da eritropoiese e da anemia.
Um sinal de anemia por deficiência de ferro é também o aumento da hemoglobina após a administração de ferro em doentes anémicos.
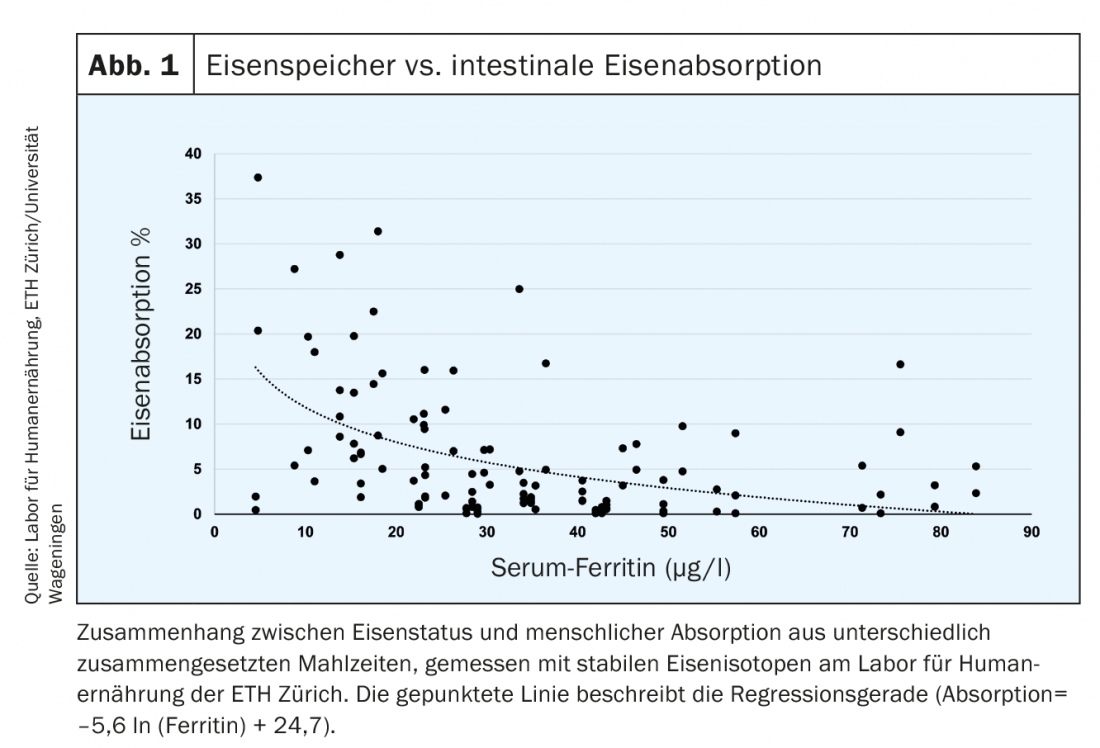
Além disso, a absorção de ferro medida com isótopos de ferro radioactivos ou estáveis é aumentada em doentes com deficiência de ferro (Fig. 1) [6]. Em pessoas saudáveis, os limites de ferritina de soro (SF) estão linearmente relacionados com armazéns de ferro. 1 µg/l SF corresponde a cerca de 120 µg armazéns de ferro/kg de peso corporal ou cerca de 8-10 mg armazéns de ferro [7]. O valor limite definido de 15 µg/l indica a ausência de ferro detectável na medula óssea e reflecte as lojas vazias. Uma redução adicional do valor abaixo de 15 µg/l não tem, portanto, qualquer significado quantitativo. Bioquimicamente, o SF é a molécula de armazenamento intracelular de ferro e reflecte a acumulação de ferritina intracelular em macrófagos e hepatócitos. Em pacientes saudáveis, o SF reflecte assim as reservas de ferro no fígado. Com eritropoiese (talassemia) defeituosa, há uma acumulação de ferro intercelular nos macrófagos, o que também leva a um aumento da ferritina. Durante uma infecção ou inflamação, o nível de hepcidina aumenta. O ferro celular só é exportado a uma extensão reduzida e deve ser armazenado celularmente (em moléculas de ferritina). Isto pode levar a um “falso” aumento da ferritina, o que neste caso não indica um aumento do armazém de ferro.
Em doentes com doenças infecciosas ou inflamatórias, deve portanto ser determinado outro marcador: o receptor de transferrina solúvel no soro (sTfR), que é proporcional às necessidades de ferro das células. Na prática, este valor reflecte a “fome” das células da medula óssea por ferro. O quociente de SF e sTfR demonstrou ser muito preditivo [8]. Infelizmente, o marcador muito útil sTfR não está bem padronizado; diferentes métodos definem diferentes limiares para a deficiência de ferro.
A saturação da transferência é outro marcador útil que representa a disponibilidade actual do ferro sistémico e que é diminuída durante a deficiência. Este marcador pode dar indicações de uma deficiência de ferro funcional, especialmente em ligação com um aumento de SF devido a infecção ou inflamação. Uma visão geral dos biomarcadores estabelecidos e experimentais para o ferro é fornecida por Lynch et al. [8].
Prevenção através da dieta correcta
A biodisponibilidade do ferro da dieta é definida tanto pelo seu teor de ferro como pela sua composição [9]. Níveis médios a altos de ferro são encontrados em leguminosas, carne, ovos, produtos de cereais integrais, alimentos fortificados, frutos secos e sementes. O ferro Haem é absorvido em quantidades crescentes (intacto) (20-50%). A absorção é menos susceptível a inibidores e promotores de absorção de ferro e é menos influenciada pelo estatuto pessoal do ferro. O ferro não heme, por outro lado, é mais sensível à composição da dieta e ao estado do ferro, resultando numa elevada variabilidade na absorção do ferro (2-50%). Apesar da pequena quantidade de ferro hemorrágico consumida na dieta, representa uma elevada percentagem do consumo de ferro dietético porque é mais biodisponível.
Vários componentes definem a absorção do ferro no intestino delgado, que também é influenciada pela solubilidade: A carne muscular ou o ácido ascórbico (vitamina C) têm um efeito de promoção. No entanto, os cereais e os produtos integrais, que na realidade são ricos em ferro, contêm ácido fítico, o que reduz a percentagem de absorção. Os polifenóis e os taninos do chá e do café têm um efeito semelhante. O ácido ascórbico em frutas e legumes contraria a inibição. As combinações de alimentos ricos em ferro e vitamina C são particularmente recomendadas (visão geral 1). Uma dieta variada com muito ácido ascórbico, carne muscular ou peixe mostra uma absorção de 15-17% [10].

Suplemento oral e intravenoso
Embora a optimização da dieta possa ser eficaz para a prevenção primária da deficiência de ferro, recomenda-se a suplementação em casos de deficiência comprovada de ferro para corrigir rapidamente a anemia, inverter a deficiência de ferro nos tecidos e reabastecer as reservas de ferro.
Os suplementos de ferro são eficazes, mas também podem causar efeitos secundários dose-dependentes. Num estudo em doentes idosos, foram administrados 15, 50 ou 150 mg de Fe durante três meses. Embora a eficácia tenha sido semelhante no final do estudo, os grupos que receberam 50 e 150 mg Fe mostraram mais efeitos secundários [11].
O ferro aumenta a concentração de hepcidina durante várias horas. Nas doses de ≥60 mg Fe, a hepcidina aumenta de forma dependente da dose após administração de um suplemento de ferro e permanece elevada até 24 horas. Este aumento está associado a uma redução na absorção de cerca de 35%. Por esta razão, podem ser dados suplementos de ferro dia sim dia não para aumentar a eficiência de absorção, mantendo a mesma dose [12]. Além disso, foi demonstrado que a divisão da dose no mesmo dia (por exemplo 2× 60 mg Fe em vez de 1× 120 mg Fe) não tem valor acrescentado em termos de aumento da absorção [13].
Doses <60 mg Fe são susceptíveis de ter um efeito menor na hepcidina. Além disso, doses mais pequenas podem não só prevenir eficazmente a deficiência de ferro, mas também ter menos efeitos secundários [14].
Deve-se notar que com a suplementação oral em doses menores, a percentagem de absorção aumenta, mas a quantidade total de ferro absorvido diminui. Ao recomendar a administração alternada do ferro, o estatuto do ferro deve, portanto, ser também tido em consideração. Os possíveis efeitos secundários devem ser ponderados em relação ao efeito a ser alcançado.
O ferro intravenoso é recomendado como terapia de primeira linha para deficiência grave, sintomática de ferro com anemia [1]. Isto é geralmente bem tolerado e raramente tem efeitos secundários. Quaisquer efeitos negativos sobre o ecossistema intestinal, por exemplo, em pacientes em pré-esforço, são contornados. Na Suíça, contudo, o uso mais frequente de terapias intravenosas também suscitou críticas, principalmente devido aos custos mais elevados [15]. O Gabinete Federal de Saúde Pública iniciou agora uma “Avaliação da Tecnologia da Saúde”.
A terapia para a deficiência de ferro e a anemia por deficiência de ferro deve ser personalizada. A escolha da terapia “certa” deve incluir possíveis causas, o grau de deficiência de ferro, comorbidades, a duração da deficiência e as preferências do paciente. Para além de razões clínicas/fisiológicas, a nutrição e o estilo de vida (desporto, contracepção) desempenham um papel importante na prevenção de deficiências e na manutenção de um estado de ferro saudável após terapia em pacientes saudáveis de outra forma.
Mensagens Take-Home
- Para a prevenção da deficiência de ferro, deve ser recomendada uma dieta variada rica em ferro e com elevada biodisponibilidade de ferro.
- Com a suplementação oral, baixas doses (entre 30 e 60 mg Fe/dia) são melhor absorvidas em termos percentuais e são susceptíveis de causar menos efeitos secundários.
- A terapia de suplementação com ferro deve ser individualizada tanto quanto possível. Deve ser recomendada terapia oral em dias alternados (por exemplo, se a deficiência de ferro não for grave: 60 mg/dia, de dois em dois dias).
Literatura:
- Camaschella C: Deficiência de ferro. Sangue 2019; 133(1): 30-39.
- Zimmermann MB, Hurrell RF: Deficiência de ferro nutritivo. Lancet 2007; 370(9586): 511-520.
- Milman N, et al: Estatuto do ferro em mulheres grávidas e mulheres em idade reprodutiva na Europa. Am J Clin Nutr 2017; 106(Suppl 6): 1655S-1662S.
- Van der Merwe LF, Eussen SR: Estatuto do ferro das crianças pequenas na Europa. Am J Clin Nutr 2017; 106(Suppl 6): 1663S-1671S.
- Hentze MW, et al.: Two to tango: regulação do metabolismo do ferro mamífero. Célula 2010; 142(1): 24-38.
- Daru J, et al: A ferritina sérica como indicador do estado do ferro: o que precisamos de saber? Am J Clin Nutr 2017; 106(Suppl 6): 1634S-1639S.
- Cook JD: Diagnóstico e gestão da anemia por deficiência de ferro. Best Pract Res Clin Haematol 2005; 18(2): 319-332.
- Lynch S, et al: Biomarkers of Nutrition for Development (BOND)-Iron Review. J Nutr 2018; 148(Suppl 1): 1001S-1067S.
- Hurrell R, Egli I: Biodisponibilidade do ferro e valores de referência dietéticos. Am J Clin Nutr 2010; 91(5): 1461s-1467s.
- OMS/FAO: Requisitos vitamínicos e minerais na nutrição humana: relatório de uma consulta conjunta FAO/OMS de peritos. Genebra: OMS/FAO 2004.
- Rimon E, et al.: Estamos a dar demasiado ferro? A terapia com baixas doses de ferro é eficaz em octogenários. American J Med 2005; 118(10): 1142-1147.
- Moretti D, et al.: Os suplementos orais de ferro aumentam a hepcidina e diminuem a absorção de ferro a partir de doses diárias ou duas vezes por dia em mulheres jovens com ingestão de ferro. Sangue 2015; 126(17): 1981-1989.
- Stoffel NU, et al: Absorção de ferro de suplementos orais de ferro em dias consecutivos versus alternados e como doses matinais únicas versus doses bifásicas em mulheres com ferro: dois ensaios controlados aleatorizados, com rótulo aberto. Lancet Haematol 2017; 4(11): e524-e533.
- Bialkowski W, et al: Estimativas do ferro total do corpo indicam que 19 mg e 38 mg de ferro oral são equivalentes para a atenuação da deficiência de ferro em indivíduos que sofrem de flebotomia repetida. Am J Hematol 2017; 92(9): 851-857.
- Giger M, Achermann R: [Substituição do ferro em pacientes externos na Suíça: aumento dos custos associados à administração intravenosa]. Z Evidência Fortibld Qual Gesundhwes 2013; 107(4-5): 320-326.
PRÁTICA DO GP 2019; 14(2): 15-18
CARDIOVASC 2020; 19(3): 6-9