Factores como el pretratamiento, la edad, el rendimiento y las comorbilidades del paciente determinan la terapia de recaída en el mieloma múltiple. Las combinaciones estándar son triples con un inhibidor del proteasoma y/o un IMID. Las terapias con anticuerpos también desempeñan un papel importante en el tratamiento del mieloma.
Para los pacientes aptos con mieloma múltiple recién diagnosticado, se realiza un tratamiento de inducción seguido de quimioterapia consolidada a dosis altas con trasplante autólogo de células madre (TACM). Para lograr un buen control de la enfermedad durante el mayor tiempo posible, se sigue un tratamiento de consolidación y/o una terapia de mantenimiento. El objetivo terapéutico es una remisión completa, a ser posible molecular. En los pacientes de edad avanzada y/o que no están en forma, la atención se centra en lograr la mejor respuesta posible al tratamiento de primera línea con pocos efectos secundarios y la preservación de la calidad de vida.
Casi todos los pacientes sufren posteriormente una recidiva. En esta situación, las combinaciones lenalidomida/dexametasona (RD) y bortezomib/dexametasona (VD) fueron los tratamientos estándar durante mucho tiempo [1–3]. Sin embargo, ambas sustancias se utilizan ahora ampliamente en el tratamiento de primera línea, lo que significa que el número de pacientes refractarios a estos fármacos está aumentando. Desde hace algunos años, hay muchos medicamentos nuevos disponibles para estos pacientes. La elección de la terapia tiene en cuenta las terapias anteriores (cambio de clase de sustancia, respuesta, tolerancia), la edad, el rendimiento, las comorbilidades y, por supuesto, la aprobación en Suiza. En pacientes aptos con un periodo libre de progresión de al menos 12 meses tras un primer TCMA, debería considerarse un segundo TCMA, ya que los resultados tras un TCMA de rescate en dichos pacientes son equivalentes o superiores a los de las combinaciones de tres fármacos más eficaces, con una duración del tratamiento más corta y unos costes totales más bajos por término medio (Tab. 1) [4,5].
Primera recaída tras una terapia basada en bortezomib
Tras la terapia de primera línea a base de bortezomib, hasta hace unos años se sugería a los pacientes el tratamiento con lenalidomida/dexametasona [1,2]. Hoy en día, en la segunda línea, con una mejor supervivencia libre de progresión (SLP), la atención debe centrarse en una combinación de tres fármacos.
La combinación de DR con el anticuerpo monoclonal SLAMF7 (“molécula de activación linfocítica de señalización F7”) elotuzumab mostró una mediana de SLP de 19,4 meses (frente a 14,9 meses con DR) en el ensayo ELOQUENT-2. Se incluyeron 646 pacientes con una mediana de dos terapias previas. El tratamiento con ERD se continuó hasta la progresión o la aparición de efectos secundarios inaceptables. La tasa de respuesta global (ORR) con ERD fue del 79% (frente al 66%). El tiempo hasta el siguiente tratamiento (TTNT) se prolongó un año (33 frente a 21 meses), la mediana de supervivencia en el grupo ERD fue de 43,7 meses (frente a 39,6 meses). Los efectos secundarios de grado 3 o 4 más frecuentes fueron hematológicos (neutropenia 34% frente a 44% y linfopenia 77% frente a 49%). Los beneficios clínicos se acompañaron de una mayor frecuencia de infecciones (88% frente a 74%), especialmente de herpes zóster [6,7]. En Suiza, la combinación de elotuzumab con lenalidomida y dexametasona (ERD) está aprobada a partir de la segunda línea de tratamiento.
Como terapia triple adicional, la combinación de lenalidomida/dexametasona junto con carfilzomib, un inhibidor del proteasoma de segunda generación, está aprobada a partir de la segunda línea de tratamiento. En el ensayo ASPIRE, esta combinación mostró una prolongación de la mediana de la SLP de 8,7 meses (26,3 frente a 17,6 meses) en 792 pacientes en comparación con la DR sola. Se administró carfilzomib con DR (KRD) durante un máximo de 18 ciclos, DR hasta la progresión. La ORR fue de un impresionante 87,1% (frente al 66,7%), con una tasa de RC para la DRK del 31,8% (frente al 9,3% en el grupo de DR). La supervivencia a 2 años en el grupo KRD fue del 73,3% (frente al 65%). El carfilzomib se administra en esta combinación hasta un máximo de 27 mg/m2 dos veces por semana. La tasa de efectos secundarios, también con respecto a la neuropatía, es comparable. De especial interés fueron los problemas cardiacos con carfilzomib: disnea (2,8% frente a 1,8%), insuficiencia cardiaca (3,8% frente a 1,8%), cardiopatía isquémica (3,3% frente a 2,1%), hipertensión (4,3% frente a 1,8%) e insuficiencia renal aguda (3,3% frente a 3,1%) [8].
Primera recaída tras una terapia basada en IMID
Tras la terapia de primera línea basada en IMID, se recomienda la terapia con inhibidores del proteasoma como terapia de segunda línea. Tradicionalmente, se utiliza la combinación bortezomib/dexametasona (VD) [3]. La combinación de carfilzomib con dexametasona (KD) demostró ser más eficaz en el ensayo ENDEAVOR. La mediana de la SLP fue significativamente más larga, 18,7 frente a 9,4 meses, en comparación con la VD. El 54% de los 929 pacientes de este estudio fueron pretratados con bortezomib, aunque no refractarios. También en estos pacientes, la SLP fue mayor con la DR, 15,6 frente a 8,1 meses. Se administró carfilzomib a la dosis de 56 mg/m2 dos veces por semana. Los acontecimientos adversos más comunes a esta dosis incluyeron anemia (14% frente a 10%), hipertensión (9% frente a 3%), trombocitopenia (8% frente a 9%) y neumonía (7% frente a 8%), mientras que la aparición de polineuropatías de grado 2 o superior fue significativamente menos frecuente con carfilzomib (6% frente a 32%) [9]. El carfilzomib no está autorizado en Suiza en esta dosis.
La norma en la primera recaída debe ser una combinación triple si es posible. Una combinación bastante favorable es la de bortezomib/dexametasona en combinación con ciclofosfamida (VCD o CyBorD). Sin embargo, este tratamiento sólo está aprobado en Suiza para el tratamiento de inducción previo a una ASZT planificada. En cambio, el régimen KRD, significativamente más caro, está aprobado a partir de la segunda línea de terapia.
Tratamiento de nuevas recidivas
A partir de la tercera línea de terapia (tras el fracaso del bortezomib y la lenalidomida), la combinación de pomalidomida con dexametasona (Pom/D) está aprobada en Suiza [10]. Debido a su elevado coste, la dosis aprobada (4 mg/día) se ha cuestionado recientemente en favor de un régimen alternante (4 mg en días alternos), lo que es potencialmente significativo en términos de economía sanitaria [11]. De forma similar al carfilzomib, las cuestiones sobre la dosificación óptima en la terapia del mieloma no se han resuelto satisfactoriamente en el frenético ritmo de lanzamiento de productos.
Como fármaco adicional, el inhibidor de la histona deacetilasa panobinostat en combinación con VD está aprobado a partir de la tercera línea. En el estudio PANORAMA-1, 768 pacientes muy pretratados fueron tratados con panobinostat/VD o panobinostat/VD. Tratados con placebo/VD. El panobinostat se administra por vía peroral tres días a la semana en las semanas 1 y 2 de un ciclo de 21 días, además del VD. Hubo una mejora en la mediana de la SLP de casi cuatro meses (12 frente a 8 meses) con la misma supervivencia global. La ORR con panobinostat/VD fue del 60,7%, lográndose una respuesta completa en el 11% de los pacientes y una respuesta parcial muy buena en el 17%. Los efectos secundarios no hematológicos más frecuentes fueron diarrea (68% frente a 42%), astenia o fatiga (57% frente a 41%) y neuropatía periférica (61% frente a 67%). Los efectos secundarios hematológicos significativos también fueron más frecuentes con el panobinostat [12].
El primer inhibidor del proteasoma disponible peroralmente, el ixazomib, está aprobado en Suiza en combinación con lenalidomida y dexametasona a partir de la tercera línea de tratamiento (o a partir de la segunda línea de tratamiento si se presentan características de alto riesgo). El ensayo TOURMALINE-MM1 comparó ixazomib en combinación con DR frente a placebo/RD. La mediana de la SLP fue significativamente más larga en el grupo de ixazomib (20,6 frente a 14,7 meses). La tolerancia hematológica de ambas terapias fue comparable. Se produjo neuropatía periférica en el 27% de los pacientes (frente al 22%) con ixazomib [13]. Como terapia completamente peroral, esta combinación es sin duda agradable para el paciente.
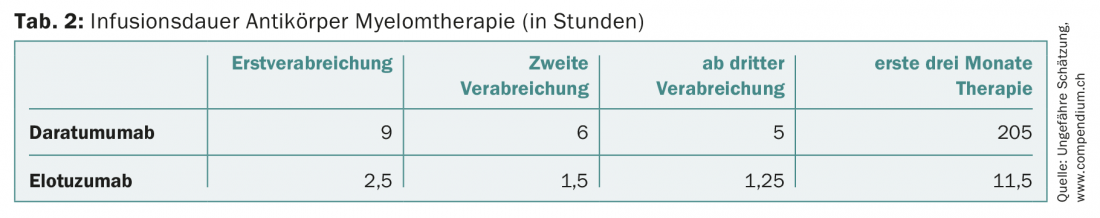
En pacientes refractarios al menos a un inhibidor del proteasoma y a un agente inmunomodulador, o que hayan recibido al menos tres terapias previas, también puede administrarse en Suiza el anticuerpo monoclonal CD38 daratumumab. Como monoterapia, el daratumumab muestra tasas de respuesta de alrededor del 30% [14]. El anticuerpo, que inicialmente se administra semanalmente, plantea un reto para las clínicas oncológicas ambulatorias cuando se utilice de forma más generalizada, dada la larga duración de la infusión, de nueve horas para la primera administración (y todavía de al menos cinco horas a partir de la tercera administración). El daratumumab también ha sido aprobado recientemente en segunda línea en combinación con dexametasona y bortezomib o lenalidomida.
Otras opciones terapéuticas
En la literatura, en rápido crecimiento, pueden encontrarse otros regímenes terapéuticos para el tratamiento del mieloma múltiple recidivante.
En el ensayo CASTOR, 498 pacientes con una mediana de dos terapias previas fueron aleatorizados a daratumumab/VD (Dara/VD) o VD solo. En ambos brazos de tratamiento, el VD se interrumpió tras ocho ciclos cada uno, y el daratumumab pudo continuarse hasta la progresión. Tras una mediana de seguimiento de 7,4 meses, se observó una SLP significativamente prolongada en el grupo de daratumumab. La ORR fue significativamente mayor en el brazo de daratumumab (82,9% frente a 63,2%) y, en particular, las tasas de remisión parcial muy buena o mejor casi se duplicaron (59,2% frente a 29,1%) [15].
En el estudio POLLUX, 569 pacientes pretratados con al menos una terapia recibieron DR o la combinación con daratumumab. Tras una mediana de seguimiento de 13,5 meses, el análisis provisional mostró una SLP prolongada en el grupo experimental (no alcanzada frente a 18,4 meses). La ORR también fue mayor en el brazo de daratumumab, con un 92,9% (frente al 76,4%), al igual que la tasa de remisiones completas (43,1% frente al 19,2%) [16]. El principal problema del uso de este anticuerpo son las reacciones a la infusión y la trombopenia.
También hay datos de combinaciones de Pom/D con una tercera sustancia para el mieloma recidivante, por ejemplo en combinación con 400 mg semanales de ciclofosfamida peroral (PomCyDex) o bortezomib (PVD) [17,18]. Ambos estudios incluyeron pacientes con mieloma refractario a la lenalidomida. También puede utilizarse la monoterapia con bendamustina, especialmente en pacientes con insuficiencia renal o que requieran diálisis [19]. Este último no está aprobado para esta indicación en Suiza.
En dos innovadores ensayos de fase II, la Asociación Suiza para la Investigación Clínica del Cáncer (SAKK) probó la combinación de nelfinavir con VD resp. RD investigado. Esto se basó en las observaciones de que este medicamento contra el VIH puede restaurar la sensibilidad a los dos medicamentos contra el mieloma. En el ensayo SAKK 39/13 se alcanzó una prometedora ORR del 65% en una población muy pretratada y a menudo refractaria al bortezomib y la lenalidomida [20]. Se están planificando más estudios SAKK con combinaciones de nelfinavir.
Outlook
Los datos hasta la fecha sobre los inhibidores de los puntos de control en el mieloma múltiple no son muy prometedores. Por el contrario, tras la aprobación por parte de la FDA de la terapia celular CAR-T para pacientes jóvenes con LLA recidivante o refractaria, esta opción de tratamiento se ha convertido en el centro de interés también para los pacientes con mieloma. Esto se basa en los datos de los ensayos clínicos iniciales en pacientes con mieloma con células BCMA-CAR-T (“antígeno de maduración de células B”) con tasas de remisión en torno al 100% [21–23].
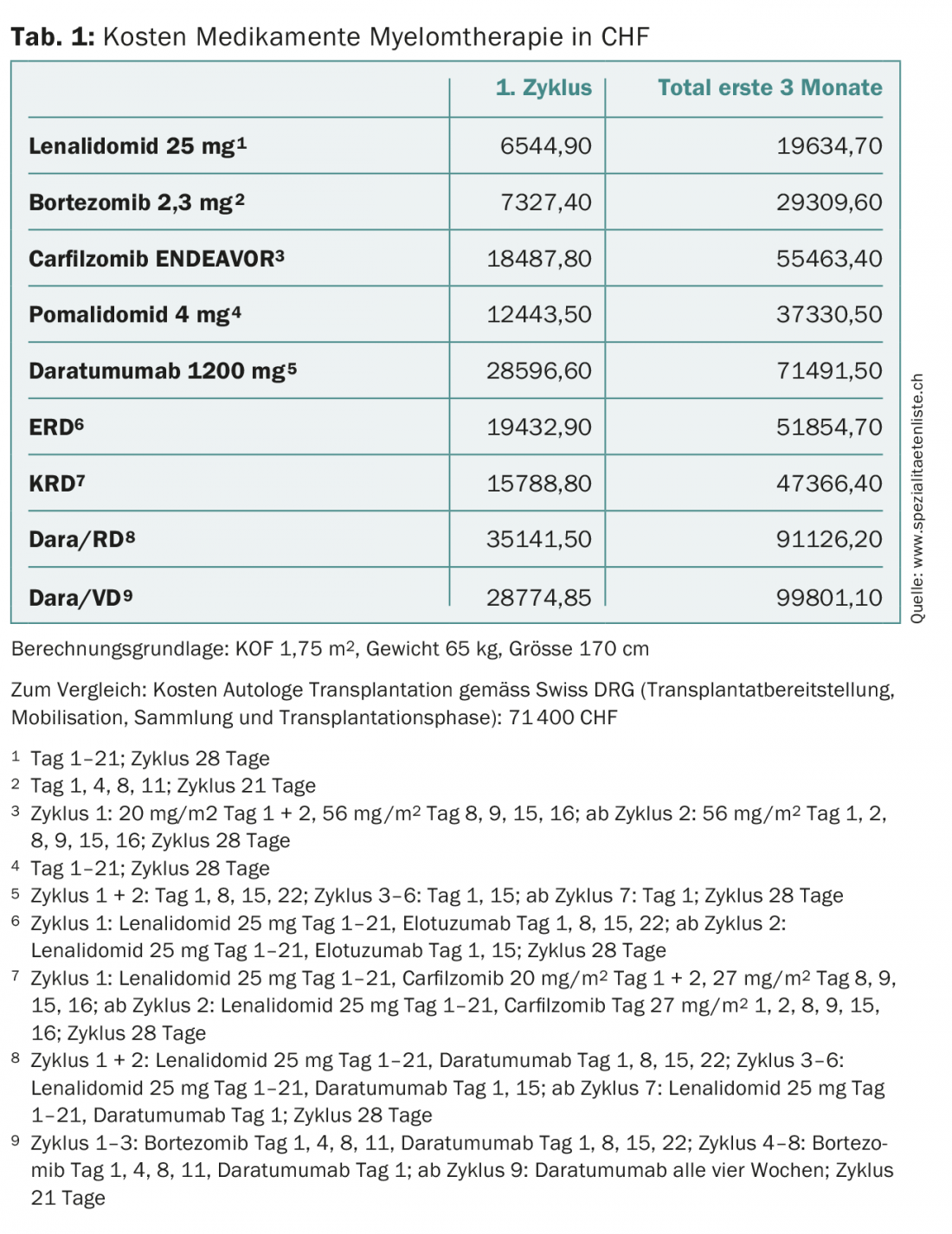
Se han producido avances sin precedentes en la terapia del mieloma. Mientras que el tiempo medio de supervivencia hace 15 años seguía siendo de dos a tres años, hoy en día un buen 40% de los pacientes con mieloma viven diez años o más. Sin embargo, esta mejora también se ha reflejado en los costes del tratamiento (tab. 1) . Esto último debe ser tenido en cuenta por los distintos actores del sistema sanitario, sobre todo porque los nuevos medicamentos, muy caros, avanzarán hacia la primera línea. Siguiendo con el ejemplo del daratumumab, esto también aumentará la presión organizativa, infraestructural y de personal sobre las clínicas y consultas externas oncológicas debido únicamente a la larga duración de la infusión (Tab. 2) . La aplicación subcutánea de este anticuerpo aliviaría el problema [24].
Además de su eficacia, el tratamiento de las enfermedades no curables debe mejorar ante todo la calidad de vida. En el caso de los nuevos fármacos, aún faltan estos datos, o la calidad de vida sólo era un criterio de valoración secundario [25].
En resumen, los pacientes con mieloma disponen hoy en día de una gran variedad de nuevas opciones de tratamiento. Si es posible, se debe incluir a los pacientes en los estudios (por ejemplo, el SAKK). Sería deseable que los protocolos examinaran también cada vez más las secuencias terapéuticas y la calidad de vida.
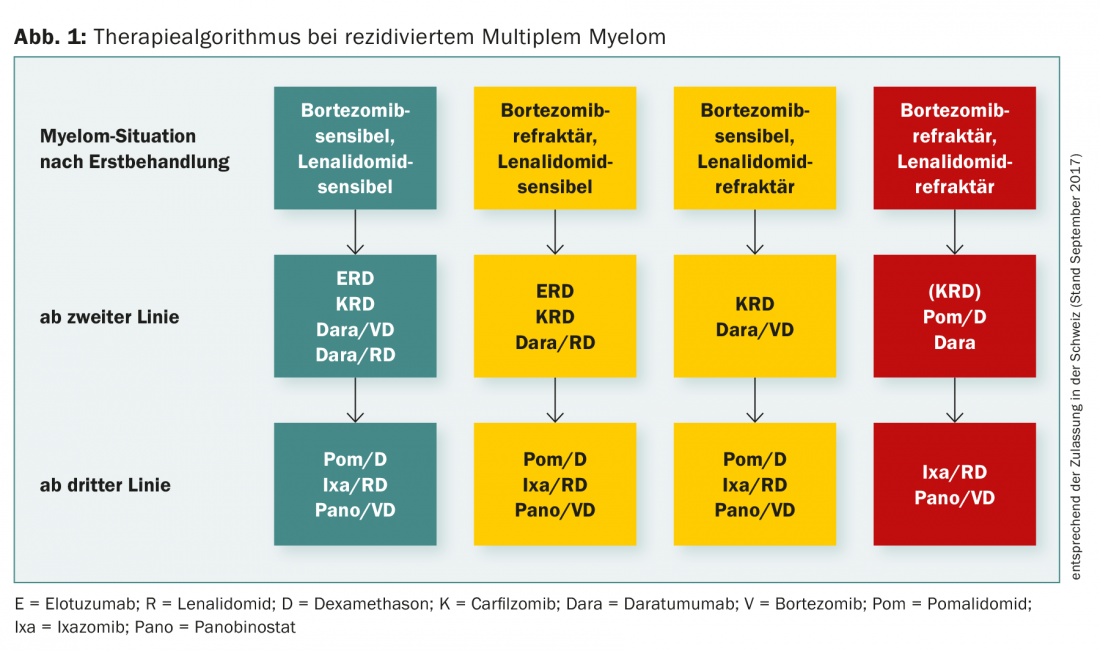
La figura 1 resume el algoritmo de tratamiento del mieloma múltiple recidivante.
Mensajes para llevarse a casa
- La elección de la terapia de recaída depende del tratamiento previo (clase de sustancia, respuesta y tolerancia), la edad, el rendimiento y las comorbilidades de los pacientes, así como de la aprobación de los fármacos.
- Lo habitual en el tratamiento de la recidiva son las combinaciones triples con un inhibidor del proteasoma y/o un IMID, dependiendo del pretratamiento.
- Las terapias con anticuerpos desempeñan un papel importante en el tratamiento del mieloma.
- Los pacientes con mieloma deben ser tratados siempre que sea posible en protocolos (por ejemplo, SAKK).
- La terapia con células T CAR podría convertirse en una opción prometedora en el mieloma.
Literatura:
- Weber DM, et al: Lenalidomida más dexametasona para el mieloma múltiple recidivante en Norteamérica. N Engl J Med 2007; 357(21): 2133-2142.
- Dimopoulos M, et al: Lenalidomida más dexametasona para el mieloma múltiple en recaída o refractario. N Engl J Med 2007; 357(21): 2123-2132.
- Richardson PG, et al: Bortezomib o dosis altas de dexametasona para el mieloma múltiple recidivante. N Engl J Med 2005; 352(24): 2487-2498.
- Grovdal M, et al.: Trasplante autólogo de células madre frente a fármacos novedosos o quimioterapia convencional para pacientes con mieloma múltiple recidivante tras un TACM previo. Trasplante de médula ósea 2015; 50(6): 808-812.
- Giralt S, et al.: American Society of Blood and Marrow Transplantation, European Society of Blood and Marrow Transplantation, Blood and Marrow Transplant Clinical Trials Network, and International Myeloma Working Group Consensus Conference on Salvage Hematopoietic Cell Transplantation in Patients with Relapsed Multiple Myeloma. Biol Trasplante de sangre y médula ósea 2015; 21(12): 2039-2051.
- Dimopoulos MA, et al: Elotuzumab más lenalidomida/dexametasona para el mieloma múltiple en recaída o refractario: seguimiento ELOQUENT-2 y análisis post-hoc sobre la supervivencia libre de progresión y el crecimiento tumoral. Br J Haematol 2017; 178(6): 896-905.
- Lonial S, et al: Terapia con elotuzumab para el mieloma múltiple recidivante o refractario. N Engl J Med 2015; 373(7): 621-631.
- Stewart AK, et al: Carfilzomib, lenalidomida y dexametasona para el mieloma múltiple recidivante. N Engl J Med 2015; 372(2): 142-152.
- Dimopoulos MA, et al: Carfilzomib y dexametasona frente a bortezomib y dexametasona para pacientes con mieloma múltiple en recaída o refractario (ENDEAVOR): un estudio aleatorizado, de fase 3, abierto y multicéntrico. Lancet Oncol 2016; 17(1): 27-38.
- Dimopoulos MA, et al: Seguridad y eficacia de la pomalidomida más dosis bajas de dexametasona en STRATUS (MM-010): un estudio de fase 3b en mieloma múltiple refractario. Sangre 2016; 128(4): 497-503.
- Zander T, et al: La pomalidomida en el punto de mira: ¿menos es más? Leucemia 2017; 31(9): 1987-1989.
- San-Miguel JF, et al: Panobinostat más bortezomib y dexametasona frente a placebo más bortezomib y dexametasona en pacientes con mieloma múltiple en recaída o en recaída y refractario: un ensayo multicéntrico, aleatorizado, doble ciego de fase 3. Lancet Oncol 2014; 15(11): 1195-1206.
- Moreau P, et al: Ixazomib oral, lenalidomida y dexametasona para el mieloma múltiple. N Engl J Med 2016; 374(17): 1621-1634.
- Usmani SZ, et al: Clinical efficacy of daratumumab monotherapy in patients with heavily pretreated relapsed or refractory multiple myeloma. Sangre 2016; 128(1): 37-44.
- Palumbo A, et al: Daratumumab, bortezomib y dexametasona para el mieloma múltiple. N Engl J Med 2016; 375(8): 754-766.
- Dimopoulos MA, et al: Daratumumab, lenalidomida y dexametasona para el mieloma múltiple. N Engl J Med 2016; 375(14): 1319-1331.
- Baz RC, et al: Estudio multicéntrico aleatorizado de fase 2 de pomalidomida, ciclofosfamida y dexametasona en el mieloma refractario recidivante. Sangre 2016; 127(21): 2561-2568.
- Paludo J, et al: Pomalidomida, bortezomib y dexametasona para pacientes con mieloma múltiple en recaída refractario a la lenalidomida. Sangre 2017; 130(10): 1198-1204.
- Hoy SM: Bendamustina: revisión de su uso en el tratamiento de la leucemia linfocítica crónica, el linfoma no Hodgkin indolente refractario al rituximab y el mieloma múltiple. Fármacos 2012; 72(14): 1929-1950.
- Driessen C, et al: The HIV Protease Inhibitor Nelfinavir in Combination with Bortezomib and Dexamethasone (NVd) Has Excellent Activity in Patients with Advanced, Proteasome Inhibitor-Refractory Multiple Myeloma: A Multicenter Phase II Trial (SAKK 39/13). Sangre 2016; 128: Resumen 487.
- Ali SA, et al: Las células T que expresan un receptor quimérico de antígenos de maduración anti-células B provocan remisiones del mieloma múltiple. Sangre 2016; 128(13): 1688-1700.
- Berdeja J, et al: First-in-human multicenter study of bb2121 anti-BCMA CAR T-cell therapy for relapsed/refractory multiple myeloma: Updated results. J Clin Oncol 2017; 35(15 suppl): 3010.
- Fan F, et al: Remisiones duraderas con células T modificadas con receptores de antígenos quiméricos (CAR) específicos de BCMA en pacientes con mieloma múltiple refractario/recidivante. J Clin Oncol 2017; 35(18 suppl): 3001.
- Usmani S, et al: Open-Label, Multicenter, Dose Escalation Phase 1b Study to Assess the Subcutaneous Delivery of Daratumumab in Patients (pts) with Relapsed or Refractory Multiple Myeloma (PAVO). Sangre 2016; 128: Resumen 1149.
- Kvam AK, Waage A: Calidad de vida relacionada con la salud en pacientes con mieloma múltiple: ¿importa? Haematologica 2015; 100(6): 704-705.
InFo ONCOLOGÍA Y HEMATOLOGÍA 2017; 5(5): 16-20