El pronóstico del carcinoma gástrico avanzado sigue siendo extremadamente desfavorable. Por lo tanto, se necesitan urgentemente nuevos enfoques de tratamiento. Los hallazgos actuales sugieren que la terapia con inhibidores de puntos de control podría cobrar más importancia en un futuro próximo.
Hasta ahora, la terapia con inhibidores de puntos de control para el cáncer gástrico sólo se ha aprobado en Suiza para casos muy avanzados. Por ejemplo, la aprobación del nivolumab se limita a la terapia de tercera línea y la del pembrolizumab al tratamiento de tumores metastásicos con alta inestabilidad de microsatélites (MSI-H) o reparación defectuosa de los errores de emparejamiento del ADN (dMMR) sin opciones terapéuticas alternativas [2]. Los resultados de diversos estudios dan ahora motivos para esperar que pronto se amplíen estas indicaciones.
Situación
Hasta ahora, el cáncer gástrico en estadio IV ha sido el dominio de la quimioterapia (Fig. 1) . Aunque la quimioterapia puede mejorar el tiempo de supervivencia en comparación con el tratamiento puramente de apoyo, sólo mejora la supervivencia en unos 6,7 meses [3]. Se puede ganar un mes adicional utilizando combinaciones de quimioterapia, pero éstas también conllevan un aumento de las toxicidades [3]. Las quimioterapias de doblete basadas en platino y una fluoropirimidina son la norma recomendada, el beneficio de las combinaciones triples se evalúa de forma controvertida [4].
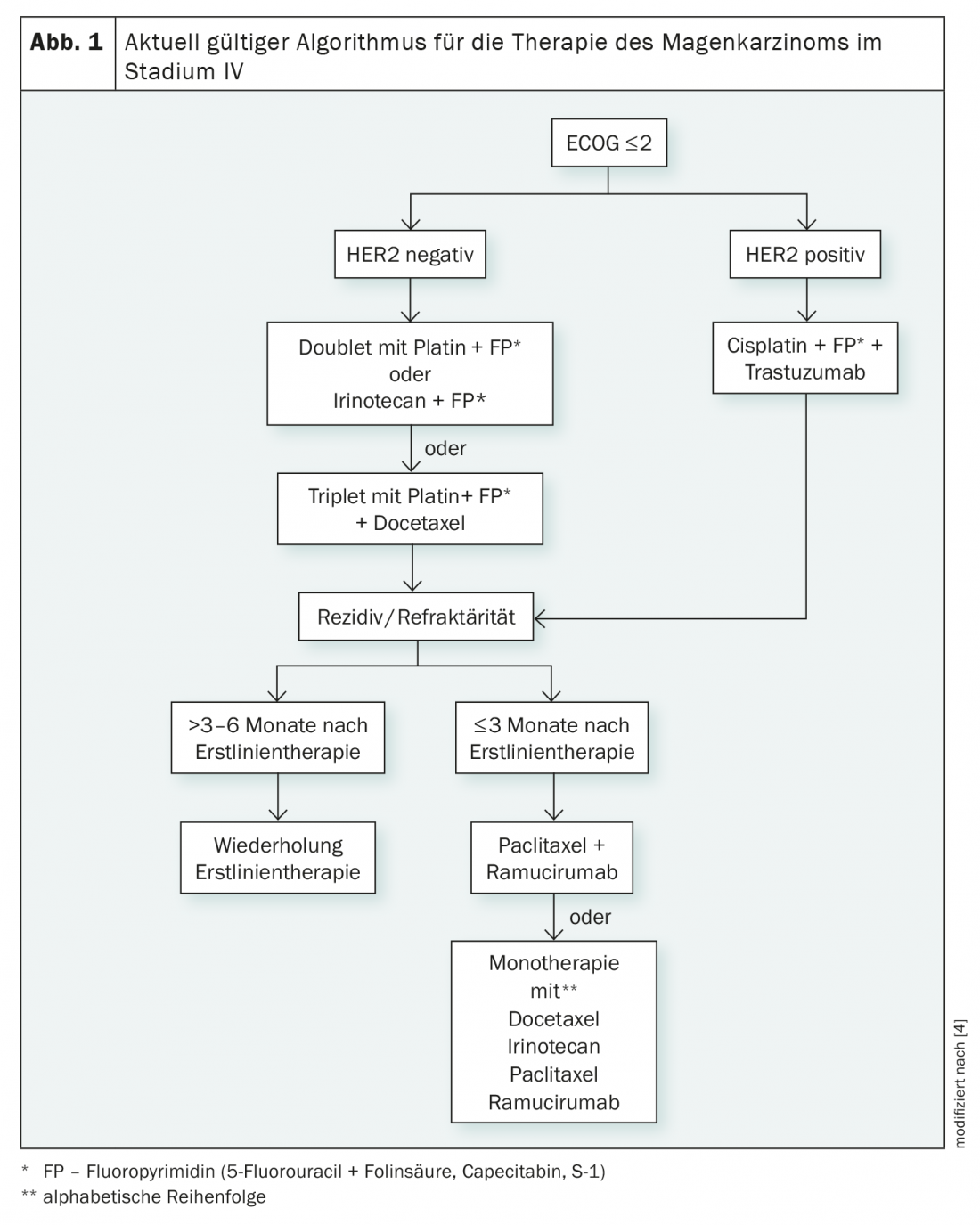
Aunque se dispone de terapias dirigidas para los tumores HER2 positivos, esta opción no existe actualmente para los casos HER2 negativos. La adición de trastuzumab a la quimioterapia conlleva un aumento de la tasa de respuesta y de la supervivencia libre de progresión y global en los tumores HER2 positivos, que representan entre el 10 y el 15% de los cánceres gástricos. El efecto es detectable, con un aumento de la mediana de supervivencia de algo más de dos meses, pero es pequeño [5]. Así que estamos lejos de una cura, independientemente del estado HER2.
Si fracasa la quimioterapia de primera línea con o sin trastuzumab, puede utilizarse el anticuerpo ramucirumab dirigido contra el VEGFR-2 (receptor 2 del factor de crecimiento endotelial vascular). Esto provoca una prolongación de la supervivencia de aproximadamente 1,5 meses en comparación con el placebo [6]. Como alternativa, también es posible la quimioterapia en segunda línea. Sus resultados son comparables a los del tratamiento con ramucirumab. Los mejores resultados se obtienen con combinaciones de paclitaxel y el anticuerpo anti-VEGFR-2 [4].
Con respecto a las demás líneas de terapia, actualmente no existen directrices claras. Las opciones incluyen ramucirumab, quimioterapia, trifluridina/tipiracilo (TAS-102) y varios inhibidores de los puntos de control. Además de mejorar las opciones terapéuticas para el tratamiento de primera y segunda línea del cáncer gástrico en estadio IV, es importante por tanto establecer un estándar terapéutico para la tercera línea en el transcurso de los próximos años.
Los inhibidores de los puntos de control como opción
Los inhibidores de los puntos de control podrían desempeñar pronto un papel de apoyo, no sólo como tratamiento estándar en tercera línea, sino también para complementar las opciones en fases anteriores del tratamiento. Actualmente se están llevando a cabo varios estudios que están probando el uso de nivolumab, pembrolizumab y otros en todas las líneas de terapia (Tab. 1). Los resultados obtenidos hasta ahora indican que el tratamiento con inhibidores de los puntos de control no es, al menos, inferior a la quimioterapia. Por ejemplo, el ensayo KEYNOTE-062 informó de una eficacia comparable del bloqueante de PD-1 pembrolizumab como monoterapia de primera línea, con una tolerabilidad significativamente mejor [7]. Parece importante considerar diferentes subgrupos en el análisis de la eficacia. Con una alta expresión de PD-L1, se observó una clara tendencia hacia una mayor supervivencia global con el tratamiento con pembrolizumab.
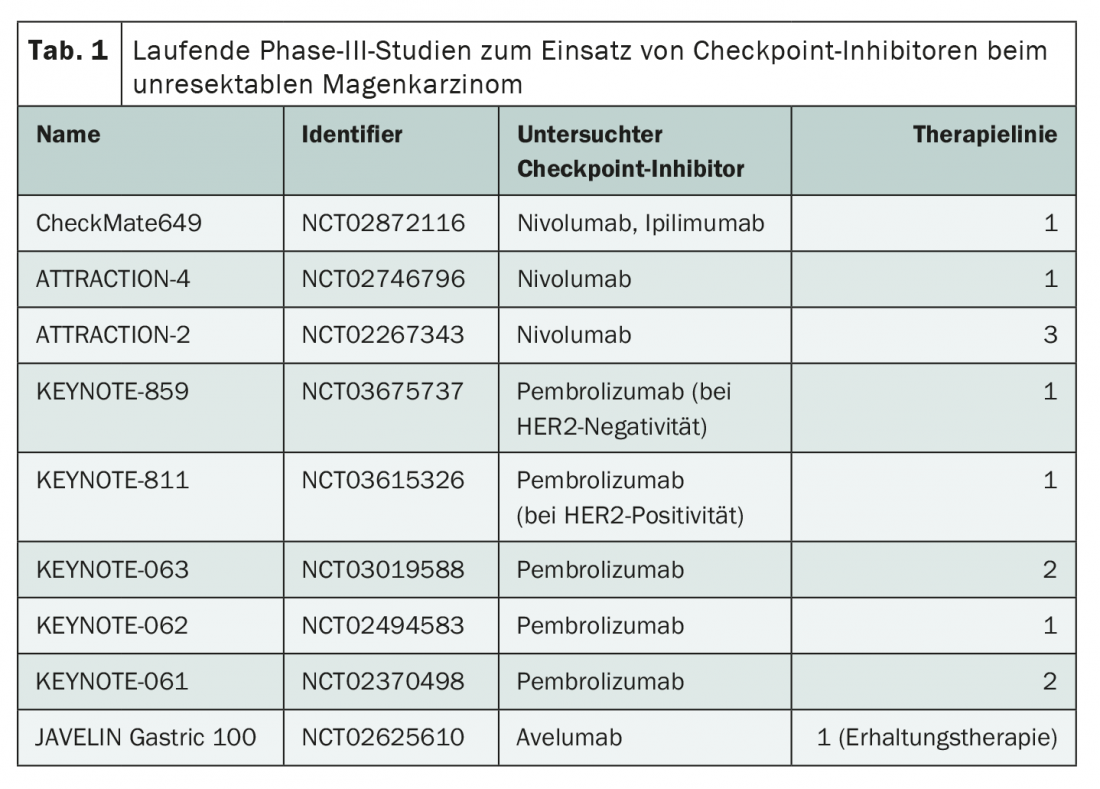
Los resultados de numerosos estudios adicionales sobre el uso de los inhibidores de los puntos de control en la terapia de primera línea están pendientes, pero en varios congresos celebrados en 2020 se aportaron datos interesantes. En el Congreso de la Sociedad Europea de Oncología Médica (ESMO), Markus Moehler presentó los primeros datos prometedores del estudio CheckMate649, que incluye a 1581 pacientes [8]. En comparación con la quimioterapia sola, la expresión de PD-L1 con la adición de nivolumab mostró una mejora significativa en la supervivencia global y la supervivencia libre de progresión. Un efecto menor -también significativo- se dio también en el grupo total.
Además, se presentaron los primeros resultados del ensayo ATTRACTION-4, que también investiga la administración adicional de nivolumab en primera línea, pero en 724 pacientes exclusivamente asiáticos [9]. Narikazu Boku informó de un aumento significativo de la supervivencia libre de progresión y de la tasa de respuesta con la adición de nivolumab a la quimioterapia. Sin embargo, la supervivencia global no se prolongó significativamente según este primer análisis.
Mientras que la administración adicional de inmunoterapéuticos suele investigarse para la terapia de primera línea, la terapia con inhibidores de puntos de control por sí sola también se está debatiendo en líneas posteriores. En el estudio ATTRACTION-2, por ejemplo, ya se observó una mejora significativa del pronóstico con el uso de nivolumab en la terapia de tercera línea. La mediana de supervivencia aumentó de 4,14 a 5,26 meses [10].
Una mirada al futuro
Aunque todavía haya que esperar datos a más largo plazo, el uso de inmunoterapéuticos en el carcinoma gástrico avanzado es una opción válida. Mientras tanto, se están llevando a cabo numerosos estudios de gran envergadura sobre este enfoque, algunos de los cuales ya han dado resultados, y otros son esperanzadores. La administración de inhibidores de los puntos de control podría ser pronto rutinaria en la terapia de primera línea del carcinoma gástrico no resecable, especialmente en los casos de expresión de PD-L1 y como complemento de la quimioterapia estándar. En líneas de tratamiento posteriores, también se está debatiendo el uso exclusivo de inmunoterapéuticos, que ha demostrado ser superior a la administración de placebo. En general, la tolerabilidad parece ser superior a la de la quimioterapia.
La identificación de biomarcadores adecuados facilitaría la selección de los pacientes adecuados para la inmunoterapia. Este tema, que también afecta a numerosas enfermedades más allá del carcinoma gástrico, probablemente nos acompañará durante mucho tiempo. Los candidatos prometedores son actualmente la expresión de PD-L1 en el tumor y el estroma (puntuación de positividad combinada), la asociación con el virus de Epstein-Barr y la inestabilidad de microsatélites [11,12]. Actualmente también se están llevando a cabo varios estudios al respecto.
Aún quedan muchas preguntas por responder, como la aplicación exacta, la selección ideal de pacientes y también la propia eficacia. No obstante, puede que pronto sea imposible imaginar un tratamiento para el carcinoma gástrico sin inmunoterapia, siempre que se amplíe la aprobación. Según los datos disponibles hasta ahora, no cabe esperar un gran avance, pero sí pequeños pasos en la dirección correcta.
Literatura:
- Smyth EC, et al: Cáncer gástrico: Guías de práctica clínica de la ESMO para el diagnóstico, tratamiento y seguimiento. Anales de Oncología. 2016; 27: v38-v49.
- Información sobre medicamentos swissmedic. www.swissmedicinfo.ch (fecha de acceso: 17.01.2021)
- Wagner AD, et al: Quimioterapia para el cáncer gástrico avanzado. Cochrane Database Syst Rev. 2017; 8: CD004064.
- Lordick F, et al.: Onkopedia – Carcinoma gástrico. www.onkopedia.com/de/onkopedia/guidelines/magenkarzinom (fecha de acceso: 17.01.2021)
- Bang YJ, et al: Trastuzumab en combinación con quimioterapia frente a quimioterapia sola para el tratamiento del cáncer gástrico o de la unión gastroesofágica avanzado HER2-positivo (ToGA): un ensayo de fase 3, abierto, aleatorizado y controlado. Lancet. 2010; 376(9742): 687-697.
- Fuchs CS, et al: Monoterapia con ramucirumab para el adenocarcinoma gástrico o de la unión gastroesofágica avanzado previamente tratado (REGARD): un ensayo internacional, aleatorizado, multicéntrico, controlado con placebo, de fase 3. Lancet. 2014; 383(9911): 31-39.
- Shitara K, et al: Eficacia y seguridad de pembrolizumab o pembrolizumab más quimioterapia frente a quimioterapia sola para pacientes con cáncer gástrico avanzado de primera línea: el ensayo clínico aleatorizado de fase 3 KEYNOTE-062. JAMA Oncol. 2020; 6(10): 1571-80.
- Moehler M, et al.: Nivolumab (nivo) más quimioterapia (quimio) frente a quimioterapia como tratamiento de primera línea (1L) para el cáncer gástrico avanzado/cáncer de la unión gastroesofágica (CG/CJGE)/adenocarcinoma esofágico (CAE): Primeros resultados del estudio CheckMate 649. Anales de Oncología. 2020; 31: S1142-1215.
- Boku N, et al: Nivolumab más quimioterapia frente a quimioterapia sola en pacientes con cáncer gástrico/de la unión gastroesofágica (G/GEJ) avanzado o recurrente no tratado previamente: estudio ATTRACTION-4 (ONO-4538-37). Anales de Oncología. 2020; 31: S1142-1215.
- Chen L-T, et al: A phase 3 study of nivolumab in previously treated advanced gastric or gastroesophageal junction cancer (ATTRACTION-2): 2-year update data. Cáncer gástrico: revista oficial de la Asociación Internacional de Cáncer Gástrico y de la Asociación Japonesa de Cáncer Gástrico. 2020; 23(3): 510-519.
- Shitara K, et al: Pembrolizumab frente a paclitaxel para el cáncer gástrico o de la unión gastroesofágica avanzado previamente tratado (KEYNOTE-061): ensayo aleatorizado, abierto, controlado, de fase 3. Lancet. 2018; 392(10142): 123-133.
- Kim ST, et al: Caracterización molecular exhaustiva de las respuestas clínicas a la inhibición de PD-1 en el cáncer gástrico metastásico. Nat Med. 2018; 24(9): 1449-1458.
- ClinicalTrials.gov. www.clinicaltrials.gov (fecha de acceso: 17.01.2021)
InFo ONCOLOGÍA Y HEMATOLOGÍA 2021; 9(1): 18-19