L’ostéoporose est un vaste problème de santé, mais il existe aujourd’hui de nombreuses options préventives et thérapeutiques. Pour une prévention et un traitement adaptés aux patients, le dépistage précoce et la stratification des risques sont des conditions préalables importantes. L’Association suisse contre l’ostéoporose a mis à jour en 2020 ses recommandations en matière de prévention, de diagnostic et de traitement.
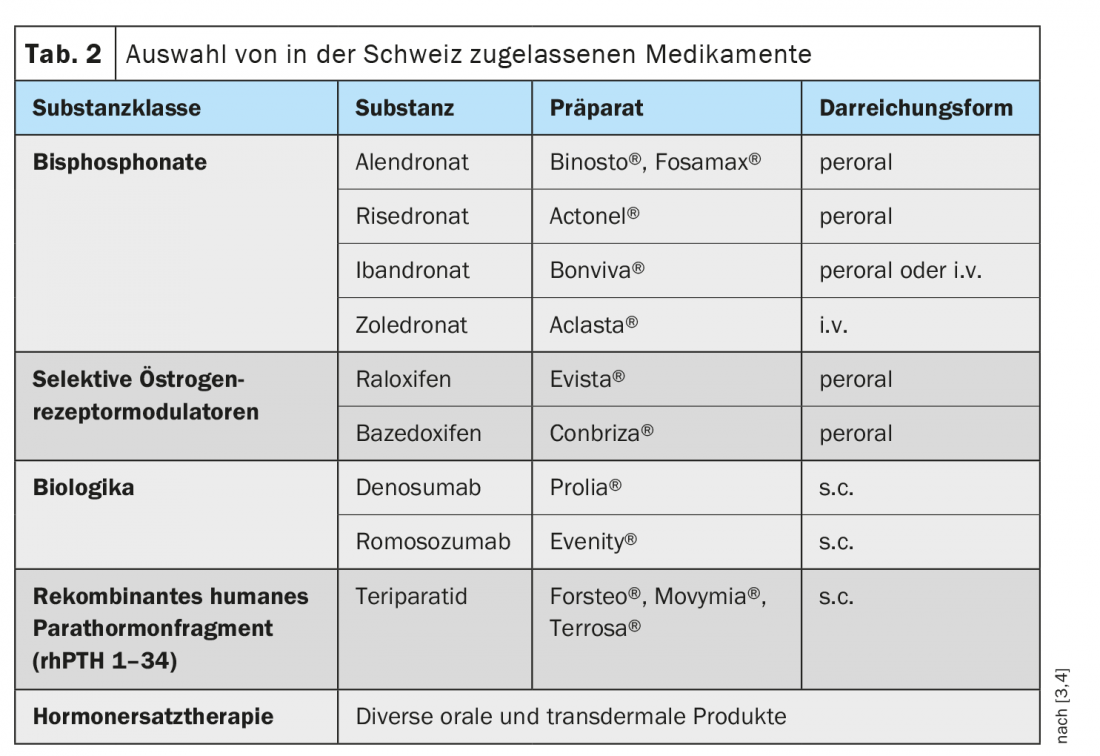
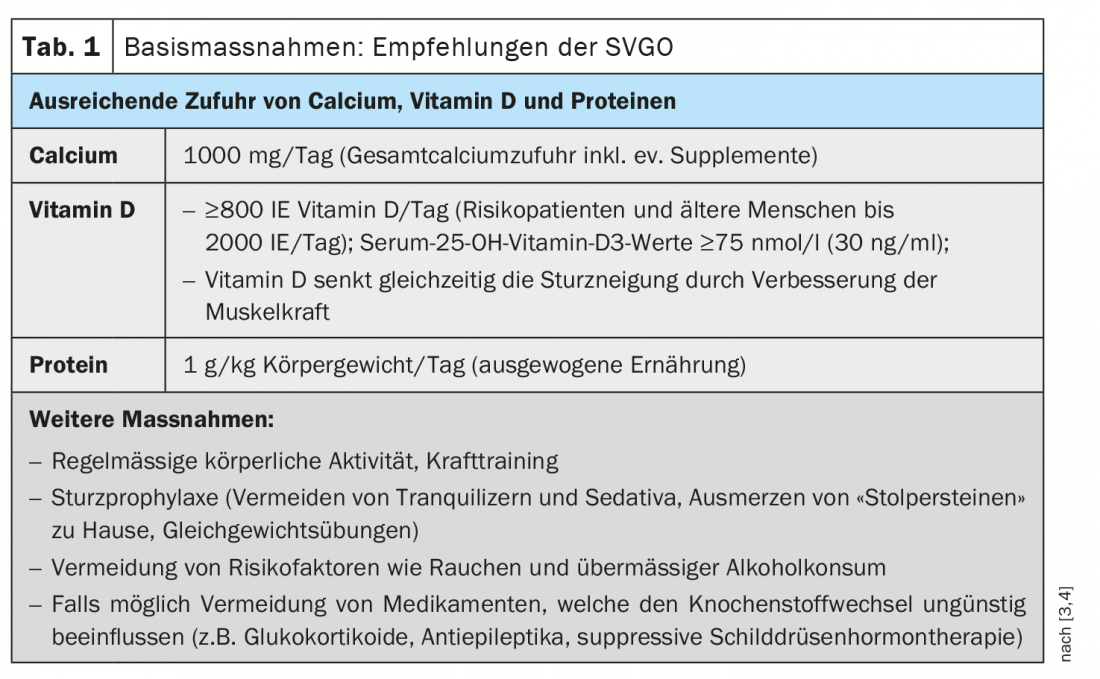
La plupart des cas d’ostéoporose se manifestent après l’âge de 45 ans pour les femmes et 55 ans pour les hommes [1]. Les formes secondaires ou idiopathiques d’ostéoporose chez les personnes plus jeunes sont rares. Le fait que les femmes soient plus de deux fois plus touchées par l’ostéoporose que les hommes est principalement dû aux changements hormonaux après la ménopause, les données épidémiologiques montrant une augmentation de la prévalence corrélée à l’âge, de 15% chez les 50-60 ans à 45% chez les plus de 70 ans [2]. Plus l’ostéoporose est détectée tôt, meilleures sont les possibilités de traitement. Outre le calcium et la vitamine D (tab. 1), il existe aujourd’hui de nombreux médicaments contre l’ostéoporose très efficaces qui, grâce à leurs substances actives, peuvent freiner la perte osseuse excessive et/ou favoriser la formation osseuse de manière ciblée (tab. 2).
La stratification des risques, une base importante pour le traitement
Dans ses recommandations mises à jour en 2020, l’Association suisse contre l’ostéoporose (ASCO) aborde la stratification du risque et, sur cette base, le traitement adapté au risque [3,4]. Le score FRAX est actuellement le meilleur outil validé pour évaluer les facteurs de risque, applicable aux hommes et aux femmes de plus de 45 ans. Il y a également quelques restrictions, comme le fait qu’il ne peut être utilisé que chez les patients non traités (exception : administration de calcium et de vitamine D) et que la colonne vertébrale n’est pas évaluée. La densitométrie osseuse permet de confirmer le diagnostic d’ostéoporose. FRAX et la densitométrie (DXA) sont des mesures diagnostiques complémentaires. Et même si la carence en œstrogènes est la cause la plus probable de l’ostéoporose ou d’un risque accru de fracture chez les femmes, le diagnostic différentiel doit exclure d’autres causes.
Antécédents et FRAX : l’algorithme FRAX (WHO Fracture Risk Assessment) permet d’estimer le risque absolu à 10 ans de fractures graves de la hanche, de la colonne vertébrale, de l’avant-bras ou de l’humérus proximal [5,6]. L’évaluation du score FRAX est basée sur différents facteurs de risque. Outre l’âge et le sexe, cela inclut un IMC <20, une fracture après l’âge de 40 ans (sauf mains, pieds, crâne) et une fracture du col du fémur chez un parent. Par ailleurs, la polyarthrite rhumatoïde et le traitement par glucocorticoïdes oraux, actuel ou passé, pendant une période d’au moins 3 mois par jour (≥5 mg d’équivalent prednisolone) constituent des facteurs de risque. En ce qui concerne les facteurs liés au mode de vie, le tabagisme et la consommation d’alcool de plus de trois unités par jour sont mentionnés.
Densitométrie par absorptiométrie Dual-X-ray (DXA) : cette technique d’imagerie doit être utilisée lorsque des facteurs de risque cliniques indiquent un risque accru d’ostéoporose. Une mesure DXA est effectuée sur la colonne lombaire (moyenne des vertèbres évaluables L1-L4), sur le fémur total et sur le col du fémur (mesure unique ou moyenne des fémurs gauche et droit). Pour estimer le risque de fracture à 10 ans, la valeur la plus basse de la colonne lombaire, du col du fémur et du fémur total est déterminante. Le résultat de la mesure DXA est exprimé sous forme de T-score et indique, sous forme d’écarts-types, l’importance des écarts entre la densité osseuse mesurée et la densité osseuse de jeunes adultes en bonne santé. Si la valeur est comprise entre -1 et -2,5, il s’agit d’un précurseur de l’ostéoporose, si elle est inférieure à -2,5, il s’agit d’une ostéoporose [7].
Nouvelle classification du groupe de risque de fracture : on distingue depuis peu les cinq groupes de risque de fracture suivants :
1.
Risque immédiat de fracture (imminent), c.-à-d. >10% de risque de fracture dans les 2 ans à venir :
Âge supérieur à 65 ans et fracture ostéoporotique (vertèbres, hanche, humérus, radius, bassin) au cours des 2 dernières années.
2.
Risque de fracture très élevé :
Le risque de fracture à 10 ans pour une fracture ostéoporotique (corps vertébral, hanche, humérus, radius, bassin) selon FRAX est supérieur d’au moins 20% au seuil d’intervention.
3.
Risque élevé de fracture :
Fracture ostéoporotique (corps vertébral, hanche, humérus, radius, bassin) il y a plus de 2 ans et/ou le risque de fracture à 10 ans pour une fracture ostéoporotique (corps vertébral, hanche, humérus, radius, bassin) selon FRAX est plus élevé que le seuil d’intervention, mais moins de 20% au-dessus. Ce groupe comprend également les personnes sous traitement continu de glucocorticoïdes, d’inhibiteurs de l’aromatase (femme) ou de suppresseurs d’androgènes (homme), dont la valeur DXA-T <est de 1,5 et/ou dont le risque de fracture ostéoporotique à 10 ans (corps vertébral, hanche, humérus, radius, bassin) selon FRAX est supérieur au seuil d’intervention.
4.
Risque modéré de fracture :
Valeur DXA-T ≤ -2,5 et pas de fractures antérieures et risque de fracture à 10 ans pour une fracture ostéoporotique (corps vertébral, hanche, humérus, radius, bassin) selon FRAX inférieur au seuil d’intervention.
5.
Faible risque de fracture :
Ostéopénie et aucun autre facteur de risque
Les mesures thérapeutiques sont basées sur le risque de fracture
La stratégie de traitement appropriée est déterminée en fonction du groupe à risque de fracture, à condition que les autres causes d’ostéoporose ou de risque accru de fracture aient été exclues. La mise en œuvre des mesures de base (tableau 1) est recommandée pour chaque groupe de risque. Différentes classes de substances sont disponibles pour le traitement spécifique (tab. 2). Les recommandations de l’ASGO proposent la procédure suivante, en soulignant qu’il faut tenir compte des contre-indications respectives.
Risque de fracture très élevé/immédiat en cas d’état post-fracture vertébrale :
Tériparatide pendant 18 à 24 mois, suivi d’un traitement d’entretien par bisphosphonates ou dénosumab.
Risque de fracture très élevé/immédiat après une fracture de la hanche : Bisphosphonate zolédronate (alternative : denosumab)
Risque très élevé/immédiat de fracture après une fracture ostéoporotique des vertèbres, de la hanche, de l’humérus, du radius ou du bassin :
Romosozumab pendant un an (à réserver en cas de risque cardiovasculaire élevé), suivi de bisphosphonates ou de dénosumab.
Risque élevé de fracture :
Bisphosphonates ou dénosumab (alternative : tériparatide en cas d’état après fracture vertébrale ou valeur T <-3,5 DS à la colonne vertébrale)
Risque modéré :
Traitement hormonal substitutif, modulateurs sélectifs des récepteurs aux œstrogènes, éventuellement bisphosphonates oraux si les marqueurs du métabolisme osseux (CTX, PINP) se situent au-dessus de la plage de référence préménopausique
Faible risque : éventuellement traitement hormonal substitutif (THS) en cas de syndrome climatérique.
Le suivi est un facteur très important. Un contrôle de l’évolution par densitométrie/DXA doit être effectué tous les 2 ans, sauf pour les groupes à faible risque (DXA seulement après 5-10 ans).
Comment éviter les effets de rebond ?
Le dénosumab (Prolia®) et le romosozumab (Evenity®) sont tous deux des agents biologiques ostéologiques très efficaces (ostéologues), mais ils peuvent entraîner une perte de la masse osseuse acquise après l’arrêt du traitement, ce que l’on appelle un effet “rebond” [8,9]. Après l’arrêt de Prolia® , il est recommandé d’utiliser des bisphosphonates tels que le zolédronate (p. ex. Aclasta®) ou l’alendronate (p. ex. Fosamax®) comme traitement de suivi [11]. Selon les connaissances actuelles, le moyen le plus efficace de contrer un rebond est le zolédronate (Aclasta®) i.v. 5 mg 1× par an, première administration 6 mois après la dernière application de Prolia® ; l’aledronate peut également être utilisé [8,10]. Pour contrôler le suivi, les marqueurs de remodelage osseux doivent être mesurés tous les trois à six mois [11]. Il faut éviter de passer directement de Prolia® à un traitement ostéoanabolique tel que le tériparatide (par exemple Forsteo®), car cela augmente l’effet de rebond [8]. L’association de Prolia® et de Forsteo® a un effet additif, mais la combinaison de biphosphonates et de Prolia® n’est pas recommandée [8,12].
Le romosozumab (Evenity®) est autorisé en Suisse depuis 2020 pour le traitement de l’ostéoporose sévère chez les femmes qui présentent un risque nettement accru de fractures après la ménopause [9]. L’application se fait 1× par mois, la durée maximale du traitement est de 12 mois, ensuite un traitement par biphosphonates est nécessaire. Les contre-indications au traitement par romosozumab sont les antécédents d’accident vasculaire cérébral ou d’infarctus du myocarde [8].
Littérature :
- OsteoSwiss, www.osteoswiss.ch (dernière consultation 16.03.2021)
- Gourlay ML, et al : Bone-density testing interval and transition to osteoporosis in older women. N Engl J Med 2012 ; 19 ; 366(3) : 225-233.
- Ferrari S, Lippuner K, Lamy O, Meier C : 2020 recommandations pour le traitement de l’ostéoporose en fonction du risque de fracture de l’Association suisse contre l’ostéoporose (ASCO). Swiss Med Wkly 2020, 150:w20352
- Stute P, Meier C : Mise à jour sur l’ostéoporose. J Gynéco Endocrino 2021, https://doi.org/10.1007/s41975-021-00181-4
- FRAX® Outil d’évaluation des risques de fracture, www.shef.ac.uk/FRAX (dernière consultation 16/03/2021)
- Kanis JA, et al : Évaluation du risque de fracture. Osteoporos Int 2005 ; 16(6) : 581-589.
- “Ostéoporose : dépister précocement la perte osseuse”, 17.10.2020, https://nachrichten.idw-online.de, (dernière consultation 16.03.2021)
- Mollet S : Ostéoporose – une mise à jour, Dr. med. Stella Mollet, Forum de formation médicale continue, 26.06.2020.
- Swissmedic : Information sur les médicaments, www.swissmedicinfo.ch (dernière consultation 16.03.2021)
- Anastasilakis AD, et al : Zoledronate for the Prevention of Bone Loss in Women Discontinuing Denosumab Treatment. Un essai clinique prospectif de 2 ans. J Bone Miner Res 2019 ; 34(12) : 2220-2228.
- “Prolia® et Evenity® : comment éviter le rebond ?”, 28.01.2021, www.rheumaliga.ch/blog/2021/prolia-evenity-rebound-effekt
- Leder BZ, et al : Response to Therapy With Teriparatide, Denosumab, or Both in Postmenopausal Women in the DATA (Denosumab and Teriparatide Administration) Study Randomized Controlled Trial. J Clin Densitom 2016 ; 19(3) : 346-351.
PRATIQUE DU MÉDECIN DE FAMILLE 2021 ; 16(4) : 22-23