Les traitements de l’ostéoporose ont prouvé leur efficacité dans la réduction du risque de fracture vertébrale et non vertébrale. Idéalement, ils sont utilisés dans le cadre d’un traitement multimodal et adaptés aux caractéristiques individuelles des patients. Compte tenu de la nécessité d’un traitement à long terme, une attention particulière doit être accordée à la gestion des effets de rebond et des effets secondaires. Aujourd’hui, il est proposé de prendre des vacances thérapeutiques (“drug holidays”) après quelques années.
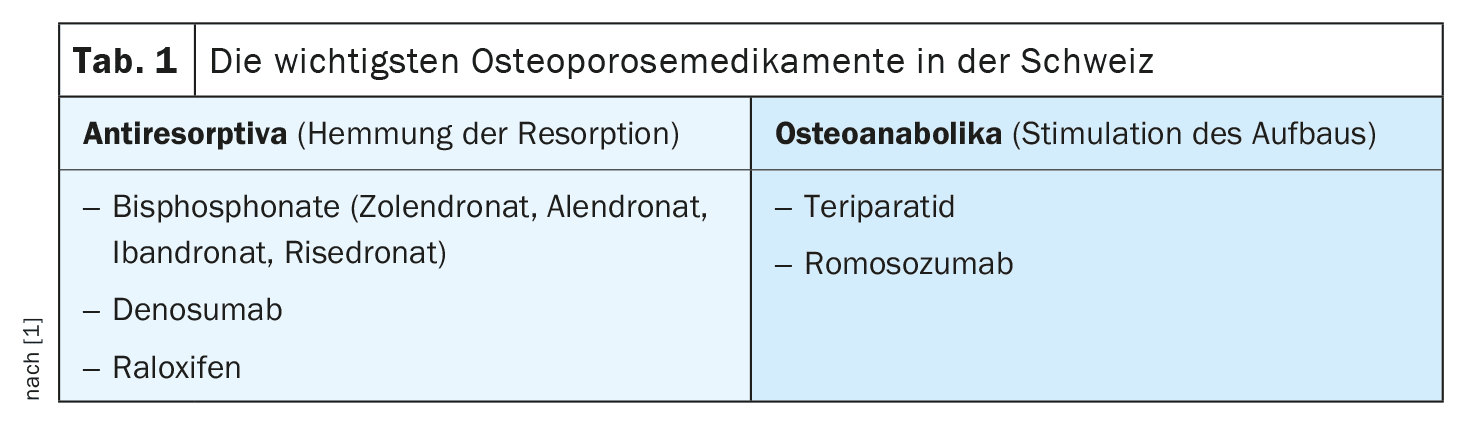
Le Dr Adrian Forster, médecin-chef de la clinique Schulthess à Zurich, et le Dr Regula Capaul, médecin généraliste en cabinet privé à Zurich-Oerlikon, ont donné un aperçu pratique de la complexité du traitement de l’ostéoporose [1]. Aujourd’hui, environ 20% des femmes et 7% des hommes de plus de 50 ans souffrent d’ostéoporose [2]. Pour la Suisse, cela représente actuellement plus de 400 000 personnes atteintes. L’ostéoporose se caractérise par une perturbation du remodelage de la substance osseuse et une microarchitecture pathologique des os qui en résulte. La diminution de la densité osseuse entraîne un risque accru de fracture. La perte osseuse touche principalement les personnes âgées et les femmes ménopausées. Une carence en œstrogènes, un poids insuffisant et un manque d’activité physique favorisent l’apparition de l’ostéoporose. Il existe également d’autres facteurs de risque. En Suisse, les principaux groupes de médicaments utilisés pour traiter l’ostéoporose sont les antirésorptifs (bisphosphonates, dénosumab, raloxifène) et les ostéoanabolisants (tériparatide, romosozumab) (tableau 1) [1]. Tous ces traitements de l’ostéoporose peuvent réduire la perte de masse osseuse et diminuer le risque de fracture, mais à des degrés divers [3].
Sélection d’un bisphosphonate adapté à chaque patient
Le traitement par bisphosphonates a un bénéfice démontré pour un traitement à long terme de 3 à 5 ans [3]. Selon le Dr Forster, le zolendronate est actuellement la substance la plus puissante et la plus affinée sur le plan osseux [1]. Il existe des preuves d’effets positifs de cette substance en termes de réduction du risque de fracture vertébrale et non vertébrale [3]. Toutefois, l’orateur a indiqué que les effets secondaires sous forme de paresthésies grippales étaient relativement fréquents dans les premiers jours suivant l’injection de zolendronate [1]. Celles-ci disparaissent toutefois généralement en quelques jours. Une stratégie pour réduire le risque d’effets secondaires consiste à perfuser le zolendronate plutôt lentement. Pour certains patients, il faut compter une heure entière. Le Dr Forster a également conseillé d’administrer au préalable un anti-inflammatoire non stéroïdien ou un analgésique à base de paracétamol [1]. Avant une perfusion de zolendronate, les patients doivent également être suffisamment hydratés, car les bisphosphonates sont en grande partie éliminés par les reins. Le conférencier a recommandé de n’utiliser le zolendronate que chez les patients ayant un DFGe >35 ml/min/1,73m2.
L’alendronate peut être envisagé comme alternative au zolendronate, comme dans l’étude de cas (encadré) . L’ibronate est utilisé avec réserve, car il a moins d’affinité pour les os que le zolendronate et l’alendronate, et il n’existe que des données sur la réduction du risque de fracture vertébrale, mais pas du risque de fracture périphérique, a déclaré le conférencier [1].
Le Dr Forster [1] a également déclaré : “Il faut toujours corriger une carence en vitamine D avant d’administrer un bisphosphonate”. Ceci afin de permettre une reminéralisation adéquate de l’os [1]. La vitamine D est connue pour favoriser le dépôt de calcium dans les os ; une supplémentation en vitamine D est facile à mettre en œuvre et peu coûteuse.
| Étude de cas : Fracture de fragilité de la colonne vertébrale |
| Le Dr Capaul a rapporté le cas d’une patiente de 56 ans qui est tombée au travail sur un sol glissant et s’est fracturée la 12e vertèbre thoracique (fracture par enfoncement du plateau). L’orthopédiste traitant a prescrit un traitement conservateur avec un corset à 3 points ainsi que du repos physique, un traitement analgésique concomitant et des contrôles radiologiques de l’évolution. La patiente a été adressée à l’intervenante pour un examen d’ostéoporose par un médecin généraliste. Les antécédents familiaux ont révélé que la sœur de la patiente souffrait d’ostéoporose. La mesure de la DEXA a révélé une ostéoporose au niveau de la colonne lombaire et une ostéopénie dans les autres cas. L’intervenante a décidé d’initier un traitement par bisphosphonates. Au moment de la première perfusion de zolendronate, trois mois s’étaient écoulés depuis la chute. Lors de la consultation de suivi chez le médecin généraliste six mois plus tard, la patiente a indiqué qu’elle ne souhaitait pas recevoir de nouvelle perfusion de zolendronate en raison des effets secondaires dans les jours suivant la perfusion (troubles du sommeil, sensation de tension au niveau de la tête). Après avoir consulté un spécialiste en rhumatologie, l’intervenante a décidé d’opter pour l’alendronate (comprimé, 1× par semaine) comme alternative, car celui-ci présente également de bonnes données concernant la prévention des fractures vertébrales. L’alendronate s’est avéré bien toléré chez cette patiente et une mesure de la DEXA après 2 ans a montré qu’il n’y avait plus d’ostéoporose dans la colonne lombaire. |
| d’après [1] |
Mesures indispensables après l’arrêt du dénosumab
Le dénosumab a un bénéfice démontré jusqu’à 3 ans [3]. L’arrêt du traitement par dénosumab entraîne une inversion complète et rapide des effets spécifiques sur l’os. Par conséquent, après l’arrêt, d’autres mesures doivent être utilisées temporairement pour maintenir la densité osseuse (tableau 2). Ce n’est qu’en 2016 environ que l’on s’est rendu compte qu’il fallait obligatoirement administrer un bisphosphonate après l’arrêt du dénosumab, explique le Dr Forster [1]. Le mieux est de donner du zolendronate au moment de l’injection de dénosumab. Il est ensuite utile de mesurer les paramètres de transformation à jeun à 3 et 6 mois. S’ils augmentent jusqu’au tiers supérieur de la norme préménopausique, il faut immédiatement administrer une deuxième perfusion. “Ce n’est que lorsque l’on constate que les paramètres métaboliques restent bas que l’on est en terrain sûr”, a expliqué l’orateur [1]. Ce n’est qu’à ce moment-là qu’une pause thérapeutique peut être envisagée. Si l’on ne détermine pas les paramètres de remodelage, on peut simplement donner du zolendronate 6 et 12 mois après la dernière injection de dénosumab [1,5]. “Il faut deux perfusions”, a souligné le Dr Forster [1]. Auparavant, on pensait qu’une seule perfusion suffisait. Il y a même des patients chez qui trois perfusions sont nécessaires pour supprimer de manière adéquate les paramètres de remodelage. Si le zolendronate n’est pas souhaité ou pas toléré, on peut utiliser l’alendronate comme alternative. Selon le Dr Forster, si l’on suspend le traitement par dénosumab sans administrer ensuite un bisphosphonate, les patients perdent pratiquement tout ce qu’ils ont gagné au niveau de la colonne vertébrale en l’espace de 12 mois [1].
Les nécroses de la mâchoire et les fractures atypiques sont-elles évitables ?
“On peut éviter les nécroses de la mâchoire et les fractures atypiques, mais c’est relativement laborieux”, a reconnu le Dr Forster [1]. En cas d’ostéoporose légère, le conférencier a recommandé de faire une pause thérapeutique pouvant aller jusqu’à 5 ans après une durée de traitement de 3 à 5 ans. En cas d’ostéoporose sévère (T-score bas, fracture de fragilité subie ou fracture vertébrale morphométrique), une pause plus courte, jusqu’à 2 ans, peut être envisagée. Il est important de surveiller les patients pendant l’interruption du traitement, c’est-à-dire d’effectuer des mesures de la densité osseuse à intervalles réguliers et de suivre le remodelage osseux en laboratoire. En fonction de ces résultats, l’interruption du traitement peut être poursuivie ou une reprise du traitement peut être envisagée (encadré). Chez les patients souffrant de nécrose de la mâchoire, des contrôles dentaires réguliers sont une mesure importante.
Congrès : Congrès du CMPR à Lucerne
Littérature :
- “Ostéoporose”, séminaire A1, Dr Adrian Forster et Dr Regula Capaul, Congrès du CMPR Lucerne, 20.06.2024.
- Ligue suisse contre le rhumatisme : Ostéoporose, brochure, 14e édition, 2022, www.rheumaliga.ch,(dernière consultation 04.07.2024).
- Obermayer-Pietsch B, Fössl I, Dimai HP : Concepts thérapeutiques à long terme pour l’ostéoporose [Long-term treatment concepts for osteoporosis]. Internist (Berl) 2021 ; 62(5) : 474-485.
- McClung M, et al : Bisphosphonate therapy for osteoporosis : benefits, risks, and drug holiday. Am J Med 2013 ; 126(1) : 13-20.
- Tsourdi E, et al : Fracture risk and management of discontinuation of denosumab therapy : a systematic review and position statement by ECTS. J Clin Endocrinol Metab 2020 Oct 26 : dgaa756.
HAUSARZT PRAXIS 2024 ; 19(8) : 44-45 (publié le 23.8.24, ahead of print)