Lorsque les patients asthmatiques utilisent un corticostéroïde inhalé (CSI) à haute dose et sur une longue période, que l’association supplémentaire avec un β2-agoniste de longue durée d’action (LABA) ne donne pas les résultats escomptés et qu’ils ne sont toujours pas suffisamment contrôlés, même avec l’ajout d’un β2-agoniste de courte durée d’action (SABA), nous nous rapprochons alors, sur le plan thérapeutique, de la fin du schéma progressif défini par les lignes directrices du GINA pour le traitement de l’asthme bronchique. L’étape suivante peut alors consister à envisager un traitement par anticorps. Mais quel médicament biologique convient à quel patient ?
Le Dr Stephanie Korn, de la clinique thoracique de Heidelberg (Allemagne) et médecin-chef du service ambulatoire d’asthme de cette clinique, a conseillé d’envisager l’utilisation de médicaments biologiques avant que le patient ne soit traité de manière permanente par la cortisone systémique [1]. Il existe aujourd’hui plusieurs anticorps qui sont utilisés depuis longtemps. Pour déterminer quel médicament est le plus approprié pour quel patient, elle prend en compte les caractéristiques du patient, les biomarqueurs et les comorbidités dans le processus décisionnel.
Biomarqueurs
Lorsque les IgE, en tant qu’anticorps antiallergique, sont responsables d’un asthme sévère, l’utilisation de l’omalizumab, un anticorps anti-IgE, peut réduire le nombre d’IgE libres, améliorant ainsi l’asthme. Chez les patients chez qui les cytokines interleukine (IL)-4 et -13 jouent un rôle, il est possible d’obtenir des résultats avec l’antagoniste des récepteurs anti-IL-4, le dupilumab (Anti-IL-4Rα), car il bloque les voies médiées par l’IL-4/13. Les patients qui ont beaucoup d’éosinophiles dans le sang périphérique peuvent être traités efficacement avec un anticorps contre l’interleukine-5 (mépolizumab, reslizumab) , car l’IL-5 recrute les éosinophiles. De plus, le benralizumab, qui se fixe sur le récepteur de l’IL-5 (anti-IL-5Rα), détruit complètement les éosinophiles et les patients ne les présentent plus du tout.
Les éosinophiles, les IgE et le FeNO sont les trois biomarqueurs qui sont généralement dosés chez tous les patients. Cela ne signifie pas qu’un patient doit être traité uniquement en fonction des biomarqueurs, a averti l’experte : “Si les IgE sont élevées, il ne recevra pas automatiquement des anti-IgE – mais le biomarqueur s’ajoute à l’image globale comme une pièce du puzzle”. Les biomarqueurs sont donc utiles comme point de départ pour le diagnostic : si un patient a un FeNO supérieur à 25 et des éosinophiles supérieurs à 150, ce sont les meilleures conditions pour une réponse au dupilumab, a cité le Dr Korn en exemple. Cela ne signifie pas pour autant que les patients présentant d’autres valeurs de biomarqueurs ne répondent pas.
Pour déterminer quel médicament biologique un médecin devrait utiliser chez son patient, le Dr Korn a fait référence à un algorithme développé par Brusselle et Koppelman [2]. (Fig.1). “C’est une idée de la manière dont vous pouvez procéder pour finalement aboutir à un anticorps avec lequel vous ne vous trompez certainement pas”. Cependant, l’algorithme indique également que la plupart du temps, il reste toujours deux, voire trois options. A la fin de la journée, il reste donc toujours une décision résiduelle au médecin traitant. Pour faciliter cette décision, le Dr Korn a évoqué les caractéristiques individuelles des patients, qui ne doivent jamais être négligées.
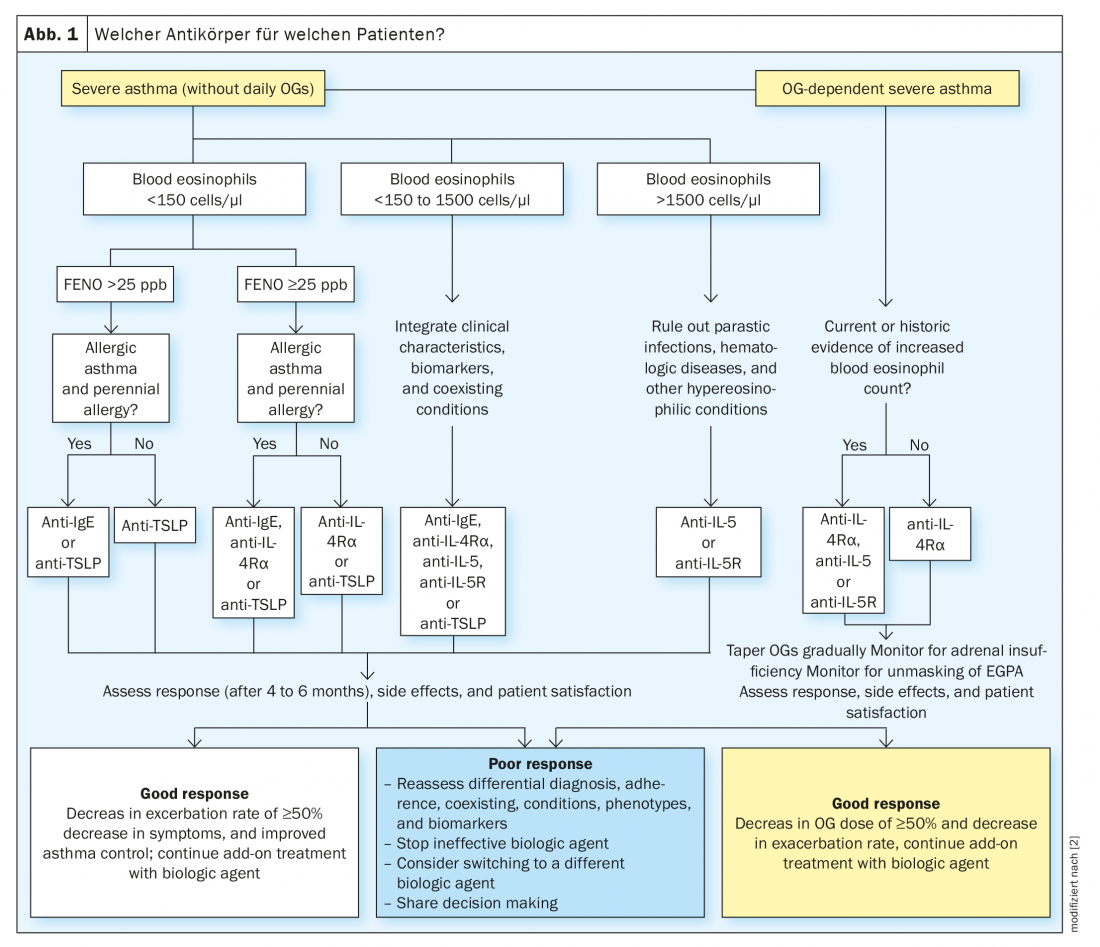
Caractéristiques des patients
“Un patient qui déclare souffrir d’asthme depuis l’âge de 50 ans, qui a tout de suite été relativement sévère, qui prend constamment des comprimés de cortisone et qui déclare en outre qu’il ne peut pas sentir, est typique d’un asthme éosinophile sévère. Un tel patient est prédestiné à recevoir un traitement anti-IL-5”. Un autre patient, qui dit avoir eu des allergies et des symptômes d’asthme légers de temps en temps dans l’enfance, qui ont parfois complètement disparu, mais qui se sont lentement aggravés au fil des ans, est en revanche typique d’un asthme allergique sévère et donc un candidat pour un traitement anti-IgE. “L’entretien avec le patient devrait donc nous donner une première indication sur la direction à prendre avec lui”.
Évolution et comorbidités
D’autres facteurs sont les biomarqueurs au cours de l’évolution et les comorbidités : Lors d’un traitement par dupilumab, le nombre d’éosinophiles augmente au début. “Chez la plupart des patients, cela n’a aucune conséquence clinique”, a rassuré le Dr Korn. Mais si, par exemple, un patient a plus de 1500 éosinophiles, elle serait prudente de le traiter avec le dupilumab, car une augmentation allant jusqu’à 40% peut tout à fait se produire. Pour les patients présentant un taux d’éosinophiles très élevé, l’experte privilégierait donc toujours les anti-IL-5.
Comme un patient asthmatique souffre souvent d’autres maladies, il peut être très utile de jeter un coup d’œil aux autres autorisations de mise sur le marché des produits biologiques. “Si vous recevez un jeune asthmatique qui a également une dermatite atopique, il est évident de le traiter avec le dupilumab, car celui-ci est également autorisé pour la dermatite atopique”. Le principe de faire d’une pierre deux coups pourrait donc bien s’appliquer ici. Si le patient répond finalement avec succès à Neuroderminis, mais qu’il continue à souffrir de son asthme, on peut envisager de conserver le dupilumab pour la DA et d’utiliser en plus un autre anticorps pour traiter l’asthme. “Mais dans de tels cas, la situation a toujours été telle que nous avons fini par avoir deux anticorps pour deux indications différentes – je n’ai pas encore utilisé deux anticorps en parallèle uniquement pour l’asthme sévère”, a déclaré le Dr Korn en appelant à la prudence dans de telles considérations.
Anti-TSLP
Les patients qui ne présentent aucun biomarqueur, c’est-à-dire qui n’ont pas d’IgE ou de FeNO élevées et dont le nombre d’éosinophiles est faible, sont très rares, mais peuvent se produire de temps en temps. L’une des raisons peut être qu’ils prennent de la cortisone. Il existe cependant des patients isolés qui ne présentent pas ces valeurs à la base et chez lesquels il est par conséquent difficile d’utiliser les anticorps conformément aux autorisations de mise sur le marché.
Un nouvel anticorps pourrait à l’avenir apporter une solution à ce problème : TSLP est une cytokine épithéliale dont l’anticorps (tezepelumab) permet d’accéder à la fois à la voie allergique, à la voie éosinophile et aux cellules structurales. “En fin de compte, la question est de savoir si l’efficacité est plus large et si je peux éventuellement l’utiliser de manière moins différenciée ou également chez les patients dont les biomarqueurs ne sont pas aussi élevés”.
Il est donc possible qu’à l’avenir, la thérapie s’oriente vers le traitement des patients présentant plusieurs de ces voies par un anticorps tel que l’anti-TSLP, qui intervient beaucoup plus en amont et bloque ainsi complètement ces voies, plutôt que d’utiliser un produit biologique qui ne supprime qu’une seule voie, selon les perspectives du Dr Korn.
62e Congrès de la Société allemande de pneumologie et de médecine respiratoire à Leipzig (D), du 25 au 28 mai 2022.
Littérature :
- Korn S : Asthme sévère et thérapie biologique – l’embarras du choix ? Symposium “State of the Art Asthma” dans le cadre du congrès de la DGP, 26.05.2022.
- Brusselle GG, Koppelman GH : Thérapies biologiques pour l’asthme sévère. N Engl J Med 2022 ; 386 : 157-171 ; doi : 10.1056/NEJMra2032506.
InFo PNEUMOLOGIE & ALLERGOLOGIE 2022 ; 4(3) : 22-24











