Présentation d’un cas par le Dr méd. Stefan Greuter
rundum onkologie ag, Sargans
Fiche signalétique
Patiente : 74 ans (née en 1949)
Diagnostic en 2022 : carcinome épidermoïde évolutif du lobe supérieur gauche du poumon (T4 N2 M1, 5-10% PD-L1, EGFR de type sauvage, ALK/ROS1 négatif, altérations induisant un saut de l’exon 14 de MET)
Traitement : traitement de deuxième ligne par 450 mg de Tepmetko® (tépotinib) une fois par jour ; ajustement de la dose à 225 mg au cours de l’évolution de la maladie
Anamnèse
En septembre 2018, la patiente s’est présentée à l’hôpital cantonal des Grisons avec des épisodes de bronchite récidivants. Elle a longtemps travaillé dans l’hôtellerie et la restauration, et a donc été fortement exposée au tabagisme passif pendant 20 à 25 ans. Un examen de tomodensitométrie thoracique a montré, outre une volumineuse masse dans le lobe supérieur (LS) gauche du poumon s’accompagnant d’une infiltration du médiastin, une lymphadénopathie médiastinale ainsi qu’une autre masse dans le LS droit. La bronchoscopie diagnostique a confirmé le diagnostic de suspicion de carcinome pulmonaire. Sur le plan histologique, il s’agissait d’un carcinome épidermoïde de grade 1-2 avec une expression de PD-L1 allant jusqu’à 10%. La tumeur a été étudiée plus précisément : EGFR de type sauvage, ALK/ROS1 négatif avec altérations induisant un saut de l’exon 14 de MET. La recherche ultérieure de métastases par TEP a permis de classer le carcinome bronchique en T4 N2 avec des ganglions lymphatiques non régionaux suspects (M1a) et un probable carcinome secondaire controlatéral. La patiente a toutefois refusé une biopsie de l’éventuel carcinome secondaire. En présence de ce résultat localement étendu et d’une possible formation de métastases à distance, le tumor board de l’Hôpital cantonal des Grisons (KSGR) a recommandé en octobre 2018 un traitement systémique en premier lieu.
Traitement
En octobre/novembre, la patiente a reçu un cycle de carboplatine/paclitaxel et, après confirmation de la prise en charge des coûts pour le traitement de première ligne par le pembrolizumab, deux cycles de pembrolizumab-carboplatine/paclitaxel ont suivi jusqu’en décembre 2018 [1]. Après la 4e administration du traitement combiné, la patiente a réagi par des poussées de fièvre, probablement en raison d’une réaction allergique au carboplatine. Lors d’une réunion du tumor board du KSGR en janvier 2019, aucune opération n’a été recommandée en raison de métastases pleurales et pulmonaires, mais plutôt un traitement d’entretien palliatif par le pembrolizumab [1]. La patiente a alors commencé une monothérapie par le pembrolizumab pour 2 ans. Celle-ci était accompagnée d’une légère hypothyroïdie ainsi que d’une légère pneumopathie inflammatoire.
En janvier 2022, une progression a été constatée dans le poumon gauche, raison pour laquelle le traitement a été remplacé par un traitement oral avec une prise de tépotinib (Tepmetko®) une fois par jour [2]. La dose a été réduite de moitié en raison d’une alopécie, d’une fatigue et d’un œdème des jambes et des avant-bras (tous ces effets indésirables étant de grade 1). La tumeur du poumon gauche est restée stable sous tépotinib, mais la patiente a développé une lassitude vis-à-vis du traitement, à la suite de quoi le traitement par le tépotinib a de nouveau été arrêté en septembre 2023.
Évolution ultérieure et situation actuelle
Environ 4 mois après l’arrêt du traitement par le tépotinib en janvier 2024, l’examen de tomodensitométrie de suivi a montré une progression de la taille de la tumeur dans le LS gauche (fig. 1). La manifestation tumorale dans le LS droit était inchangée, de même que l’épaississement de la plèvre gauche, constitué de petits nodules, probablement néoplasique. La métastase du ganglion lymphatique infracarinaire a montré une faible progression, mais dans l’ensemble, il n’y avait pas d’autres éléments indiquant de nouvelles manifestations tumorales. Lors de la consultation, il a été convenu avec la patiente de reprendre le traitement palliatif par le tépotinib à demi-dose, traitement qu’elle suit jusqu’à présent sans récidive d’œdèmes [2]. Les objectifs thérapeutiques, parmi lesquels figurent la prévention des complications, le maintien d’une très bonne qualité de vie ainsi qu’une prolongation de la vie, ont tous été atteints sous tépotinib, selon l’état actuel des connaissances. L’objectif palliatif de contrôle de la tumeur a été partiellement atteint sous tépotinib et un nouveau suivi sera effectué en avril 2024.
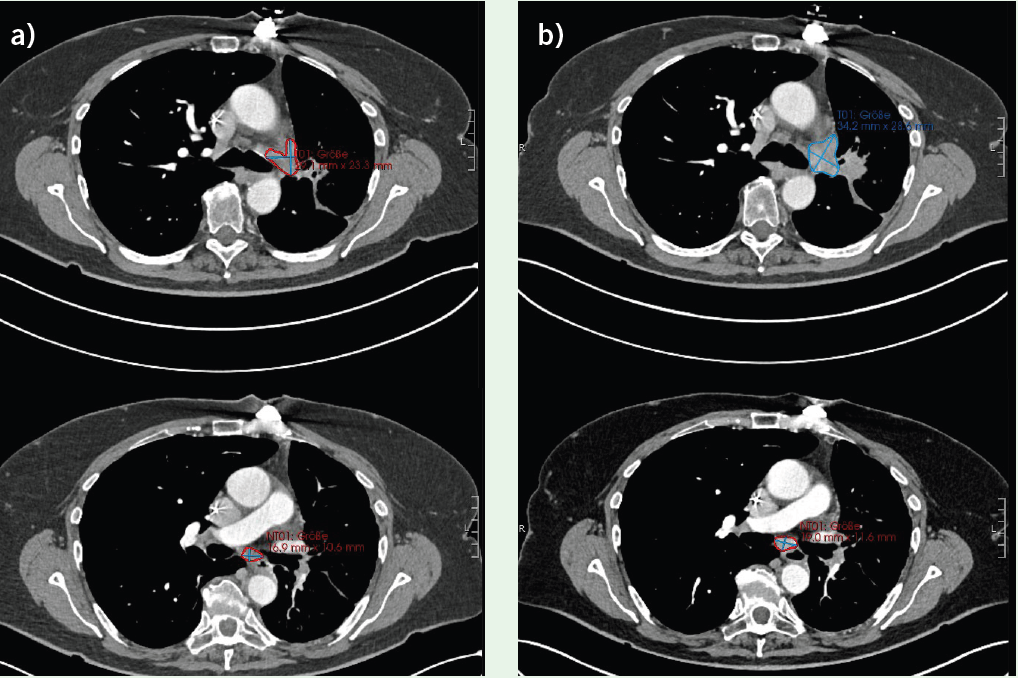
Figure 1) Évolution de la maladie à l’examen de tomodensitométrie avant et après l’arrêt du traitement de deuxième ligne par le tépotinib a) Contrôle en septembre 2023: évolution stable de la maladie (image du haut: tumeur primaire de 29,1 × 23,3 mm; image du bas: métastase du ganglion lymphatique infracarinaire de 16,9 × 10,6 mm) sous tépotinib et arrêt du traitement par le tépotinib à ce moment-là b) Contrôle de suivi en janvier 2024 (4 mois après l’arrêt du traitement par le tépotinib): progression de la taille de la tumeur primaire dans le LS et faible progression de la métastase du ganglion lymphatique infracarinaire (image du haut: tumeur primaire de 34,2 × 28,6 mm; image du bas: métastase du ganglion lymphatique infracarinaire de 19,0 × 11,6 mm). © S. Greuter
Commentaire du Dr méd. Stefan Greuter
rundum onkologie ag, Sargans

Ce qui est intéressant dans ce cas, c’est de voir combien de temps on arrive aujourd’hui à contrôler les carcinomes bronchiques métastatiques (de même que d’autres carcinomes) avec une thérapie ciblée. Ainsi, en cas de translocations du gène ALK, de mutations de l’EGFR ou, dans le cas présent, d’une mutation MET, il est aujourd’hui possible de contrôler la tumeur pendant des années grâce à une thérapie ciblée. Je trouve cela extrêmement satisfaisant, car on repousse ainsi longtemps la progression de la tumeur grâce à un traitement souvent bien toléré, même sur une longue période. Pour moi, cet exemple illustre aussi très clairement qu’en cas d’arrêt du traitement en septembre 2023, une progression se produit à nouveau après seulement quelques mois. Avec le tépotinib, nous avons interrompu la cinétique, et si nous obtenons maintenant une réponse lors de la réutilisation du traitement, nous pourrons voir si le tépotinib agit à nouveau lors de cette nouvelle administration. En résumé, il est passionnant de voir à quel point ces nouvelles thérapies ciblées permettent de contrôler les maladies tumorales sur une longue période, tout en étant souvent très bien tolérées.
Abréviations :
ALK = kinase du lymphome anaplasique (anaplastic lymphoma kinase); EGFR = endothelial growth factor receptor (récepteur du facteur de croissance endothéliale); PD-L1 = programmed death-ligand 1 (ligand de la protéine de mort programmée 1); TEP = tomographie par émission de positons; ROS1 = ROS proto-oncogène 1
L’information professionnelle abrégée de TEPMETKO®.
CH-TEP-00182 06/2024
Avec le soutien financier de Merck (Schweiz) AG.
Références
1. Information professionnelle de KEYTRUDA®. www.swissmedicinfo.ch. État actuel.
2. Information professionnelle de TEPMETKO®. www.swissmedicinfo.ch. État actuel.
Les références sont disponibles sur demande.












