| Dans l’étude “BioDay-Register”, le traitement par dupilumab de patients pédiatriques atteints de dermatite atopique dans le cadre d’une étude “en vie réelle” a entraîné une amélioration significative de la sévérité de la maladie et des symptômes associés. La tolérance s’est avérée bonne et le profil de sécurité est conforme aux résultats des études cliniques. |
Jusqu’à présent, le dupilumab s’est avéré être un traitement efficace et sûr de la dermatite atopique (DA) [1]. En se liant à la sous-unité IL-4Rα des complexes récepteurs de l’IL-4 et de l’IL-13, l’anticorps monoclonal inhibe spécifiquement l’effet pro-inflammatoire de ces deux cytokines clés [1]. En Suisse, le dupilumab (Dupixent®) est autorisé pour les patients atteints de MA à partir de 6 ans [1]. L’étude “BioDay-Register” a été menée afin d’évaluer les effets thérapeutiques du dupilumab chez les patients pédiatriques atteints de la MA dans le cadre d’une étude “en vie réelle” [2]. Cette étude de cohorte prospective a porté sur des enfants (≥6 à <12 ans) et des adolescents (≥12 à <18 ans) traités par dupilumab et présentant une MA modérée à sévère. Les patients ayant un poids corporel <60 kg ont reçu du dupilumab (s.c.) toutes les deux semaines (q2w) après une dose de charge initiale de 400 mg. Chez les patients d’un poids corporel ≥60 kg, une dose de charge de 600 mg a été administrée, suivie de 300 mg q2w. Les enfants pesant entre 15 et 60 kg ont reçu 300 mg à la ligne de base et après 2 semaines, puis 300 mg de dupilumab toutes les quatre semaines. Un traitement concomitant par des corticostéroïdes topiques était autorisé.
Aux moments de l’enquête, à la semaine 0 (ligne de base) et aux semaines 4, 16 et 28, la gravité de la maladie a été évaluée à l’aide de scores validés : “Eczema Area and Severity Index” (EASI), “Investigator Global Assessment” (IGA), “Numeric Rating Scale” (NRS) pour les démangeaisons et la douleur, “Patient-Oriented Eczema Measure” (POEM) [2]. En outre, les biomarqueurs sériques associés à la sévérité ont été mesurés.
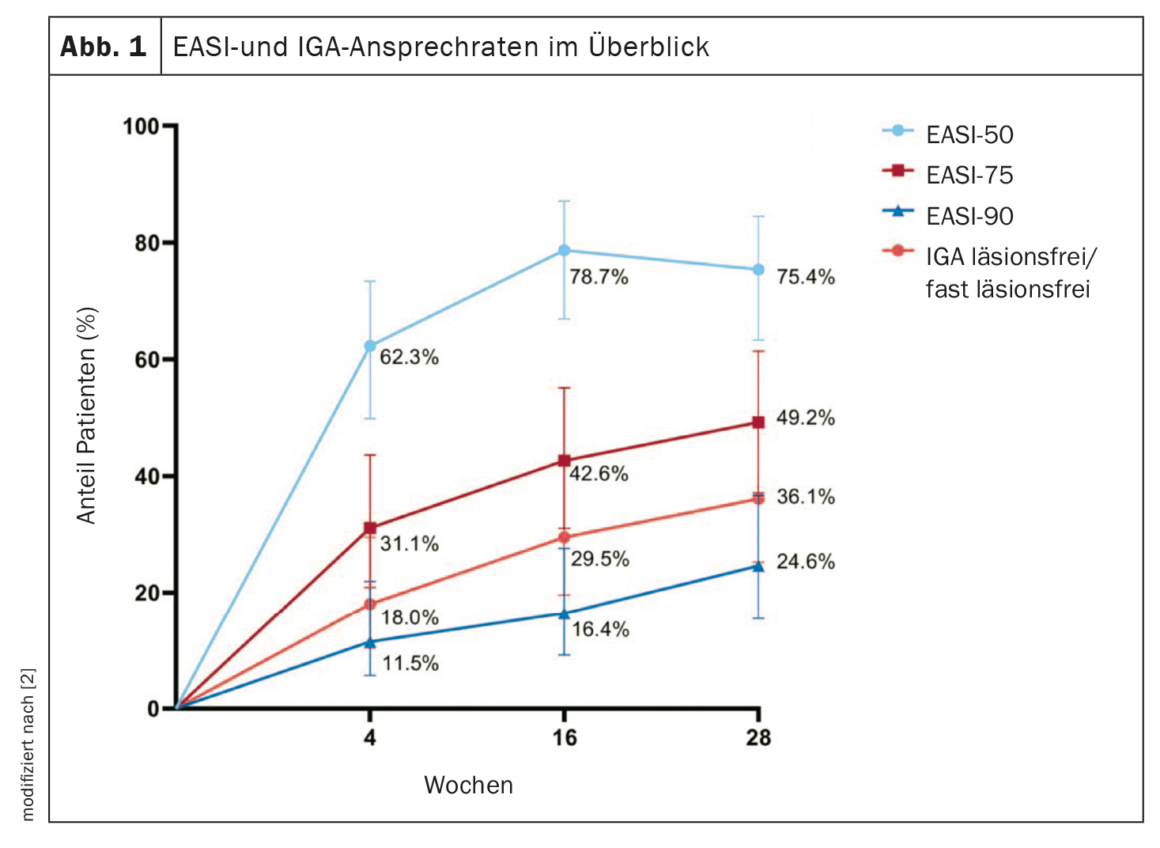
Sur les 61 patients inclus, 75,4% et 49,2% ont obtenu respectivement une réponse EASI-50 et EASI-75 (figure 1) [2]. Le taux de réponse EASI-90 était de 24,6%. Selon le score IGA, 36,1% étaient exempts de lésions ou presque. Une amélioration de ≥4 points dans le POEM a été obtenue par 84,7%, alors que ce pourcentage était de 45,3% et 77,4% respectivement pour les démangeaisons NRS et les douleurs NRS. Les biomarqueurs TARC, PARC, périostine, sIL-2Ra et éotaxine-3 ont diminué de manière significative pendant le traitement. Le p-EASI a montré une corrélation significative avec la sévérité de la maladie. Les effets secondaires les plus fréquents ont été la conjonctivite (n=10) et les céphalées (n=4) (tableau 1).
Littérature :
- Informations sur les médicaments, www.swissmedicinfo.ch,(dernière consultation 13.04.23).
- Kamphuis E, et al : Dupilumab en pratique quotidienne pour le traitement de la dermatite atopique pédiatrique : 28-week clinical and biomarker results from the BioDay registry. Pediatr Allergy Immunol 2022 ; 33(12) : e13887.
DERMATOLOGIE PRATIQUE 2023 ; 33(2) : 52