L’insuffisance respiratoire est une source de grande souffrance pour les patients, leurs proches et les professionnels de santé. L’insuffisance respiratoire est un phénomène fréquent qui touche plus de 50% des patients en fin de vie. Des données indiquent même une augmentation de la charge de symptômes due à l’insuffisance respiratoire jusqu’au décès. La maladie COVID-19 peut également provoquer, surtout chez les patients instables ou mourants, d’une part une hypoxie et une tachypnée, d’autre part une charge symptomatique élevée avec dyspnée et anxiété.
La dyspnée provoque une très grande souffrance, tant chez les personnes concernées [1] que chez leurs proches [2] et leur entourage professionnel. L’insuffisance respiratoire est un phénomène fréquent qui touche plus de 50% des patients en fin de vie [3]. Des données indiquent même une augmentation de la charge symptomatique due à l’insuffisance respiratoire jusqu’au décès [1]. De même, la maladie COVID-19, récemment apparue, peut provoquer, surtout chez les patients instables ou mourants, d’une part une hypoxie et une tachypnée, d’autre part une charge symptomatique élevée avec dyspnée et anxiété [4].
La dyspnée et les modifications respiratoires peuvent survenir au cours de l’évolution de diverses maladies chroniques et évolutives, notamment dans les domaines de l’oncologie, de la neurologie, de la pneumologie ou de la cardiologie [5]. Cela entraîne souvent des consultations et des hospitalisations d’urgence au cours des derniers mois et semaines de vie des personnes concernées [6]. Les termes d’essoufflement ou de dyspnée font référence à une perception subjective des personnes concernées. Ainsi, la dyspnée est également décrite par les récits des patients comme une soif d’air, un essoufflement, un essoufflement, un blocage de la respiration, une respiration difficile et, dans les cas extrêmes, une sensation d’étouffement. L’essoufflement ne peut donc pas être mesuré, mais doit être demandé.
En revanche, les termes d’insuffisance respiratoire ou d’insuffisance respiratoire désignent des modifications objectivement observables de la respiration mécanique externe ou des échanges gazeux pulmonaires. Les changements subjectifs et objectifs peuvent être simultanés, mais aussi indépendants les uns des autres et ne doivent pas être corrélés [7,8]. Ce phénomène a également été observé récemment avec COVID-19 [9]. Cela signifie, par exemple, qu’une patiente peut ne pas ressentir de dyspnée malgré une saturation en oxygène de seulement 70% et une tachypnée, mais qu’un patient peut ressentir la plus grande dyspnée avec une saturation en oxygène de 95%. La reconnaissance et la différenciation de ces phénomènes par les médecins traitants sont fondamentales, non seulement dans la dernière phase de vie et dans le processus de mort, mais aussi et surtout pour pouvoir soulager de manière adéquate les souffrances et bien accompagner les personnes concernées [10]. Nous allons maintenant aborder le thème de la détresse respiratoire, de ses causes possibles et des thérapies en fin de vie.
Définition et étiologie
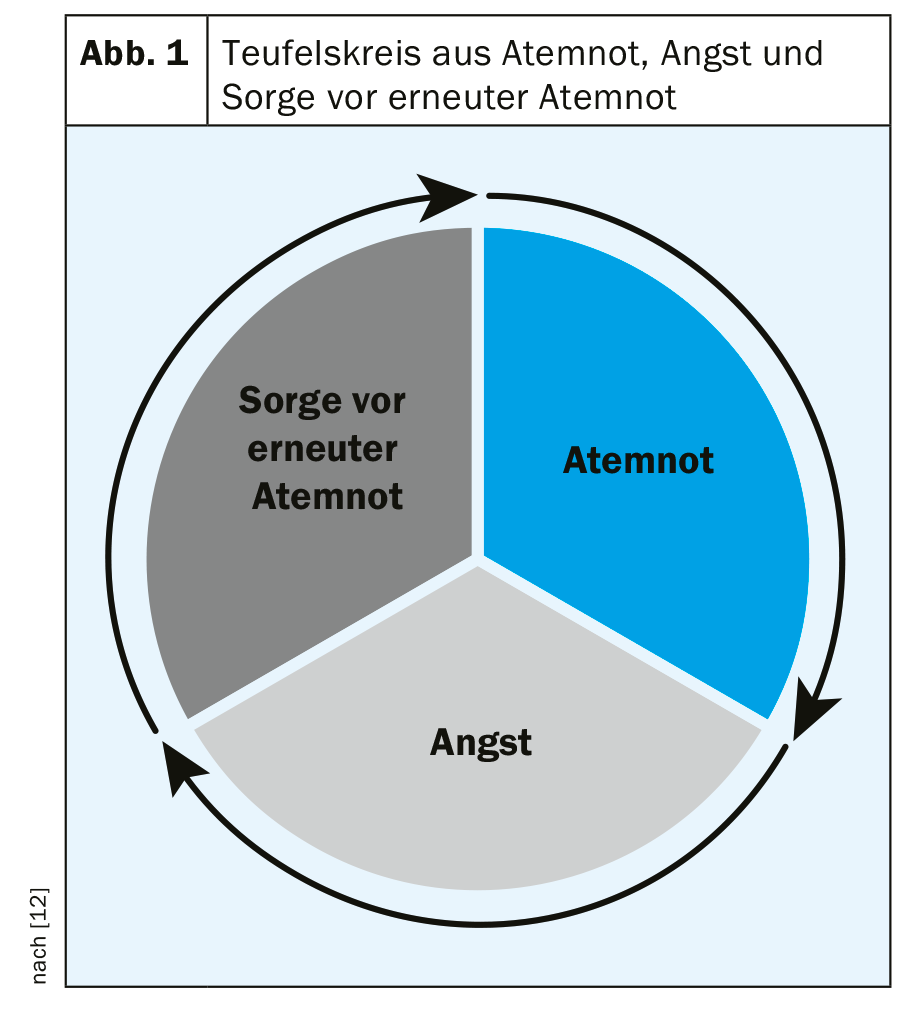
L’American Thoracic Society (ATS) définit l’essoufflement comme une perception subjective d’une difficulté à respirer, constituée de sensations qualitativement différentes et dont l’intensité peut varier. La perception résulte de l’interaction entre de multiples facteurs physiques, psychologiques, sociaux et environnementaux et peut secondairement conditionner des réponses physiologiques et comportementales. Cependant, il est explicitement souligné dans ce contexte que seule la personne concernée peut ressentir et évaluer la dyspnée [11]. Dans la genèse et le maintien de la dyspnée, les facteurs psychologiques ne sont souvent pas des facteurs d’influence secondaires. Ainsi, la peur joue très souvent un rôle important [7], ce qui crée une spirale de potentialisation mutuelle (Fig. 1) [12]. Le stress au niveau physique et psychologique et les restrictions de participation sociale qui en découlent sont démoralisants pour les personnes concernées. La dyspnée peut être continue, mais aussi intermittente sous forme de crises d’essoufflement [13]. Dans certains cas, les déclencheurs peuvent être délimités, dans d’autres, ils ne sont pas identifiables.
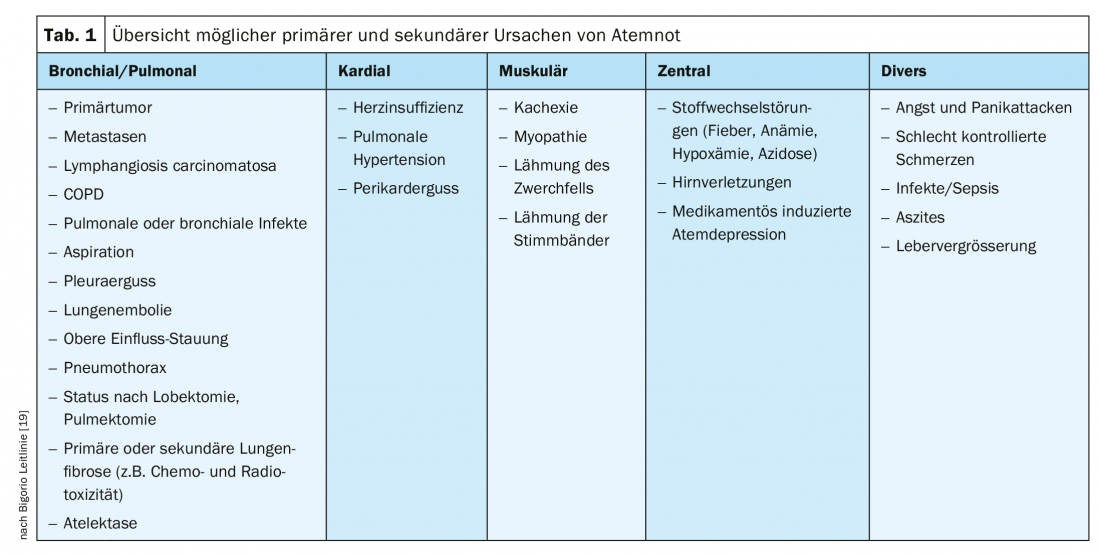
La dyspnée est un symptôme fréquent chez les patients en fin de vie, qu’ils soient atteints d’une maladie tumorale ou non [15]. Ainsi, dans le contexte des soins palliatifs, les maladies tumorales malignes avec des manifestations pulmonaires et leurs complications (embolies pulmonaires, épanchements pleuraux, anémie, etc.), les maladies neuromusculaires (par ex. SLA), l’insuffisance cardiaque avancée ou la BPCO sont notamment à l’origine de modifications de la respiration et de l’apparition de dyspnée [11]. Le tableau 1 donne un aperçu des pathologies possibles qui peuvent entraîner une insuffisance respiratoire. Il est important ici de rechercher et de traiter les causes réversibles.
Évaluation et diagnostic
En raison de la subjectivité de la dyspnée et du fait que les médecins sous-estiment souvent la charge symptomatique [16], il est en principe utile de procéder à un enregistrement systématique et standardisé de la charge symptomatique. En principe, cela se fait par l’évaluation de la personne concernée elle-même. Une classification numérique, par exemple selon l’échelle d’évaluation numérique (NRS) ou l’échelle visuelle analogique (VAS), peut être utilisée et aider à évaluer l’évolution en cas d’utilisation répétée. Outre l’évaluation quantitative de la charge symptomatique sensorielle, il convient également d’évaluer les limitations fonctionnelles ressenties du fait de la dyspnée ainsi que la charge émotionnelle [17].
En cas de diminution de la vigilance, de troubles cognitifs ou physiques graves, comme ceux qui surviennent en phase terminale, une évaluation par un tiers peut s’avérer nécessaire. Un instrument validé est le Respiratory Distress Observation Scale (RDOS) [18]. Celle-ci comprend différents aspects objectivement détectables qui, lorsqu’ils sont combinés, peuvent fournir une information valide sur le niveau de détresse respiratoire.
Dans les contextes de soins palliatifs, l’évaluation des causes remédiables de la dyspnée en fait également partie [17,19]. En raison des entités pathologiques malignes et non malignes fréquentes déjà mentionnées, des déclencheurs réversibles de la dyspnée peuvent apparaître. Il peut s’agir par exemple d’un épanchement pleural en cas de tumeur pulmonaire ou d’insuffisance cardiaque, d’une augmentation du volume abdominal due à une ascite, d’un pneumothorax ou d’une pneumonie (voir également le tableau 1). L’examen clinique et l’évaluation sont les premiers éléments du diagnostic. Des moyens de diagnostic plus poussés tels que le laboratoire, la radiographie, l’échographie, la tomodensitométrie ou l’analyse des gaz du sang peuvent être utiles. Les décisions concernant les examens complémentaires doivent cependant toujours être basées sur la situation globale et le pronostic du patient, ainsi que sur l’objectif de traitement défini conjointement par le patient, ses proches et l’équipe soignante. Tout ce qui est possible n’est pas forcément utile et ne permet pas d’atteindre le but recherché. Souvent, le soulagement des symptômes est bien plus important que des examens contraignants.
Thérapie
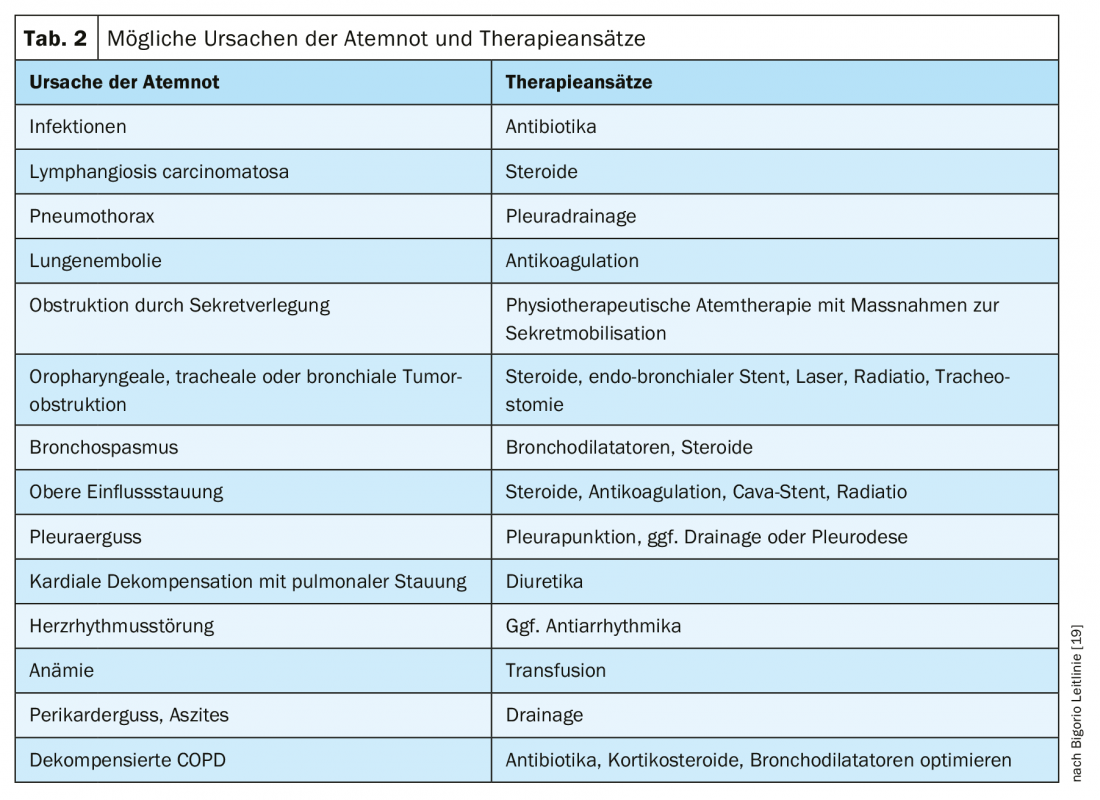
S’il existe des causes potentiellement remédiables à la dyspnée, il convient d’essayer de les traiter – mais là encore, selon le paradigme “tout ce qui est possible n’est pas utile”. Le tableau 2 présente les causes traitables de l’essoufflement et leurs options de traitement spécifiques respectives. Ces interventions sont particulièrement pertinentes dans les phases de soins palliatifs et de fin de vie. En phase terminale, ils passent au second plan, la charge serait ici plus importante que les bénéfices. Il est toujours important d’évaluer explicitement le bénéfice apporté par la mesure concrète. Si et dans quelle mesure l’intervention (par ex. transfusion, ponction pleurale) a réduit la dyspnée ? L’évaluation sert de base aux décisions concernant la poursuite ou la répétition de l’intervention.
Parallèlement au traitement éventuel des causes réversibles, on applique un traitement symptomatique. L’utilisation de mesures non médicamenteuses et médicamenteuses est recommandée [19]. Les interventions non médicamenteuses [20] comprennent des aides à la marche [20], des exercices de relaxation [21], des exercices respiratoires [21] et l’utilisation de ventilateurs pour créer un flux d’air dans la région du visage [22]. En cas de crise d’essoufflement ou d’exacerbation de l’essoufflement, un environnement calme, une personne présente, une position assise confortable et un courant d’air rafraîchissant sur le visage (par un ventilateur, une fenêtre ouverte) sont utiles. L’éducation des personnes concernées et de leurs proches est également un aspect important. L’éducation peut également inclure des instructions sur les moyens de se prendre en charge, au sens d’un plan d’urgence sur lequel figurent des instructions concrètes sur les actions non médicamenteuses et médicamenteuses, par exemple en cas de crise d’insuffisance respiratoire. Il est important que le plan et les mesures soient concrètement discutés à l’avance et pratiqués avec le patient et ses proches. Grâce au plan d’urgence, le patient et ses proches sont habilités à agir eux-mêmes, ce qui renforce leur autonomie [23].
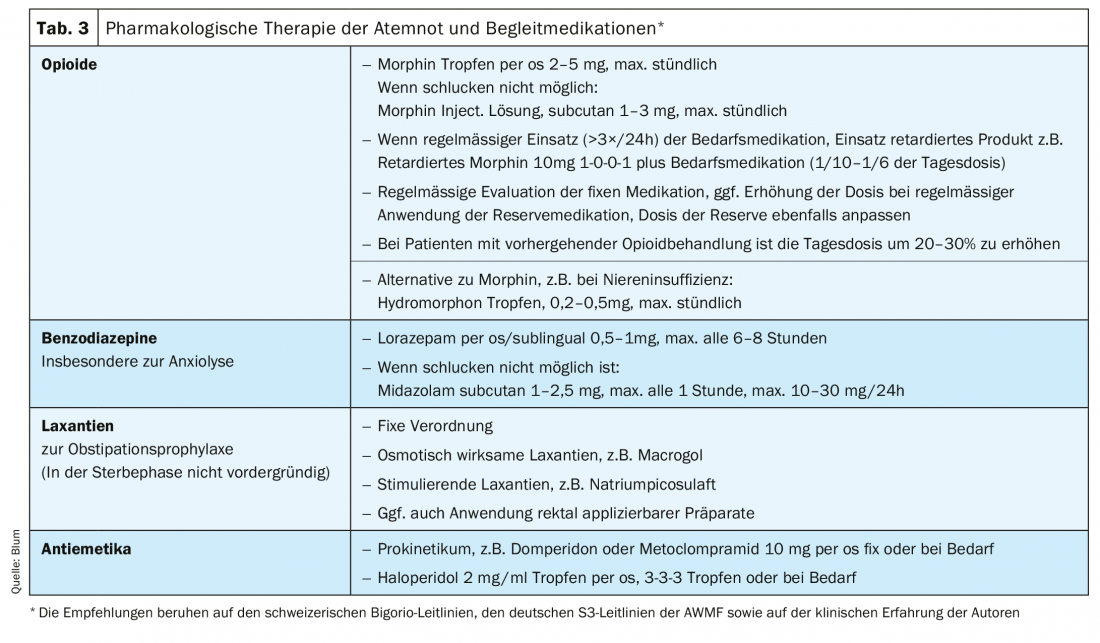
Pour le traitement pharmacologique symptomatique, l’utilisation d’opioïdes est recommandée en premier lieu [17,19]. Les études sur l’efficacité de la morphine dans le traitement de la dyspnée réfractaire sont les plus nombreuses par rapport aux autres opioïdes, bien que les résultats ne soient pas non plus homogènes [24–27]. Les résultats concernant l’efficacité de substances telles que le fentanyl, l’hydromorphone et l’oxycodone sont également hétérogènes et moins concluants [27–30]. Il n’existe pas de données sur l’efficacité de la buprénorphine dans le traitement de l’insuffisance respiratoire. Néanmoins, d’autres opioïdes font partie des alternatives utilisées en pratique clinique, par exemple en cas de contre-indication à la morphine (insuffisance rénale [31], intolérance). Outre la forme orale, il existe également des voies d’administration parentérales (sous-cutanées ou intraveineuses). On ne trouve pas de données montrant l’efficacité de la voie nasale/inhalée ou transdermique [27]. Pour les patients vigilants qui peuvent avaler, la forme orale est préférée. En cas de crises d’insuffisance respiratoire difficiles à interrompre, et en phase terminale, on passe généralement à une application parentérale. Dans le cas des patients présentant des troubles de la déglutition, la voie d’administration transdermique du fentanyl peut être envisagée malgré l’absence de preuves en l’absence d’alternatives proportionnées.
Il est recommandé d’utiliser initialement des préparations à faible dose et à courte durée d’action (par ex. morphine en gouttes). En cas d’utilisation régulière, il est judicieux de prescrire des préparations à libération prolongée associées à des préparations à courte durée d’action si nécessaire. Il est également recommandé d’utiliser des préparations à courte durée d’action à titre préventif avant l’effort, afin d’éviter la survenue de crises d’essoufflement. La posologie dépend en principe de la clinique et de l’intensité de la détresse respiratoire. La tolérance joue également un rôle important. Ainsi, des nausées et de la fatigue peuvent apparaître, en particulier au début d’un traitement par opioïdes [27], mais elles disparaissent généralement après quelques jours. Un traitement antiémétique prophylactique avec un prokinétique ou de l’halopéridol peut être envisagé. L’apparition de la constipation n’est pas soumise à l’effet d’accoutumance et doit être traitée de manière cohérente et préventive. En particulier chez les patients gériatriques, l’utilisation d’opioïdes peut provoquer un délire [32], de sorte qu’il est conseillé de procéder avec prudence. Le risque de dépression respiratoire ou de complication respiratoire importante, redouté par de nombreux médecins, est pratiquement inexistant si le dosage est effectué selon les principes de titration et d’adaptation [33].

Les mécanismes d’action de la thérapie opioïde pour le traitement de la dyspnée sont, entre autres, l’augmentation de latolérance cérébraleau CO2, la réduction de la fréquence respiratoire, l’augmentation du volume respiratoire, l’amélioration de l’élimination du CO2 et la diminution du travail respiratoire. Outre l’atténuation de la réponse émotionnelle dans le système limbique, il y a donc une amélioration de la mécanique respiratoire.
Les benzodiazépines sont également utilisées [34,35]. En particulier, l’utilisation de benzodiazépines est recommandée dans les situations où l’effet d’amplification par l’anxiété est pertinent [17,19]. Outre le midazolam, qui peut être administré par voie parentérale (sous-cutanée ou intraveineuse), mais aussi par voie nasale, le lorazépam (sublingual, oral) est souvent utilisé. Les benzodiazépines sont donc utilisées en complément d’un opioïde et non à sa place. Les stéroïdes peuvent également être utilisés lorsqu’une cause unique ne peut pas être clairement identifiée et qu’un événement multifactoriel est suspecté [36]. Il existe également des données récentes selon lesquelles la mirtazapine pourrait aider à lutter contre l’insuffisance respiratoire [37].
Les études ne montrent pas de soulagement significatif de la dyspnée par l’utilisation d’oxygène chez les patients proches de la mort [38,39]. Si l’utilisation d’oxygène apporte un bénéfice subjectif aux personnes concernées dans un cas individuel, son utilisation à un niveau modéré (1-2 l, max. 4 l) peut néanmoins être utile [19]. Chez le mourant, ce sont toutefois les aspects indésirables qui l’emportent, comme la sensation gênante sur le visage, le dessèchement des muqueuses et l’accent mis sur la médecine d’appareil.
En résumé, le traitement de la dyspnée nécessite un concept thérapeutique adapté à chaque individu, dont l’efficacité et les effets secondaires doivent être vérifiés à intervalles rapprochés et régulièrement adaptés. Le concept thérapeutique se base sur les approches thérapeutiques pharmacologiques et non pharmacologiques mentionnées ci-dessus, qui doivent et peuvent être choisies en fonction de la situation individuelle du patient. Toutes les options de traitement médicamenteux mentionnées ici sont des applications hors étiquette – une réalité quotidienne dans les soins palliatifs [40].
Sédation palliative
Dans les cas où, malgré l’application des mesures thérapeutiques médicamenteuses et non médicamenteuses disponibles, il n’est pas possible d’obtenir une réduction significative des souffrances et que celles-ci ne sont plus supportables pour le patient, la sédation peut être envisagée en tant qu’option de dernier recours. Dans sa directive de 2019, l’Académie Suisse des Sciences Médicales (ASSM) formule l’option d’action pour ces situations de la manière suivante : “Dans les situations où un symptôme est néanmoins réfractaire et persistant de manière insupportable pour le patient, l’option de traitement consiste en une sédation palliative temporaire ou continue, c’est-à-dire en l’utilisation contrôlée de médicaments sédatifs afin de réduire la perception des symptômes par une diminution ou une suppression de l’état de conscience. Le dosage et le choix des médicaments dépendent de l’objectif du traitement (p. ex. disparition des symptômes, soulagement du patient). La durée de la sédation dépend de la situation déclenchante”. [45]. Il est important de noter que la sédation profonde continue ne doit être utilisée que lorsque les options thérapeutiques disponibles ont été épuisées et chez les patients dont le processus de fin de vie a déjà commencé [45]. L’objectif de la sédation est de réduire la souffrance et non d’abréger la vie.
Si une sédation est envisagée en raison d’une détresse respiratoire non maîtrisable en fin de vie, il convient de vérifier que plusieurs conditions sont remplies. Elles concernent aussi bien le patient, ses proches que l’équipe soignante [48]. Il est également recommandé de suivre une procédure clairement structurée et prédéfinie afin d’éviter les erreurs et les abus dans ce domaine sensible. En cas de doute, une consultation à bas seuil d’une équipe spécialisée en soins palliatifs ou d’une équipe d’éthique clinique doit également être envisagée. Ces mesures permettent de renforcer la réflexion et d’assurer la qualité de la décision.
Enfin, il convient de souligner que la dyspnée est un symptôme complexe dans les maladies chroniques évolutives et les stades terminaux de la maladie. Le patient est au centre du sujet et la pression de la souffrance est élevée. Seul le patient peut évaluer les symptômes au sens propre du terme. Les concepts thérapeutiques s’orientent aussi bien vers le traitement des causes réversibles que vers des approches de traitement symptomatique non médicamenteux et médicamenteux. La sédation profonde continue est une mesure qui ne doit être utilisée qu’en cas d’échec des autres approches thérapeutiques, de souffrance importante et dans le cas d’un processus de fin de vie déjà entamé. L’objectif réaliste du traitement, défini en collaboration avec le patient, ses proches et l’équipe soignante, est déterminant pour toutes les décisions thérapeutiques. Des discussions précoces sur les préférences, les idées et les priorités des patients aident à planifier à l’avance, favorisent l’autonomie des patients et nous fournissent, à nous médecins traitants, des informations précieuses pour un bon traitement en fin de vie.
Messages Take-Home
- La détresse respiratoire est toujours subjective.
- La dyspnée et les modifications objectives de la respiration/de la fonction pulmonaire peuvent survenir indépendamment les unes des autres.
- L’insuffisance respiratoire est un symptôme complexe qui peut être déclenché par différents facteurs biologiques, psychologiques, sociaux et spirituels.
- Le traitement concerne les causes potentiellement réversibles et le traitement symptomatique.
- Le traitement symptomatique comprend des mesures médicamenteuses et non médicamenteuses.
- Les décisions thérapeutiques se réfèrent à l’objectif de traitement défini en commun.
Littérature :
- Campbell ML, et al. : Trajectoire de la dyspnée et de la détresse respiratoire chez les patients au cours du dernier mois de vie. J. Palliat. Med 2018 ; 21 : 194-199.
- Malik FA, et al. : Living with breathlessness : a survey of caregivers of breathless patients with lung cancer or heart failure. Palliat. Med 2013 ; 27 : 647-656).
- Simon ST, et al : Characteristics of patients with breathlessness – results of the german hospice and palliative care evaluation. Dtsch. Med. Wochenschr 2016 ; 141 : e87-95.
- Zhu J, et al : Caractéristiques cliniques de 3,062 patients COVID-19 : une méta-analyse. J. Med. Virol 2020 ; doi : 10.1002/jmv.25884.
- Palmieri L : Characteristics of SARS-CoV-2 patients dying in Italy Rapport basé sur les données disponibles au 16 avril 2020.
- Barbera L, et al : Pourquoi les patients atteints de cancer se rendent-ils au service d’urgence à l’approche de la fin de leur vie ? CMAJ Can. Med. Assoc. J 2010 ; 182 : 563-568.
- Bruera E, et al : The frequency and correlates of dyspnea in patients with advanced cancer. J. Pain Symptom Manage 2000 ; 19 : 357-362.
- Hui D, et al. : Dyspnée chez les patients hospitalisés atteints de cancer avancé : corrélations subjectives et physiologiques. J. Palliat. Med 2013 ; 16 : 274-280.
- Bertran Recasens B, et al : Lack of dyspnea in Covid-19 patients ; another neurological conundrum ? Eur. J. Neurol 2020 ; doi : 10.1111/ene.14265.
- Mitchell GK, et al : Systematic review of general practice end-of-life symptom control. BMJ Support. Palliat. Care 2018 ; 8 : 411-420.
- Parshall MB, et al. : An Official American Thoracic Society Statement : Update on the Mechanisms, Assessment, and Management of Dyspnea. Am. J. Respir. Crit. Care Med 2012 ; 185 : 435-452.
- Sigurgeirsdottir J, et al. : COPD patients’ experiences, self-reported needs, and needs-driven strategies to cope with self-management. Int. J. Chron. Obstruct. Pulmon. Dis 2019 ; 14 : 1033-1043.
- Simon ST, et al. : Episodes d’apnée : types et modèles – une étude qualitative explorant les expériences de patients atteints de maladies avancées. Palliat. Med 2013 ; 27 : 524-532.
- Weingärtner V, et al : Characteristics of episodic breathlessness as reported by patients with advanced chronic obstructive pulmonary disease and lung cancer : Results of a descriptive cohort study. Palliat. Med 2015 ; 29 : 420-428.
- Moens K, et al : Y a-t-il des différences dans la prévalence des problèmes liés aux soins palliatifs chez les personnes souffrant d’un cancer avancé et de huit maladies non cancéreuses ? Une revue systématique. J. Pain Symptom Manage 2014 ; 48 : 660-677.
- Oechsle K, et al. : Symptom burden in palliative care patients : perspectives of patients, their family caregivers, and their attending physicians. Support. Care Cancer Off. J. Multinatl. Assoc. support. Care Cancer 2013 ; 21 : 1955-1962.
- Programme de lignes directrices en oncologie (Deutsche Krebsgesellschaft, Deutsche Krebshilfe, AWMF) : Soins palliatifs pour les patients atteints d’un cancer non curable, version longue 2.1. (2020).
- Campbell ML, et al : A Respiratory Distress Observation Scale for patients unable to self-report dyspnea. J. Palliat. Med 2010 ; 13 : 285-290.
- palliative.ch Dyspnée – Consensus on best practice in Palliative Care in Switzerland – expert group Swiss Society for Palliative Care 2003. (PDF)
- Bausewein C, et al : Non-pharmacological interventions for breathlessness in advanced stages of malignant and non-malignant diseases. Cochrane Database Syst. Rev. 2013.
- Bolzani A, et al : Cognitive-emotional interventions for breathlessness in adults with advanced diseases. Cochrane Database Syst. Rev. 2017 ; doi : 10.1002/14651858.CD012682.
- Kako J, et al : Effet immédiat de la thérapie par ventilateur dans le cancer terminal avec dyspnée au repos : une méta-analyse. Am. J. Hosp. Palliat. Care 2020 ; 37 : 294-299.
- Skoch BM, Sinclair CT : Management of Urgent Medical Conditions at the End of Life. Med. Clin. North Am 2020 ; 104 : 525-538.
- Abdallah SJ, et al : Effect of morphine on breathlessness and exercise endurance in advanced COPD : a randomised crossover trial. Eur. Respir. J 2017 ; 50.
- Mazzocato C, et al : The effects of morphine on dyspnea and ventilatory function in elderly patients with advanced cancer : a randomized double-blind controlled trial. Ann. Oncol. Off. J. Eur. Soc. Med. Oncol 1999 ; 10 : 1511-1514.
- Oxberry SG, et al : Short-term opioids for breathlessness in stable chronic heart failure : a randomized controlled trial. Eur. J. Heart Fail 2011 ; 13 : 1006-1012.
- Barnes H, et al : Opioids for the palliation of refractory breathlessness in adults with advanced disease and terminal illness. Cochrane Database Syst. Rev 2016 ; 3 : CD011008.
- Ferreira DH, et al : Controlled-Release Oxycodone vs Placebo in the Treatment of Chronic Breathlessness-A Multisite Randomized Placebo Controlled Trial. J. Pain Symptom Manage 2020 ; 59 : 581-589.
- Simon ST, et al : EffenDys-Fentanyl Buccal Tablet for the Relief of Episodic Breathlessness in Patients With Advanced Cancer : A Multicenter, Open-Label, Randomized, Morphine-Controlled, Crossover, Phase II Trial. J. Pain Symptom Manage 2016 ; 52 : 617-625.
- Simon ST, et al : Fentanyl for the relief of refractory breathlessness : a systematic review. J. Pain Symptom Manage 2013 ; 46 : 874-886.
- King S, et al. : A systematic review of the use of opioid medication for those with moderate to severe cancer pain and renal impairment : a European Palliative Care Research Collaborative opioid guidelines project. Palliat. Med 2011 ; 25 : 525-552.
- Swart LM, et al : The Comparative Risk of Delirium with Different Opioids : A Systematic Review. Drugs Aging 2017 ; 34 : 437-443.
- Verberkt CA, et al : Respiratory adverse effects of opioids for breathlessness : a systematic review and meta-analysis. Eur. Respir. J 2017 ; 50.
- Simon ST, et al : Benzodiazépines pour le soulagement de l’essoufflement dans les maladies malignes et non malignes avancées chez les adultes. Cochrane Database Syst. Rev 2016 ; 10 : CD007354.
- Navigante AH, et al : Morphine versus midazolam comme traitement de première intention pour contrôler la perception de la dyspnée chez les patients cancéreux alors que sa cause sous-jacente est recherchée ou traitée. J. Pain Symptom Manage 2010 ; 39 : 820-830.
- Haywood A, et al : Systemic corticosteroids for the management of cancer-related breathlessness (dyspnoea) in adults. Cochrane Database Syst. Rev 2019 ; 2 : CD012704.
- Lovell N, et al : Use of mirtazapine in patients with chronic breathlessness : A case series. Palliat. Med 2018 ; 32 : 1518-1521.
- Campbell ML, et al : Oxygen is nonbeneficial for most patients who are near death. J. Pain Symptom Manage 2013 ; 45 : 517-523.
- Baldwin J, Cox J : Traitement de la dyspnée : l’oxygénothérapie est-elle la meilleure option pour tous les patients ? Med. Clin. North Am 2016 ; 100 : 1123-1130.
- Kwon JH, et al : Off-label Medication Use in the Inpatient Palliative Care Unit. J. Pain Symptom Manage 2017 ; 54 : 46-54.
- Fusi-Schmidhauser T, et al : Conservative management of Covid-19 patients – emergency palliative care in action. J. Pain Symptom Manage 2020 ; doi : 10.1016/j.jpainsymman.2020.03.030.
- Lovell N, et al. : Characteristics, symptom management and outcomes of 101 patients with COVID-19 referred for hospital palliative care. J. Pain Symptom Manage 2020 ; doi : 10.1016/j.jpainsymman.2020.04.015.
- Couzin-Frankel J. Le mystère de la ‘happy hypoxia’ de la pandémie. Science 2020 ; 368 : 455-456.
- Hendin A et al. : Soins de fin de vie dans les services d’urgence pour le patient en fin de vie d’une infection respiratoire aiguë hautement transmissible (telle que COVID-19). CJEM 2020 ; 1-4 doi : 10.1017/cem.2020.352.
- Académie Suisse des Sciences Médicales. Faire face à la fin de vie et à la mort 2019.
- Ziegler S, et al. : A. Continuous Deep Sedation Until Death-a Swiss Death Certificate Study. J. Gen. Intern. Med 2018 ; 33 : 1052-1059.
- Twycross R. Réflexions sur la sédation palliative. Palliat. Care 2019 : 12.
- Mazzocato C : Info palliative – Utilisation de la sédation palliative : dimensions cliniques et éthiques 2016.
- Campbell ML, Yarandi HN. Le râle de la mort n’est pas associé à une détresse respiratoire du patient : un traitement pharmacologique est-il indiqué ? J. Palliat. Med 2013 ; 16 : 1255-1259.
- Wildiers H, Menten J : Death rattle : prévalence, prévention et traitement. J. Pain Symptom Manage 2002 ; 23 : 310-317.
- Mercadante S, et al. : Bromure de butyle d’hyoscine pour la prise en charge des râles de la mort : plus tôt que plus tard. J. Pain Symptom Manage 2018 ; 56 : 902-907.
InFo DOULEUR & GERIATRIE 2020 ; 2(1) : 12-17