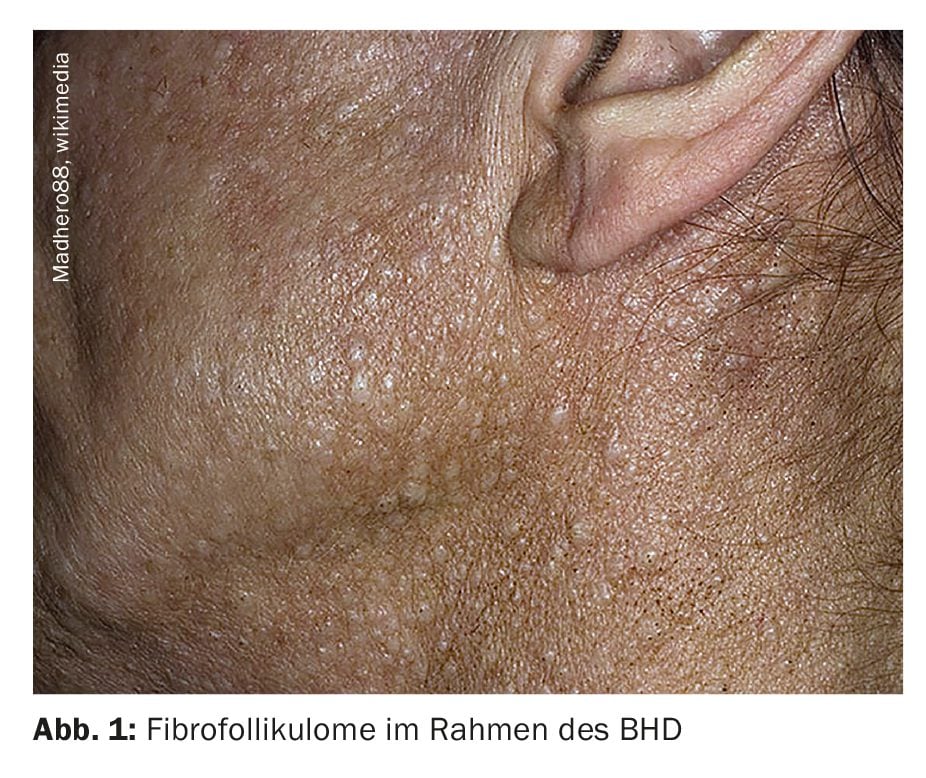
La grande majorité des patients atteints de ce syndrome tumoral héréditaire rare développent de nombreux fibrofolliculomes à l’âge moyen, principalement sur le visage et le torse. Pour confirmer le diagnostic du syndrome de Birt-Hogg-Dubé, il est nécessaire de procéder à une identification génétique. Les personnes concernées doivent être orientées vers un spécialiste des poumons et des reins ainsi que vers un conseil génétique.
Les caractéristiques cutanées de la maladie et le mécanisme de transmission autosomique dominant ont été décrits en 1977 par trois médecins canadiens (Birt, Hogg, Dubé) [1]. Par la suite, de nombreuses descriptions de cas ont montré qu’il pouvait exister une association avec des tumeurs rénales, des kystes pulmonaires et la survenue d’un pneumothorax spontané. La prévalence du syndrome de Birt-Hogg-Dubé (BHD) est estimée à 1/200 000, mais l’incidence exacte est inconnue [2]. La cause du BHD est une mutation du gène FLCN au locus 17p11.2. Ce gène code pour la folliculine. La fonction exacte de cette protéine fait actuellement l’objet de recherches fondamentales. On pense toutefois que FLCN joue un rôle de protéine suppresseur de tumeur. Le diagnostic de BHD est confirmé par la mise en évidence de la mutation génétique par biologie moléculaire. La distribution et la morphologie des kystes à l’imagerie peuvent être indicatives. Typiquement, les kystes pulmonaires ont des parois fines et sont localisés dans les parties basales du poumon, sous-pleurales et paramédiastinales.
Manifestations cutanées et extracutanées
Les lésions cutanées caractéristiques de la BHD sont des fibrofolliculomes. Elles se présentent sous la forme de multiples efflorescences blanchâtres et jaunâtres de 2 à 5 mm de diamètre, qui ne provoquent pas de démangeaisons [1]. La présentation clinique exacte est variable – les tumeurs peuvent se présenter sous forme de plaques relativement discrètes ou de papules plus grandes avec un bouchon corné, rappelant les comédons ou les petits kystes épidermoïdes. Histologiquement, il s’agit de nids de fibroblastes circonscrits avec une accumulation de collagène autour de follicules pileux déformés, à partir desquels des cellules basaloïdes s’étendent dans les tissus environnants. Typiquement, les efflorescences apparaissent généralement sur le visage, le cou et le torse. Le nombre de tumeurs et leur taille augmentent avec le temps. Les angiofibromes et les acrochordons sont d’autres manifestations cutanées fréquentes.
Les manifestations extracutanées possibles de la BHD sont nombreuses [1] :
- Appareil génito-urinaire : risque fortement accru de tumeurs rénales de différentes natures (oncocytomes bénins, carcinomes à cellules rénales et tumeurs mixtes).
- Tractus gastro-intestinal : polypes coliques multiples pouvant dégénérer en carcinomes colorectaux
- Voies respiratoires : kystes pulmonaires, bronchectasies et bulles d’emphysème, hamartomes pulmonaires ; le risque de pneumothorax est environ 50 fois plus élevé en cas de BHD
- Autres : des modifications de l’œil (rétinopathies, glaucome) et de la thyroïde (carcinome de la thyroïde, hypothyroïdie) peuvent également survenir.
Étude de cas
Dans un numéro de l’année dernière de l’Aesthetic Surgery Journal Open Forum, le cas d’une patiente caucasienne de 53 ans qui se plaignait d’une peau irrégulière avec de petites excroissances au niveau du visage et du cou a été décrit. Jusqu’à présent, elles avaient été traitées comme des verrues ordinaires ou des papillomes cutanés [3]. Il n’y avait aucun signe clinique ou de laboratoire d’auto-immunité ou d’immunodéficience. La patiente a déclaré que les problèmes de peau avaient commencé à l’âge de 25 ans et qu’elle avait depuis essayé différents traitements tels que la thérapie au laser, les peelings cutanés, la cryothérapie et les produits topiques.
Apparence clinique : son visage était couvert de zones tachées et hypopigmentées, peut-être en rapport avec les différents traitements utilisés pour éliminer les excroissances cutanées (verrues présumées). La peau du visage, du cou et de l’abdomen était recouverte de nombreuses papules de couleur chair de 2 à 8 mm de diamètre, qui démangeaient occasionnellement. L’aspect correspondait à celui des fibrodermes décrits par Tong et al. décrits dans les fibrofolliculomes [4]. En outre, plusieurs acrochordons ont été observés dans le cou et dans la partie supérieure de la poitrine de la patiente [5]. L’aspect grumeleux et irrégulier, en particulier au niveau du cou, a été considéré comme stigmatisant par la patiente.
Antécédents : l’enquête anamnestique a révélé quatre pneumothorax spontanés dans sa jeunesse et une pleurectomie à l’âge de 30 ans. Elle a également subi l’ablation de plusieurs polypes du côlon dans le passé. Il s’est également avéré que la patiente souffrait d’une dystrophie endothéliale de Fuchs, qui affectait ses deux yeux. A l’âge de 23 ans, elle a subi l’ablation chirurgicale d’un kyste bénin du cuir chevelu et, plus récemment, d’un kyste digital de la muqueuse de la main gauche. Elle a également indiqué qu’on lui avait diagnostiqué un syndrome des ovaires polykystiques, auquel elle attribue ses problèmes de fertilité qui durent depuis sept ans. La patiente a également indiqué qu’il n’y avait pas de BHD connu dans sa famille.
Procédure de diagnostic : Une petite papule de 3 mm de diamètre, de couleur chair et en forme de dôme, a été retirée chirurgicalement du cou et envoyée en pathologie. Selon l’évaluation pathologique, il s’agissait d’un fibrofolliculome qui se présentait comme un follicule central dilaté de manière kystique et entouré de tissu conjonctif lâche. Dans ce cas, la cavité kystique était remplie de dépôts de kératine et tapissée d’un épithélium squameux kératinisant, semblable à l’épiderme normal. La patiente a subi une tomodensitométrie du corps entier, qui a révélé des kystes bénins dans les deux poumons et le rein droit. Le diagnostic clinique de BHD a été posé et la patiente a été invitée à se soumettre à un test génétique pour les mutations du gène FLCN 17p 11.2. Le test génétique s’est révélé positif, confirmant ainsi le diagnostic de BHD. En outre, la patiente a été orientée vers un spécialiste des poumons et des reins ainsi que vers un conseil génétique.
Traitement : pour éliminer les fibrofolliculomes et les papillomes esthétiquement gênants au niveau du cou et de l’abdomen, une intervention électrochirurgicale a été recommandée, tandis que pour le relâchement de la peau et la pigmentation irrégulière, le microneedling a été utilisé avec l’application d’exosomes topiques. L’objectif de cette thérapie combinée était de traiter la structure irrégulière de la peau due au processus de vieillissement et aux traitements antérieurs des fibrofolliculomes. En outre, la thérapie combinée visait à remodeler le tissu dermique superficiel. Le protocole comprenait trois épisodes de traitement à environ un mois d’intervalle :
- Dans un premier temps, dix séries de Michroneedling (Dermapen 4ème génération ; Derma Pen, LLC ; Terrey Hills, Australie) ont été réalisées dans chaque zone (visage, cou, poitrine) à une profondeur de 0,5 à 1,0 mm dans le sens horizontal, vertical et oblique.
- Pendant et après le microneedling, des exosomes topiques (Exocode Radiance ; ExoCoBio, Séoul, Corée du Sud) ont été appliqués en massant délicatement la peau.
La patiente a bien toléré le traitement et a été satisfaite des résultats obtenus jusqu’à présent. Le degré de dépigmentation et la présence de papilomes se sont nettement améliorés. Les améliorations visibles ont été plus rapides sur le visage que sur le cou et le décolleté [6]. Il a été recommandé à la patiente de poursuivre les traitements pendant trois autres séances, en particulier au niveau du cou et du décolleté. Theodorakopoulou et al. notent que les fibrofolliculomes récurrents sont certes inoffensifs et faciles à traiter, mais qu’il est important, en termes de pronostic, d’entreprendre des investigations diagnostiques appropriées en cas de suspicion de BHD.
| Aucun traitement causal n’est disponible à ce jour Comme il n’existe actuellement (en 2024) aucun traitement causal pour cette anomalie génétique, le traitement est exclusivement symptomatique [1]. Les fibrofolliculomes peuvent être enlevés par dermatochirurgie (par exemple par ablation au laser ou par curetage). Les patients sont régulièrement examinés à l’aide de techniques d’imagerie (sonographie, IRM) afin de détecter d’éventuelles tumeurs rénales. Si une tumeur apparaît, une néphrectomie partielle ou totale peut être nécessaire. Si une atteinte pulmonaire survient, elle n’est généralement pas associée à une réduction progressive de la fonction pulmonaire et à une insuffisance respiratoire. |
Conclusion pour la pratique
- Chez >90% des patients atteints du syndrome de Birt-Hogg-Dubé (BHD), de nombreux fibrofolliculomes se manifestent généralement entre 20 et 40 ans.
- Un dépistage ciblé des tumeurs est essentiel pour le pronostic de la BHD, car il existe un risque à vie de 12 à 34% de tumeurs rénales bénignes et malignes.
- Le diagnostic précoce ainsi que le suivi à long terme des familles atteintes de BHD nécessitent une collaboration interdisciplinaire.
- En cas de suspicion clinique, un test génétique pour une mutation dans le gène FLCN au locus 17p11.2 apporte la certitude. Le syndrome BHD se transmet sur le mode autosomique dominant.
Littérature :
- “Syndrome de Birt-Hogg-Dubé”, https://flexikon.doccheck.com,(dernière consultation 12.08.2024).
- “Syndrome de Birt-Hogg-Dubé”, www.orpha.net/de/disease/detail/122,(dernière consultation 12.08.2024).
- Theodorakopoulou E, et al.: Birt-Hogg-Dubé Syndrome: A Rare Genodermatosis Presenting as Skin Papillomas. Aesthet Surg J Open Forum. 2023 Jul 12;5: ojad064. doi: 10.1093/asjof/ojad064.
- Tong Y, et al : Birt-Hogg-Dubé syndrome : a review of dermatological manifestations and other symptoms. Am J Clin Dermatol 2018 ; 19 : 87-101.
- Schmidt LS, Linehan WM: FLCN: the causative gene for Birt-Hogg-Dubé syndrome. Gene 2018; 640: 28–42.
- Ablon G: Safety and effectiveness of an automated microneedling device in improving the signs of aging skin. J Clin Aesthetic Dermatol 2018; 11(8): 29–34.
- Steinlein OK, et al.: Birt-Hogg-Dubé-Syndrom: ein zu selten diagnostiziertes erbliches Tumorsyndrom. J Dtsch Dermatol Ges 2018; 16(3): 278–284.
DERMATOLOGIE PRAXIS 2024; 34(4): 42–43
InFo ONKOLOGIE HÄMATOLOGIE 2024; 12(4): 26–27