Aujourd’hui, le furoate de fluticasone est le corticostéroïde inhalé (CSI) le plus puissant, avec l’indice thérapeutique le plus élevé à ce jour [2,3]. Il fait partie, avec le vilanterol, de Relvar Ellipta. Daley-Yates et al. ont montré que le furoate de fluticasone offre une protection 3,4 fois supérieure à celle des autres CSI, avec des effets systémiques moindres [2,3]. De même, l’étude Salford Lung Study a confirmé que, dans la pratique quotidienne, 25% de patients en plus obtenaient un contrôle pertinent de l’asthme avec Relvar Ellipta qu’avec d’autres contrôleurs [1]. Nous en avons parlé avec le Professeur Dr Laurent Nicod, Clinique privée Hirslanden, Lausanne, et le Dr Jean-Luc Kurzen, médecin-chef, Pneumologie, Hôpital de Männedorf.
Le terme “contrôle de l’asthme” est aujourd’hui utilisé de façon si naturelle que tout le monde pense la même chose – loin de là. Par contrôle de l’asthme, tous les médecins et tous les patients n’entendent pas la même chose [4]. De nombreux médecins surestiment même le degré de contrôle de l’asthme de leurs patients, comme l’a montré une étude [5]. Ce n’était pas le cas pour environ la moitié des asthmatiques considérés comme contrôlés [5]. De même, les patients pensent souvent qu’ils contrôlent leur asthme en adaptant leur mode de vie à la charge des symptômes [4]. Ils évitent les activités physiques, souffrent de symptômes diurnes et de réveils nocturnes dus à l’essoufflement et/ou à la toux, et sont dépendants de leur médication d’urgence [4]. De facto, jusqu’à 71 % des patients ne parviennent pas à contrôler leur asthme malgré le traitement [1]. Cela souligne l’importance d’un contrôle proactif de l’asthme qui évite les symptômes et améliore ainsi la qualité de vie [6].
Proactif plutôt qu’axé sur les symptômes
Si le traitement s’oriente uniquement sur les symptômes actuels, l’objectif d’un bon contrôle de l’asthme n’est pas atteint [7]. Dans les MART
*
– le contrôle des symptômes est basé sur la perception des patients, et celle-ci laisse souvent à désirer [4,7]. Contrairement à la MART, la méthode proactive Le traitement par Relvar Ellipta traite à la fois les symptômes et l’inflammation chronique, le remodelage des voies respiratoires et l’hyperréactivité bronchique [8].
Le Relvar Ellipta augmente notamment le nombre de jours et de nuits sans symptômes par rapport au furoate de fluticasone ou au propionate de fluticasone [9]. Les patients peuvent bénéficier de cette gestion proactive de l’asthme en reprenant leurs activités quotidiennes, comme le souligne également le professeur Nicod dans son interview [9].
L’étude Salford Lung Study est une étude phare [1].
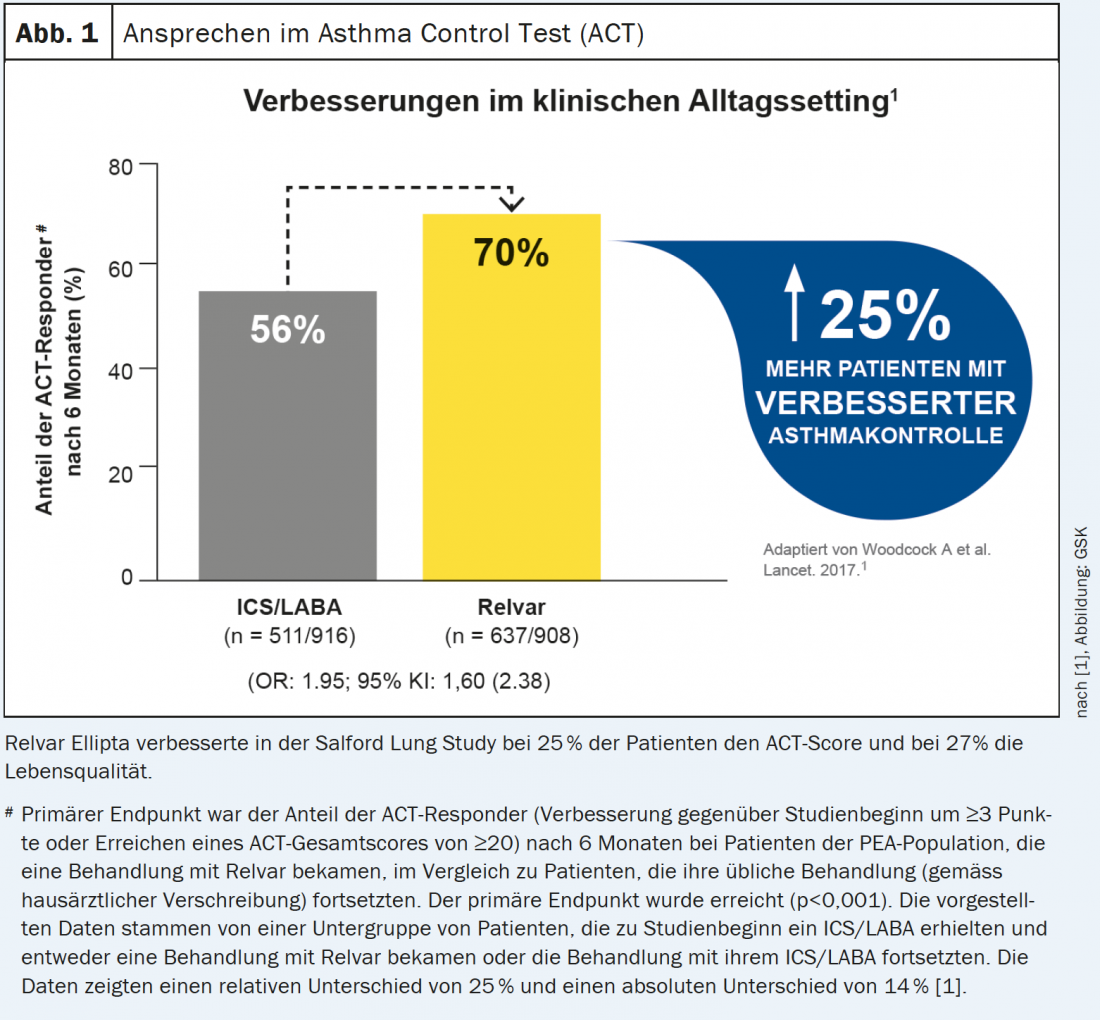
L’étude Salford Lung Study, une étude en vie réelle, a inclus 4233 patients souffrant d’asthme insuffisamment contrôlé, randomisés pour recevoir soit Relvar Ellipta, soit le traitement précédent (CSI ou CSI/LABA) pendant 52 semaines, avec possibilité d’optimisation si nécessaire [1]. Critère d’évaluation principal : obtention d’un score ACT (Asthma Control Test) >20 ou amélioration du score de ≥3 points après 24 semaines [1].
Résultats
- Le contrôle proactif de l’asthme a permis d’améliorer le contrôle au quotidien chez 25% de patients en plus (56% dans le groupe témoin vs 70% sous Relvar Ellipta) [1] (Fig. 1).
- Outre les symptômes, la qualité de vie s’est améliorée chez 27% de patients en plus [1,10].
- Le profil d’effets indésirables dans les deux bras de l’étude était comparable, les pneumonies étant rares [1].
Un indice thérapeutique élevé, une étape importante
Le furoate de fluticasone dans Relvar a un indice thérapeutique nettement plus élevé que les autres CSI, ce qui permet d’obtenir un effet anti-inflammatoire plus important avec une exposition systémique plus faible [2,3]. Ainsi, à la dose la plus faible, il présente un effet anti-inflammatoire 3,4 fois supérieur à celui du budésonide [2,3]. Utilisé une fois par jour, Relvar dans le dispositif Ellipta offre une valeur ajoutée que les patients ressentent immédiatement, à savoir que l’inflammation des voies respiratoires diminue [8], l’hyperréactivité bronchique diminue [8] et le remodelage dans les voies respiratoires est freiné [8].
Amélioration de la qualité de vie
L’effet perceptible, qui se manifeste par une amélioration de toutes les composantes de l’ACT, est contrebalancé par des effets systémiques indésirables très faibles [10]. En particulier, les patients ont bénéficié d’une amélioration significative de leur qualité de vie [10].



Mentions légales
texte :
Dr. Renate Weber
Première publication :
Medical Tribune 40/2021. Les personnes interviewées sont d’accord avec la deuxième publication. Tribune Médicale
Cet article a été rédigé avec l’aimable soutien de GlaxoSmithKline AG, Talstrasse 3-5, 3053 Münchenbuchsee.
PM-CH-FFV-ADVR-210003-11/2021
Prime Public Media AG, Zurich 2021
Littérature :
1. Woodcock A, et al : Efficacité du furoate de fluticasone plus vilanterol sur le contrôle de l’asthme en pratique clinique : un essai contrôlé randomisé, en groupes parallèles et en ouvert. Lancet 2017 ; 390 : 2247-2255.
2. Daley-Yates P : Inhaled corticosteroids : potency, dose equivalence and therapeutic index. BJCP 2015 ; 80(3) : 372-380.
3. Daley-Yates P, et al : Therapeutic index of inhaled corticosteroids in asthma : A dose-response comparison on airway hyperresponsiveness and adrenal axis suppression. BJCP 2021 ; 87 : 483-493.
4 Fletcher M, Hiles D : Continuing discrepancy between patient perception of asthma control and real world-symptoms : a quantitative online survey of 1.083 adults with asthma from the UK. Prim Care Respir J 2013 ; 22 : 431-438.
5. Greenblatt M, et al : Comparaison de l’évaluation du contrôle de l’asthme par le médecin et le patient. Respiratory Medicine 2010 ; 104(3) ; 356-361.
6. Correira de Sousa J, et al : Contrôle de l’asthme, qualité de vie, et le rôle de l’habilitation du patient : une étude observationnelle transversale. Prim Care Respir J 2013 ; 22(2) : 181-187.
7. Chapman KR, et al : Single maintenance and reliever therapy (SMART) of asthma : a critical appraisal. Thorax 2021 ; 65 : 47-52.
8. Ishmael FT : La réponse inflammatoire dans la pathogenèse de l’asthme. The Journal of the American Osteopathic Association 2011 ; 111 : S11-S17.
9. Kerwin E, et al : Fluticasone furoate/vilanterol once daily improves nighttime awakenings in asthma patients with night symptoms : Post-hoc analysis of three randomized controlled trials. J Asthma 2018 ; 55 : 890-897.
10. Svedsater H, et al : Patient-reported outcomes with initiation of flutucasone furoate/vilanterol versus continuing usual care in the Salford Lung Study. Respir Med 2018 ; 141 : 198-206.
11. Katsaounou P, et al : Omalizumab as alternative to chronic use of oral corticosteroids in severe asthma. Respir. Med. 2019 ; 150 : 51-62.
12 Wells KE, et al. : Real-world effects of once vs. greater daily inhaled corticosteroid dosing on medication adherence. Ann. Allergy, Asthma Immunol. 2013 ; 111 : 216-220.
13. Molimard M, et al : Chronic obstructive pulmonary disease exacerbation and inhaler device handling : real-life assessment of 2935 patients. Eur Respir J 2017 ; 49(2) : 1601794.
Relvar Ellipta (poudre monodose pour inhalation). W : Fluticasone furoate 92 ou 184 μg, vilanterol 22 μg. I : Asthme bronchique : traitement régulier chez les adultes et les adolescents de 12 ans et plus si symptomatique sous CSI et bronchodilatateur de courte durée d’action. BPCO : traitement symptomatique chez les patients avec VEMS
1
<70% et ≥2 exacerbations au cours des 12 derniers mois. D: Asthme bronchique : adultes et adolescents à partir de 12 ans : 1×/jour. 1 inhalation de Relvar Ellipta 92/22 ou 184/22. BPCO : adultes à partir de 40 ans : 1×/jour 1 inhalation de Relvar Ellipta 92/22. Relvar Ellipta 184/22 n’est pas approuvé pour la BPCO.
KI :
Hypersensibilité à l’un des ingrédients, allergie sévère aux protéines de lait. W/V : Ne pas utiliser pour le traitement des symptômes aigus de l’asthme ou des exacerbations aiguës de la BPCO. En cas de bronchospasme paradoxal, traiter immédiatement avec un bronchodilatateur de courte durée d’action, arrêter Relvar Ellipta, envisager d’autres traitements. Possibilité d’effets cardiovasculaires tels que des arythmies ; avant le traitement, vérifier la présence de maladies cardiovasculaires concomitantes (il est notamment recommandé d’effectuer un ECG pour vérifier l’allongement de l’intervalle QTc). Prudence en cas de diabète, de tuberculose pulmonaire, d’infections chroniques/non traitées. Relvar Ellipta 184/22 ne doit pas être utilisé en cas d’altération modérée ou sévère de la fonction hépatique. Des effets indésirables systémiques peuvent survenir à des doses élevées et prolongées. L’utilisation de corticostéroïdes par voie systémique et topique peut entraîner des troubles de la vision et il convient d’envisager d’orienter le patient vers un ophtalmologue pour évaluer les causes possibles. Les cas de pneumonie ont été plus fréquents chez les patients atteints de BPCO sous Relvar Ellipta. Chez les patients asthmatiques, les pneumonies ont été plus fréquentes avec Relvar Ellipta 184/22 qu’avec Relvar Ellipta 92/22 ou un placebo. IA : Prudence en cas d’administration concomitante de β-bloquants, ainsi que de médicaments qui allongent l’intervalle QTc, ont des effets sympathomimétiques ou influencent les taux de potassium. L’administration concomitante d’inhibiteurs puissants du CYP3A4 (par ex. kétoconazole, itraconazole, clarithromycine, ritonavir ou produits contenant du cobicistat) doit être évitée, sauf si le bénéfice l’emporte sur le risque accru d’effets indésirables systémiques liés aux corticostéroïdes ; dans ce cas, les patients doivent être surveillés pour les effets indésirables systémiques liés aux corticostéroïdes. S/E : Grossesse : Relvar Ellipta ne doit pas être utilisé pendant la grossesse, sauf si cela est clairement nécessaire. Allaitement : arrêtez l’allaitement ou le traitement par Relvar Ellipta. EI : Très fréquent : maux de tête, rhinopharyngite. Fréquent : pneumonie , infection des voies respiratoires supérieures, bronchite, symptômes grippaux, douleur ou candidose dans la bouche et la gorge, sinusite, pharyngite, rhinite, toux, enrouement, douleurs abdominales, articulaires, dorsales, fractures, pyrexie. Occasionnellement : extrasystoles. Expériences post-marketing : fréquent : crampes musculaires ; occasionnel : palpitations, tachycardie, hyperglycémie ; rare/inconnu : Réactions d’hypersensibilité (y compris anaphylaxie, œdème de Quincke, urticaire, rash), tremblements, anxiété, bronchospasme paradoxal. AK : B, admissible par les caisses. Mise à jour de l’information : Janvier 2019. GlaxoSmithKline AG, 3053 Münchenbuchsee. Vous trouverez des informations détaillées sur www.swissmedicinfo. ch. Veuillez signaler les effets indésirables des médicaments à l’adresse pv.swiss@gsk.com. Les professionnels peuvent demander les références mentionnées à GlaxoSmithKline AG.