Les infections de prothèses prennent de plus en plus d’importance en raison d’un nombre croissant de prothèses primaires. Le médecin généraliste est généralement le premier interlocuteur des patients lorsque des symptômes apparaissent au niveau d’une prothèse. En cas d’infection par tout type de matériel étranger dans l’organisme, il est essentiel de prendre les mesures diagnostiques et thérapeutiques appropriées dans les plus brefs délais, car la durée de l’infection est déterminante pour le traitement possible ou son succès.
Les infections de prothèses prennent de plus en plus d’importance en raison d’un nombre croissant de prothèses primaires. Le médecin généraliste est généralement le premier interlocuteur des patients lorsque des symptômes apparaissent au niveau d’une prothèse. En cas d’infection par tout type de matériel étranger dans l’organisme, il est essentiel de prendre les mesures diagnostiques et thérapeutiques appropriées dans les plus brefs délais, car la durée de l’infection est déterminante pour le traitement possible ou son succès. Il est donc important d’avoir une connaissance approfondie des différents types d’infections et une vue d’ensemble des traitements pour assurer le suivi de ces patients en médecine générale.
Type d’infection
Les infections peuvent provenir soit de l’extérieur, à la suite d’une opération ou d’une blessure, c’est-à-dire de manière exogène, soit d’une dissémination hématogène à partir d’un autre site d’infection dans l’organisme. C’est pourquoi, en cas de suspicion d’infection de prothèse, il est toujours important de rechercher activement d’éventuels foyers infectieux et de les exclure ou de les confirmer à l’aide des moyens de diagnostic appropriés. Les localisations typiques des foyers infectieux disséminés sont les poumons, la vessie, le tractus gastro-intestinal ainsi que les ulcères chroniques du pied. En outre, il faut également penser à l’endocardite ou à l’ostéomyélite (par exemple des corps vertébraux). Cette liste n’est pas exhaustive, mais comprend les causes qui doivent être exclues par un examen clinique et instrumental approfondi. Connaître la nature de l’infection (exogène ou hématogène) est un facteur important pour le traitement ultérieur, tout comme la durée de l’infection.
Durée de l’infection
Dans les trois premiers mois suivant l’implantation d’une prothèse, on parle d’infection précoce, et à partir de 24 mois après l’implantation, d’infection tardive. Entre les deux, il y a une phase intermédiaire qui ne peut être raisonnablement divisée et traitée qu’en tenant compte du type d’infection et du germe. Les infections précoces ont plutôt des causes exogènes (c’est-à-dire dans le cadre de l’implantation) et les infections tardives plutôt des causes hématogènes.
Une autre possibilité de classification en infection aiguë versus infection chronique est nettement plus décisive pour le traitement que la référence temporelle à l’opération index. Les infections aiguës sont considérées comme telles si elles surviennent dans les 4 semaines suivant l’opération index ou si elles sont symptomatiques à tout moment par la suite depuis 3 semaines maximum. Tous les autres cas d’infection sont traités comme des cas chroniques. Cette classification est importante dans la mesure où le maintien de la prothèse est possible pendant cette période. Après cela, le taux d’échec de cette procédure augmente considérablement, de sorte qu’il est généralement recommandé de changer complètement la prothèse [1].
Articulation touchée
Pour suspecter en premier lieu une infection de prothèse, l’examinateur initial doit connaître les différentes présentations d’une telle infection sur les différentes articulations. Le genou et la cheville réagissent souvent par un gonflement, une rougeur et un échauffement significatifs. En revanche, l’épaule et la hanche sont moins faciles à appréhender cliniquement, car il existe également un manteau de tissus mous plus important. Dans ce cas, la douleur et, le cas échéant, la limitation des mouvements sont généralement au premier plan. Cependant, toutes les articulations peuvent être le siège d’infections dites “de bas grade”, dont la présentation clinique initiale est généralement très subtile [2].
Diagnostic
Une anamnèse et un examen physique approfondis constituent la base du diagnostic, mais ils sont malheureusement souvent négligés au profit de l’utilisation d’appareils. Les principaux systèmes à étudier ont été énumérés plus haut. Il convient toutefois de souligner que les petites lésions doivent également être activement recherchées comme porte d’entrée, en particulier au niveau des pieds (plante des pieds, espaces entre les orteils). Souvent, les patients eux-mêmes ne les remarquent pas (par exemple en raison d’une sensibilité réduite). Des examens de laboratoire (leucocytes, CRP, interleukine-6, hémogramme, analyse/culture d’urine) ainsi que des examens radiologiques de l’articulation concernée et, le cas échéant, des poumons, sont ensuite indiqués [3].
Des valeurs élevées de leucocytes et de CRP peuvent indiquer une infection, selon le moment postopératoire. Les valeurs normales n’excluent toutefois pas une infection. Par exemple, en cas d’infection par Proprionibacterium acnes, on ne constate pas d’augmentation de la CRP dans 75% des cas, ni du nombre de leucocytes dans 93% des cas [4].
De nombreux germes dits de bas niveau se comportent de manière similaire. La radiographie de l’articulation concernée doit rechercher des signes de relâchement, d’épanchement ou de poches d’air, qui sont des signes indirects d’infection. En outre, cela permet d’exclure le diagnostic différentiel d’une fracture périprothétique.
La ponction articulaire est maintenant traitée comme l’instrument le plus important pour le diagnostic de l’infection. Celle-ci, qui comporte elle-même un risque d’infection, ne doit être réalisée qu’en cas de suspicion raisonnable d’infection articulaire. Un champ stérile, des gants stériles et, si possible, une petite table stérile sont fortement recommandés. L’anesthésie locale peut entraîner une contamination de la zone d’injection et fausser le résultat de la culture si elle est appliquée trop profondément. Elle ne doit être pratiquée que si elle est absolument nécessaire et uniquement par voie intradermique. Pour éviter toute contamination par des germes cutanés, il est recommandé de pratiquer une incision par piqûre à l’aide d’un scalpel pointu. La ponction proprement dite est ensuite réalisée en profondeur à travers ce site cutané déjà ouvert. Le point est analysé en termes de différenciation et de nombre de cellules, de microbiologie et de cristaux. Malheureusement, la sensibilité de la ponction de l’épaule, par exemple, est plutôt mauvaise (33%), de sorte que les échantillons peropératoires gagnent ici en importance. Les ponctions de la hanche et du genou ont une bien meilleure sensibilité, d’environ 90% [5,6].
Techniquement, cela est certainement réalisable par un médecin généraliste, mais il est préférable de laisser la ponction au chirurgien qui, le cas échéant, pratiquera également la thérapie chirurgicale. En effet, ce dernier peut discuter des possibilités de diagnostic de manière interdisciplinaire avec l’infectiologue compétent et peut également évaluer directement le point au niveau macroscopique. En cas de ponction par un médecin généraliste, ces observations “secondaires”, qui sont pourtant en partie importantes pour la procédure finale, passent inaperçues. En outre, il peut y avoir des retards dans la transmission des résultats.
Globalement, en ce qui concerne le diagnostic, il faut retenir que dans certains cas, lorsque les signes d’infection sont fulminants et que le germe est détecté dans la ponction, le diagnostic est simple et clair. Malheureusement, il arrive au moins aussi souvent que le diagnostic soit difficile. Par exemple, en cas d’absence de détection de germes suite à une ponction sèche ou chez des patients déjà traités par antibiotiques. C’est surtout dans ces cas qu’il faut faire appel le plus rapidement possible à un spécialiste avec une équipe interdisciplinaire afin de pouvoir exploiter au mieux toutes les mesures diagnostiques.
Spectre de germes
Dans cette section, nous n’aborderons pas explicitement les différents agents pathogènes, mais nous rappellerons brièvement qu’il existe en principe deux types d’agents pathogènes. Le premier groupe est facilement identifiable et attire l’attention par une inflammation massive, des paramètres de laboratoire élevés, la formation de pus, la fièvre et finalement la septicémie. Dans ces cas, il est nécessaire d’agir rapidement afin d’écarter la menace potentiellement vitale pour le patient.
Le second groupe est plus subtil, souvent “seule” la douleur ou le gonflement sont des symptômes cliniques. Les résultats de laboratoire peuvent être normaux et la détection des germes est difficile en raison d’une croissance lente. Les causes en sont généralement les germes “de bas niveau” mentionnés plus haut, ou encore des champignons. Malgré une évolution primaire peu fulminante, de telles infections peuvent également se terminer par une septicémie. Dans tous les cas, ils provoquent une gêne évidente pour les patients. Dans ce cas, il est surtout nécessaire d’agir rapidement pour éviter un changement complet de la prothèse (qui présente un risque évident de complications). Les prothèses d’épaule sont ici particulièrement menacées, car les infections de bas grade sont nettement plus fréquentes au niveau de l’épaule que des autres articulations [7].
Thérapie chirurgicale
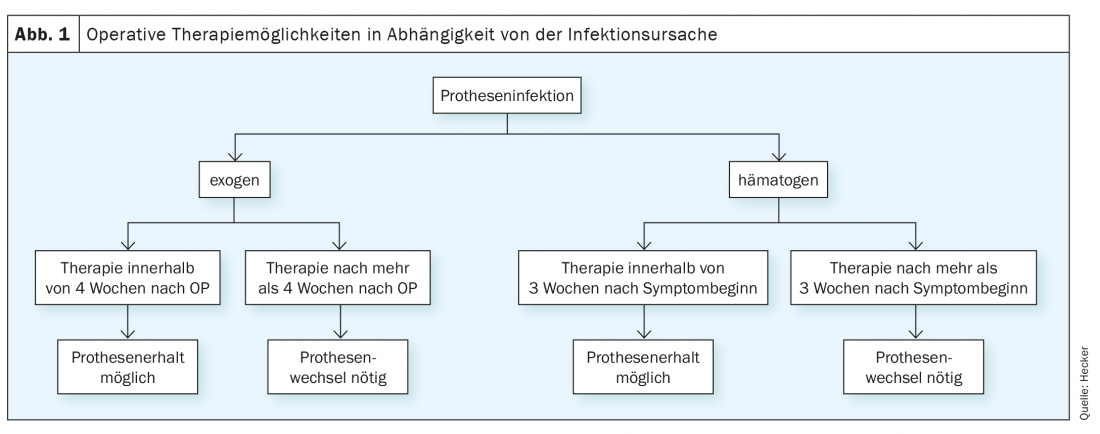
En cas d’infection articulaire confirmée, l’assainissement chirurgical est la base du traitement. Il existe ici différents niveaux d’escalade, qui peuvent être choisis en fonction de la durée de l’infection, du germe, de la situation des tissus mous et des comorbidités (Fig. 1).
Débridement soigneux avec synovectomie complète et changement de toutes les parties mobiles (surtout l’inlay en polyéthylène). Cette méthode, également connue sous le nom de DAIR (débridement, antibiotiques, rétention d’implant), a un taux de réussite de 30 à 100 % lorsqu’elle est appliquée à des infections aiguës. En cas d’infection chronique, la plupart des études estiment que les chances de succès sont inférieures à 50%, c’est pourquoi cette intervention n’est alors réalisée que dans des cas exceptionnels. Pour tous les cas qui ne peuvent pas être traités dans l’intervalle correspondant, un changement complet de la prothèse est indiqué [8].
Le remplacement de la prothèse en un temps représente l’étape suivante de l’escalade et peut être effectué si le germe est connu, si la circulation sanguine et les tissus mous sont bons et si les comorbidités sont faibles. Par rapport au DAIR, il s’agit toutefois d’une intervention beaucoup plus importante, car le retrait de la prothèse en cas d’assise fixe est généralement coûteux et une perte osseuse peut également survenir dans ce cas. Une telle perte osseuse doit être compensée à grands frais, ce qui nécessite souvent des implants de révision avec une distance d’ancrage plus longue [9].
L’option la plus sûre, qui est recommandée comme gold standard en cas de doute, est le changement de prothèse en deux temps. Dans ce cas, la première intervention consiste à retirer la prothèse, à procéder à un débridement approfondi et à mettre en place une prothèse en ciment chargée d’antibiotiques pour maintenir l’espace. La remise en place d’une prothèse se fait alors après un intervalle court (environ 4 semaines) ou long (environ 3 mois), selon le germe et la situation des tissus mous. Pendant cette période, il n’est pas possible de solliciter le membre concerné, ce qui représente pour le patient une limitation physique massive et également un stress psychologique [10].
Les autres options, qui ne seront pas abordées ici, sont l’extension permanente de l’articulation (situation de Girdlestone) et l’arthrodèse.
Traitement antibiotique
Chacune des thérapies chirurgicales décrites ci-dessus n’est efficace que si elle est suivie d’un traitement antibiotique. Celle-ci ne doit être commencée qu’en cas d’urgence (patient septique) avant les premiers soins chirurgicaux, car cela peut rendre la détection des germes plus difficile, voire impossible. La connaissance de l’agent pathogène est toutefois déterminante pour le succès du traitement et doit donc être absolument respectée ! Si le germe est déjà connu grâce à une ponction préalable, il est possible de déroger à cette règle après avoir consulté les infectiologues.
Après la première opération, le patient reçoit généralement un traitement antibiotique intraveineux de deux semaines qui, si le germe est inconnu, est initié en premier lieu de manière empirique, puis modifié de manière ciblée après réception des résultats bactériologiques. La durée totale du traitement antibiotique est généralement comprise entre 3 et 6 mois [10].
Il convient ici de rappeler explicitement qu’en cas d’infection de la prothèse (par ex. en cas de troubles de la cicatrisation après l’implantation), un traitement antibiotique empirique initié par le médecin généraliste est contre-indiqué.
Exemples de cas avec erreurs possibles de diagnostic et de traitement
2 semaines après l’implantation d’un KTP, la plaie présente une sécrétion persistante. Un traitement antibiotique oral empirique est instauré, puis la plaie se referme. Après 6 semaines, un gonflement et une rougeur massifs ainsi qu’une douleur intense apparaissent. La ponction révèle la présence de pus.
–> Il s’agit d’une infection aiguë après implantation. Si le diagnostic avait été correctement posé 2 semaines après l’opération, celle-ci aurait pu être traitée par débridement chirurgical et traitement antibiotique tout en conservant la prothèse. Cependant, 6 semaines après l’opération, un changement complet de la prothèse est nécessaire. Le traitement peut en outre être plus difficile et un changement en deux temps peut être nécessaire, car le traitement antibiotique peut ne pas permettre de détecter les germes.
6 ans après l’implantation de sa prothèse, un patient se présente chez son médecin généraliste et signale des douleurs aiguës au niveau de la prothèse depuis 2 semaines. Le médecin généraliste établit un diagnostic correct au moyen de radiographies, d’examens de laboratoire et d’une ponction qu’il effectue lui-même. Le laboratoire et les radiographies sont normaux, le prélèvement montre un nombre élevé de cellules, mais le praticien souhaite attendre le résultat de la culture avant de procéder à un transfert. 10 jours plus tard, la culture révèle un germe de bas niveau qui a probablement été introduit dans le système par une ouverture au pied. Le transfert est maintenant effectué. 6 semaines après le début des symptômes, le patient se présente finalement à une consultation orthopédique.
–> En soi, le médecin généraliste a initié un diagnostic complet et correct, il n’a simplement pas tenu compte du facteur temps. Cependant, cela signifie qu’un traitement de préservation de la prothèse, qui aurait été prometteur au cours des 3 premières semaines, ne peut plus être effectué. Par conséquent, un changement de prothèse doit désormais être effectué avec un surcoût important (à la fois pour le patient et sur le plan socio-économique).
Littérature :
- Izakovicova P, Borens O, Trampuz A : Infection périprothétique des articulations : concepts actuels et perspectives. EFORT Open Rev 2019 ; 4 : 482-494.
- Romano CL, Khawashki HA, Benzakour T, et al : The W.A.I.O.T. Definition of High-Grade and Low-Grade Peri-Prosthetic Joint Infection. J Clin Med 2019 ; 8 : 650.
- Li C, Renz N, Trampuz A : Prise en charge de l’infection de la jonction périprothétique. Hip Pelvis 2018 ; 30 : 138-146.
- Topolski MS, Chin PY, Sperling JW, et al : Révision de l’arthroplastie de l’épaule avec cultures peropératoires positives : la valeur des études préopératoires et de l’histologie peropératoire. J Shoulder Elbow Surg 2006 ; 15 : 402-406.
- Hecker A, Jungwirth-Weinberger A, Bauer MR, et al : The accuracy of joint aspiration for the diagnosis of shoulder infections. J Shoulder Elbow Surg 2020 ; 29 : 516-520.
- Yee DK, Chiu KY, Yan CH, et al : Review article : Joint aspiration for diagnosis of periprosthetic infection. J Orthop Surg (Hong Kong) 2013 ; 21 : 236-240.
- Cooper ME, Trivedi NN, Sivasundaram L, et al : Diagnostic et prise en charge de l’infection de la jonction périprothétique après une arthroplastie de l’épaule. JBJS Rev 2019 ; 7 : e3.
- Di Benedetto P, Di Benedetto ED, Salviato D, et al : Infection aiguë du genou périprothétique : y a-t-il encore un rôle pour le DAIR ? Acta Biomed 2017 ; 88 : 84-91.
- Pangaud C, Ollivier M, Argenson JN : Résultat d’un échange en une ou deux journées pour une arthroplastie de révision du genou en cas d’infection périprothétique chronique. EFORT Open Rev 2019 ; 4 : 495-502.
- Kuzyk PR, Dhotar HS, Sternheim A, et al : Two-stage revision arthroplasty for management of chronic periprosthetic hip and knee infection : techniques, controverses, and outcomes. J Am Acad Orthop Surg 2014 ; 22 : 153-164.
PRATIQUE DU MÉDECIN DE FAMILLE 2021 ; 16(2) : 10-13











