Pas de congrès de l’ESC sans nouvelles études sur le traitement antithrombotique après une intervention coronarienne percutanée. Récemment, la monothérapie avec un bloqueur de P2Y12 est devenue une alternative intéressante à la double antiagrégation plaquettaire (DAPT) avec un bloqueur de P2Y12 et un ASA, en raison d’un risque hémorragique plus faible. L’étude STOPADAPT-3 vise à déterminer s’il est possible de se passer totalement d’ASS dans ce contexte [2].
Les patients souffrant d’un syndrome coronarien aigu (SCA) auraient un risque plus élevé d’événements ischémiques [3]. Par conséquent, les lignes directrices actuelles recommandent des inhibiteurs des récepteurs P2Y12 plus récents et plus efficaces, comme le ticagrelor et le prasugrel, chez les patients atteints de SCA, tandis que le clopidogrel reste recommandé chez les patients atteints de maladie coronarienne stable (MCS) [4,5]. Chez les patients atteints de SCA, les lignes directrices actuelles recommandent également l’utilisation d’anticoagulants avant une intervention coronarienne percutanée (ICP), l’administration d’antiplaquettaires et un traitement antiplaquettaire double (DAPT) prolongé en l’absence de risque hémorragique élevé [4,5]. En outre, l’accès transfémoral est souvent choisi pour l’ICP en cas de SCA, et il a été signalé qu’il était associé à un risque de saignement plus élevé [6]. Par conséquent, les patients atteints de SCA peuvent également présenter un risque de saignement plus élevé que les patients souffrant d’une maladie coronarienne stable. Néanmoins, la présentation clinique de l’ACS n’a pas été incluse comme critère dans l’Academic Research Consortium (ARC)-HBR, notamment parce qu’il n’existait pas d’études antérieures comparant le risque de saignement après ICP entre les patients atteints d’ACS et les patients coronariens stables [7].
Une méta-analyse d’essais randomisés portant sur des patients atteints de SCA a rapporté que la nouvelle génération de stents recouverts de médicaments (DES) réduisait le risque à long terme de thrombose de stent, d’infarctus du myocarde et de décès cardiaque par rapport aux stents à métal nu [8]. L’équilibre entre le risque d’ischémie et le risque de saignement après une ICP chez les patients atteints de SCA pourrait avoir été considérablement modifié à l’ère de la nouvelle génération de DES.
Conception et résultats de STOPDAPT-3
L’objectif de STOPDAPT-3 était de déterminer si l’arrêt précoce du DAPT après l’implantation d’un DES dans le cadre d’un SCA avec RBH pouvait réduire les saignements graves sans augmenter le risque de complications cardiovasculaires.
Parmi les 13 258 patients, 5521 patients (42%) présentaient un SCA (groupe SCA) et 7737 patients (58%) présentaient une coronaropathie stable (groupe coronaropathie stable). Le groupe ACS comprenait 4081 patients (74%) atteints de STEMI et 1440 patients (26%) atteints de SCA non ST (NSTEACS), dont 1235 patients (22%) atteints de NSTEMI et 205 patients (3,7%) atteints d’EI. Les patients ont été répartis en quatre groupes combinés sur la base de la présentation clinique (SCA, coronaropathie stable) et de la présence d’ARC-HBR (SCA/HBR : 2502 patients ; SCA/No-HBR : 3019 patients ; coronaropathie stable/HBR : 3905 patients ; coronaropathie stable/No-HBR : 3832 patients).
Caractéristiques de base : ACS vs. coronaropathie stable
Dans la population étudiée ici, 48% des patients présentaient un ARC-HBR. Les patients du groupe ACS étaient plus jeunes, souvent des hommes et des fumeurs, avaient un indice de masse corporelle plus faible et souffraient plus souvent d’insuffisance cardiaque et de fragilité sévère que les patients du groupe ACS stable.
En ce qui concerne les caractéristiques procédurales, le nombre total de stents était plus important, la longueur totale des stents plus longue et la taille minimale des stents plus petite dans le groupe coronarien stable que dans le groupe ACS. La voie transfémorale a été choisie plus fréquemment dans le groupe ACS que dans le groupe coronarien stable. En outre, les patients du groupe SCA ont reçu plus fréquemment des statines, des β-bloqueurs, des inhibiteurs de l’enzyme de conversion de l’angiotensine/bloqueurs des récepteurs de l’angiotensine II, des anticoagulants oraux et des inhibiteurs de la pompe à protons/bloqueurs H2 que les patients du groupe coronarien stable. La prévalence d’un traitement par statine à haute intensité était très faible dans les deux groupes.
Résultats cliniques à long terme : ACS vs. coronaropathie stable
La durée médiane de suivi pour les survivants était de 6,0 ans et des données de suivi clinique complètes à 1, 3 et 5 ans ont été recueillies pour 96,9%, 93,4% et 78,6% des patients, respectivement. L’incidence cumulée de l’interruption permanente du DAPT était significativement plus élevée dans le groupe ACS que dans le groupe coronarien stable, ce qui suggère que la durée du DAPT était significativement plus courte dans le groupe ACS que dans le groupe coronarien stable.
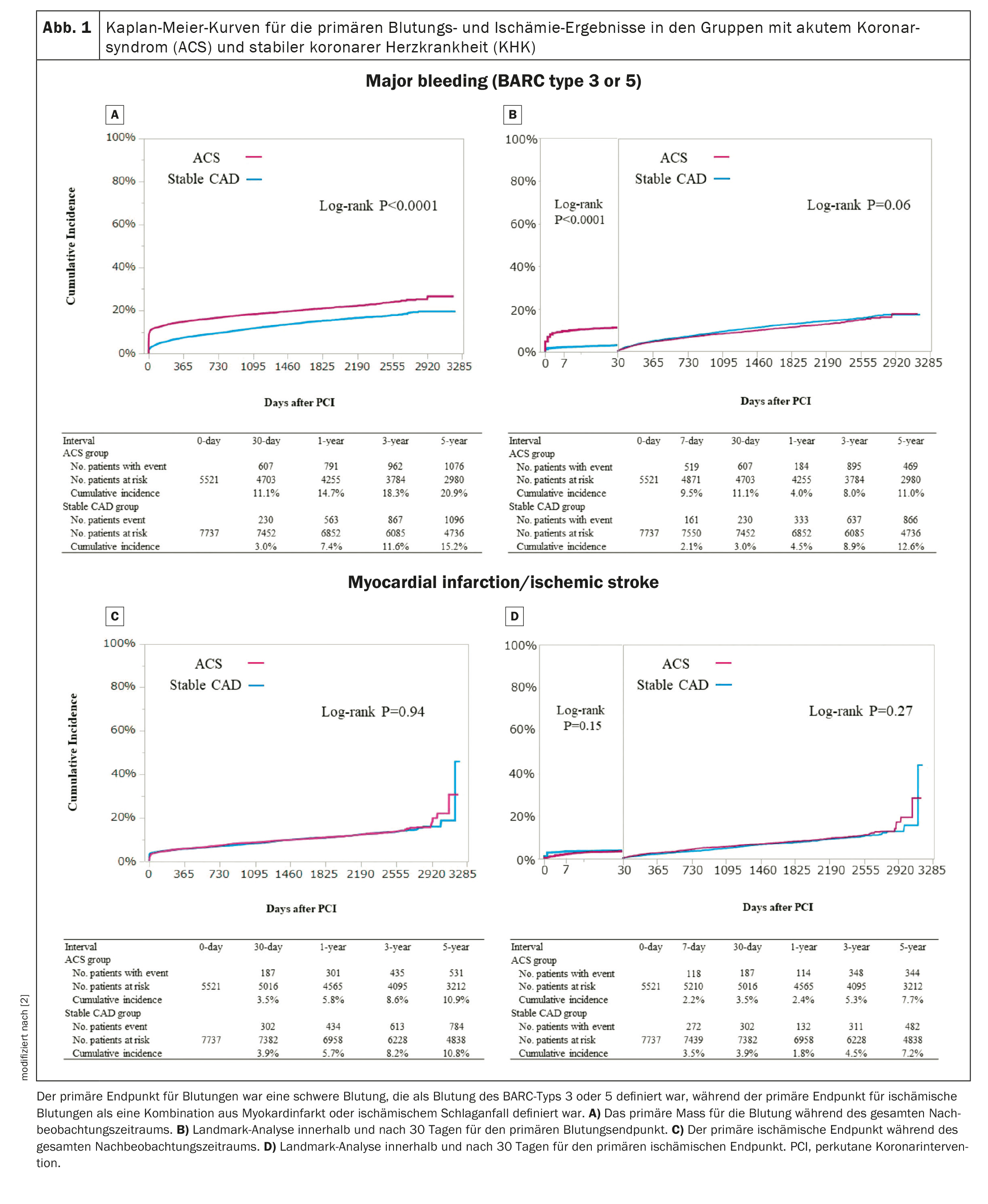
L’incidence cumulée sur 5 ans du résultat primaire de l’hémorragie (BARC type 3 ou 5 hémorragies) était significativement plus élevée dans le groupe ACS que dans le groupe coronarien stable (figure 1A) [2]. Dans l’analyse de Landmark à 30 jours, l’incidence cumulée du résultat primaire de l’hémorragie dans les 30 jours était également nettement plus élevée dans le groupe ACS que dans le groupe coronarien stable (figure 1B) [2]. Après ajustement des facteurs confondants, l’augmentation du risque de SCA par rapport à l’IC stable est restée significative pour la mesure primaire du saignement pendant toute la période de suivi et dans les 30 jours, alors qu’elle n’était plus significative après 30 jours. En ce qui concerne les types de saignement, l’incidence cumulée des saignements au site d’accès, des saignements gastro-intestinaux et des autres saignements était significativement plus élevée dans le groupe ACS que dans le groupe coronarien stable, tandis que l’incidence cumulée des saignements intracrâniens ne différait pas entre les deux groupes. L’incidence cumulée de l’issue primaire de l’hémorragie n’était pas différente entre les STEMI et les NSTEACS.
L’incidence cumulée sur 5 ans du critère ischémique primaire n’était pas significativement différente entre les deux groupes pendant toute la période de suivi ou dans les 30 jours (Fig. 1C, 1D) [2]. Après ajustement pour les constructeurs, l’augmentation du risque d’ACS par rapport à une coronaropathie stable est restée non significative pour le critère ischémique primaire. Le risque d’ACS par rapport à une coronaropathie stable pour le critère d’évaluation ischémique primaire était significativement plus faible dans les 30 jours, mais plus élevé après 30 jours. L’augmentation du risque de SCA par rapport à une coronaropathie stable était significative pour toutes les causes de décès, la mort cardiaque, la mort cardiovasculaire, la mort non cardiovasculaire, l’accident vasculaire cérébral ischémique, la thrombose définitive de stent et la revascularisation des vaisseaux cibles, mais pas pour l’infarctus du myocarde selon la définition de l’ARTS. L’incidence cumulée du résultat ischémique primaire ne différait pas entre les STEMI et les NSTEACS.
Caractéristiques initiales selon le tableau clinique et le RBH
Les caractéristiques initiales et le traitement médicamenteux différaient significativement entre les quatre catégories en fonction des antécédents cliniques (SCA et coronaropathie stable) et de la présence d’ARC-HBR. Les patients du groupe ACS/HBR étaient plus âgés, avaient un indice de masse corporelle plus faible et souffraient plus souvent d’insuffisance cardiaque et de fragilité sévère.
Résultats cliniques à long terme en fonction de la présentation clinique et du RBH
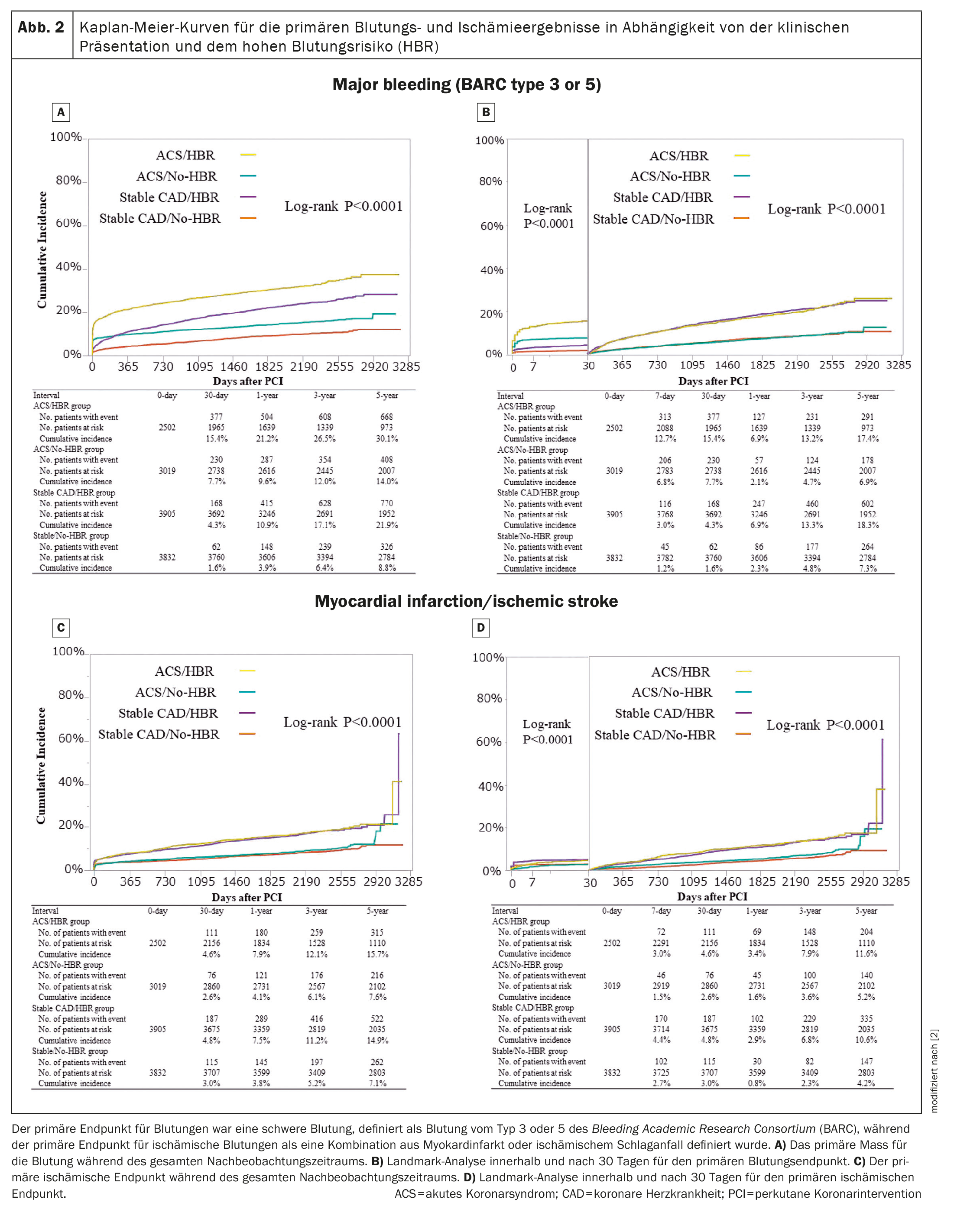
Dans les quatre groupes, l’incidence cumulée de l’interruption permanente du DAPT était la plus élevée dans le groupe ACS/HBR. L’incidence cumulée sur 5 ans du résultat de l’hémorragie primaire a diminué dans l’ordre suivant : ACS/HBR, coronaropathie stable/HBR et ACS/No-HBR, suivi par le groupe coronaropathie stable/No-HBR (figure 2A) [2]. Dans les 30 jours, l’incidence cumulée du résultat primaire de l’hémorragie était plus élevée dans les deux groupes de SCA avec et sans RBH que dans les deux groupes de coronarographie stable avec et sans RBH (figure 2B) [2]. Le risque ajusté pour le résultat primaire de l’hémorragie était beaucoup plus élevé dans le groupe ACS/HBR et modérément plus élevé dans les groupes ACS/No-HBR et coronarographie stable/HBR que dans le groupe coronarographie stable/No-HBR (respectivement HR 3,05 [IC 95% 2,64-3,54 ; p<0,0001], HR 1,69 [IC 95% 1,45-1,98 ; p<0,0001] et HR 1,69 [IC 95% 2,64-3,54 ; p<0,0001]). HR 1,89 [IC 95% 1,66-2,15 ; p<0,0001]).
Dans les 30 jours, le risque ajusté de résultat hémorragique primaire était nettement plus élevé dans les deux groupes ACS avec et sans RBH, et modérément plus élevé dans le groupe avec RC/ RBH stable que dans le groupe avec RC/ RBH non stable. À 30 jours, le risque ajusté de résultat hémorragique primaire était significativement plus élevé dans les deux groupes RBH avec et sans SCA que dans le groupe RBH stable/non RBH.
L’incidence cumulée sur 5 ans du résultat ischémique primaire était significativement plus élevée dans les deux groupes RBH que dans les deux groupes non RBH tout au long de la période de suivi. L’incidence cumulée sur 5 ans du résultat ischémique primaire était significativement plus élevée dans les deux groupes RBH que dans les deux groupes sans RBH pendant toute la période de suivi (Fig. 2C) [2] ainsi que dans et après 30 jours (Fig. 2D) [2]. Le risque ajusté de résultat ischémique primaire était légèrement plus élevé dans les deux groupes RBH que dans le groupe coronarien stable/non RBH, alors qu’il ne différait pas significativement entre les groupes SCA/non RBH et coronarien stable/non RBH.
Résultat de l’hémorragie primaire à 30 jours selon le site d’accès
L’incidence cumulée à 30 jours du résultat primaire de l’hémorragie (BARC type 3 ou 5 hémorragies) était significativement plus élevée chez les patients ayant une voie fémorale que chez ceux ayant une voie radiale.
L’aspirine reste la “pierre angulaire” du traitement
L’auteur de l’étude, le Dr Masahiro Natsuaki de l’Université de Saga au Japon, a résumé les résultats de l’étude STOPDAPT-3 comme suit : “La stratégie sans aspirine n’a pas permis de réduire le nombre d’hémorragies graves dans le mois suivant l’ICP par rapport à la stratégie DAPT, mais elle n’était pas inférieure en termes de critère d’évaluation cardiovasculaire co-primaire avec une marge relative de 50%. L’aspirine, utilisée dans le cadre du DAPT pendant une période limitée d’un mois après l’ICP, pourrait avoir exercé un effet protecteur sur les lésions coronaires vulnérables, notamment chez les patients atteints de SCA, sans entraîner d’augmentation importante des saignements graves. La DAPT devrait rester la stratégie de référence pour l’ICP, même à l’ère de la nouvelle génération de stents recouverts de médicaments”. [1]
Lors de la discussion des résultats de STOPDAPT-3 après la présentation à chaud, Marco Valgimigli, directeur adjoint de la cardiologie interventionnelle au Cardiocentro Ticino Institute de Lugano en Suisse, a déclaré que les données de STOPDAPT-3 ne montrent aucun bénéfice pour les hémorragies graves et un signal de dommages potentiels en termes de thromboses de stents subaiguës si le traitement à l’aspirine est omis après une ICP. “Les taux d’événements absolus étaient extrêmement faibles, 0,2% contre 0,6%, mais sans aucun doute plus élevés dans le groupe sans aspirine”, a conclu Valgimigli. “L’impact sur la pratique clinique est clair. L’aspirine reste une pierre angulaire dans la phase périprocédurale et aiguë de l’ICP chez les patients sans indication d’anticoagulation orale”.
Les lignes directrices recommandent une DAPT de six mois pour les patients atteints de SCA et de RBH, et de 12 mois sans RBH. Pour les patients non-ACS, la ligne directrice recommande un DAPT de 1 à 3 mois.
Congrès : ESC 2023
Littérature :
- Natsuaki M : STOPDAPT-3 : une stratégie antithrombotique sans aspirine pour l’intervention coronarienne percutanée. Hot Line Session 3, Congrès ESC 2023, Amsterdam, 26.08.2023.
- Natsuaki M, et al : Effets du syndrome coronarien aigu et de l’artériopathie coronarienne stable sur les saignements et le risque ischémique après une intervention coronarienne percutanée. Circ J. 2021;85 : 1928-1941.
- Yamaji K, et al : Résultats à long terme après l’implantation d’un stent coronaire chez des patients présentant une infarctus du myocarde aigu ou non (une observation de l’étude sur les résultats de la démonstration de la revascularisation coronaire-Kyoto Registry Cohort-2). Am J Cardiol 2015 ; 116 : 15-23.
- Valgimigli M, et al : 2017 ESC focused update on dual antiplatelet therapy in coronary artery disease developed in collaboration with EACTS : The task force for dual antiplatelet therapy in coronary artery disease of the European Society of Cardiology (ESC) and of the European Association for Cardio-Thoracic Surgery (EACTS). Eur Heart J 2018 ; 39 : 213-260.
- Nakamura M, et al : JCS 2020 guideline focused update on anti-thrombotic therapy in patients with coronary artery disease. Circ J 2020 ; 84 : 831-865.
- Valgimigli M, et al : Radial versus femoral access in patients with acute coro- nary syndromes undergoing invasive management : A randomised multicentre trial. Lancet 2015 ; 385 : 2465-2476.
- Urban P, et al : Définition du risque élevé d’hémorragie chez les patients subissant une intervention coronarienne percutanée. Circulation 2019 ; 140 : 240-261.
- Valgimigli M, et al : Effects of cobalt-chromium everolimus eluting stents or bare metal stent on fatal and non- fatal cardiovascular events : Patient level meta-analysis. BMJ 2014 ; 349 : g6427.
CARDIOVASC 2023 ; 22(4) : 46-50 (publié le 28.11.23, ahead of print)