Compte tenu des nouvelles thérapies, pour la plupart bien tolérées, la durée de vie et de traitement palliatifs des patients oncologiques s’allonge de plus en plus. Identifier les patients ayant besoin d’un soutien palliatif de manière précise et en fonction de leurs besoins, comme le recommandent les lignes directrices, est un défi de taille. Dans le contexte de l’Allemagne et de la Suisse, on distingue les soins palliatifs généraux (APV) et les soins palliatifs spécialisés (SPV).
Compte tenu des nouvelles thérapies, pour la plupart bien tolérées, la durée de vie et de traitement palliatifs des patients oncologiques s’allonge de plus en plus. C’est un grand défi d’identifier les patients nécessitant un soutien palliatif de manière adaptée et en fonction de leurs besoins, comme le recommandent les directives internationales et nationales dans l’esprit de la timely integration [1]. Dans le contexte de l’Allemagne et de la Suisse, on distingue les soins palliatifs généraux (APV) et les soins palliatifs spécialisés (SPV). L’APV est fournie par l’équipe de soins primaires et, dans le domaine ambulatoire, généralement par le médecin généraliste. En milieu hospitalier, les soins spécialisés sont assurés par les services de soins palliatifs, les unités de soins palliatifs et les hospices. Les soins palliatifs ambulatoires spécialisés (SAPV) sont dispensés par des équipes qui interviennent à domicile ou dans des maisons de soins. C’est pourquoi le dépistage des besoins en soins palliatifs a des objectifs et des approches différents. Il convient de déterminer si un dépistage à bas seuil, même peu spécifique, doit permettre d’identifier à la fois les patients ayant des besoins généraux en matière de soins palliatifs et les personnes concernées ayant besoin d’un soutien spécialisé en soins palliatifs (dépistage des besoins en matière de soins palliatifs, APV&SPV), ou si un dépistage doit permettre d’identifier de manière ciblée les patients ayant besoin d’un soutien spécialisé en matière de soins palliatifs (dépistage des besoins en SPV). Le dépistage des besoins en soins palliatifs (APV&SPV) utilise le plus souvent le dépistage pronostique pour identifier les patients dont la durée de vie est potentiellement limitée. Le dépistage des besoins en SPV vise à identifier les patients non curatifs ayant des besoins complexes. C’est pourquoi le groupe de patients à dépister est généralement limité de manière ciblée, par exemple au groupe des patients atteints d’un cancer non curable ou métastasé (comme opérationnalisé dans le nouvel indicateur de soins palliatifs dans le questionnaire d’enquête pour la certification des centres d’oncologie par la DKG).
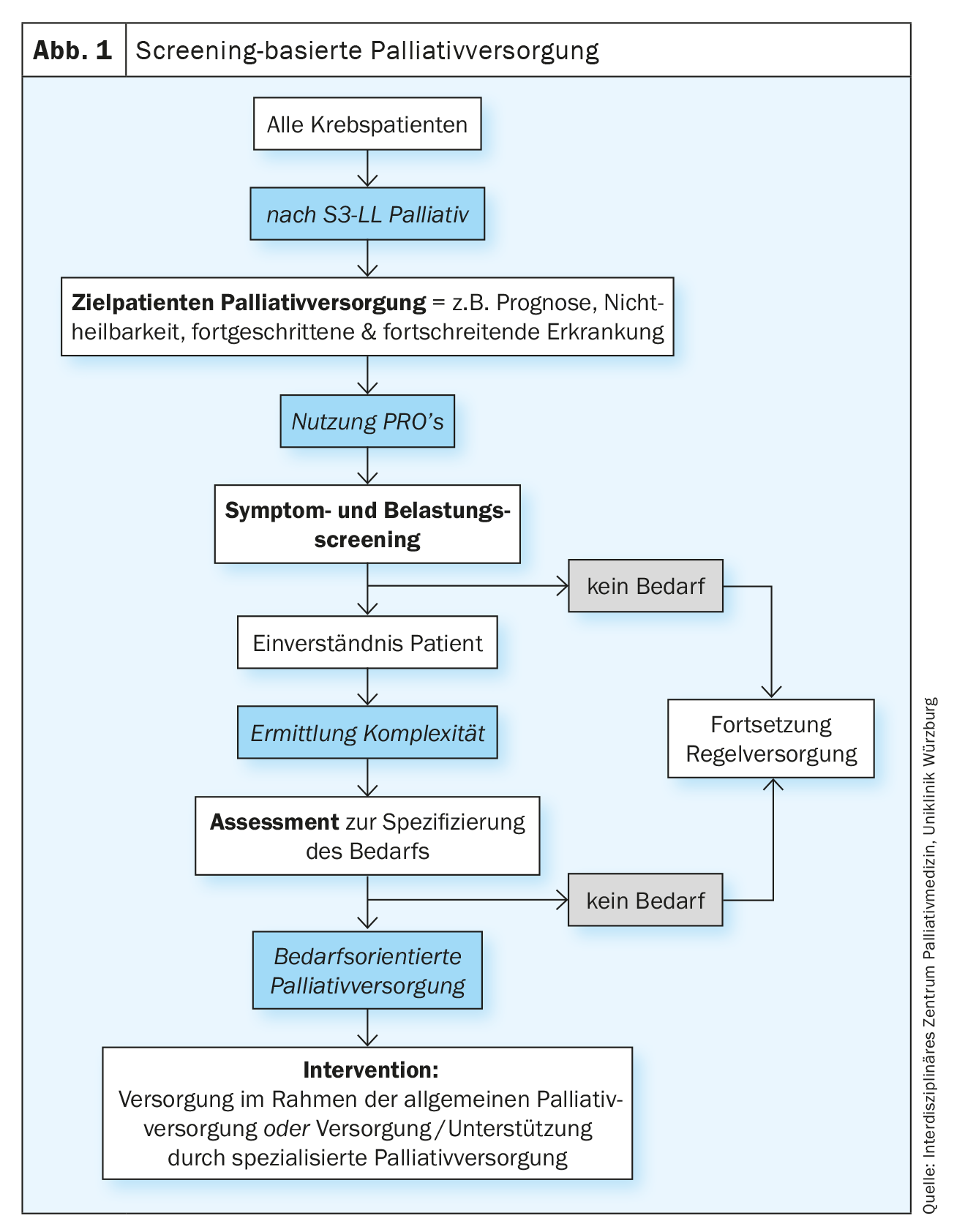
Les approches de dépistage réussies se caractérisent également, entre autres, par une présélection optimale du groupe de personnes que le dépistage doit diviser en groupes à forte probabilité et à faible probabilité par rapport à la maladie cible ou aux risques. La procédure de dépistage se déroule généralement en deux étapes. Afin de négliger le moins possible de personnes potentiellement atteintes/malades, un test sensible, mais pas nécessairement spécifique, est d’abord effectué sur le groupe cible défini (dépistage). Les personnes positives au dépistage sont classées dans le groupe des “malades” ou des “personnes affectées” ou dans le groupe des “non malades” ou des “non affectés” dans le cadre d’une évaluation professionnelle spécifique (assessment). Les personnes malades ou affectées sont ensuite orientées vers une intervention (figure 1). Le dépistage et l’évaluation sont généralement placés sous la responsabilité des prestataires de soins primaires, tandis que l’évaluation après un dépistage positif est ensuite prise en charge par les spécialistes concernés (comme recommandé par exemple pour le dépistage du stress psycho-oncologique). Selon les directives du National Comprehensive Cancer Network (NCCN) pour les soins palliatifs et de soutien basés sur le dépistage, ce sont les médecins de premier recours qui orientent les patients vers les spécialistes après un dépistage positif [2]. Transposé au dépistage des besoins en soins palliatifs en oncologie, cela signifie que le dépistage des besoins en soins palliatifs ne devrait pas être effectué par des spécialistes des soins palliatifs, mais par le personnel des équipes d’oncologie. Le guide S3 allemand sur les soins palliatifs pour les patients atteints d’un cancer non curable (S3-LL Palliativmedizin) reprend cette idée dans le chapitre 5 “Structures de soins”, sans référence explicite à un dépistage préalable, de la manière suivante : “Chaque personne impliquée dans les soins aux patients atteints d’un cancer […] doit être en mesure d’identifier les besoins en matière de soins palliatifs et de reconnaître la nécessité d’une action palliative afin de mettre en place des soins palliatifs. […] Les patients doivent se voir proposer une évaluation de leurs besoins par une équipe ASP après le diagnostic d’un cancer avancé non curable”, Rec. 5.8 [3].
L’évaluation des besoins en soins palliatifs doit permettre d’évaluer les patients dont la situation globale est très complexe dans les domaines physique, psychologique, social et spirituel, afin de personnaliser les soins en fonction des besoins. L’évaluation des besoins de l’ASP correspond à l’évaluation de base des soins palliatifs lors du premier contact avec l’ASP, qu’un dépistage ait été effectué ou non au préalable. Les différentes possibilités de dépistage des besoins en soins palliatifs ainsi que l’évaluation de base des soins palliatifs sont expliquées plus en détail ci-dessous.
Dépistage pronostique pour l’identification des patients nécessitant des soins palliatifs (APV&SPV)
En médecine, les dépistages sont utilisés pour estimer la survie, afin de donner une idée d’une pathologie ou d’un modèle de blessure en peu de temps, sur la base de paramètres comparables. Les dépistages pronostiques peuvent également être utilisés pour identifier les patients nécessitant des soins palliatifs et, le cas échéant, des soins de fin de vie. Plusieurs outils sont disponibles pour estimer le pronostic temporel des patients atteints de cancers avancés. L’état des connaissances a été évalué pour la dernière fois en 2019 dans une revue de Hui et al. a été élaboré [4]. Dans le contexte des recommandations basées sur le pronostic pour l’identification des patients nécessitant des soins palliatifs (APV&SPV), les outils d’identification des patients dont la durée de survie attendue est de 6 à 12 mois et d’identification des patients en fin de vie, c’est-à-dire des patients dont la durée de survie attendue est de 3 à 7 jours maximum, sont particulièrement pertinents. L’instrument le plus ancien est probablement la “question surprise”, c’est-à-dire la question : “Seriez-vous surpris si ce patient décédait dans les 12 prochains mois ?” La réponse : “Non, je ne serais pas surpris” indique un pronostic limité. La question Surprise varie beaucoup en termes de temps de survie à estimer (“heures”, “jours”, “semaines”, “6 mois”, …). Van Lummel et al. ont analysé 59 études dans une revue récente et ont trouvé une sensibilité de 71,4% (IC 95% 66,3-76,4) et une spécificité de 88,6% (IC 95% 69,3-78,6) pour la survenue de la survenue originale. Contrairement aux analyses précédentes, aucune différence n’a été observée en fonction de la profession de l’évaluateur (personnel médical vs infirmier). Même avec des taux de mortalité très variables, la valeur prédictive négative était élevée [5].
Dans d’autres dépistages pronostiques, qui ont également été développés pour les patients atteints de cancer à un stade avancé, la plupart des paramètres liés à la maladie et à l’anamnèse sont combinés avec des items cliniques tels que l’état fonctionnel, la mobilité ou la prise alimentaire, parfois complétés par des symptômes cliniques pertinents tels que la détresse respiratoire ou la perte d’appétit. Les différents paramètres sont parfois pondérés différemment. L’addition donne ensuite des valeurs en points, accompagnées de pourcentages pour la survie attendue, par exemple à 6 mois ou à 4 semaines [6]. Différents dépistages pronostiques ont été développés dans des cadres spécifiques, par exemple en radiothérapie, en médecine générale ou en soins palliatifs spécialisés, ou sont recommandés pour des situations cliniques spécifiques, comme l’hospitalisation. Kirkland et al. ont analysé 35 publications contenant 14 outils de dépistage des besoins en soins palliatifs dans les services d’urgence. L’outil le plus utilisé était la Surprise-Question, suivie de l’outil de dépistage des soins palliatifs et des urgences rapides (P-CaRES) et de l’outil de dépistage des besoins en soins palliatifs et de fin de vie dans les services d’urgence (SPEED). La sensibilité médiane était de 63% (IQR 16-40%) et la spécificité était de 75% (IQR 57-84%). La valeur prédictive négative médiane était élevée (91%). Entre 5% et 85% des patients avaient besoin de soins palliatifs [7]. Une approche nouvelle et peu gourmande en ressources consiste à utiliser les données de routine. Gensheimer et al. ont développé un modèle prometteur d’évaluation du pronostic à partir des dossiers électroniques de 12 588 patients atteints de cancer métastasé, qui est actuellement testé de manière prospective [8].
Les dépistages pronostiques doivent sensibiliser les équipes soignantes à la durée de vie potentiellement très limitée de leurs patients et contribuer à identifier la nécessité d’une action palliative et, le cas échéant, à mettre en place des soins palliatifs (APV&SPV). Cela est également utile et possible en même temps qu’un traitement causal. Des études montrent qu’environ 60% des médecins surestimaient nettement le pronostic des patients atteints de tumeurs avancées et que seuls 5% sous-estimaient la durée de vie restante. Un team-approach L’utilisation de la question Surprise ou d’outils de dépistage standardisés peut contribuer à une évaluation plus réaliste de la situation par toutes les parties concernées et aider à adapter les objectifs thérapeutiques et les plans de traitement, à optimiser le soulagement des symptômes, à vérifier le niveau d’éducation et d’information des patients et des proches, à (re)parler des possibilités de planification anticipée de la santé et, le cas échéant, à adapter le concept de soins. Dans ce contexte, le besoin d’une assistance spécialisée en soins palliatifs devrait également être clarifié.
Dépistage à l’aide de fiches d’auto-évaluation du patient (PROs, APV&SPV)
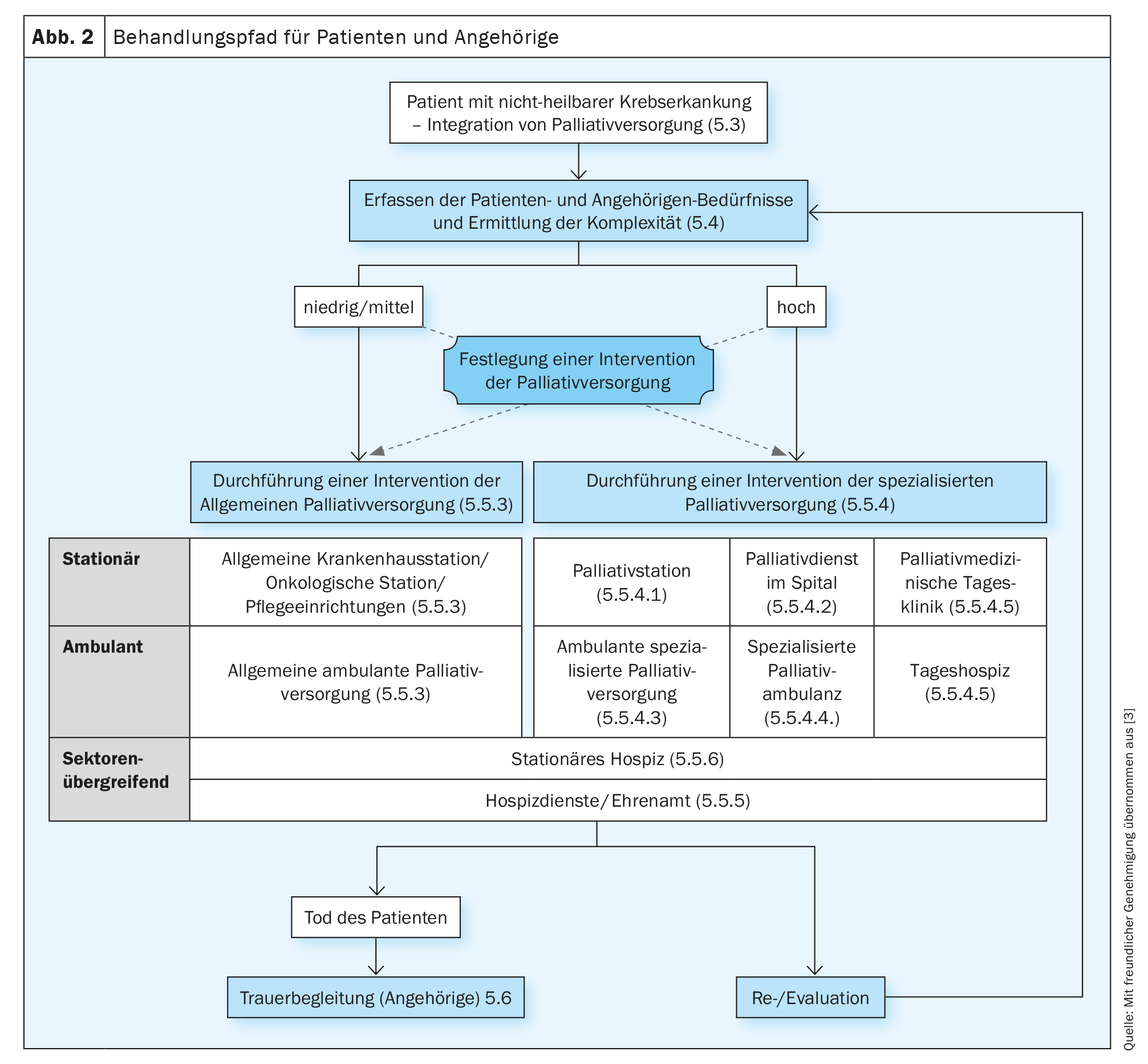
La S3-LL Soins palliatifs pour les patients atteints de cancer non curable recommande un enregistrement répété des symptômes, du stress et des besoins d’information afin d’adapter de manière adéquate les objectifs de traitement et le plan de traitement individuel. Pour ce faire, il convient d’utiliser des outils de collecte multidimensionnels validés (S3-LL Palliative Medicine, recommandation 5.5), idéalement des questionnaires d’auto-évaluation (Patient Reported Outcome-Instruments, PROs). Dans la S3-LL Palliative Medicine, il n’est pas explicitement question de dépistage à ce stade, mais d’une évaluation des besoins par l’ASP, au cours de laquelle la complexité de la situation doit être évaluée en plus des symptômes, des besoins et du fardeau. Même si l’évaluation des besoins ne doit pas nécessairement être réalisée par le personnel des soins palliatifs spécialisés (SPV), les critères de demande d’intervention en soins palliatifs spécialisés doivent être définis par les soins palliatifs spécialisés (SPV). Un algorithme correspondant est disponible dans la S3-LL Palliative Medicine (“Behandlungspfad für Patienten und Angehörige”, p. 47 S3-LL Palliative Medicine, Fig. 2). Le besoin d’un soutien spécialisé en soins palliatifs doit être évalué en fonction de sa complexité. Pour déterminer la complexité, il convient de prendre en compte les besoins du patient et de ses proches, l’état fonctionnel et la phase de la maladie (recommandation 5.7, S3-LL Palliative Medicine). L’évaluation de la complexité est différenciée entre “faible/moyenne” et “élevée”. Les patients faiblement/moyennement complexes doivent bénéficier d’interventions de soins palliatifs généraux (APV, estimés à 70-80% de tous les patients) et les patients très complexes doivent être (co)pris en charge par des soins palliatifs spécialisés (SPV, estimés à 20-30% des patients).
L’étalon-or pour l’enregistrement des symptômes, du stress et des problèmes sont les questionnaires d’auto-évaluation (PRO), dans lesquels les patients documentent leurs préoccupations sans autre “support intermédiaire”. Dans l’évaluation par des tiers (tant par les professionnels que par les proches), les erreurs de jugement sont fréquentes, qu’il s’agisse d’une sous-estimation ou d’une surestimation des symptômes et du fardeau. Hart et al. ont passé en revue 81 études menées entre 2002 et 2022 sur les besoins non satisfaits de patients atteints de tumeurs solides et de maladies hématologiques à un stade avancé et ne nécessitant pas de traitement curatif, ainsi que de leurs proches [9]. Les chercheurs ont identifié six dimensions auxquelles les besoins non satisfaits des quatre groupes concernés pouvaient être rattachés (cf. (voir le tableau 1 pour plus de détails ). 5/81 études portant sur 962/19 382 patients ont été menées dans les pays germanophones (6,1% des études portant sur 4,9% des patients), de sorte que les résultats ne sont pas nécessairement transposables. La différenciation des domaines semble extrêmement utile pour développer la collaboration entre les disciplines de soutien.
Par analogie avec le dépistage du stress psycho-oncologique établi dans les centres certifiés par la DKG, des questionnaires d’auto-évaluation en médecine palliative sont désormais utilisés pour dépister les besoins en soins palliatifs, parfois en combinaison avec les questionnaires d’auto-évaluation psycho-oncologique des patients recommandés [10]. Les PRO étant également pris en compte dans l’évaluation de la complexité, un dépistage des symptômes et du fardeau à l’aide de questionnaires d’auto-évaluation en médecine palliative contribue non seulement à sensibiliser les soignants de première ligne aux préoccupations des patients, mais aussi à faciliter l’orientation vers une (co)prise en charge spécialisée en médecine palliative en fonction des besoins. Les discussions actuelles et les projets de recherche visent à déterminer comment les questionnaires d’auto-évaluation en soins palliatifs peuvent être utilisés de manière optimale pour identifier les patients nécessitant des soins palliatifs spécialisés (SPV).
Pour recenser les problèmes et les besoins des patients, la S3-LL Palliative Medicine recommande, à titre d’exemple, quatre instruments d’auto-évaluation validés : le système de documentation minimal (MIDOS-2 [11]), le système d’évaluation des symptômes d’Edmonton (ESAS/revised version ESAS-r [12]), l’échelle de résultats des soins palliatifs intégrés (IPOS [13]) et le thermomètre de détresse avec liste de problèmes [14]. Comme le MIDOS-2 est dans la version validée allemande de l’ESAS-r, ce nombre est réduit à trois instruments recommandés. De manière surprenante pour le lecteur, seuls les instruments MIDOS et IPOS sont recommandés pour la saisie de l’indicateur de qualité qui se réfère à la recommandation 5.5 mentionnée (QI10, saisie des symptômes le plus souvent possible au moyen de MIDOS ou IPOS chez les patients atteints d’un cancer non curable). Il est possible qu’il faille éviter toute ambiguïté, car le thermomètre de détresse est déjà recommandé dans le guide S3 Psycho-oncologie en vigueur en 2015 en tant qu’instrument de dépistage pour évaluer la nécessité d’un traitement psycho-oncologique. D’autre part, cette duplication offre également la possibilité d’une approche coordonnée et d’une exploitation des synergies qui préservent les ressources.
Lors du pilote multicentrique du nouvel indicateur “Enregistrement des symptômes avec MIDOS/IPOS chez les patients atteints d’un cancer non curable” (projet KeSBa [10]), le MIDOS a été plus souvent utilisé que l’IPOS (plus récent) dans les centres d’oncologie certifiés par la DKG. L’un des points forts du MIDOS est une graduation simple permettant d’évaluer l’intensité de dix symptômes physiques/psychiques (aucun, léger, moyen, fort) et une question sur l’état de santé (très mauvais, mauvais, moyen, bon, très bon). L’un des points forts de l’IPOS – outre sa sensibilité avérée au changement [13] – est l’accent mis sur le fardeau que représentent les symptômes et les problèmes interrogés, en partant du principe que ce n’est pas l’intensité des symptômes qui est déterminante pour le soulagement des symptômes, mais leur impact sur le patient (“fardeau”). En outre, l’IPOS évalue non seulement le fardeau des répondants pour dix symptômes physiques/psychiques, mais aussi le fardeau lié, entre autres, à l’inquiétude des proches, au manque d’information et aux problèmes pratiques non résolus.
Évaluation de base des soins palliatifs
L’évaluation structurée des soins palliatifs de base (PBA) vise à refléter les besoins particuliers d’un patient en soins palliatifs dans toutes ses dimensions. En Allemagne, le PBA s’appuie sur les recommandations de l’association professionnelle DGP (Deutsche Gesellschaft für Palliativmedizin e.V.), et sur la définition de l’OPS 1-774 (“standardisiertes palliativmedizinisches Basisassessment”). Le PBA peut être réalisé en tant qu’évaluation des soins palliatifs après un dépistage positif ou en tant que partie intégrante de l’évaluation initiale des soins palliatifs après une orientation vers des soins palliatifs spécialisés déclenchée par le médecin. Dans le PBA, outre une anamnèse détaillée, la situation de vie individuelle et actuelle du patient est enregistrée. Étant donné que les soins palliatifs ne se limitent pas aux dimensions physiques, au moins cinq dimensions/domaines des soins palliatifs doivent être évalués dans le PBA. Il s’agit notamment de l’intensité des symptômes, de la charge psychosociale, du degré de capacité à se prendre en charge, du degré d’implication sociale du patient ainsi que de sa situation sociale et de ses compétences quotidiennes. L’enquête sur ces domaines est réalisée à l’aide de méthodes de mesure standardisées, y compris les méthodes de mesure de l’efficacité. Les formulaires d’auto-évaluation des patients sont recommandés. Par conséquent, si MIDOS ou IPOS ont déjà été utilisés pour le dépistage, ils peuvent également être utilisés dans le cadre de l’APB (si le dépistage et l’APB ont lieu en même temps). Une sélection d’autres outils recommandés est disponible sur le site web de la DGP. Il convient de noter qu’il n’est pas nécessaire d’enquêter sur chaque domaine avec un instrument séparé, mais que des instruments multidimensionnels peuvent également être utilisés. La composition judicieuse d’un PBA doit idéalement refléter non seulement la situation initiale des patients, mais aussi leurs besoins en soins et les efforts (attendus) de l’équipe traitante. En outre, les données collectées devraient également être utilisables pour l’assurance qualité, la comparabilité, l’évaluation et la recherche et, en fin de compte, répondre à un droit à rémunération qui s’est développé.
En résumé, une évaluation structurée des symptômes et des besoins des patients atteints de cancer est utile et également fortement recommandée dans le cadre de l’empowerment des patients. On peut s’attendre à une efficacité en termes de critères de résultats rapportés par les patients lorsque la détection des symptômes et du stress est complétée par des algorithmes vécus pour l’approche – idéalement coordonnée avec les autres disciplines de soutien – des patients présentant des anomalies de dépistage [10]. Les questionnaires de soins palliatifs contribuent à une compréhension plus large des préoccupations des patients en recueillant des symptômes physiques et en se concentrant sur les préoccupations des proches, les besoins d’information, les aspects spirituels et les problèmes pratiques, complétant ainsi le dépistage du stress psychosocial. L’évaluation de base des soins palliatifs sert à évaluer de manière multidimensionnelle le soutien et les besoins en soins des patients en soins palliatifs spécialisés. Comme les outils d’auto-évaluation recommandés sont recommandés à la fois pour le dépistage et pour l’évaluation des soins palliatifs, l’évaluation peut facilement s’appuyer sur le dépistage. Des recommandations de traitement au niveau des items individuels pour les soins aux patients dans le cadre des soins palliatifs ambulatoires spécialisés (SAPV) sont publiées pour l’IPOS.
Messages Take-Home
- L’estimation du pronostic (screening pronostique) est utile pour
identifier en temps voulu les patients ayant potentiellement besoin de soins palliatifs - Les soins palliatifs impliquent une approche proactive des soins, l’orientation du traitement vers la qualité de vie, le soulagement des symptômes et le soutien des proches (caregivers informels).
- L’identification des patients nécessitant des soins palliatifs et la mise en place de soins palliatifs relèvent de la responsabilité des équipes de soins primaires (soins palliatifs généraux).
- L’implication des soins palliatifs spécialisés doit se faire sur la base de la complexité de la situation du patient.
- Pour évaluer la complexité, les besoins des patients et des proches doivent être évalués à l’aide de questionnaires d’auto-évaluation (PROM), complétés par l’état fonctionnel et la phase de la maladie.
Littérature :
- Hui D, et al : Timely Palliative Care : Personalizing the Process of Referral. Cancers 2022 ; 14(4).
- Riba MB, et al. : Gestion de la détresse, version 3.2019. J Natl Compr Canc Netw 2019 ; 17(10) : 1229-1249 ; doi : 10.6004/jnccn.2019.0048.
- Programme de lignes directrices en oncologie (Deutsche Krebsgesellschaft, Deutsche Krebshilfe, AWMF) : Soins palliatifs pour les patients atteints d’un cancer non curable, version longue 2.2, 2020, numéro de registre AWMF : 128/001OL, www.leitlinienprogramm-onkologie.de/leitlinien/palliativmedizin/ (consulté le : 14.05.2023).
- Hui D, et al : Prognostication in advanced cancer : update and directions for future research. Support Care Cancer 2019 ; 27(6) : 1973-1984 ; doi : 10.1007/s00520-019-04727-y.
- Van Lummel EV, et al. : L’utilité de la question surprise : un outil utile pour identifier les patients approchant de la dernière phase de leur vie ? A systematic review and meta-analysis. Médecine palliative 2022 ; 36(7) : 1023-1046 ; doi : 10.1177/02692163221099116.
- Ueno Y, Kanai M : Prognosis Prediction Models and their Clinical Utility in Palliative Care 2017 ; www.intechopen.com/bookshighlights-on-several-underestimated-topics-in-palliative-care/prognosis-prediction-models-and-their-clinical-utility-in-palliative-care (consulté le : 18.2.2021).
- Kirkland SW, et al : Screening tools to identify patients with unmet palliative care needs in the emergency department : A systematic review. Acad Emerg Med 2022 ; 29(10) : 1229-1246 ; doi : 10.1111/acem.14492.
- Gensheimer MF, et al : Automated Survival Prediction in Metastatic Cancer Patients Using High-Dimensional Electronic Medical Record Data. JNCI J Natl Cancer Inst 2019 ; 111(6) : djy178 ; doi : 10.1093/jnci/djy178.
- Hart NH, et al : Unmet supportive care needs of people with advanced cancer and their caregivers : A systematic scoping review. Crit Rev Oncol Hematol 2022 ; 176 : 103728 ; doi : 10.1016/j.critrevonc.2022.103728.
- Braulke F, et al : Systematic symptom screening in patients with advanced cancer treated in certified oncology centers : results of the prospective multicenter German KeSBa project. J Cancer Res Clin Oncol 2023 ; doi : 10.1007/s00432-023-04818-8.
- Bruera E, et al : The Edmonton Symptom Assessment System (ESAS) : a simple method for the assessment of palliative care patients. J Palliat Care 1991 ; 7(2) : 6-9.
- Stiel S, et al. : Validation de la nouvelle version du système de documentation minimale (MIDOS) pour les patients en soins palliatifs : la version allemande de l’échelle d’évaluation des symptômes d’edmonton (ESAS). Douleur 2010 ; 24(6) : 596-604.
- Murtagh FE, et al. : A brief, patient- and proxy-reported outcome measure in advanced illness : Validity, reliability and responsiveness of the Integrated Palliative care Outcome Scale (IPOS). Palliat Med 2019 ; 33(8) : 1045-1057.
- Mehnert A, et al : La version allemande du thermomètre de détresse du NCCN. Z Psychosom Med Psychother 2006 ; 54(3) : 213-223.
PRATIQUE DU MÉDECIN DE FAMILLE 2023 ; 18(9) : 10-14