L’acidocétose diabétique (ACD) est une complication du diabète sucré qui met en jeu le pronostic vital et qui survient principalement dans le cadre du diabète de type 1, mais de plus en plus souvent chez les personnes atteintes de diabète de type 2. Une forme particulière est l’ACDeuglycémique, qui survient principalement sous traitement par inhibiteurs du SGLT2. Même si elle est devenue rare et que la mortalité n’est aujourd’hui que d’un peu plus de 1%, ces décès sont généralement évitables. Les facteurs décisifs pour le pronostic sont un diagnostic précoce, des protocoles thérapeutiques standardisés et surtout une prophylaxie.
Vous pouvez passer le test de FMC sur notre plateforme d’apprentissage après avoir lu le matériel recommandé. Pour ce faire, veuillez cliquer sur le bouton suivant :
L’acidocétose diabétique (ACD) est une complication du diabète sucré qui met en jeu le pronostic vital et qui survient principalement dans le cadre du diabète de type 1, mais de plus en plus souvent chez les personnes atteintes de diabète de type 2. Une forme particulière est l’ACD euglycémique, qui survient principalement sous traitement par inhibiteurs du SGLT2.
Même si elle est devenue rare et que la mortalité n’est plus aujourd’hui que d’un peu plus de 1%, ces décès sont généralement évitables. Les facteurs décisifs pour le pronostic sont un diagnostic précoce, des protocoles de traitement standardisés et surtout une prophylaxie – notamment par une formation appropriée des patients et des médecins.
Étude de cas
Beat R., 23 ans, est diabétique de type 1 depuis l’âge de 14 ans. L’étudiant est équipé d’une pompe à insuline depuis 6 ans et utilise depuis un peu plus d’un an un système AID, c’est-à-dire que la pompe à insuline adapte l’administration d’insuline aux taux de glycémie. M. R. trouve cela très confortable et ne se préoccupe plus autant de son diabète, d’autant plus que des examens sont en cours. Après le dîner, M. R. ressent de légères nausées et vomit plusieurs fois au cours de la nuit. Il interprète cela comme une infection et ne s’inquiète pas davantage. Le lendemain matin, il se sent fatigué, les nausées ont augmenté et la concentration de glucose dans le sang est de 23,5 mmol/l. Il appelle un bolus d’insuline de 8 unités et décide de ne pas aller travailler à cause de l’infection, se couche et s’endort. Vers midi, il est réveillé par des douleurs abdominales, la glycémie ne peut plus être mesurée (avec son système CGM, cela correspond à >30 mmol/l.). Beat R. appelle alors son médecin traitant. Celui-ci soupçonne fortement une acidocétose et envoie donc le patient à l’hôpital de soins aigus le plus proche via les services de secours.
A son arrivée à la clinique, M. R. est somnolent, mais peut être réveillé. La glycémie est de 36,7 mmol/l, le β-hydroxybutyrate de 6,3 mmol/l, le bicarbonate de 6 mmol/l et le pH de 7,1. La pression artérielle est de 100/60 mmHg.
Beat R. est admis aux soins intensifs de la clinique en raison d’une acidocétose sévère. Après 3 jours de traitement standardisé, il s’est complètement rétabli. La cause de l’acidocétose n’était d’ailleurs pas une infection, mais un dysfonctionnement de la pompe auquel le patient n’a pas réagi.
Au cours des entretiens qui ont suivi, il s’avère que M. R. s’est lassé des alarmes fréquentes de la pompe et les a généralement ignorées.
Épidémiologie et clinique des urgences hyperglycémiques
Il existe deux formes d’états hyperglycémiques potentiellement mortels. L’acidocétose diabétique (ACD) se produit principalement chez les personnes atteintes de diabète de type 1 et a une faible létalité. En revanche, le syndrome hyperglycémique-hyperosmolaire (SHH) survient généralement chez les personnes atteintes de diabète de type 2 et se caractérise toujours par une mortalité élevée. On trouve très souvent des formes mixtes, surtout en présence de maladies aiguës. Celles-ci peuvent souvent masquer l’aspect clinique de l’ACD, par exemple lorsqu’il s’agit d’infections aiguës (gastro-entérite, pneumonie, infection des voies urinaires), d’autres maladies aiguës (par exemple infarctus du myocarde) ou encore d’opérations (programmées). Il est donc important de penser à cette possibilité et d’entamer à temps une clarification diagnostique (tableau 1).
Dans le monde entier, le nombre d’hospitalisations pour dérapages hyperglycémiques a considérablement augmenté, avec une hausse particulièrement frappante chez les personnes de plus de 45 ans, de >55% au cours des dix dernières années. Chez les enfants et les adolescents, l’ACD est la complication la plus fréquente du diabète. Environ une manifestation sur trois se produit dans le cadre d’une ACD.
Clinique
La symptomatologie typique est très variable, le tableau clinique complet avec déshydratation, odeur de cétone, respiration de Kussmaul et coma est rarement observé. Les symptômes qui peuvent facilement être confondus avec des maladies bénignes sont beaucoup plus fréquents, en particulier chez les enfants : Nausées, douleurs abdominales, vomissements sont des événements fréquents. Il est donc d’autant plus important d’être attentif aux anomalies qui les accompagnent : L’abattement, la somnolence, mais aussi les états confusionnels, la perte de poids, la polyurie et la polydipsie sont également typiques de la présence d’une ACD, mais ne sont guère présents dans les maladies gastro-intestinales banales (fig. 1).
En cas de déficit relatif en insuline, la maladie déclenchante est généralement au premier plan et l’ACD qui se développe peut être masquée. Le diagnostic différentiel peut être particulièrement difficile à établir chez les patients gravement malades ou en postopératoire – il est d’autant plus important de penser à la possibilité d’une acidocétose et de mettre en place le diagnostic approprié. Il faut également garder à l’esprit que les déterminations habituelles du glucose au chevet ne donnent pas toujours des résultats fiables dans des conditions de soins intensifs. En cas de suspicion de déséquilibre métabolique du diabète, une prise de sang veineux doit toujours être effectuée pour déterminer le taux de glucose.
Diagnostic
L’ACD est définie comme un état d’hyperglycémie, d’acétonémie et d’acidose métabolique. On distingue 3 stades en fonction de l’importance de la cétonémie et de l’acidose (tableau 2).
Malheureusement, un diagnostic qualifié de l’acidocétose diabétique n’est guère possible dans la pratique ambulatoire, car il n’existe généralement pas de possibilité d’analyse des gaz du sang et des acides/bases. Il ne reste donc comme paramètre fiable et immédiatement déterminable que le β-hydroxybutyrate dans le sang capillaire. Cela signifie également que dans des conditions ambulatoires, seul un diagnostic de suspicion peut être établi. Lorsqu’il existe une suspicion fondée d’ACD, l’hospitalisation est généralement inévitable.
L’acidocétose diabétique euglycémique (AED) est une forme particulière. Elle est souvent diagnostiquée tardivement (en raison d’une glycémie indétectable) et est donc souvent grave. En particulier sous traitement par inhibiteurs SGLT2, chez les femmes enceintes souffrant de diabète gestationnel ou de diabète sucré préexistant, chez les personnes diabétiques souffrant d’une maladie hépatique supplémentaire et chez les jeunes patients atteints de diabète de type 1, une acidose métabolique avec un taux de bicarbonate sérique <10 mM se produit sans que les valeurs de la glycémie soient nettement élevées. C’est la raison pour laquelle les dernières recommandations ont abaissé la valeur de la glycémie de 14 à 11 mmol.
Pour éviter cette complication, les patients doivent être informés qu’ils doivent interrompre la médication en question, par exemple en cas d’infections aiguës, avant une intervention chirurgicale sous anesthésie générale, mais aussi pendant les périodes de jeûne. Comme outil de soutien, la SSE a créé une carte “Sick Day Rules” qui peut être donnée aux patients dans le cadre d’une telle instruction.
L’hyperglycémie et sa physiopathologie : un aperçu
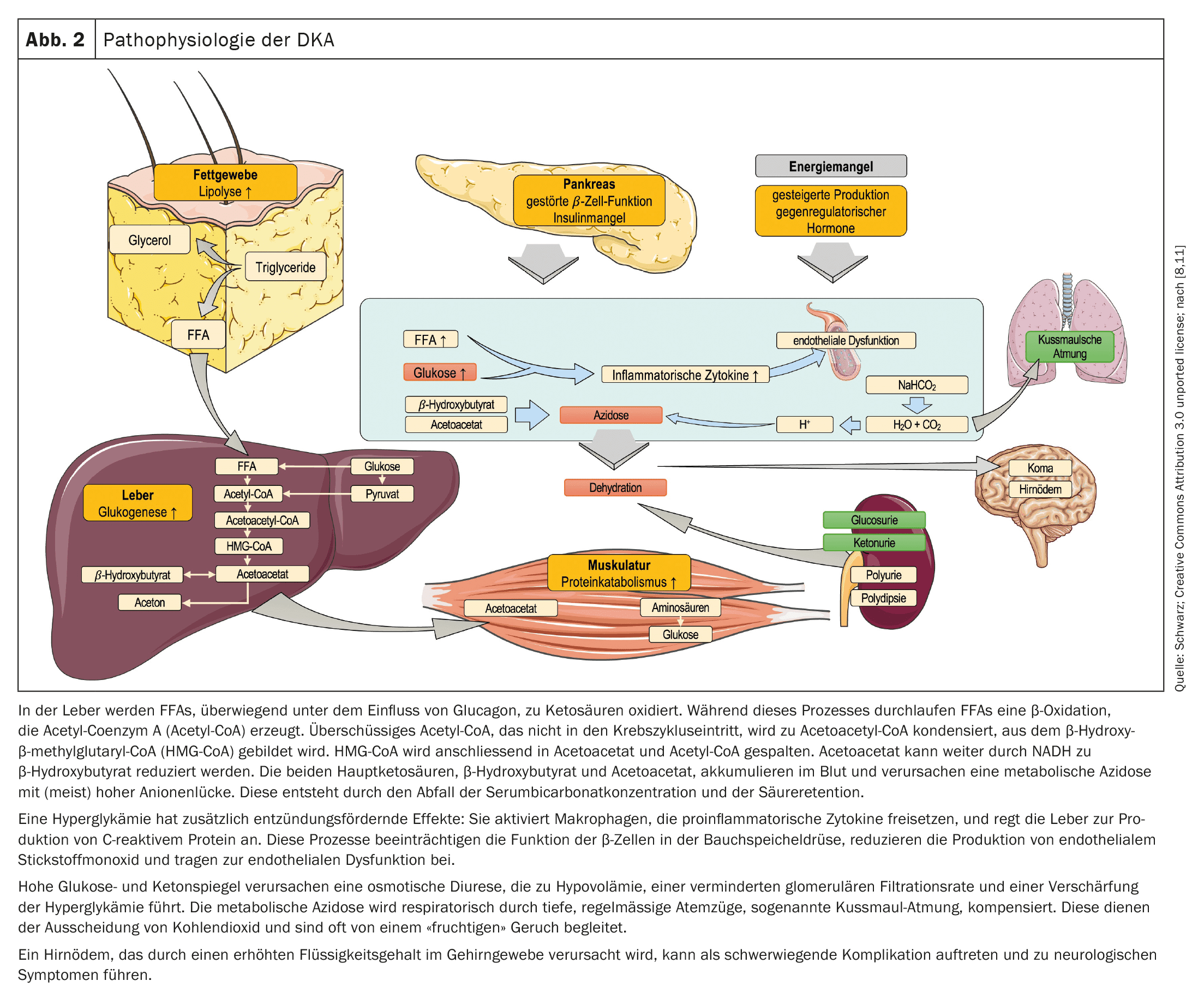
L’hyperglycémie résulte de trois processus principaux en cas de déficit en insuline : une augmentation de la gluconéogenèse, une accélération de la glycogénolyse et une altération de l’utilisation du glucose dans les tissus périphériques. La baisse de la concentration d’insuline, combinée à une augmentation des hormones de contre-régulation (glucagon, adrénaline, noradrénaline, cortisol et hormone de croissance), active la lipase hormonosensible dans le tissu adipeux. Cela entraîne la dégradation des triglycérides en glycérol et en acides gras libres (AGL) (figure 2).
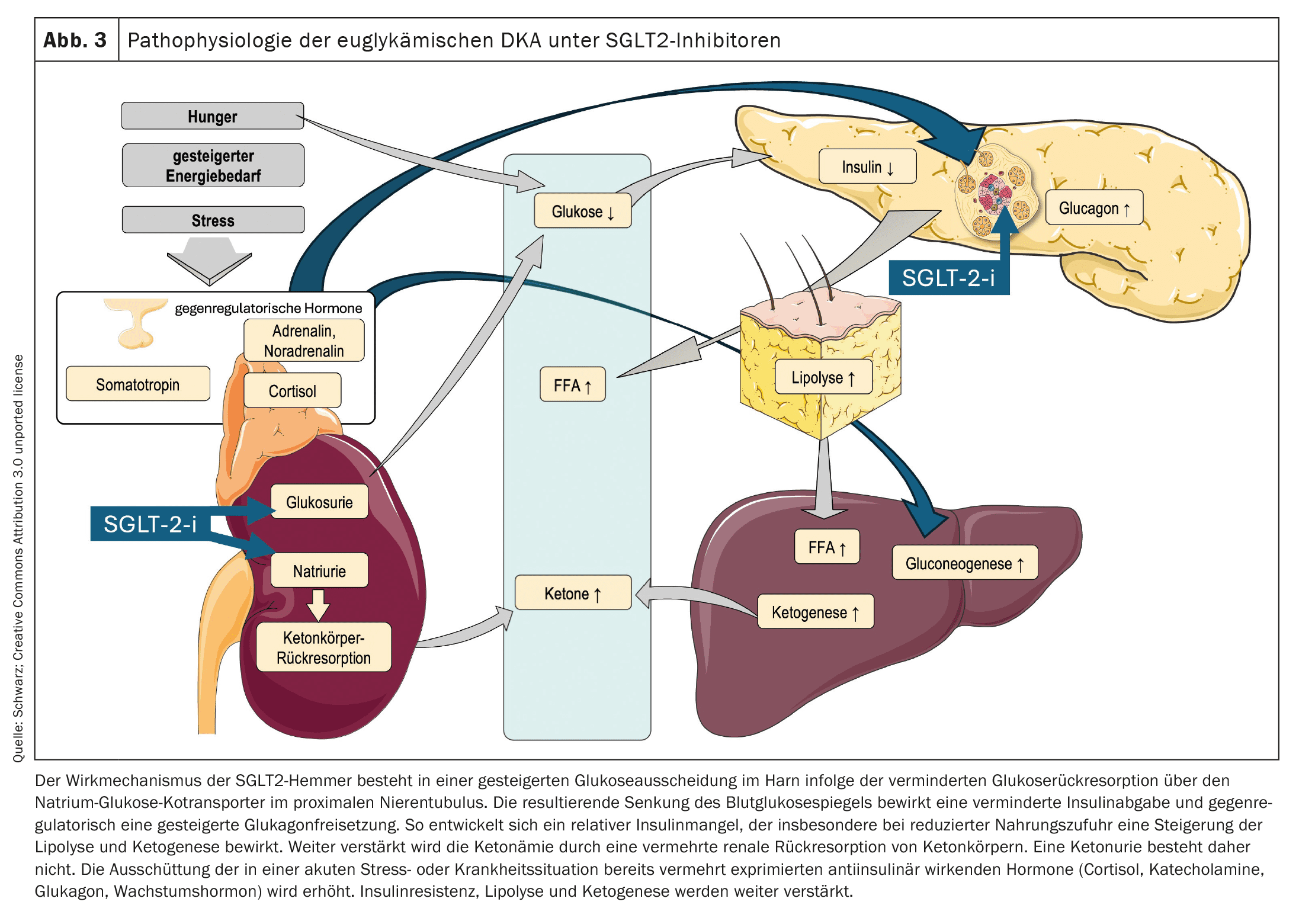
La physiopathologie de l’acidocétose euglycémique sous inhibiteurs SGLT2 n’est pas encore totalement comprise. On ne sait pas encore si les inhibiteurs du SGLT2 peuvent être à l’origine du développement d’une ACD ou s’ils ne font que masquer l’hyperglycémie en augmentant l’excrétion de glucose. Les mécanismes possibles sont présentés dans la figure 3.
Remarque : un manque d’insuline entraîne une hyperglycémie et, comme le glucose n’est pas absorbé par les cellules musculaires et adipeuses, un manque de glucose intracellulaire. Cela entraîne une augmentation de la concentration des hormones de contre-régulation. La production d’énergie se fait désormais principalement par cétogenèse, déclenchée par la lipolyse, au cours de laquelle les triglycérides sont décomposés en acides gras libres et en glycérol. Les corps cétoniques qui en résultent entraînent une acidose métabolique et sont détectables dans le sang et l’urine. L’hyperglycémie provoque une diurèse osmotique, des pertes de liquides et d’électrolytes et un risque de déshydratation.
Causes
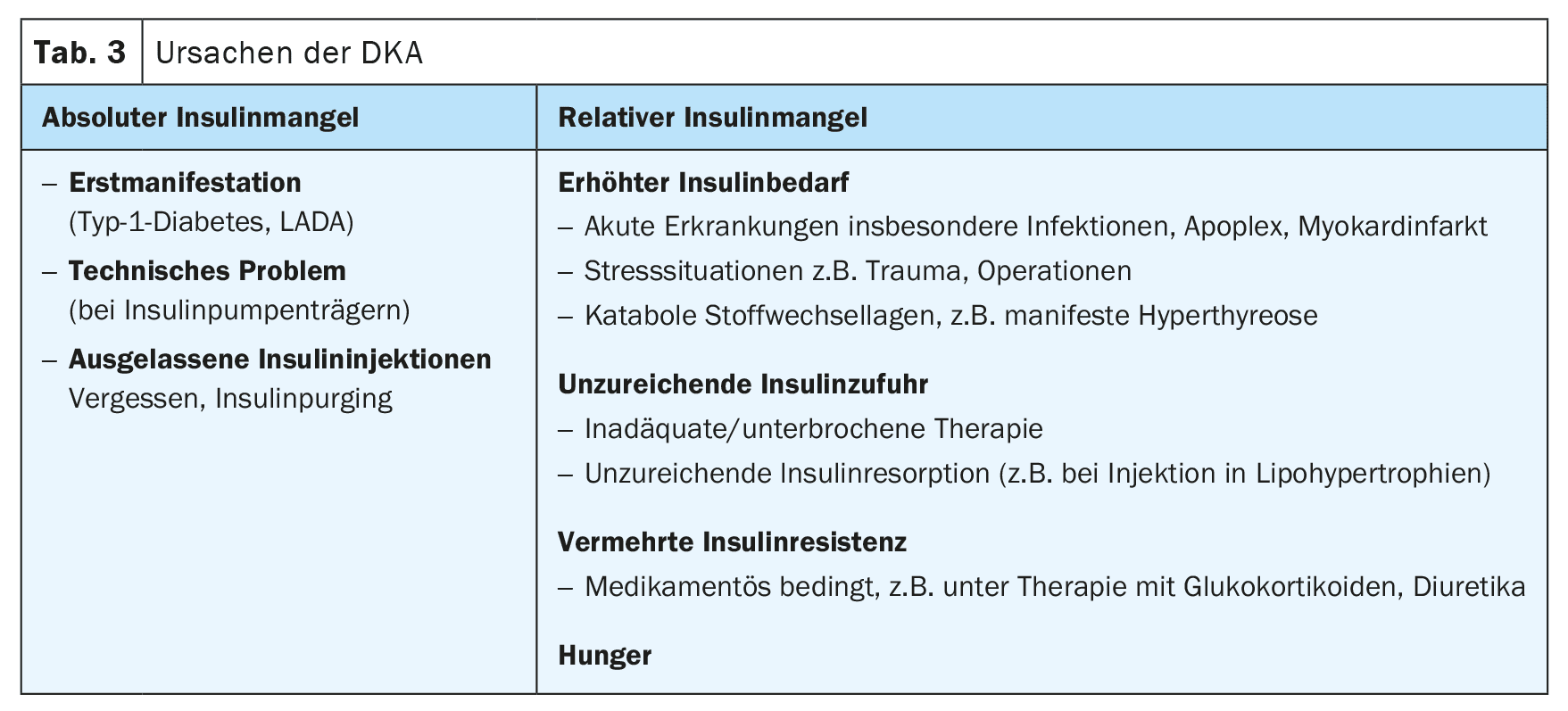
La condition préalable au développement d’un ACD est une carence en insuline. Celle-ci peut être due, comme dans le cas de la première manifestation d’un diabète de type 1, à une absence ou à une insuffisance d’apport en insuline ou être causée par un besoin accru, par exemple en cas de maladie aiguë ou d’opération (tableau 3).
Thérapie
Dans tous les cas, le traitement repose sur la compensation du déficit hydrique et électrolytique et du manque d’insuline. Il convient également de penser à une prophylaxie de la thrombose, en particulier en cas d’exsiccose.
Lorsqu’un patient se présente au cabinet médical avec une suspicion d’ACD, la première chose à faire (en plus de la mesure des paramètres vitaux et d’un examen clinique d’orientation) est de déterminer le glucose (à partir du plasma veineux) et le β-hydroxybutyrate (laboratoire du cabinet médical, les résultats doivent être disponibles au plus tard après 15 minutes). L’impossibilité de diagnostiquer l’acidose en ambulatoire laisse généralement peu de marge de manœuvre à cet égard. Dans la mesure où il n’y a pas d’acidocétose, mais seulement une cétonémie (β-HB <3 mmol/l), un traitement ambulatoire peut être mis en place (fig. 4, 5). Les patients doivent également suivre ce schéma après la mesure de taux élevés de cétones, dans la mesure où une consultation médicale n’est pas possible ou pas immédiatement possible. Cela présuppose une information et une instruction adéquates des patients (voir Prophylaxie).
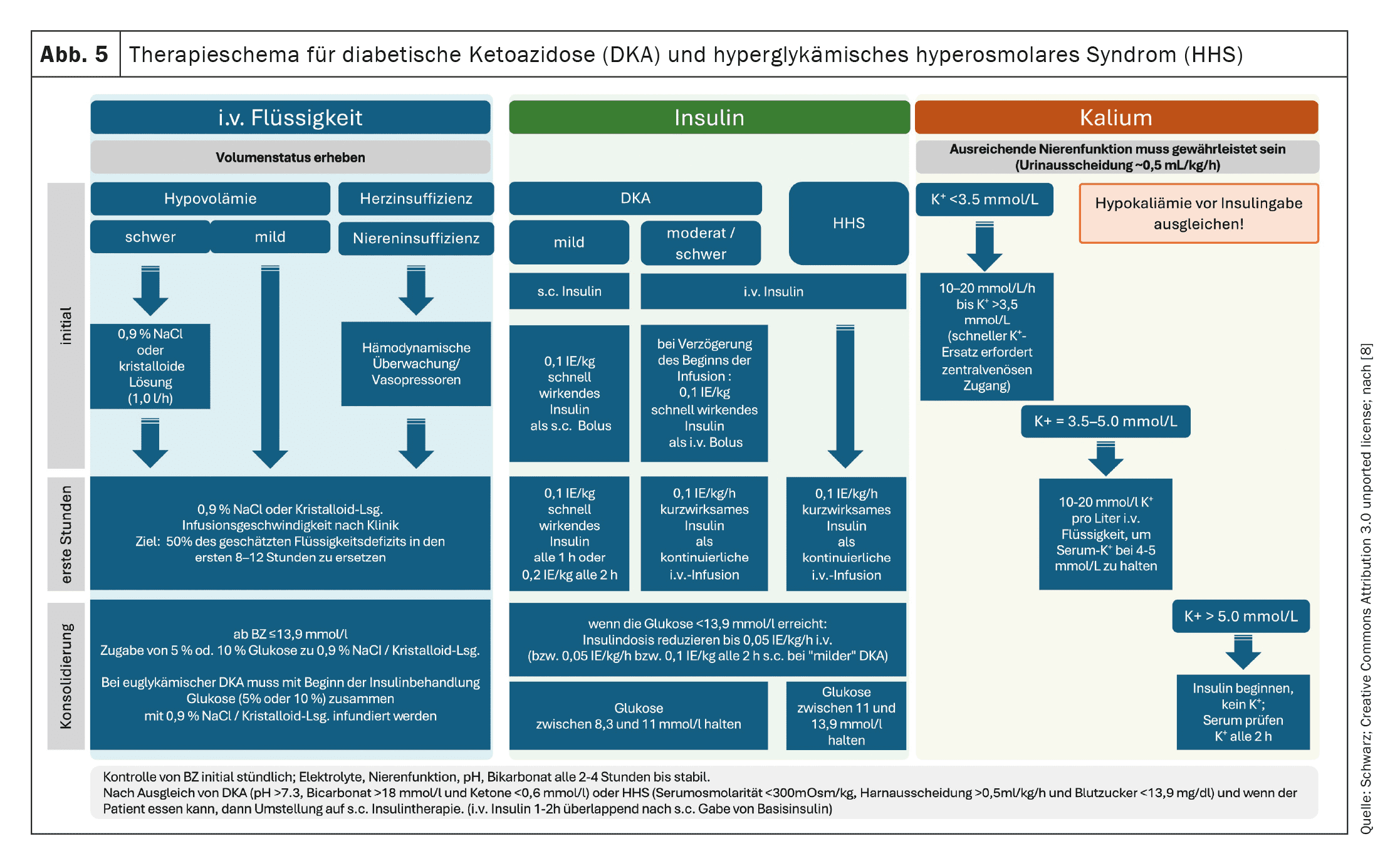
Si le taux est >3 mmol/l, une ACD est probable et donc un traitement hospitalier est généralement obligatoire. En attendant le transport (par ambulance), l’hydratation orale est arrêtée, une voie veineuse de grand volume est mise en place et la perfusion de solution cristalloïde isotonique équilibrée (uniquement, à défaut également du NaCl 0,9%) est commencée. La vitesse de perfusion doit être de 1 l/h. L’utilisation d’une solution saline “physiologique” présente non seulement l’inconvénient, par rapport aux solutions équilibrées, d’entraîner un risque d’acidose métabolique hyperchlorémique en cas de volumes importants, mais elle ne contient pas non plus de potassium, bien que celui-ci soit nécessaire. Une compensation ciblée de la perte de potassium causée par le manque d’insuline ne peut toutefois être effectuée que dans des conditions hospitalières.
Les patients souffrant d’une ACD de faible gravité peuvent être pris en charge dans une unité de soins normale, voire aux urgences si celles-ci offrent la possibilité d’un séjour de plusieurs heures. Pour les formes modérées et sévères, il est recommandé de les prendre en charge dans une unité de soins intermédiaires ou de soins intensifs.
La surveillance est effectuée en continu sur le moniteur selon un protocole standardisé, avec un contrôle initial de la fréquence cardiaque et respiratoire et de la pression artérielle toutes les 30 minutes, et une évaluation du GCS toutes les heures. Des contrôles de laboratoire doivent être effectués toutes les heures (glucose) ou toutes les 2 à 4 heures (électrolytes, fonction rénale, pH veineux, osmolalité).
Le déficit hydrique doit être corrigé dans les 24 à 48 premières heures. Un débit initial de 500-1000 ml/h pendant les 2-4 premières heures est recommandé. Toutefois, la prudence est de mise en cas d’administration rapide de liquide chez les personnes souffrant de maladies cardiaques ou rénales, les femmes enceintes, les personnes âgées ou les personnes présentant des comorbidités graves. En cas d’insuffisance cardiaque et/ou de maladie rénale terminale, il convient de traiter avec prudence en utilisant de plus petits bolus de solutions isotoniques ou cristalloïdes (par exemple, 250 ml chacun). On a longtemps pensé qu’une réhydratation trop rapide pouvait provoquer un œdème cérébral. Le mécanisme physiopathologique à l’origine de l’œdème cérébral lié à l’acidocétose diabétique est controversé. Le risque de lésions cérébrales n’est pas influencé par le débit de perfusion ni par la concentration de chlorure de sodium.
Typiquement, la concentration de glucose plasmatique chute à <11 mmol/l ou <200 mg/dl avant que l’acétonémie ne disparaisse. Il est donc nécessaire d’administrer du glucose supplémentaire à partir de ce niveau pour éviter l’hypoglycémie et permettre la poursuite de l’administration d’insuline.
La plupart des patients atteints d’ACD ont initialement un taux de potassium normal ou élevé. En raison de l’acidose et du manque d’insuline, il y a un déplacement des ions potassium de l’espace intracellulaire vers l’espace extracellulaire. La diurèse osmotique et l’augmentation de l’excrétion urinaire de potassium contribuent à un nouvel épuisement des réserves de potassium. Par conséquent, la substitution de potassium doit être initiée en même temps que l’administration d’insuline, même si les taux sériques de potassium sont normaux, afin d’éviter une hypokaliémie. Si une hypokaliémie sérique est présente au moment du diagnostic de l’ACD, une substitution de potassium doit être initiée en même temps que l’administration de liquides et la perfusion initiale d’insuline doit être retardée. L’administration de potassium doit être maintenue jusqu’à ce que le taux de potassium se normalise, que la fonction rénale soit normale et que la miction soit intacte.
L’hyponatrémie est également fréquente en cas d’ACD. Elle est due à une redistribution de l’eau de l’espace intracellulaire vers l’espace extracellulaire. En raison de la présence de glucose osmotiquement actif, il n’y a pas d’hypoosmolalité. L’hyponatrémie isotonique/hypertonique qui en résulte ne nécessite pas de traitement. Il est donc nécessaire de calculer la concentration sérique de sodium corrigée. Une correction n’est nécessaire que si elle révèle une carence en sodium. L’administration de bicarbonate pour traiter l’acidose métabolique n’est généralement pas utile, sauf en cas d’hyperkaliémie potentiellement mortelle et d’acidose sévère (pH <6,9).
L’insuline doit être administrée au moins une heure après le début de la réanimation liquide. Après un bolus initial (non recommandé chez les patients pédiatriques), de l’insuline normale ou une insuline analogue à courte durée d’action doit être administrée au moyen d’un perfuseur. En cas d’ACD légère, l’administration d’insuline peut également se faire par voie sous-cutanée. Le débit de perfusion d’insuline ne doit pas être réduit avant que l’acidocétose ne soit corrigée ou presque.
L’ACD est traitée lorsque les critères suivants sont remplis :
- aucun symptôme gastro-intestinal, l’administration orale de nourriture et de médicaments est possible
- les concentrations de glucose sanguin sont inférieures à 11 mmol/l ou 200 mg/dl
- β-hydroxybutyrate <0,6 mmol/l
- pH veineux ≥7,3 ou bicarbonate ≥18 mmol/l.
Lors du passage de l’insuline intraveineuse aux injections sous-cutanées, il convient de ne pas procéder trop brutalement et de procéder à une transition chevauchante. Une insuline analogue à longue durée d’action (Glargine U100 ou U300 ou Degludec, mais pas Icodec) est administrée 1 à 2 heures avant la fin de la perfusion d’insuline. Le moment optimal pour arrêter l’administration d’insuline i.v. est avant un repas, au cours duquel l’insuline s.c. est administrée pour la première fois. L’insuline doit être administrée avant le repas.
Prophylaxie
Les acidocétoses diabétiques sont des événements rares, la plupart des personnes atteintes de diabète n’en font heureusement jamais l’expérience. Cependant, celles qui se présentent à l’hospitalisation avec une ACD ont un risque très élevé de récidive. Étant donné que chaque ACD est une complication grave et, aujourd’hui encore, potentiellement mortelle, la prévention revêt une importance particulière. Le soutien et l’éducation sont les pierres angulaires de la prise en charge, et non la nécessité d’un régime d’insuline différent.
Les personnes ayant des problèmes psychosociaux, les malades mentaux et les groupes sociaux défavorisés sont particulièrement vulnérables. La consommation d’alcool et de cannabis augmente également le risque d’acidocétose. Ce sont précisément ces patients qui sont plus difficiles à atteindre avec nos scénarios de prise en charge et nos mesures d’éducation habituels. Un accompagnement psychologique est indiqué, mais généralement impossible pour des raisons de capacité.
Le thème de la gestion des situations d’urgence doit faire partie intégrante des formations régulières des diabétiques. Chaque patient devrait également recevoir un plan d’urgence individualisé. La dose moyenne d’insuline quotidienne y est également notée. Les utilisateurs d’une pompe à insuline (quel que soit le type, y compris l’AID) doivent savoir qu’ils ne doivent jamais effectuer les corrections nécessaires via la pompe.
Conclusion
L’acidocétose diabétique (ACD) est une urgence potentiellement mortelle chez les personnes atteintes de diabète sucré. Dans 1/3 des cas, elle touche les patients atteints de diabète de type 2. Les facteurs déclencheurs sont généralement des infections et/ou des erreurs dans l’insulinothérapie. Un manque absolu ou relatif d’insuline entraîne une lipolyse et une cétogenèse non inhibées. Il en résulte une hyperglycémie, une cétonémie et une acidose métabolique. L’hyperglycémie peut être absente (ACD euglycémique), en particulier sous traitement par inhibiteurs du SGLT2.
La base du traitement est la substitution volumétrique, l’administration d’insuline et la substitution potassique, accompagnées d’une surveillance étroite. Une fois l’ACD compensée, il est nécessaire d’en déterminer la cause. Une éducation de qualité et répétée est essentielle pour le pronostic des patients. Du côté des soignants, l’information et la connaissance de la maladie sont essentielles pour prendre des décisions rapides et correctes.
Messages Take-Home
- L’acidocétose diabétique (ACD) est une urgence potentiellement mortelle chez les personnes atteintes de diabète sucré. Les diabétiques de type 2 sont concernés dans 1/3 des cas. Les facteurs déclenchants sont généralement des infections et/ou des erreurs dans l’insulinothérapie.
- Une carence absolue ou relative en insuline entraîne une lipolyse et une cétogenèse non inhibées. Il en résulte une hyperglycémie, une cétonémie et une acidose métabolique. L’hyperglycémie peut être absente (ACD euglycémique), en particulier sous traitement par inhibiteurs du SGLT2.
- La base du traitement est la substitution volumétrique, l’administration d’insuline et la substitution potassique, accompagnées d’une surveillance étroite. Une fois l’ACD compensée, il est nécessaire d’en déterminer la cause.
- Une éducation de qualité et répétée est essentielle pour le pronostic des patients. Du côté des soignants, l’information et la connaissance de la maladie sont essentielles pour prendre des décisions rapides et correctes.
| Illustrations créées à l’aide de Servier Medical Art, sous licence Creative Commons Attribution 3.0 unported license. |
Littérature :
- American Diabetes Association Professional Practice C. 16. Prise en charge du diabète à l’hôpital : Standards de soins en matière de diabète-2025. Diabetes Care 2025 ; 48 : S321-S334 ; doi : 10.2337/dc25-S016.
- Perschinka F, Koglberger P, Klein SJ, et al : Hyponatrémie : Etiologie, diagnostic et traitement aigu. Med Klin Intensivmed Notfmed 2023 ; 118 : 505-517 ; doi : 10.1007/s00063-023-01049-0.
- Stewart PA, Nestor CC, Clancy C, et al : The peri-operative implications of sodium-glucose co-transporter 2 inhibitors : a narrative review. Anaesthesia 2025 ; 80 : 85-94 ; doi : 10.1111/anae.16461.
- Yan JW, Slim A, Van Aarsen K, et al : Balanced crystalloids (Ringer’s lactate) versus normal Saline in adults with diabetic cetoacidosis in the Emergency Department (BRISK-ED) : a pilot randomised controlled trial. Emerg Med J 2024 ; 41 : 103-111 ; doi : 10.1136/emermed-2023-213290.
- Dhatariya K, James J, Kong MF, et al : Diabetes at the front door. A guideline for handling with glucose related emergencies at the time of acute hospital admission from the Joint British Diabetes Society (JBDS) for Inpatient Care Group. Diabet Med 2020 ; 37 : 1578-1589 ; doi : 10.1111/dme.14304.
- Tamsett Z, James S, Brown F, et al : Modifiable factors to prevent severe hypoglycaemic and diabetic ketoacidosis presentations in people with type 1 diabetes. Diabet Med 2024 ; 41 : e15384 ;
doi : 10.1111/dme.15384. - Gupta A, Brazier B, Rengarajan L, et al : Determining factors influencing hospital stay for individuals admitted with diabetes-related ketoacidosis – findings from DEKODE length of stay quality improvement project. Clin Med (Lond) 2024 ; 24 : 100255 ; doi : 10.1016/j.clinme.2024.100255.
- Umpierrez GE, Davis GM, El Sayed NA, et al : Hyperglycaemic crises in adults with diabetes : a consensus report. Diabetologia 2024 ; 67 : 1455-1479 ; doi : 10.1007/s00125-024-06183-8.
- Sacks DB, Arnold M, Bakris GL, et al : Guidelines and Recommendations for Laboratory Analysis in the Diagnosis and Management of Diabetes Mellitus. Diabetes Care 2023 ; 46 : e151-e199 ; doi : 10.2337/dci23-0036.
- Holt RIG, De Vries JH, Hess-Fischl A, et al : The Management of Type 1 Diabetes in Adults. Un rapport de consensus de l’American Diabetes Association (ADA) et de l’Association européenne pour l’étude du diabète (EASD). Diabetes Care 2021 ; 44 : 2589-2625 ; doi : 10.2337/dci21-0043.
- Dhatariya KK, Glaser NS, Codner E, et al : Diabetic ketoacidosis. Nat Rev Dis Primers 2020 ; 6 : 40 ; doi : 10.1038/s41572-020-0165-1.
InFo DIABETOLOGIE & ENDOKRINOLOGIE 2025 ; 2(1) : 6-12