Une équipe de recherche a collecté des données dans dix pays afin d’évaluer les avantages des stratégies de traitement actuelles et antérieures de la dermatite atopique. Les résultats devraient contribuer à améliorer la “gestion de la maladie”. L’une des conclusions de l’étude était qu’à partir d’un certain degré de sévérité, le traitement topique seul ne suffit souvent pas à répondre aux principales attentes du traitement (soulagement des démangeaisons et guérison des lésions cutanées), et que l’utilisation d’agents thérapeutiques systémiques est nécessaire.
Pour cette étude d’enquête “en monde réel”, des patients adultes atteints de dermatite atopique (DA) ont été recrutés via des panels Internet pour une enquête basée sur le Web entre juillet et septembre 2019 [1]. Au total, 1988 patients atteints de la MA, originaires d’Allemagne, de France, de Grande-Bretagne, de Belgique, des Pays-Bas, d’Italie, d’Espagne, du Canada, d’Australie et du Japon ont été inclus dans l’analyse. Les critères d’inclusion comprenaient notamment l’âge (≥18 à ≤75 ans**) et le traitement en cours. Outre les données démographiques, les caractéristiques de la maladie, y compris la pire BSA (Body Surface Area) évaluée par les patients au cours de l’année précédente, les stratégies de traitement (traitements antérieurs/actuels, raisons de l’arrêt, traitement des poussées aiguës de la MA) et les bénéfices du traitement (attentes du traitement de la MA et mesure dans laquelle les attentes ont été satisfaites) ont été recueillis. Les participants inclus dans l’analyse étaient traités au moment de l’enquête par des monothérapies topiques (corticostéroïdes topiques, inhibiteurs de la calcineurine) ou des traitements systémiques conventionnels (cSys ; corticostéroïdes systémiques, immunosuppresseurs) ou biologiques (à ce moment-là, uniquement dupilumab$). Les participants recevant actuellement une photothérapie ou un traitement combiné par cSys et des produits biologiques ont été exclus.
** Au Japon, la limite d’âge inférieure était de ≥18 ans.
$ avec ou sans traitements topiques
Chez les BSA≥10%, davantage de flares sont apparus sous traitement topique seul
Un BSA<10% a été observé chez 86,6% des participants à l’étude [1]. La durée moyenne de la maladie était plus longue chez les patients dont la BSA était ≥10% que chez ceux dont la BSA était<10%. Les traitements de la DA les plus utilisés dans les deux groupes de BSA étaient les monothérapies topiques (69,69%), suivies par les traitements systémiques conventionnels (28,1%) – y compris les corticostéroïdes (16%) et les immunosuppresseurs (12,1%) – et les produits biologiques (2,3%). Le nombre moyen de poussées au cours de l’année écoulée était plus élevé chez les patients ayant un BSA≥10% que chez les patients ayant un BSA<10%. Indépendamment de l’implication de la BSA, la plupart des patients ont traité les flashes aigus avec des médicaments topiques (73,4%), suivis par les traitements systémiques conventionnels (25,3%) et les médicaments biologiques (1,3%). Les patients avec un BSA≥10%, comparés à ceux avec un BSA<10%, ont utilisé moins de monothérapies topiques pendant une poussée (67,5% contre 74,1%), tandis que la proportion de traitements cSys était plus élevée (31,7% contre 24,6%).
Les participants présentant un BSA ≥10% et traités par monothérapie topique ont connu davantage de poussées de la maladie et étaient plus susceptibles d’arrêter le traitement topique en raison d’une tolérance cutanée insuffisante. Cela souligne la nécessité de solutions de traitement systémique à long terme pour ces patients adultes [2,3].
| La dermatite atopique (DA) est une maladie inflammatoire chronique de la peau qui se caractérise par des lésions eczémateuses, très prurigineuses et souvent douloureuses, affectant le sommeil, le bien-être et la qualité de vie des patients [9]. La DA modérée à sévère justifie généralement un traitement systémique et est définie par un indice de surface et de sévérité de l’eczéma (EASI) ≥16 ou EASI <16 plus ≥1 des conditions suivantes : Localisation sur le visage, les mains ou la région génitale ; démangeaisons avec un score de rating numérique (NRS) >7 ; troubles du sommeil avec NRS >7 ; altération de la qualité de vie avec un indice de qualité de vie en dermatologie (DLQI) >10 ou une participation minimale de ≥10% de la surface corporelle (BSA) [4,5,10,11]. |
Dans quelle mesure les attentes en matière de thérapie ont-elles été satisfaites ?
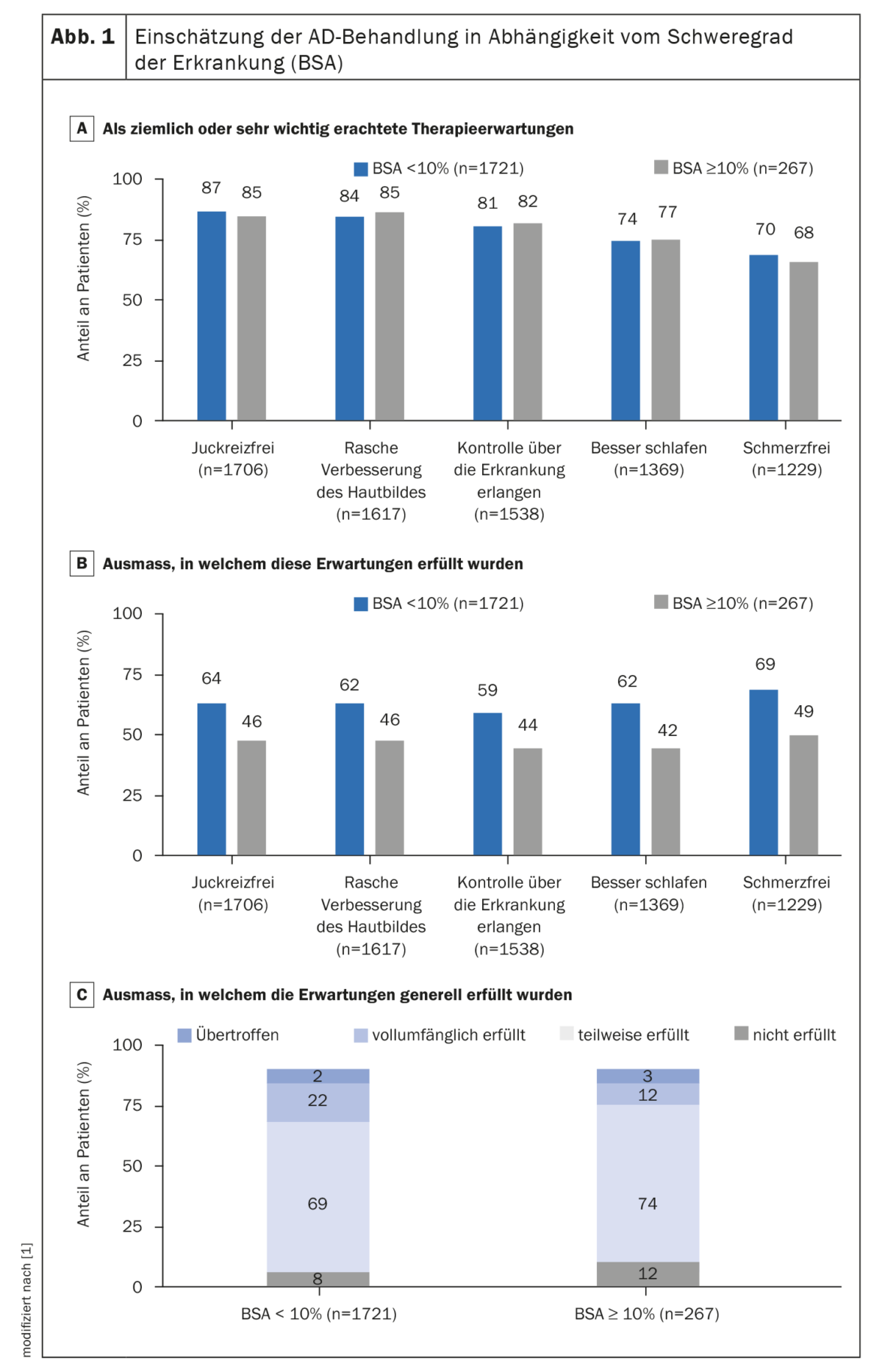
Les principales attentes des participants vis-à-vis du traitement, indépendamment de leur participation au BSA, étaient de ne plus avoir de démangeaisons, d’avoir rapidement une meilleure apparence de la peau, de contrôler à nouveau la maladie, de mieux dormir et de ne plus ressentir de douleurs (Fig. 1A) [1]. Au total, 75% des patients ont déclaré que leurs attentes n’avaient été que partiellement ou pas du tout satisfaites. Les patients ayant un BSA≥10% sont moins susceptibles de déclarer que leurs attentes ont été entièrement satisfaites que les patients ayant un BSA<10% (figures 1B, 1C) [1].
La principale raison de l’arrêt d’un traitement AD antérieur était une tolérance cutanée insuffisante chez 31,9% des patients. Les autres raisons de l’arrêt des traitements antérieurs étaient les recommandations du médecin (26,3%), un effet non persistant (26,5%) et un début d’action lent du médicament (24,9%). Lorsqu’il a été demandé aux patients d’indiquer les raisons de l’arrêt des traitements par classe de médicaments, les préparations topiques ont été arrêtées principalement en raison d’une absence de manifestation insuffisante (35,5%), les traitements cSys principalement en raison d’un changement de traitement recommandé par le médecin (29,4%) et les produits biologiques principalement en raison d’un début d’action trop lent (32,3%).
Ceux dont la participation à la surface du corps était ≥10% ont signalé une moindre satisfaction vis-à-vis du traitement. Dans l’ensemble, cette étude indique qu’il existe des besoins médicaux non satisfaits dans le domaine du traitement de la MA.
Discussion
Afin d’obtenir un contrôle adéquat de la DA modérée/sévère, il est recommandé d’adopter une stratégie de traitement personnalisée en tenant compte de différents facteurs tels que la BSA, la fréquence des poussées, la qualité de vie et les spécificités de chaque option thérapeutique systémique [2,4–7]. Le fait que, dans cette étude, les attentes de la plupart des patients adultes n’aient pas été satisfaites ou ne l’aient été que partiellement, et qu’un pourcentage plus élevé de patients avec un BSA ≥10% aient déclaré que leurs attentes en matière de traitement n’avaient pas été satisfaites, est peut-être lié à un contrôle insuffisant des symptômes par une monothérapie topique.
Les auteurs de l’étude soulignent qu’il est important de ne pas priver les patients éligibles à un traitement systémique. Ils indiquent en outre que des thérapies combinées peuvent être utiles pour atteindre les objectifs thérapeutiques visés [2,7,8]. Parmi les limites méthodologiques, les auteurs citent le nombre relativement faible de participants sous traitement biologique, la participation BSA auto-déclarée et un éventuel biais de sélection et d’information. Comme l’enquête a été réalisée en 2019, elle ne reflète pas entièrement l’environnement de traitement actuel, a-t-il ajouté.
Néanmoins, les résultats de l’étude sont instructifs car ils montrent que le soulagement des démangeaisons et l’amélioration de l’aspect de la peau, qui sont des objectifs prioritaires dans le traitement de la dermatite atopique, ne sont souvent pas atteints avec un traitement topique seul et qu’il peut être important de ne pas manquer le moment d’un traitement systémique.
Littérature :
- Augustin M, et al : Real-World Treatment Patterns and Treatment Benefits among Adult Patients with Atopic Dermatitis : Results from the Atopic Dermatitis Patient Satisfaction and Unmet Need Survey. Acta Derm Venereol 2022 ; 102 : adv00830.
- Boguniewicz M, et al : Expert perspectives on management of moderate-to-severe atopic dermatitis : a multidisciplinary consensus addressing current and emerging therapies. J Allergy Clin Immunol Pract 2017 ; 5 : 1519-1531.
- Fougerousse A-C, et al : Utilisation des médicaments systémiques pour le traitement de la dermatite atopique de l’adulte en France : résultats d’une enquête de pratique. Clin Cosmet Investig Dermatol 2021 ; 14 : 179-183.
- Wollenberg A, et al : Consensus-based European guidelines for treatment of atopic eczema (atopic dermatitis) in adults and children : part I. J Eur Acad Dermatol Venereol 2018 ; 32 : 657-682.
- Wollenberg A, et al : ETFAD/EADV Eczema task force 2020 position paper on diagnosis and treatment of atopic dermatitis in adults and children. J Eur Acad of Dermatol and Venereol 2020 ; 34 : 2717-2744.
- Simpson EL, et al : When does atopic dermatitis warranty systemic therapy ? Recommendations from an expert panel of the International Eczema Council. J Am Acad Dermatol 2017 ; 77 : 623-633.
- Fougerousse A-C, et al : Utilisation des médicaments systémiques pour le traitement de la dermatite atopique de l’adulte en France : résultats d’une enquête de pratique. Clin Cosmet Investig Dermatol 2021 ; 14 : 179-183.
- Bieber T : Dermatite atopique : un pipeline thérapeutique en expansion pour une maladie complexe. Nat Rev Drug Discov 2022 ; 21 : 21-40.
- Augustin M, et al : Characterizing treatment-related patient needs in atopic eczema : insights for personalized goal orientation. J Eur Acad Dermatol Venereol 2020 ; 34 : 142-152.
- Calzavara Pinton P, et al. : Diagnostic et prise en charge de la dermatite atopique modérée à sévère de l’adulte : un consensus de la Société italienne de dermatologie et de vénéréologie (SIDeMaST), de l’Association italienne des dermatologues hospitaliers (ADOI), de la Société italienne d’allergie, d’asthme et d’immunologie clinique (SIAAIC), et de la Société italienne de dermatologie allergologique, environnementale et professionnelle (SIDAPA). G Ital Dermatol Venereol 2018 ; 153 : 133-145.
- Schmitt J, et al : Determinants of treatment goals and satisfaction of patients with atopic eczema. J Dtsch Dermatol Ges 2008 ; 6 : 458-465.
DERMATOLOGIE PRATIQUE 2023 ; 33(3) : 20-21