Le diabète sucré de type 2 est une maladie fréquente chez les patients âgés, dont la prévalence est en augmentation. Outre les aspects typiques du diabète, il existe souvent des syndromes gériatriques spécifiques tels que la démence ou un risque accru de chute. Les grands principes du traitement du diabète à prendre en compte chez les patients âgés sont les suivants : Éviter les hypoglycémies ; déterminer individuellement le taux d’HbA1c-Le choix des antidiabétiques en fonction de l’effet hypoglycémiant attendu, du profil d’effets secondaires et de l’adaptation de la dose de médicament en cas d’insuffisance rénale ; “start low and go slow !” L’insulinothérapie est souvent commencée trop tard, mais elle peut améliorer de manière décisive la qualité de vie et a un effet anabolisant.
Le diabète sucré de type 2 est une maladie fréquente chez les personnes âgées. Le risque de développer un diabète augmente avec l’âge – en association avec des facteurs de risque également croissants tels que l’obésité, la malnutrition et le manque d’activité physique. L’allongement de l’espérance de vie entraînera une nouvelle augmentation du nombre de diabétiques dans cette tranche d’âge au cours des prochaines décennies. D’ores et déjà, jusqu’à 15% des personnes de plus de 60 ans sont atteintes de diabète sucré.
Outre le contrôle du métabolisme, la prévention des hypoglycémies et le traitement des complications secondaires, le traitement doit également tenir compte des syndromes gériatriques fréquents tels que la démence, le risque de chute, l’incontinence ou la dépression. Il convient de noter que la plupart des études d’intervention sur le diabète se concentrent principalement sur les jeunes patients. Selon une compilation récente, à peine 0,6% de ces études ont examiné des groupes de patients spécifiquement âgés, près d’un tiers ont exclu les patients de plus de 65 ans et presque toutes n’ont pas inclus de personnes de plus de 75 ans [1]. De plus, les données à long terme ne sont pas encore disponibles pour la plupart des préparations récentes. Cela relativise l’influence des guidelines basées sur les preuves [2,3], mais souligne également l’importance de l’approche thérapeutique individualisée. Le présent article a donc pour but de fournir un aperçu actuel et pratique du traitement de ce groupe de patients, qui est fréquemment rencontré dans la pratique clinique quotidienne et qui présente de multiples facettes.
Modifications du métabolisme des glucides avec l’âge
Avec l’âge, la masse fonctionnelle des cellules bêta diminue, associée à une baisse de la sécrétion d’insuline stimulée par le glucose et à une diminution de la réponse des cellules bêta aux incrétines endogènes (GLP-1 et GIP). De plus, la résistance à l’insuline déjà présente s’aggrave généralement. Les causes en sont une augmentation de la masse grasse (viscérale) due à une activité physique réduite et une diminution de la sensibilité à l’insuline due aux médicaments (par exemple les glucocorticoïdes). Le tissu musculaire, qui est l’un des trois principaux organes cibles du métabolisme des glucides avec le foie et le tissu adipeux, est de plus en plus visé par les changements liés à l’âge chez les patients diabétiques. La diminution excessive et multifactorielle de la masse ou de la force musculaire (sarcopénie) chez les personnes âgées joue un rôle central dans l’homéostasie complexe entre l’action de l’insuline et le métabolisme du glucose et constitue une autre cause de l’augmentation de la résistance à l’insuline chez les personnes âgées [4].
Aspects particuliers chez les patients âgés atteints de diabète sucré
Un grand nombre de syndromes gériatriques sont plus fréquents chez les patients âgés atteints de diabète sucré et ont un impact négatif sur le contrôle métabolique, l’état fonctionnel, la qualité de vie et la mortalité. Par exemple, les troubles cognitifs et les syndromes démentiels détériorent considérablement l’autogestion du diabète, augmentent le risque d’hypoglycémie et rendent ainsi plus difficile un bon contrôle du métabolisme. La dépression est nettement plus fréquente chez les diabétiques âgés, mais elle n’est souvent pas diagnostiquée ou traitée de manière adéquate et a – outre des effets sur les capacités cognitives – une influence sur le contrôle du diabète.
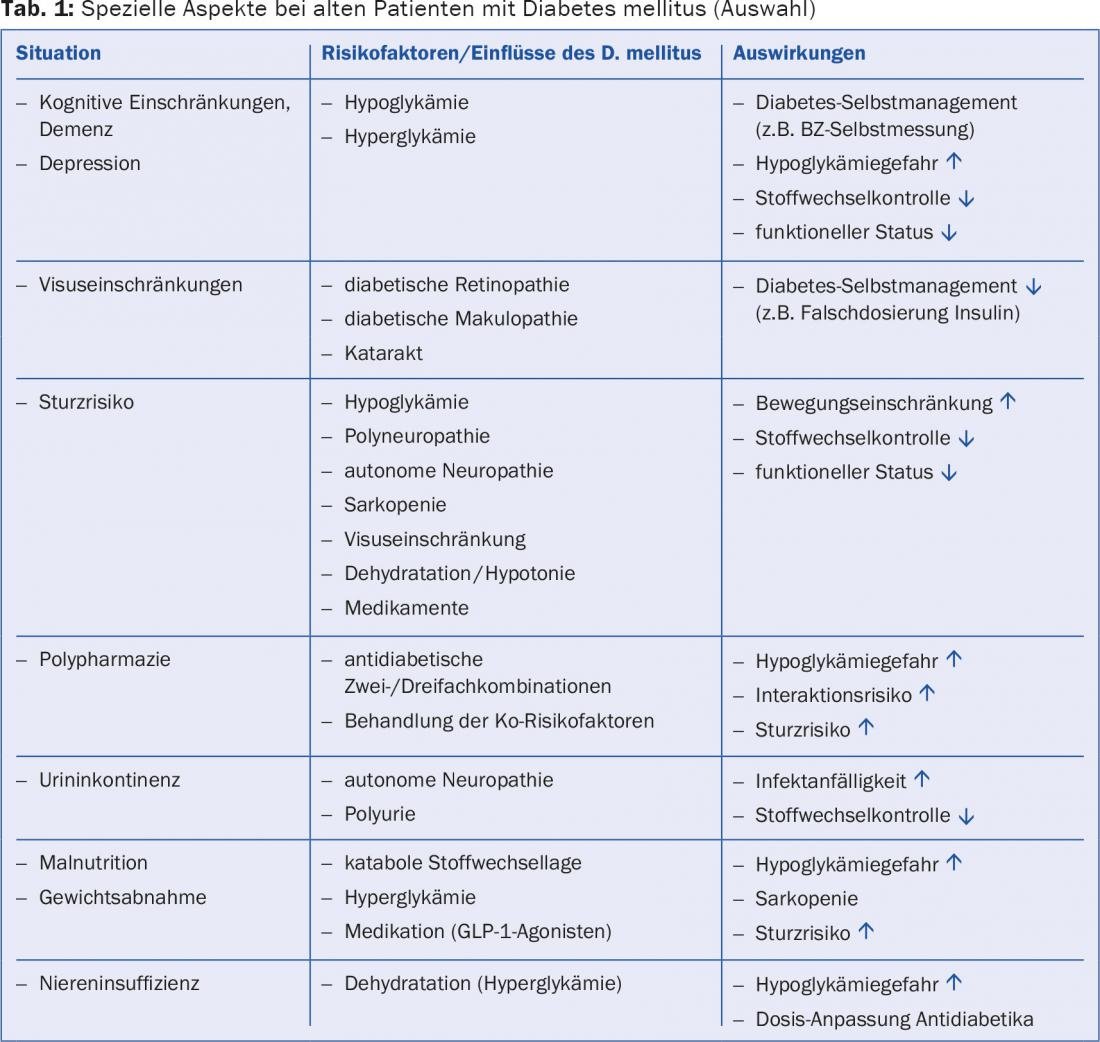
Outre les aspects spécifiquement gériatriques, il convient d’accorder une grande attention aux limitations des fonctions rénales, hépatiques et cardiaques liées à l’âge ou aux comorbidités. Cela est particulièrement important pour le choix et le dosage des antidiabétiques et pour les interactions avec d’autres médicaments, car cela modifie également les paramètres pharmacodynamiques et pharmacocinétiques. Il convient également de noter que la créatinine, mais aussi le DFG estimé à l’aide d’une formule (eGFR), peuvent en soi refléter de manière imprécise la fonction rénale chez les patients âgés et que le degré d’altération de la fonction rénale est donc souvent sous-estimé. Le tableau 1 donne un aperçu des aspects particuliers de la prise en charge des patients âgés atteints de diabète sucré.
Traitement
Les quatre grands principes du traitement du diabète sucré chez les patients âgés sont les suivants :
- Éviter les hypoglycémies
- Définition individuelle de la plage cible d’HbA1c
- Sélection des antidiabétiques en fonction de l’effet hypoglycémiant attendu, du profil d’effets secondaires et de l’adaptation de la dose de médicament en cas d’insuffisance rénale.
- Start low and go slow !
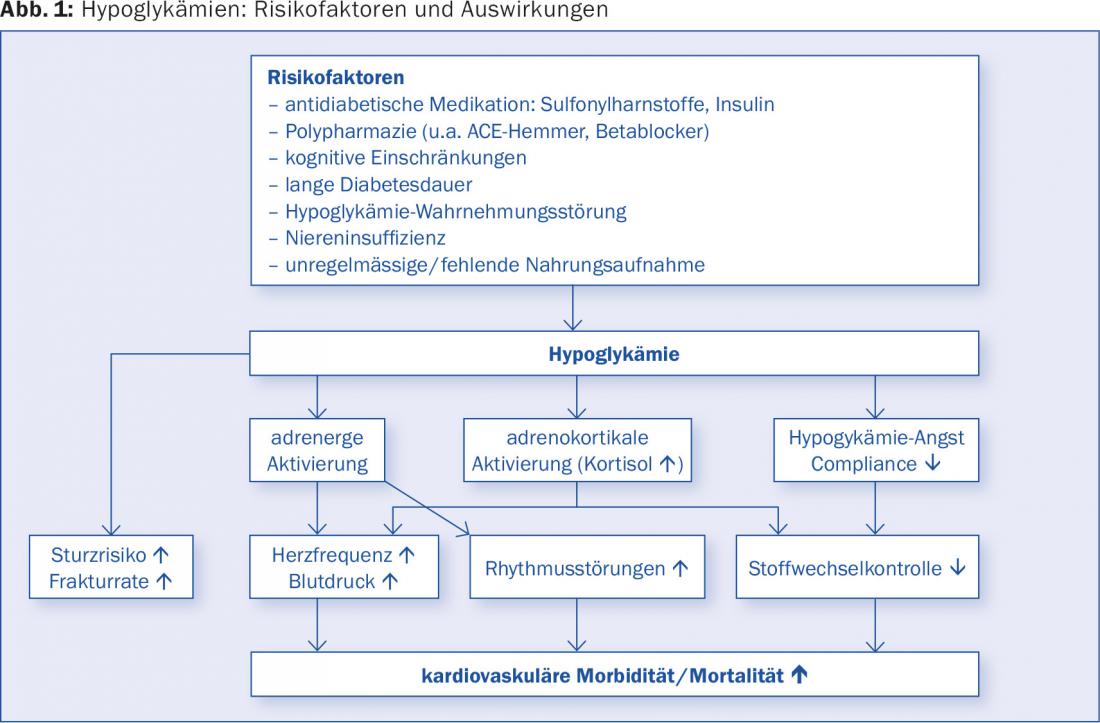
Éviter les hypoglycémies (Fig. 1) : Le risque d’hypoglycémie augmente avec la durée du diabète. Il est fréquent que les patients âgés ne perçoivent pas suffisamment les symptômes d’hypoglycémie adrénergique. Il n’est pas rare que les symptômes neuroglycopéniques soient considérés comme des symptômes de démence ou de troubles circulatoires cérébraux, ce qui sous-estime considérablement la véritable prévalence des hypoglycémies au quotidien chez ces patients. Les hypoglycémies sévères récurrentes sont un facteur de risque important de démence [5]. Elles provoquent des chutes, augmentent le risque de fracture et entraînent une augmentation des hospitalisations [6]. Toute hypoglycémie active le système sympathoadrénal et peut donc déclencher des troubles du rythme et augmenter la pression artérielle, ce qui accroît la morbidité et la mortalité cardiovasculaires. Les hypoglycémies peuvent être réduites, d’une part, en évitant les facteurs de risque qui prédisposent le patient à l’hypoglycémie et, d’autre part, en choisissant les thérapeutiques appropriées. Le nombre croissant de nouveaux antidiabétiques (agents thérapeutiques à base d’incrétine et inhibiteurs du SGLT-2) constitue un complément précieux, car ces produits ne présentent pas de risque hypoglycémique intrinsèque.
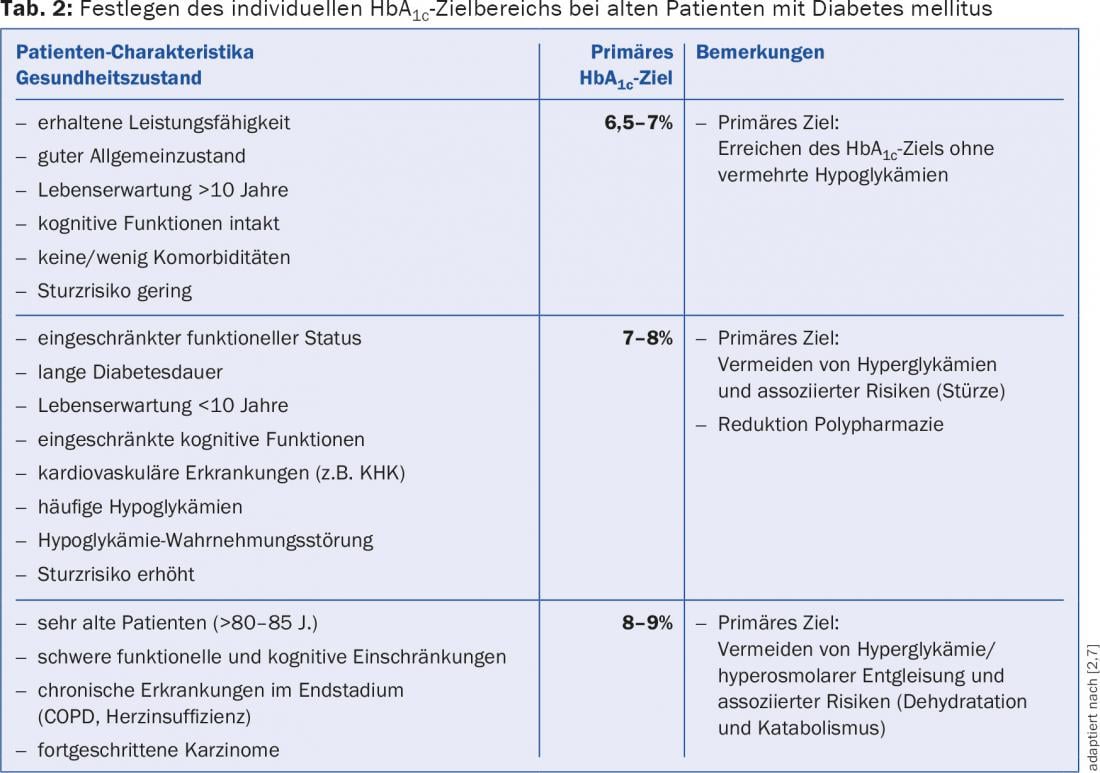
Définition de la plage cible individuelle d’HbA1c (tableau 2) : Le but du traitement global du diabète est de prévenir ou de réduire les complications secondaires micro et macrovasculaires grâce à un contrôle métabolique adéquat et au traitement des co-facteurs de risque. Outre les hypoglycémies, les états hyperglycémiques persistants (c’est-à-dire des valeurs supérieures à 15-20 mmol/l) doivent être évités, car ils entraînent – outre des effets défavorables sur la fonction cérébrale et l’acuité visuelle – une déshydratation et un bilan calorique négatif dus à la glucosurie et aggravent la malnutrition. Les valeurs cibles sont fixées en fonction de facteurs très divers (espérance de vie, risque d’hypoglycémie, ressources du patient, etc.), comme pour les patients plus jeunes et en fonction des recommandations actuelles [7] (tableau 2).
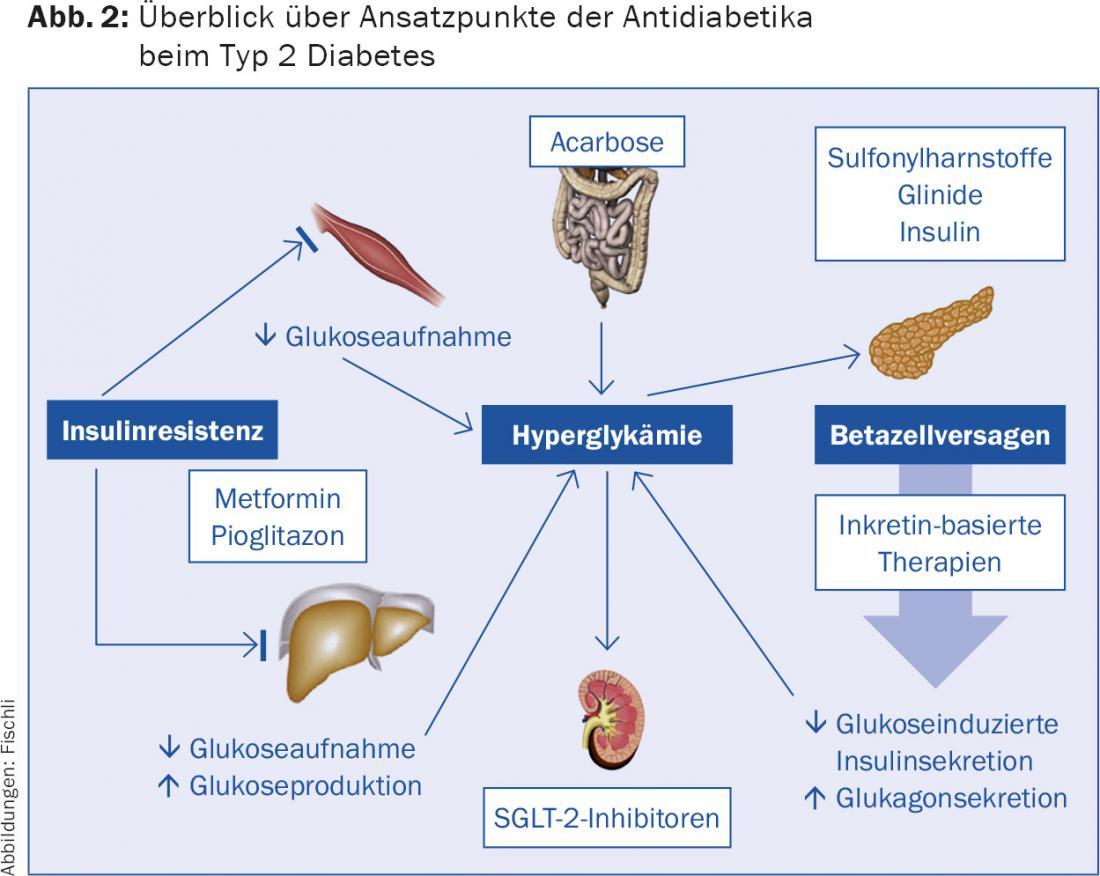
Sélectionner les antidiabétiques en fonction de l’effet hypoglycémiant et du profil d’effets secondaires attendus (fig. 2, tab. 3) : Une fois que la zone cible appropriée pour le patient [7,8] a été définie, les régimes thérapeutiques correspondants sont établis. Il faut tenir compte de l’effet hypoglycémiant attendu ainsi que des profils d’effets secondaires. Toute altération de la fonction rénale avec diminution du DFG en dessous de 60 ml/min doit faire l’objet d’une réévaluation critique du traitement antidiabétique [9]. Si nécessaire, un ajustement de la dose doit être effectué ou le médicament doit être arrêté (tableau 3).
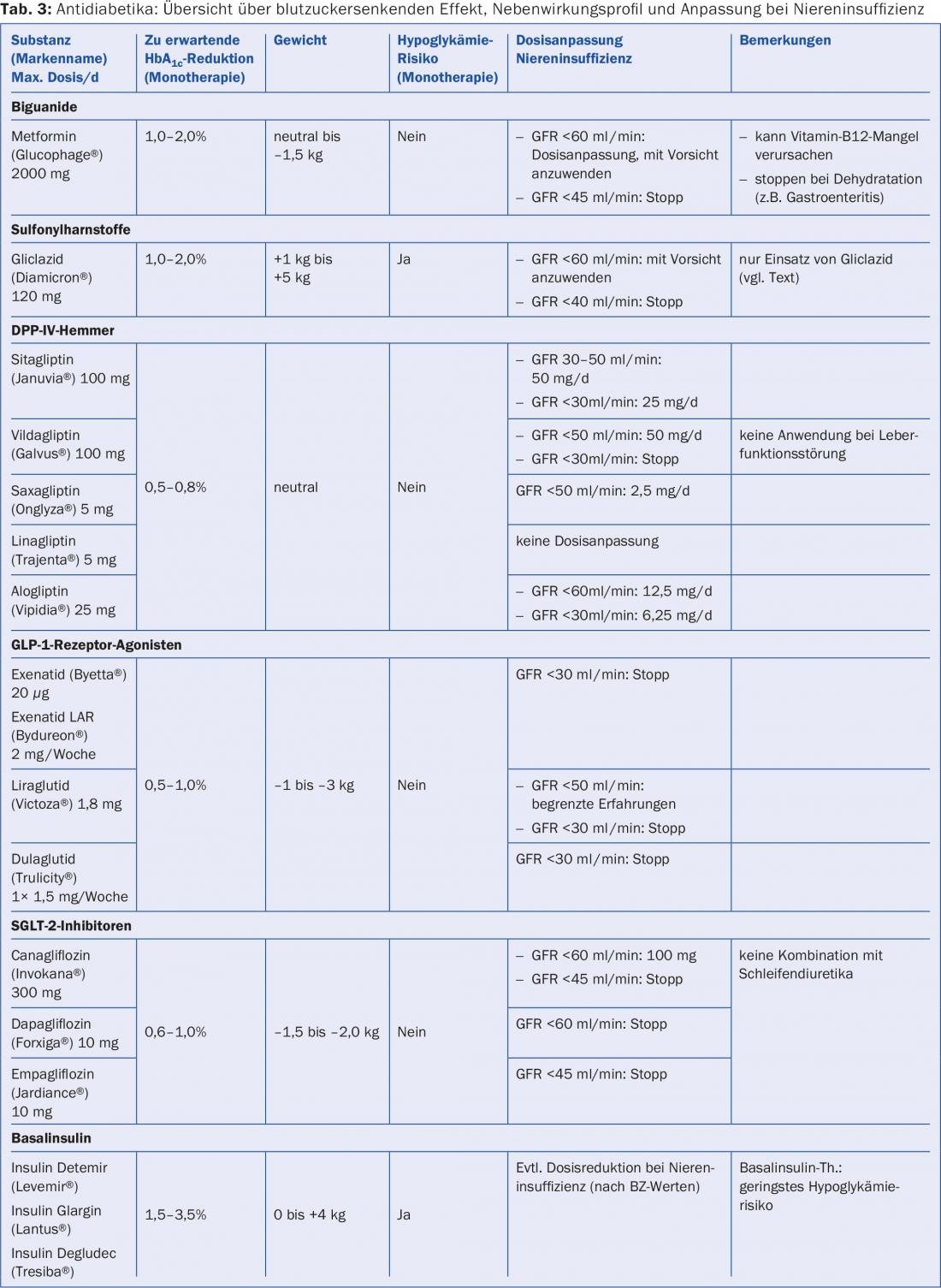
Aperçu des agents thérapeutiques les plus utilisés
La metformine : La metformine reste le traitement médicamenteux de choix du diabète sucré de type 2. La metformine ne doit généralement plus être utilisée chez les patients âgés dont le DFG est inférieur à 60 ml/min. Le risque d’acidose lactique est surtout accru en présence d’autres maladies (insuffisance cardiaque sévère, insuffisance hépatique, BPCO sévère). Les patients doivent être informés que la metformine doit impérativement être interrompue en cas d’état de déshydratation et de risque de développement rapide d’une insuffisance rénale pré-rénale (par exemple fièvre élevée, gastro-entérite) et avant l’application d’un produit de contraste radiologique. Il convient de noter que la metformine réduit l’absorption intestinale de la vitamine B12 et peut entraîner des carences en vitamine B12, ce qui peut aggraver une polyneuropathie ou les fonctions cognitives.
Sulfonylurées : les sulfonylurées présentent un risque d’hypoglycémie et sont particulièrement problématiques chez les patients souffrant de malnutrition et de prise alimentaire irrégulière (syndromes démentiels !). Parmi les préparations disponibles en Suisse, seul le gliclazide (p. ex. Diamicron®) devrait être utilisé en premier lieu, car cette substance présente le plus faible potentiel d’hypoglycémie et – contrairement au glibenclamide et au glimépiride – est métabolisée par voie hépatique en métabolites inactifs. Le gliclazide doit être arrêté si le DFG est inférieur à 40 ml/min.
Gliptines : en raison de leur bonne tolérance, de leur faible potentiel d’effets secondaires (neutralité pondérale), de leur administration par voie orale et de l’absence de risque intrinsèque d’hypoglycémie, les gliptines constituent une bonne option thérapeutique chez les patients âgés. Il convient de noter que, sauf pour la linagliptine (Trajenta®), la dose doit être adaptée en cas d’insuffisance rénale (tableau 3). L’effet hypoglycémiant est cependant moindre comparé aux sulfonylurées ou aux analogues du GLP-1.
Agonistes des récepteurs du GLP-1 : le liraglutide (Victoza®) et l’exénatide (Byetta®/Bydureon®) doivent être injectés par voie sous-cutanée et sont associés à des effets secondaires gastro-intestinaux dans 10 à 20% des cas, surtout pendant la phase initiale. Ils entraînent une perte de poids et ne sont donc pas adaptés aux patients souffrant de malnutrition. Chez les diabétiques obèses et insulinorésistants, ils représentent une option raisonnable et peuvent être associés à l’insuline (liraglutide, exénatide ou l’association insuline dégludec et liraglutide Xultophy®). Les agonistes des récepteurs du GLP-1 sont arrêtés si le DFG est inférieur à 30 ml/min.
Inhibiteurs du SGLT-2 : ces nouvelles préparations inhibent l’absorption tubulaire rénale du glucose et agissent indépendamment de la fonction résiduelle des cellules bêta et de la résistance à l’insuline. Cela en fait – outre l’absence de risque d’hypoglycémie et l’effet de réduction du poids – une option thérapeutique valable également pour les diabétiques âgés dont le diabète est installé depuis longtemps. Les inhibiteurs de SGLT-2 peuvent être associés à l’insuline. Il convient de noter le risque accru d’infections urogénitales (en particulier chez les femmes) et le risque de déplétion volumique (hypotension orthostatique) lorsque ces substances sont associées à des diurétiques de l’anse. L’effet est limité avec l’augmentation de l’insuffisance rénale, c’est pourquoi les préparations sont arrêtées à partir d’un certain degré de restriction de la fonction rénale (tab. 3).
Insuline : souvent commencée trop tard, l’insulinothérapie présente de nombreux avantages et peut améliorer considérablement la qualité de vie des diabétiques âgés [10]. L’insuline reste l’antidiabétique ayant la plus grande puissance thérapeutique et peut corriger efficacement les symptômes de l’hyperglycémie tels que la fatigue, la diurèse osmotique, la déshydratation et les modifications de l’acuité visuelle. L’insuline n’a pratiquement aucun potentiel d’interaction et a un effet anabolisant, ce qui constitue un avantage décisif chez les patients malnutris et sarcopéniques. L’insuffisance rénale ralentit la dégradation de l’insuline, ce qui nécessite une réduction de la dose. Les hypoglycémies peuvent être considérablement réduites par le choix d’un régime approprié et une titration lente de la dose. L’insulinothérapie basale, généralement associée à des antidiabétiques oraux, présente le plus faible potentiel hypoglycémique. Il est essentiel d’éduquer les patients ou d’identifier les limitations des fonctions cognitives qui empêchent l’auto-application d’insuline ou qui mettent le patient en danger en raison d’une mauvaise gestion ou d’un mauvais dosage de l’insuline.
Littérature :
- Lakey, WC, et al : Are current clinical trials in diabetes addressing important issues in diabetes care ? Diabetologia 2013 ; 56(6) : 1226-1235.
- Kirkman MS, et al : Diabetes in older adults. Diabetes Care 2012 ; 35(12) : 2650-2664.
- Sinclair AJ, et al : Groupe de travail européen sur le diabète pour les personnes âgées 2011 lignes directrices cliniques pour le diabète sucré de type 2. Résumé exécutif. Diabetes Metab 2011 ; 37(Suppl 3) : S27-S38.
- Kalyani RR, Egan JM : Diabetes and altered glucose metabolism with aging. Endocrinol Metab Clin North Am 2013 ; 42(2) : 333-347.
- Yaffe K, et al : Association between hypoglycemia and dementia in a biracial cohort of older adults with diabetes mellitus. JAMA Intern Med 2013 ; 173(14) : 1300-1306.
- Yau RK, et al : Diabetes and risk of hospitalized fall injury among older adults. Diabetes Care 2013 ; 36(12) : 3985-3991.
- Inzucchi SE, et al : Gestion de l’hyperglycémie dans le diabète de type 2 : une approche centrée sur le patient : déclaration de position de l’American Diabetes Association (ADA) et de l’Association européenne pour l’étude du diabète (EASD). Diabetes Care 2012 ; 35(6) : 1364-1379.
- Girlich C, Hoffmann U, Bollheimer C : Traitement du diabète de type 2 chez les patients âgés. Internist (Berl) 2014 ; 55(7) : 762-768.
- Zanchi A, Lehmann R, Philippe J : Antidiabetic drugs and kidney disease–recommendations of the Swiss Society for Endocrinology and Diabetology. Swiss Med Wkly 2012 ; 142 : w13629.
- Reza M, et al : Insulin improves well-being for selected elderly type 2 diabetic subjects. Diabetes Res Clin Pract 2002 ; 55(3) : 201-207.
- Meneghini LF, et al : Traitements bénéfiques pour le poids pour le diabète de type 2. J Clin Endocrinol Metab 2011 ; 96(11) : 3337-3353.
- Vasilakou D, et al : Sodium-glucose cotransporter 2 inhibitors for type 2 diabetes : a systematic review and meta-analysis. Ann Intern Med 2013 ; 159(4) : 262-274.
PRATIQUE DU MÉDECIN DE FAMILLE 2015 ; 10(10) : 20-26