Le score de focalisation (FS) sur les biopsies des petites glandes salivaires labiales est l’un des deux principaux critères (avec une positivité anti-SSA) pour le diagnostic du syndrome de Sjögren primaire (pSS). Afin de réduire les taux d’erreur dans les diagnostics, des algorithmes d’apprentissage en profondeur utilisant des réseaux neuronaux artificiels pourraient être utilisés à l’avenir pour aider les pathologistes.
Selon les critères ACR/EULAR pour le pSS, la classification du score focal (FS) est l’un des trois critères de classification, mais elle nécessite une expertise qui n’est pas toujours disponible dans la pratique. 53% des cas conduisent à une révision du diagnostic lorsqu’ils sont évalués par des experts.
L’apprentissage automatique (machine learning) est une famille d’algorithmes capables d’absorber un grand nombre de données et de les utiliser, par exemple, pour prédire quelque chose. Le deep learning est un sous-ensemble de ce domaine qui se concentre sur une seule famille d’algorithmes et est appelé “réseaux de neurones profonds”, a expliqué en introduction Louis Basseto, Scienta Lab, département de recherche, Paris [1].
Le deep learning est déjà utilisé en pathologie médicale, par exemple dans le cas du cancer du sein, où il permet déjà, grâce à des algorithmes, de détecter très précisément les métastases dans les échantillons de tissus des ganglions lymphatiques avec de meilleures performances que les pathologistes. “Notre groupe a également montré que l’apprentissage automatique peut être utilisé dans la polyarthrite rhumatoïde pour prédire la réponse au méthotrexate et aux inhibiteurs du TNF”. Les chercheurs se sont maintenant attelés à la tâche d’appliquer le deep learning au syndrome de Sjögren et de voir s’il pouvait aider à classer le score focal et à diagnostiquer le pSS ?
Deep Learning basé sur des biopsies de glandes salivaires
Pour ce faire, ils ont développé deux réseaux d’apprentissage en profondeur en utilisant des biopsies labiales numérisées de glandes salivaires de patients pour prédire le score de focalisation (FS ≥1 ou FS <1) et le diagnostic du syndrome de Sjögren primaire sur la base de l’histologie uniquement (pSS+ ou pSS-). 325 patients ont été inclus dans l’étude (145 de l’Université Paris-Saclay, Hôpital Bicêtre, 71 de l’Université Queen Mary de Londres et 109 de l’Université de Birmingham), en utilisant des biopsies prélevées en routine clinique. Les participants ont été divisés en trois groupes :
- pSS- et FS <1 (32%, symptômes de sicca)
- pSS+ et FS ≥1 (47%)
- pSS+ et FS <1 (21%)
Tous les FS ont été préalablement confirmés par des pathologistes et les diagnostics de pSS par des experts.
Pour faire une prédiction, on utilise une ou plusieurs images de la biopsie. Chaque image est divisée en tuiles et l’algorithme attribue de manière autonome un score de risque à chacune de ces tuiles. Toutes ces informations sont ensuite combinées pour établir une prédiction soit du score de focalisation, soit du diagnostic, en fonction de l’algorithme utilisé.
“Nous utilisons deux ensembles de données différents”, a expliqué Basseto : un ensemble de formation (70% des patients) et un ensemble de validation (30% des patients). Les deux ensembles contiennent la même proportion de classes positives et négatives (pSS+/pSS- ou FS ≥1/FS <1) und die verschiedenen Zentren, aus denen sich die Teilnehmer zusammensetzen, sind im Training und in der Validierung gemischt. Diese beiden Aufgaben nennt man «semi-supervised learning», also halbüberwachtes Lernen. «Das ist der Schlüssel zum Verständnis der Arbeit: Halbüberwachtes Lernen bedeutet, dass wir dem Modell im Training zwar Informationen geben – z.B. sagen wir ihm, wenn ein Patient einen FS>a 1. Cependant, nous ne disons pas quelles parties de l’imagerie amèneraient un pathologiste à penser cela. Le modèle le détermine à partir des données elles-mêmes”.
Nouveaux biomarqueurs potentiels
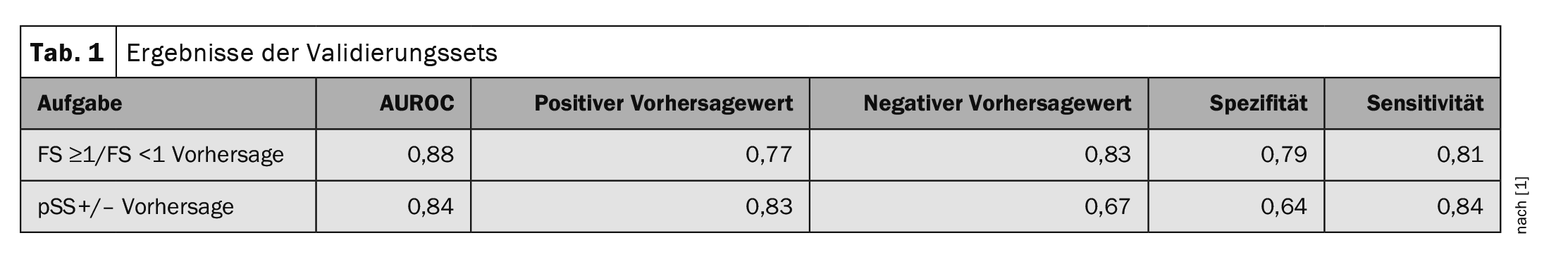
La performance de l’algorithme a été mesurée par l’aire sous la courbe ROC (AUROC). En ce qui concerne le score de focalisation (FS ≥1/FS <1), l’algorithme a obtenu un AUROC de 0,88. 77% des prédictions positives étaient en fait des patients avec un score de focalisation de ≥1. Pour la valeur prédictive négative, 83% ont même indiqué correctement qu’il s’agissait d’un FS<1. Dans le cas de la prédiction de diagnostic, l’AUROC était de 0,84. 83% des patients avec une prédiction positive de l’algorithme étaient en fait atteints de Sjögren positif (pSS+) et 67% des patients avec une prédiction négative étaient en fait atteints de Sjögren négatif (pSS-) (tableau 1).
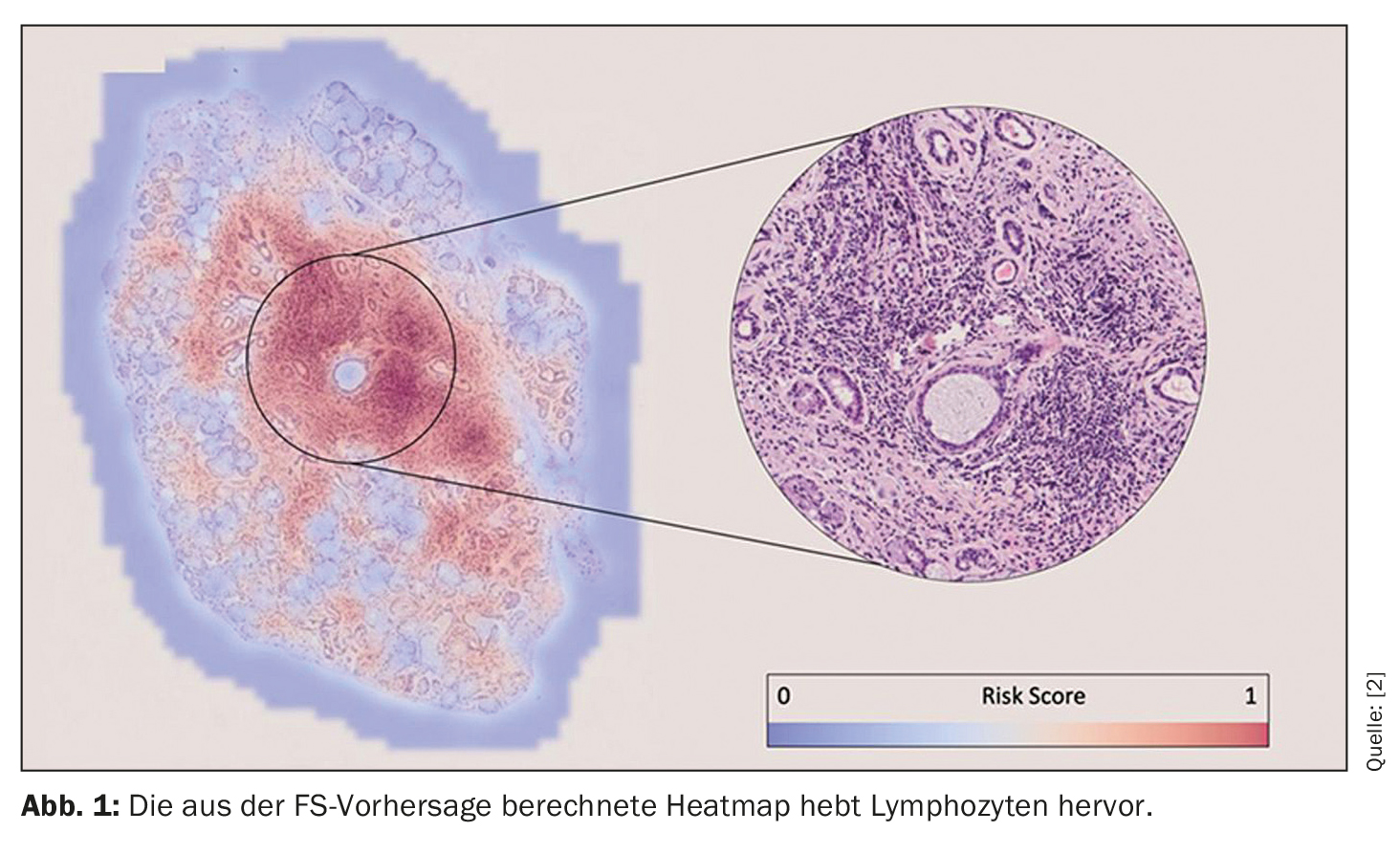
“Ces prédictions ont été faites uniquement à partir des images. Bien que nous n’ayons pas dit à l’algorithme où chercher pour prendre sa décision, – mais après la formation, nous pouvons vérifier les algorithmes pour voir sur quelle base ils ont fait leurs prédictions”. La conclusion des chercheurs est que l’algorithme du score de focalisation a identifié des foyers lymphocytaires pour faire une prédiction (Fig. 1). Cela permet d’expliquer et de confirmer visuellement les résultats de la prédiction. C’est donc rassurant pour le FS, selon Basseto, “mais ce qui est rassurant pour le FS est très excitant pour le diagnostic, car cela pourrait conduire à l’identification potentielle de nouveaux biomarqueurs histologiques qui ne sont intéressants que pour la population pSS+ et FS<1)”. Selon lui, cet aspect est particulièrement intéressant pour les futurs travaux du groupe de recherche.
Messages Take-Home
- Le deep learning prédit avec précision le score de focalisation et le diagnostic du syndrome de Sjögren primaire à partir de biopsies labiales des glandes salivaires.
- Le deep learning pourrait potentiellement réduire le taux d’erreur de diagnostic de ~2,5 fois. Le taux d’erreur dû au deep learning est de 19,7% vs 53% pour les centres non-experts.
perspectives :
- Des évaluations cliniques supplémentaires sont nécessaires pour valider les algorithmes dans la pratique clinique réelle.
- Validation supplémentaire sur une plus grande cohorte.
- Les travaux en cours visent à identifier de nouveaux biomarqueurs histologiques associés au diagnostic du pSS.
Congrès : EULAR 2023
Source :
- Basseto L: Vortrag «Deep Learning Accurately Predicts Focus Score and Diagnosis of Primary Sjögren Syndrome using Labial Salivary Gland Biopsies»; EULAR 2023, Mailand, 2.6.2023 (online).
- Basseto L: Scientific Abstract OP0232, EULAR 2023; doi: 10.1136/annrheumdis-2023-eular.418.
InFo RHEUMATOLOGIE 2023: 5(2): 20–21