Les anémies sont un problème fréquent dans la pratique de la médecine générale. L’anamnèse et quelques paramètres de laboratoire permettent de clarifier et d’expliquer la cause d’environ 90% des anémies dans le cabinet du médecin généraliste [1]. Christoph Merlo, Lucerne, a présenté un algorithme d’évaluation simple dans le cadre d’un atelier.
L’anémie est définie par une diminution de la concentration d’hémoglobine, la limite inférieure d’hémoglobine définissant l’anémie dépendant de la population de référence et parfois de l’analyseur. Les valeurs normales d’hémoglobine utilisées par différents laboratoires peuvent donc différer des valeurs normales définies par l’OMS(tableau 1). La définition de l’OMS ne tient pas non plus compte du fait que les taux moyens d’hémoglobine diminuent physiologiquement chez les hommes à partir de 65 ans environ, mais pas chez les femmes. “Dans la pratique, vous prenez de toute façon la décision individuelle de faire ou non un bilan d’anémie. Les antécédents, les symptômes et les comorbidités d’un patient sont bien plus importants que le taux d’hémoglobine absolu”, a expliqué le Dr Christoph Merlo, Lucerne. Outre les symptômes classiques que sont la fatigue, la dyspnée d’effort, l’intolérance à l’effort, les palpitations/la tachycardie, l’anémie peut également provoquer des maux de tête.

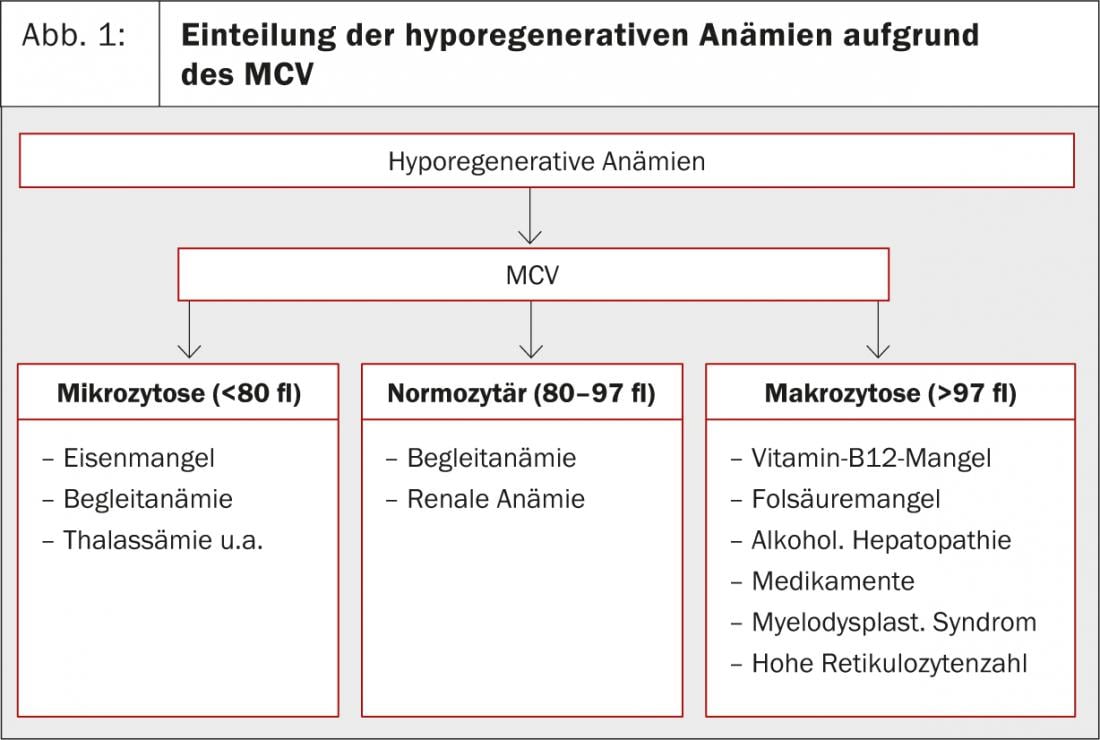
Les anémies sont classées en fonction du nombre de réticulocytes et du MCV (volume corpusculaire moyen). Si le nombre de réticulocytes est inférieur à 100 G/l, il s’agit d’une anémie hyporégénérative. Si elle est supérieure à 100 G/l, il s’agit d’une anémie hyperrégénérative. Pour cette dernière, il n’y a que deux causes possibles : l’hémorragie subaiguë et l’hémolyse. “Une augmentation passagère des réticulocytes peut également être observée lorsqu’un patient souffrant d’une carence en fer ou d’une carence en vitamine B12 vient d’être substitué”, a ajouté le Dr Merlo. Les anémies hyporégénératives sont encore divisées en anémies microcytaires, normocytaires et macrocytaires sur la base du MCV(Fig. 1).
Dans certains cas, l’anamnèse permet déjà de déterminer la cause de l’anémie, qui est évaluée en premier lieu par un hémogramme composé de l’hémoglobine, de l’hématocrite, du nombre d’érythrocytes, des indices et du nombre de leucocytes (par exemple, une anémie due à une chimiothérapie). Si le MCV correspond également, il n’est pas nécessaire de procéder à des examens supplémentaires. Cependant, la plupart du temps, un simple laboratoire de base composé de la numération des réticulocytes, de la ferritine, y compris la CRP et l’ALAT (GPT), de la vitamine B12, de l’acide folique érythrocytaire et de la créatinine (pour déterminer la clairance de la créatinine) est nécessaire pour clarifier la cause de l’anémie. Cet algorithme simple, qui permet de clarifier définitivement environ 90% des anémies dans la pratique de la médecine générale [1], est présenté dans la figure 2. Si l’on soupçonne une maladie de la moelle osseuse ou si l’on veut clarifier des anémies hémolytiques particulières, le patient doit être adressé à un hématologue pour un examen plus approfondi (tableau 2).

La carence en fer, l’insuffisance rénale chronique et d’autres maladies chroniques (tumeurs, inflammations) font partie des causes d’anémie les plus fréquentes dans un cabinet de médecine interne de premier recours [1]. “Dans une enquête personnelle, environ un tiers des patients présentaient plus d’une cause d’anémie”, ajoute le Dr Merlo.
La ferritine indique une carence en fer
Le meilleur paramètre pour détecter une carence en fer est la ferritine. Le fer sérique ne convient pas à cet effet, car il est soumis à de fortes variations diurnes. La seule cause d’une baisse de la ferritine est la carence en fer. “En pratique, la règle générale suivante a fait ses preuves : si le taux de ferritine sérique est inférieur à 50 μg/l, une carence en fer est possible, très probable en dessous de 30 μg/l et avérée en dessous de 15 μg/l”, explique le Dr Merlo. Comme la ferritine réagit comme une protéine de phase aiguë, c’est-à-dire qu’elle est élevée en cas d’inflammation, et qu’elle peut également être élevée en cas de maladie chronique du foie, il convient de toujours déterminer la CRP et l’alanine aminotransférase (ALAT) en même temps que la ferritine. Dans les états inflammatoires chroniques avec une CRP élevée, la carence en fer peut être détectée, en plus d’autres tests spécialisés, à l’aide de l’augmentation du récepteur de la transferrine soluble.
Il va de soi qu’une substitution en fer ne doit être effectuée qu’en cas de carence avérée. Les besoins en fer peuvent être calculés à partir du déficit en hémoglobine et en ferritine à l’aide d’une formule simple (tableau 3).

Il convient également de noter qu’en cas de substitution orale, seuls 10% du fer administré sont absorbés. Pour un besoin en fer de 2000 mg, il faut donc donner un total de 20 000 mg. Les préparations de fer bivalent doivent être administrées à jeun, sinon l’absorption est encore plus mauvaise. Le fer trivalent (Maltofer®) n’est transformé en fer divalent que dans l’intestin et peut être pris avec les repas, ce qui peut améliorer la tolérance. En cas de manque d’observance, par exemple chez les patients multimorbides souffrant de polypharmacie, d’anémie rénale ou de mauvaise tolérance, la substitution de fer par voie i.v. constitue une alternative. Pour contrôler le succès du traitement, on peut observer une augmentation des réticulocytes après 5 à 10 jours et une augmentation de l’hémoglobine après deux semaines. Le fer intraveineux stimule la ferritine, c’est pourquoi il faut dans ce cas attendre au moins quatre semaines avant de contrôler ce taux.
Source : “Anämieabklärung in der Praxis”, atelier lors de la 81e réunion annuelle de la SSMI, 29-31 mai 2013, Bâle.
Littérature :
- Merlo CM, Wuillemin WA : Prévalence et causes des anémies dans un cabinet de médecine générale en ville. Pratique 2008 ; 97 : 713-718.
- Merlo CM, Wuillemin WA : Diagnostic et traitement de l’anémie dans la pratique. Pratique 2009 ; 98 : 191-199.